盐酸安妥沙星注射液的稳定性试验
2012-11-06堵伟锋
瑛,堵伟锋
(1.安徽省蚌埠市食品药品检验所,安徽 蚌埠 233000;2.安徽省食品药品检验所,安徽 合肥 230051)
盐酸安妥沙星是我国拥有自主知识产权的一类新药,为左氧氟沙星的8-NH2衍生物,8-NH2的引入使其抗菌活性有所提高。体外抗菌试验结果显示,盐酸安妥沙星具有广谱抗菌作用,对革兰阴性菌包括流感嗜血杆菌、克雷伯菌属、变形杆菌属、柠檬酸杆菌、不动杆菌属、沙门菌属等具有良好的抗菌活性;对革兰阳性球菌包括溶血性链球菌等也具有较好的抗菌作用,特别是对甲氧西林耐药的葡萄球菌的抗菌活性较环丙沙星、氧氟沙星、司帕沙星和洛美沙星强8~16倍;对厌氧菌中的脆弱类杆菌和分枝杆菌也有一定的抗菌作用[1]。目前,尚未见有关盐酸安妥沙星注射液稳定性的文献报道。现根据《药物稳定性研究技术指导原则[2](以下简称指导原则)》和盐酸安妥沙星注射液的质量标准,并参考相关文献[3],考察了盐酸安妥沙星注射液的稳定性,现报道如下。
1 仪器与试药
Shimadzu 20A型系列高效液相色谱仪,包括LC-20AD型四元泵、SIL-20A型自动进样器、SPD-M20A型二极管阵列检测器、CTO-20A型柱温箱;MA 235型pH计(瑞士梅特勒);YB-2型澄明度检测仪(天津大学精密仪器厂)。盐酸安妥沙星注射液[安徽环球药业股份有限公司,规格为5 mL∶0.1 g(安妥沙星),批号分别为100202-1,100203-1,100204-1];盐酸安妥沙星对照品[安徽环球药业股份有限公司,含量为89.7%(以安妥沙星计),水分为0.1%];乙腈为色谱纯,磷酸二氢钾、己烷磺酸钠、乙二胺四乙酸二钠均为分析纯,水为纯化水。
2 方法与结果
2.1 色谱条件[4]
色谱柱:WondaSil C18柱(250 mm×4.6 mm,5μm);流动相:0.05 mol/L磷酸二氢钾溶液(含0.005 mol/L己烷磺酸钠,0.007%乙二胺四乙酸二钠,调节pH至2.4)-乙腈(84∶16);检测波长:297 nm;流速:1.0 mL/min;进样10μL;柱温:35℃。
2.2 含量测定方法
精密称取盐酸安妥沙星对照品适量,加水溶解并稀释成每1 mL中含安妥沙星0.2 mg的溶液,作为对照品溶液;精密量取盐酸安妥沙星注射液适量,加水稀释成每1 mL中含安妥沙星0.2 mg的溶液,作为供试品溶液。分别精密量取上述两种溶液各10μL,注入液相色谱仪,记录色谱图,按外标法以峰面积计算。
2.3 有关物质检查方法
取盐酸安妥沙星注射液适量,加水稀释成每1 mL中含安妥沙星0.2 mg的溶液,作为供试品溶液;精密量取供试品溶液1 mL,置100 mL量瓶中,加水稀释至刻度,摇匀,作为对照溶液。精密量取对照溶液10μL,注入液相色谱仪,调节检测灵敏度,使主成分峰高约为满量程的20%~25%。再精密量取供试品溶液与对照溶液各10μL,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的2倍。供试品溶液如显杂质峰,各杂质峰面积的和不得大于对照溶液主峰面积。
2.4 稳定性试验
2.4.1 影响因素试验
高温试验:按指导原则要求,取样品,分别置60℃恒温干燥箱中,分别于0,5,10 d时取样,考察样品的性状、可见异物、pH、含量及有关物质。结果样品性状均为黄色澄明液体,可见异物均符合规定,其他见表1。
强光照射试验:按指导原则要求,取样品进行光照(5 000 lx)试验,分别于0,5,10 d时取样,考察样品的性状、可见异物、pH、含量及有关物质。结果样品性状均为黄色澄明液体,可见异物均符合规定,其他见表1。
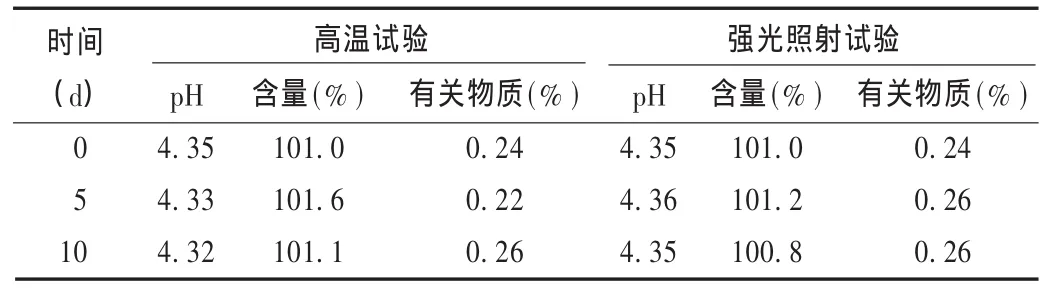
表1 高温与强光照射试验结果(批号100202-1)
低温试验:按指导原则要求,取样品进行低温试验,分3次循环,每次循环在4℃条件下放置2 d,然后在40℃加速条件下考察2 d,取样检测,考察其性状、可见异物、pH、含量及有关物质。结果样品性状均为黄色澄明液体,可见异物均符合规定,其他见表2。
冻融试验:按指导原则要求,取样品进行冻融试验,分3次循环,每次循环在-20℃条件下放置2 d,然后在40℃加速条件下考察2 d,取样检测,考察其性状、可见异物、pH、含量及有关物质。结果样品性状均为黄色澄明液体,可见异物均符合规定,其他见表2。
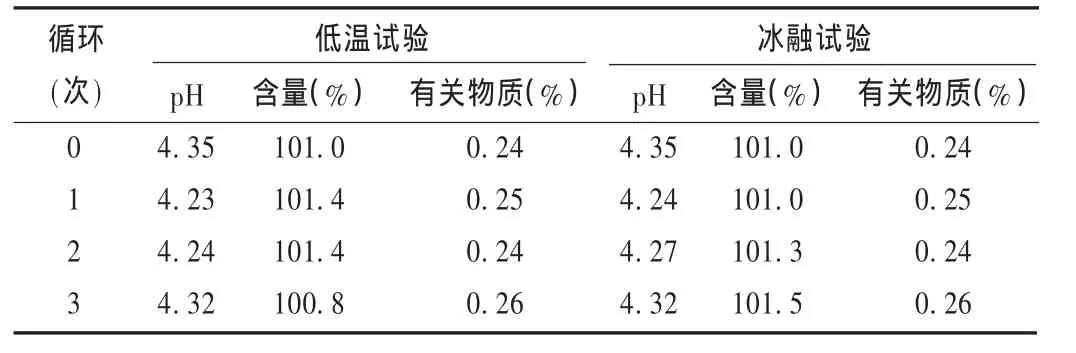
表2 低温与冻融试验结果(批号为100202-1)
2.4.2 加速试验
按指导原则要求,进行加速试验。将3批市售包装样品置40℃的恒温箱中,分别于0,1,2,3,6个月末取样检测,考察其性状、可见异物、pH、含量及有关物质。结果样品性状均为黄色澄明液体,可见异物均符合规定,其他见表3。
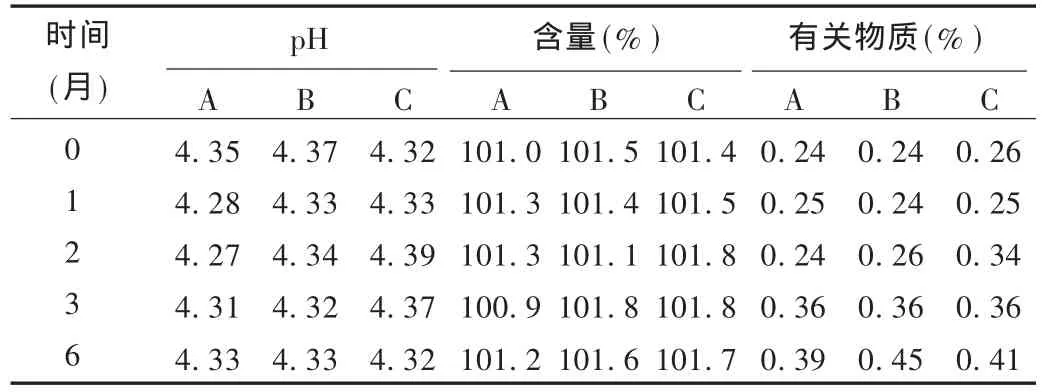
表3 加速试验结果
长期试验:按指导原则要求,进行长期试验。将3批市售包装样品室温放置,分别于 0,3,6,9,12,18,24,36 个月末取样检测,考察其性状、可见异物、pH、含量及有关物质。结果样品性状均为黄色澄明液体,可见异物均符合规定,其他见表4。
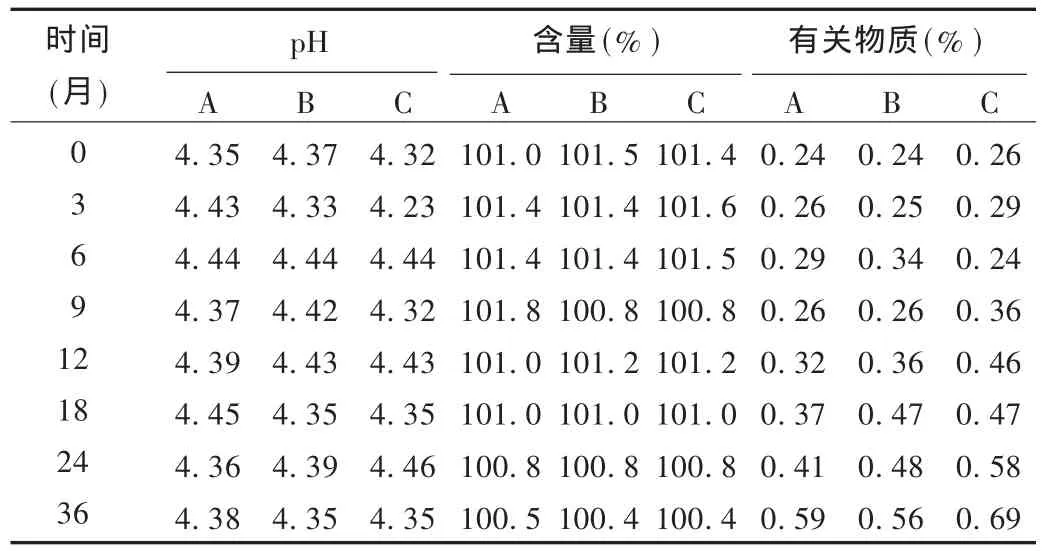
表4 长期试验结果
3 讨论
指导原则要求,对于易发生相分离、黏度减小、沉淀或聚集的药品,需通过低温或冻融试验来验证其运输或使用过程中的稳定性。由于本品浓度较高,有可能发生沉淀或聚集,因此有必要进行低温试验和冻融试验来验证其稳定性。试验结果显示,本品在低温或冻融条件下均比较稳定。
长期试验结果显示,本品在室温条件下3年内较稳定,各项指标均未发生明显变化,因此本品的有效期至少可以定为2年。另外强光照射试验结果显示,本品的光稳定性较好,优于一般沙星类药物。
由于本品为液体制剂,因此在考察影响因素时无需再做高湿度试验。高温试验时,本品在60℃条件下各项指标均无明显变化,因此不再进行40℃ 试验。
[1]梅友健.新型高效广谱抗菌药物 —— 安妥沙星[J].安徽医药,2010,14(2):229-231.
[2]【H】GPH6-1.化学药物稳定性研究技术指导原则[S].
[3]陈吉生,黎行山,陆志勇,等.复方奥硝唑栓的稳定性试验[J].中国医院药学杂志,2005,25(10):944-946.
[4]洪建文,胡昌勤.HPLC对盐酸安妥沙星含量及有关物质测定的研究[J].中国药学杂志,2007,42(14):1 101-1 103.
