果糖基甘氨酸的合成及其与铜(Ⅱ)、镍(Ⅱ)配位特性的研究
2012-11-02薛晓丽王忠合于淑娟
薛晓丽,王忠合,于淑娟
(华南理工大学轻工与食品学院,广东广州510640)
果糖基甘氨酸的合成及其与铜(Ⅱ)、镍(Ⅱ)配位特性的研究
薛晓丽,王忠合,于淑娟*
(华南理工大学轻工与食品学院,广东广州510640)
合成并纯化了Maillard反应初级阶段产物——果糖基甘氨酸(DFG),并且利用离子色谱、质谱、核磁共振等方法分析其纯度及结构。结果表明:合成产物为目标化合物,且分子式为C8H15NO7,相对分子质量237。采用pH电位滴定法测定了温度(303±0.1)K,离子强度I=0.1mol/L的NaCl溶液中DFG与铜(Ⅱ)、镍(Ⅱ)配合物稳定常数,DFG合铜配合物稳定常数对数值分别为lgK1=7.24±0.09,lgK2=6.57±0.05,lgK3=3.31±0.02;DFG合镍配合物稳定常数对数值分别为lgK1=5.73±0.03,lgK2=4.69±0.02,lgK3=3.59±0.05,且DFG合铜配合物稳定性大于DFG合镍配合物的稳定性。
Maillard反应,果糖基甘氨酸,配位特性,铜(Ⅱ),镍(Ⅱ)
果糖基氨基酸是美拉德反应(还原糖与氨基化合物发生的非酶褐变)初级阶段形成的一类关键的中间产物,是由N-取代葡萄糖胺经Amadori重排而来,被称为Amadori重排产物(ARPs)[1],又称为N-取代-1-脱氧-D-果糖基氨基酸,反应路径见图1。果糖基氨基酸是白色固体,常温下化学性质相对较稳定,没有气味;但是经过加热后产生具有芳香气味的化合物,如吡嗪类、呋喃类以及吡喃类化合物等[2-3]。该类化合物是重要的非挥发性香味前体物质,在烟草加工中添加这类物质可以增加烟草的甜香和烘烤香,改善吸味[4]。此外,在食品的加工与储藏过程中也会产生这类物质,尤其是在干制的果蔬中,可达每干重水可溶物含量的10%以上[2,5-6]。与其它糖胺类物质类似,果糖基氨基酸对 Mg2+,Cu2+,Pt2+,Ni2+等金属离子也具有一定的络合能力[5-7]。从结构上分析,它可看作是相应氨基酸的衍生物,作为二齿配体以α-碳上的氨基和羧基作为配位基团同金属离子配位。同时,果糖基氨基酸具有人体内源性结构特征,既有半缩醛结构,又引入L-构型氨基酸,对人体毒害性小[8]。因此,这类物质也可作为一种重金属离子捕集剂应用于医药领域。本文采用葡萄糖和甘氨酸作为原料,直接加热回流合成果糖基甘基酸,用阳离子交换树脂分离纯化,产物采用光谱与波普法进行结构表征,最后采用pH电位滴定法测定该化合物与铜(Ⅱ)、镍(Ⅱ)配合物的稳定常数,为研究果糖基甘基酸(DFG)的金属配位特性及其应用提供一定的理论依据。
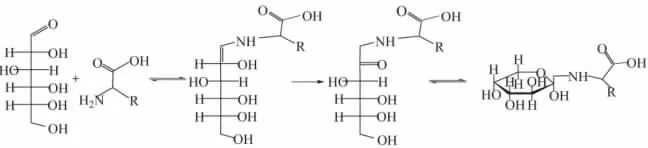
图1 果糖基氨基酸反应生成式Fig.1 Mechanism of formation of fructose-amino acids
1 材料与方法
1.1 材料与仪器
Amberlite IRN-77氢型离子交换树脂 美国Fluke公司;无水葡萄糖、甘氨酸、焦亚硫酸钠、铁氰化钾、无水甲醇、无水乙醇、氨水、氢氧化钠、氯化钠、硝酸铜等 均为国产分析纯。
DF-101S集热式恒温加热磁力搅拌器 河南巩义予华仪器有限责任公司;RE-2000旋转蒸发仪,SHZ-Ⅲ循环水真空泵 上海亚荣生化仪器厂;硅胶G薄层层析板 青岛海洋化工厂;Dionex ICS-5000型离子色谱仪 美国Dionex公司;Esquire HCT PLUS色谱-质谱联用仪、BrukerAVANCE-400型核磁共振仪(采用 D2O为溶剂) 德国 Bruker公司; Titrando888型智能电位滴定仪 瑞士万通。
1.2 实验方法
1.2.1 果糖基甘氨酸的合成 葡萄糖和甘氨酸摩尔比4∶1,加入一定量的焦亚硫酸钠作为催化剂,溶于80mL 1∶1甲醇-水溶液中,混合物于室温下搅拌20min,回流加热8h,反应结束后体系呈棕黄色糖浆状,冷却后加入到250mL 1∶1乙醇-水体系中,用阳离子交换柱(2.5×45cm,H+)分离纯化,分别用750mL 1∶1乙醇-水、250mL水和2.5L 0.1mol/L氨水洗脱。用茚三酮法和普鲁士蓝法对洗出液进行检验[9-10]。收集洗脱液,减压浓缩,向浓缩液中加入3倍体积的甲醇(超声),4℃放置过夜,析出白色晶体,重结晶,干燥,称重,产率约为14.6%(以甘氨酸重计)。
1.2.2 薄层色谱(TLC)法检测 溶解少量甘氨酸和样品,点样于硅胶板上,以正丁醇-冰醋酸-水(4∶1∶1)为展开剂,展开,取出,晾干,喷以0.2%的茚三酮丙酮溶液,120℃加热2~5min,日光检视。
1.2.3 离子色谱-积分安培法(HPAEC-PAD)检测 称取一定量的样品配制成浓度为5mg/L的溶液,过0.22μm滤膜,采用离子色谱-积分安培法检测果糖基甘氨酸的含量。检测条件为:CarboPac PA1糖分析柱(i.d.4×250mm),积分安培电化学检测器,淋洗速度1mL/min,洗脱剂为NaOAc(300mmol/L)、超纯水和NaOH(300mmol/L),淋洗梯度见表1。
1.2.4 质谱及13C核磁共振分析 选用电喷雾离子源质谱(ESI-MS)进行分析,电喷雾离子源(ESI);电离模式:正离子模式;质量扫描范围,m/z50~800amu;毛细管电压:-103.0V。以氘代水(D2O)为溶剂,将分离纯化得到的产物作碳谱分析。
1.2.5 电位滴定法测定质子化常数 在50.00mL滴定体系中,DFG浓度为1.0×10-2mol/L,实验条件为(303±0.1)K,用0.2mol/L NaCl溶液调整体系的离子强度I为0.1mol/L,实验溶液均用重蒸水配制,在氮气保护下,选择动态滴定模式,用已除去CO2的氢氧化钠标准溶液(0.1038mol/L)滴定,平行滴定两次,记录NaOH溶液消耗量和溶液pH的变化,采用Bjerrum[11]提出的半整数法求得DFG的累积质子化常数,计算公式归纳如下[11-13]:

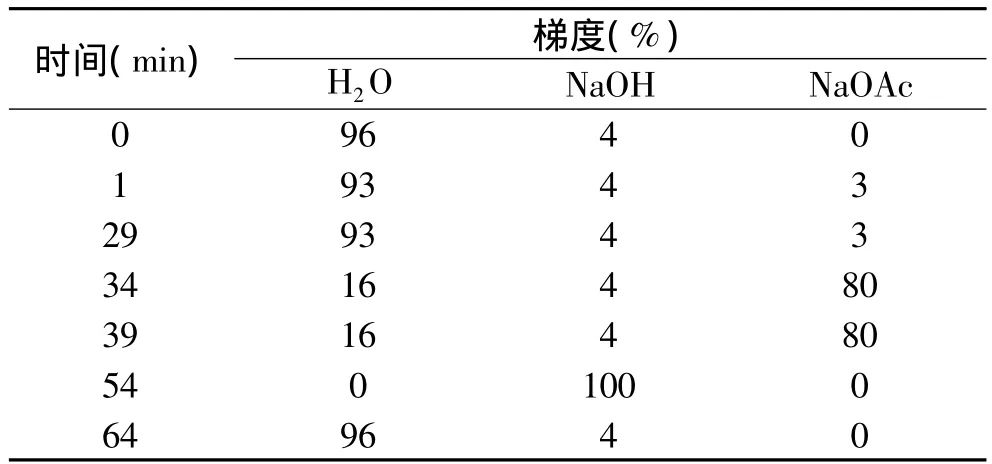
表1 洗脱液淋洗梯度Table 1 Gradient program for N-(1-deoxy-D-fructos-1-yl)-glycine
1.2.6 DFG与Cu2+、Ni2+配合物稳定常数的测定在50.00mL滴定体系中,金属离子浓度为1.0×10-3mol/L,DFG浓度为5.0×10-3mol/L,实验条件为(303 ±0.1)K,用0.2mol/L NaCl溶液维持溶液的离子强度为0.1mol/L,其余步骤同1.2.5,求得DFG与金属离子所生成的配合物的稳定常数对数值lgK,络合物稳定常数的计算公式归纳如下:
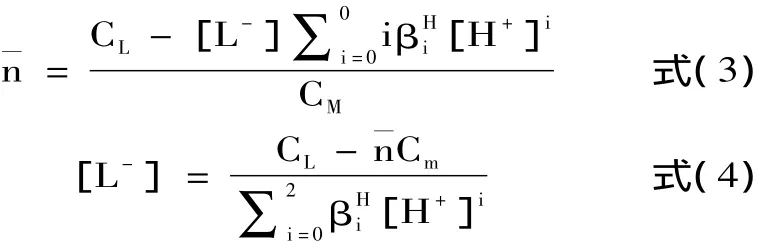
式中,CM为金属离子的总浓度,mol/L;[L-]为体系中游离配位体DFG的浓度,mol/L;其余符号的意义同1.2.5。
以[L-]的负对数p[L-]对做生成函数曲线图,为半整数点对应的p[L-]值即为所求络合稳定常数的对数值lgK。
2 结果与讨论
2.1 TLC检测
葡萄糖与甘氨酸溶液加热反应后为橙褐色,经阳离子交换树脂分离后得到的结晶为白色,薄层色谱检测比移值 Rf为0.14,甘氨酸的比移值 Rf为0.24,与文献报道的数据一致[5]。因此,采用薄层色谱法可区分产物与合成原料甘氨酸的差异。
2.2 离子色谱-积分安培(HPAEC-PAD)检测结果
目前,果糖基氨基酸的测定方法主要有高效液相色谱-示差折光检测(HPLC-RD)和紫外检测(HPLC-UV)分析法、离子色谱-积分安培检测法(HPAEC-PAD)等。液相色谱法检测糖类化合物存在一些问题,例如糖类化合物的紫外吸收很弱,需要采用示差折光检测器,但其灵敏度较低。离子色谱法测定糖类物质,不仅前处理简单,而且采用高灵敏度和高选择性的脉冲安培检测器,准确度高,重现性好[14-15]。因此,离子色谱法可用以区分产物与合成原料中的葡萄糖。阳离子树脂分离前后产物的离子色谱图,如图2和图3所示,通过与葡萄糖标准品对比以及相关文献[16-17]的报道,图2中15min峰即1号峰为葡萄糖,在35min洗脱液梯度变化后出现的峰为果糖基甘氨酸产物峰。所以直接加热反应后的粗产物经阳离子交换柱分离后,分离效果显著,产物纯度得到大幅度提升。
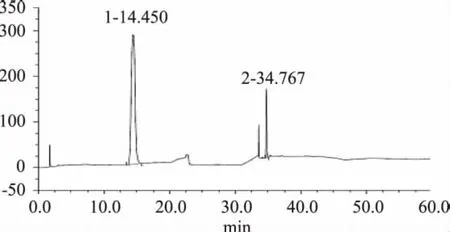
图2 柱分离前离子色谱图Fig.2 Chromatogram before column separation
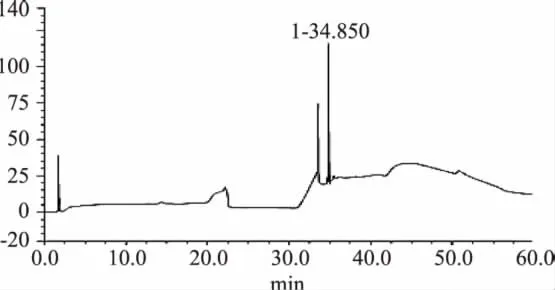
图3 柱分离后离子色谱图Fig.3 Chromatogram after column separation
2.3 质谱(EMI-MS)及13C核磁共振分析
对结晶产物进行一级电喷雾离子源质谱分析,从分子量上即可确定产物为目标产物。从图4可以看出其分子离子峰[M+H]+为237.5,可以判断相对分子质量为236.5(237),与DFG理论相对分子质量相符,相对分子质量为奇数,根据氮规律,分子中含有奇数个氮原子,DFG的分子式为C8H15NO7。由于产物中含有果糖基,在水溶液中有四种异构体及开环式,使其碳谱较为复杂,结果见表2。
2.4 DFG与Cu2+、Ni2+配合物的稳定常数
pH电位滴定法测定配合物稳定常数的原理是:当配体为弱酸或弱碱时,配合物的形成会改变溶液的pH,凡金属离子与配体形成配合物的反应中,伴随有质子释放的体系,均可用pH法进行研究,且该测定方法精确,较为常用。滴定曲线如图5所示,分别对比图中DFG的滴定曲线与有金属离子存在的DFG滴定曲线中相同pH下消耗NaOH溶液的体积,可以看出DFG与Cu2+和Ni2+均可发生配位反应。
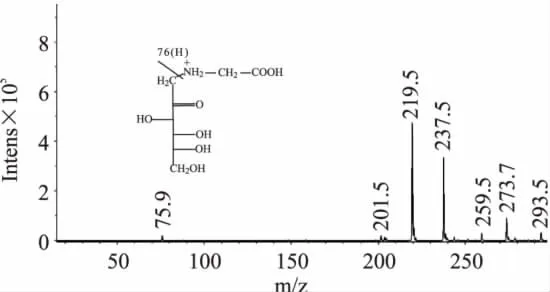
图4 DFG一级电离质谱图(1.3min)Fig.4 The positive ion ESI-MS spectrometry of DFG(1.3min)
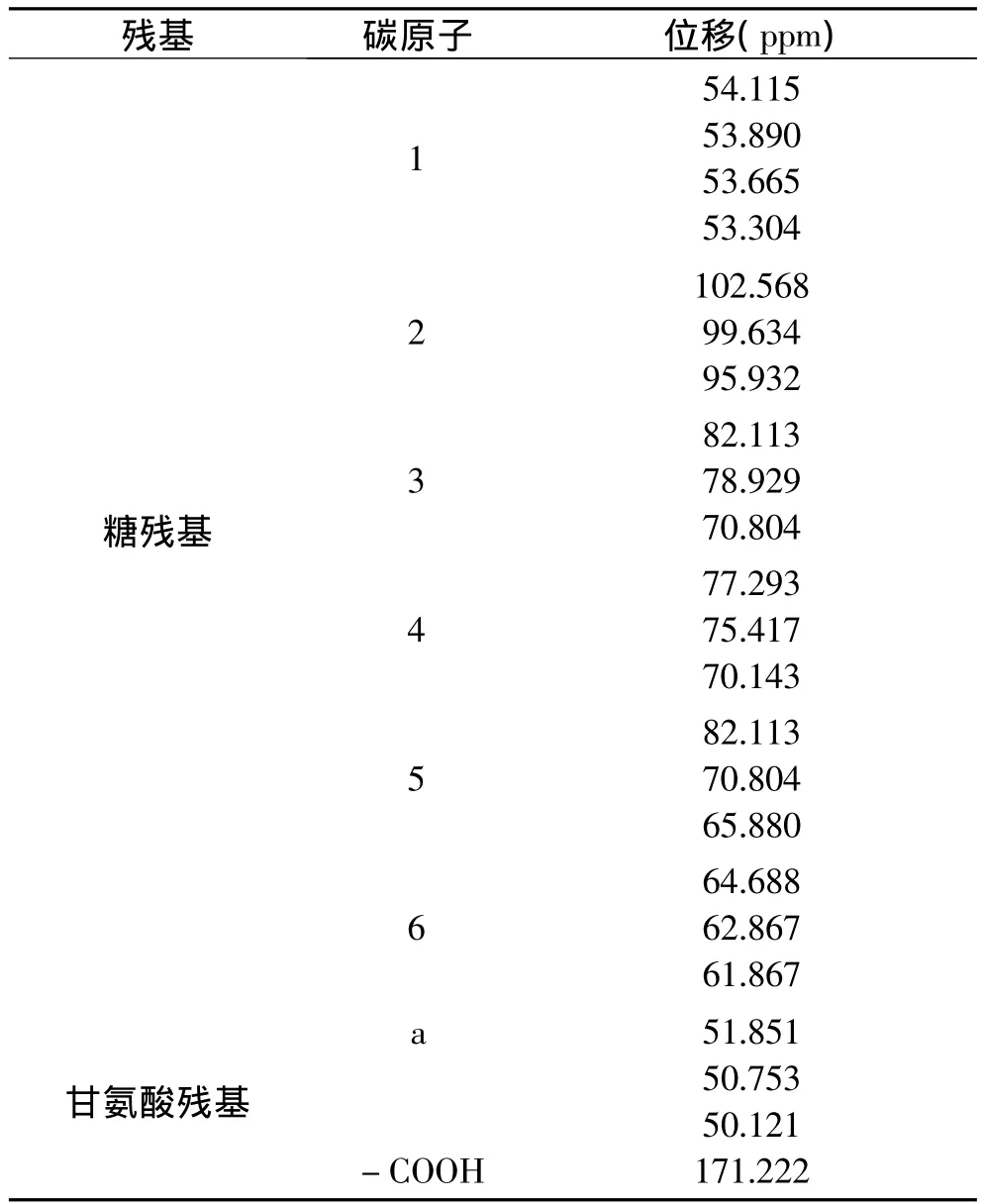
表2 DFG碳谱化学位移Table 2 13C-N.M.R chemical shifts
溶液中Cu2+、Ni2+能形成配位数为4或6的配合物,DFG与甘氨酸类似,作为二齿配体可通过氧原子和氮原子与金属离子配位而形成配合物,故限制了金属离子最多只能与2个或3个DFG配位。经计算DFG与Cu2+配合物稳定常数的对数值分别为lgK1= 7.24±0.09,lgK2=6.57±0.05,lgK3=3.31±0.02,DFG与Ni2+配合物稳定常数的对数值分别为lgK1=5.73 ±0.03,lgK2=4.69±0.02,lgK3=3.59±0.05。由以上数据可知,DFG对Cu2+的配位能力比对Ni2+的配位能力强,形成相应配合物DFG合铜的稳定性也比DFG合镍的稳定性高。
3 结论
以葡萄糖和甘氨酸为原料合成Maillard反应的初级阶段反应产物——果糖基甘氨酸(DFG),并用阳离子交换树脂分离纯化,利用离子色谱、质谱、核磁共振等方法分析其结构及纯度,证明所得产物为目标化合物,并得出如下结果:外观为白色晶体,无味,极易溶于水,分子式为C8H15NO7,相对分子质量237。该方法操作简便,使用原料及试剂价格低廉,而且可得到纯度较好的产品。pH电位滴定法测得DFG对Cu2+的配位能力大于对Ni2+的配位能力,且DFG合铜配合物稳定性大于DFG合镍配合物稳定性,为针对螯合剂筛选金属离子,拓宽果糖基甘氨酸的应用领域提供了一定的理论依据。

图5 滴定曲线Fig.5 pH-Titration curves
[1]Ledl F,Schleicher E.New aspects of the Maillard reaction in foods and in the human body[J].Angew Chem,1990,29: 565-594.
[2]Yaylayan V A,Huyghues D A.Chemistry of Amadori rearrangement products:analysis,synthesis,kinetics,reactions and spectroscopic properties[J].Crit ReV Food Sci Nutr,1994,34: 321-369.
[3]Silván J M,Lagemaat J,Olano A.Analysis and biological properties of amino acid derivates formed by Maillard reaction in foods[J].Journal of Pharmaceutical and Biomedical Analysis,2006,41:1543-1551.
[4]刘立全,王月霞.梅拉德反应在烟草增香中的应用研究进展[J].烟草科技,1994(6):21-24.
[5]O’Brien J,Morrissey P A.Metal ion complexation by products of Maillard reaction[J].Food Chemistry,1996,58(1-2):17-27.
[6]Mossine V,Thomas P.Nα-(1-Deoxy-D-fructos-1-yl)-L-histidine(“D-Fructose-L-histidine”):a Potent Copper Chelator from Tomato Powder[J].J Agric Food Chem,2007,55:10373-10381.
[7]Gyurcsik B,Gajda T,Nagy L,et al.Proton,copper(II)and nickel(II)complexes of some Amadori rearrangement products of D-glucose and amino acids[J].Inorganica Chimica Acta,1993,214:57-66.
[8]Eybl V,Kotyzová D,Koutensky J,et al.Effect of cadmium chelating agents on organ cadmium and trace element levels in mice[J].Analyst,1998,123:25-26.
[9]Abrams A,Lowy P H,Borsook H.Preparation of 1-Amino-1-deoxy-2-ketohexoses from Aldohexoses and α-Amino Acids[J].J Am Chem Soc,1955,77(18):4794-4796.
[10]Staempfli A A,Blank I,Fumeaux R,et al.Study on the decomposition of the amadori compound N-(1-deoxy-D-fructos-1-yl)-glycine in model systems Quantification by fast atom bombardment tandem mass spectrometry[J].Biological Mass Spectrometry,1994,23(10):642-646.
[11]Bjerrum J.Metal ammine formation in aqueous solution[J]. Theory of the Reversible Step Reactions,1957(26):296.
[12]苏小宝,戴丽君,陈少平,等.黑荆树单宁与金属离子络合性质的研究[J].林产化学与工业,2007,27(4):37-41.
[13]张云.计算滴定分析法的理论及应用[M].科学出版社,2010:210-216.
[14]Kenjiro R,Nagatoshi I,Hiromichi M,et al.Nα-(1-Deoxy-D-fructos-1-yl)-L-arginine,an antioxidant compound identified in aged garlic extract[J].The Journal of Nutrition,2001,131:972S-976S.
[15]Davidek T,Blank I K,Kraehenbuehl J,et al.New approaches in the analysis of amadori compounds[J].State-of-the-Art in Flavour Chemistry and Biology,2005,91-97.
[16]Davidek T,Clety N,Devaud S P,et al.Simultaneous quantitative analysis of Maillard reaction precursors and products by high-performance anion exchange chromatography[J].J Agric Food Chem,2003,51:7259-7265.
[17]Davidek T,Clety N,Aubin S,et al.Degradation of the amadori compound N-(1-Deoxy-D-fructos-1-yl)glycine in aqueous model systems[J].J Agric Food Chem,2002,50:5472-5479.
Synthesis of N-(1-deoxy-D-fructos-1-yl)-glycine(DFG) and its coordination properties to Cu(Ⅱ),Ni(Ⅱ)
XUE Xiao-li,WANG Zhong-he,YU Shu-juan*(College of Light Industry and Food Sciences,South China University of Technology,Guangzhou 510640,China)
N-(1-deoxy-D-fructos-1-yl)-glycine(DFG)was synthesized and purified,which was believed to be the key intermediate in the early stages of the model for the glucose/glycine Maillard reaction.Thin layer chromatography,ion chromatography,mass spectrometry and13C nuclear magnetic resonance were used to analyze and verify the desired product.The results indicated that C8H15NO7was DFG’s molecular formula with relative molecular mass of 237.DFG’s protonation constants and metal-complex stability constants with Cu2+,Ni2+ions were determined by pH potentiometric titration under(303±0.1)K in ionic strength I=0.1mol/L NaCl solution. Stability constants of DFG complexed with Cu2+were lgK1=7.24±0.09,lgK2=6.57±0.05,lgK3=3.31±0.02,respectively,which were higher than stability constants of DFG complexed with Ni2+(lgK1=5.73±0.03,lgK2=4.69 ±0.02,lgK3=3.59±0.05).
Maillard reaction;N-(1-deoxy-D-fructos-1-yl)-glycine(DFG);coordination properties;Cu(Ⅱ);Ni (Ⅱ)
TS201.2
A
1002-0306(2012)08-0121-04
2011-06-30 *通讯联系人
薛晓丽(1986-),女,硕士研究生,研究方向:食品化学。
广东省自然科学基金(10251064101000014);华南理工大学基本科研业务费(2011ZP009);粤港关键领域重点突破项目(2009A020700007)。
