紫甘薯花色苷酶法提取及纯化
2012-10-27汤海宾申京宇
鲍 诚,李 玲,汤海宾,申京宇,*
(1.烟台大学生命科学院,山东 烟台 264005;2.威海亿晶原果蔬有限公司,山东 威海 264400)
紫甘薯花色苷酶法提取及纯化
鲍 诚1,李 玲1,汤海宾2,申京宇1,*
(1.烟台大学生命科学院,山东 烟台 264005;2.威海亿晶原果蔬有限公司,山东 威海 264400)
研究酶法提取紫甘薯花色苷的工艺条件。通过单因素和正交试验,探讨酶解温度、pH值、料液比、酶用量对花色苷提取率的影向,确定最佳提取工艺。结果表明,最佳提取工艺为温度50℃、pH5.5、料液比1:15、α-淀粉酶用量0.25%、果胶酶用量0.10%。利用AB-8型大孔树脂,在吸附液pH2、流速为1mL/min时,吸附质量浓度为26.57mg/100mL;用pH3、60%乙醇溶液为解吸液,流速为2mL/min的条件下解吸,紫甘薯花色苷得率2.71mg/g,色价为43.2。
紫甘薯花色苷;酶法提取;α-淀粉酶;果胶酶;大孔树脂;纯化
紫甘薯(Ipomoes batatasL.)属旋花科一年或多年生草本植物,其肉色呈紫或深紫色,故称为紫甘薯,又称为紫心甘薯、紫薯、山川紫等[1]。它除具有普通甘薯的营养成分外,还富含花色苷等生物活性成分[2]。由于紫甘薯的花色苷含量很高,常作为提取天然花色苷的主要原料。紫甘薯花色苷的提取常用水提法、酸化水提法和酸化乙醇提法[3-4]。酶法提取紫甘薯花色苷的研究甚少,一般采用纤维素酶[5]或果胶酶[6]等单一酶提取方法,本实验选取α-淀粉酶和果胶酶进行双酶法提取工艺研究,旨在更有效地破坏细胞壁和细胞膜,使存在于液泡内的花色苷能扩散至溶剂中,提高花色苷的得率[6]。酶法提取的花色苷粗提液中含有糖、蛋白质等杂质,极大地影响了花色苷的品质和稳定性[7],需对其进行纯化。本实验选用大孔树脂对紫甘薯花色苷进行纯化最终得到较高色价的紫甘薯花色苷。
1 材料与方法
1.1 材料与试剂
紫甘薯 威海亿晶原果蔬有限公司;α-淀粉酶(2000U/g) 北京奥博星生物技术有限责任公司;酸性果胶酶(4000U/mL) 帝斯曼食品有限公司;AB-8大孔树脂上海蓝季科技发展有限公司。
1.2 仪器与设备
RE-52A型旋转蒸发器 上海亚荣生化仪器厂;JENCO 6173型酸度计 上海任氏电子有限公司;TU-1900双光束紫外-可见分光光度计 北京普析通用仪器有限责任公司;HH-4型数显恒温水浴锅 国华电器有限公司;7312-Ⅰ型电动搅拌机 上海标本模型厂;DD-5M低速离心机 长沙湘仪离心机仪器有限公司。
1.3 方法
1.3.1 紫甘薯花色苷提取工艺
紫甘薯解冻后,削皮、擦丝,于护色液(0.15%异VC钠,0.45%柠檬酸溶液)中护色40min,在护色液中糊化(80℃、5min)后打浆,调至酶解所需pH值,加入α-淀粉酶,电动搅拌辅助酶解1h后,加入果胶酶继续酶解2h,酶解液4000r/min离心30min后,抽滤取上清液,于90℃灭酶10min,冷却后调至pH3,得花色苷初提液。
对α-淀粉酶和果胶酶的用量、酶解温度、p H值、料液比等因素进行单因素试验,根据单因素试验结果进行4因素3水平的正交试验,以确定最佳提取工艺。
1.3.2 紫甘薯花色苷的纯化
参照岳静[8]和王智勇[9]的方法,对纯化条件进行优化,得到最佳吸附液质量浓度及pH值、最佳解析液浓度及pH值。将适量AB-8大孔树脂装入3cm×30cm层析柱,将粗提液浓缩至最佳吸附质量浓度26.57mg/100mL、酸度调节至最佳吸附酸度条件pH2.0,以1mL/min速度上样,解析前用pH3的柠檬酸-柠檬酸钠缓冲液洗去极性较大的杂质成分[10-11],用pH3、60%乙醇溶液,以2mL/min流速进行解吸,解吸液经浓缩后得到紫甘薯花色苷浓缩液。
1.3.3 色价测定方法
参照杨朝霞[12]的色价测定方法,计算色价。

式中:A为吸光度;m为样品质量/g;k为稀释倍数。
1.3.4 总糖及还原糖的测定方法
参照国标GB 6194—1986《水果、蔬菜可溶性糖测定法》方法测定总糖和还原糖的含量。
1.3.5 花色苷含量的测定
参照王智勇[9]的方法,采用苋菜红作为对照品,在525nm波长处测定吸光度(A),按下列公式计算紫甘薯花色苷的含量和得率。

式中:C为花色苷含量/(μg/mL);V为样液总体积/mL;m为紫甘薯取样量/g。
2 结果与分析
2.1 最佳提取工艺单因素试验
2.1.1α-淀粉酶用量对紫甘薯花色苷得率的影响
取50g紫甘薯在料液比1:5、酶解温度45℃、α-淀粉酶0.1%~0.35%、果胶酶0.15%、酶解pH5的条件下,按1.3.1节所述工艺进行提取。由图1可知,花色苷得率随α-淀粉酶用量的增加而增加,α-淀粉酶用量达到0.3%时,得率达到最高。随后得率急剧下降,可能是由于过量的α-淀粉酶虽然分解包裹色素的淀粉,使色素游离出来;但同时也分解了保护色素的糊精类物质,降低了色素的稳定性,使色素含量降低[13]。故选择0.3%为最佳α-淀粉酶用量。

图1 α-淀粉酶用量对紫甘薯花色苷得率的影响Fig. 1 Effect of α-amylase dosage on extraction rate of purple sweet potato anthocyanins
2.1.2 果胶酶用量对紫甘薯花色苷得率的影响
取50g紫甘薯在料液比1:5、酶解温度45℃、α-淀粉酶0.3%、果胶酶0.05%~0.25%、酶解pH5的条件下,按1.3.1节所述工艺进行提取。由图2可知,花色苷得率随果胶酶用量的增加而提高,到果胶酶用量达到0.15%时,得率达到最大。随后得率明显下降,是由于过量的果胶酶虽然能破坏细胞壁,促进花色苷暴露并与提取溶剂接触,但同时也让部分原来被包裹的可溶性成分如果胶等物质溶出,增加对花色苷的包裹,结果使得率降低[14]。因此,选择0.15%为最佳果胶酶用量。

图2 果胶酶用量对紫甘薯花色苷得率的影响Fig.2 Effect of pectinase dosage on extraction rate of purple sweet potato anthocyanins
2.1.3 料液比对紫甘薯花色苷得率的影响
取50g紫甘薯在料液比1:5~1:25,酶解温度45℃、α-淀粉酶0.3%、果胶酶0.15%、酶解pH5条件下,按1.3.1节所述工艺进行提取。由图3可知,花色苷得率随提取液体积的增加而增大,料液比1:15时达到最高,随后提取液体积增加到1:20和1:25时,得率急剧下降。故选择1:15为最佳料液比。

图3 料液比对紫甘薯花色苷得率的影响Fig.3 Effect of solid-to-solvent ratio on extraction rate of purple sweet potato anthocyanins
2.1.4 酶解温度对紫甘薯花色苷得率的影响
取50g紫甘薯在料液比为1:15,酶解温度40~60℃、α-淀粉酶0.3%、果胶酶0.15%、酶解pH5条件下,按1.3.1节所述工艺进行提取。实验中使用的α-淀粉酶最适温度为50~70℃,果胶酶为40~55℃。由图4可知,由于在较低温度条件下两种酶活力未完全激活,酶反应不充分而导致花色苷得率较低,当温度升高到45℃时,酶反应速度加快而花色苷的得率有了明显的提高。但是,温度达到50℃时,得率反而降低,这主要是由于此时α-淀粉酶的反应能力较弱的原因之外,花色苷结构随温度的升高,向无色的查尔酮和甲醇假碱式结构转化而引起的[15]。在55℃时,得率有所反弹,可能是由于α-淀粉酶和果胶酶的反应加速而引起的。温度达到60℃时,得率显著下降,是除了果胶酶的反应能力降低因素外,温度对花色苷结构稳定性的影响增加,大量花色苷转化为不可逆的查尔酮无色结构而造成的[15]。故选择45℃为最佳酶解温度。

图4 酶解温度对紫甘薯花色苷得率的影响Fig.4 Effect of hydrolysis temperature on extraction rate of purple sweet potato anthocyanins
2.1.5 酶解pH值对紫甘薯花色苷得率的影响
取50g紫甘薯在料液比1:15,酶解温度45℃、α-淀粉酶0.3%、果胶酶0.15%、酶解pH3.5~6.0的条件下,按1.3.1节所述工艺进行提取。由图5可知,由于实验用的α-淀粉酶最适pH5.5~7.5,果胶酶最适pH4.0~5.5。为此,在pH4.0~5.5范围内,花色苷得率较pH3.5和pH6.0时明显提高。但是,由于花色苷在pH4~6时,主要以无色的甲醇假碱和查尔酮假碱形式存在,就直接应影响了花色苷的得率[15]。当pH5.5时,花色苷得率突然反弹,可能是α-淀粉酶的反应速度加快起了主要作用而引起的。pH值提高到6.0时,得率显著下降是由于果胶酶活力丧失和花色苷本身结构的转化等因素综合引起的。故选择pH4为最佳酶解pH值。
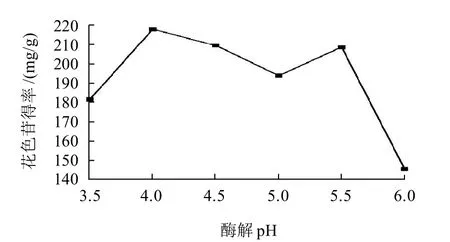
图5 酶解pH对紫甘薯得率的影响Fig.5 Effect of hydrolysis pH on extraction rate of purple sweet potato anthocyanins
2.2 提取工艺条件正交试验优化
在单因素试验的基础上,进行L9(34)正交试验优化提取工艺条件。
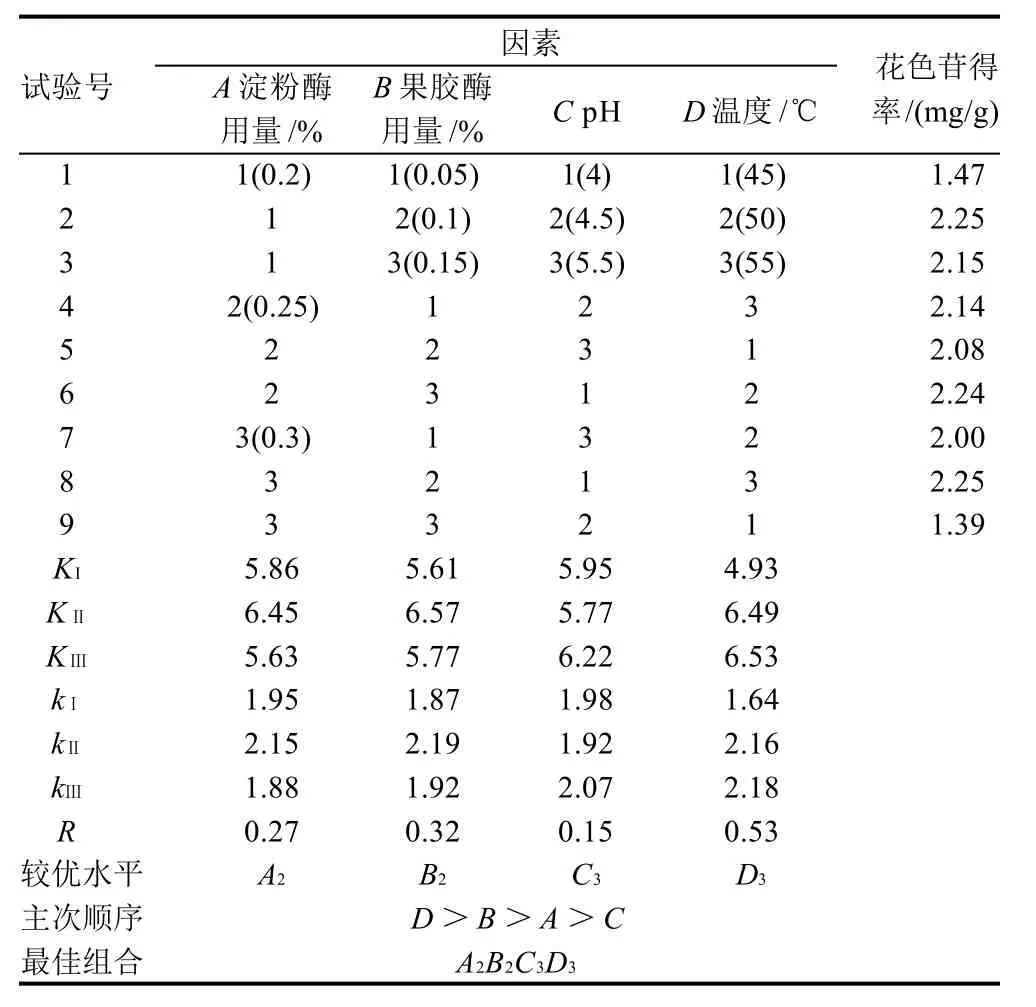
表1 酶法提取紫甘薯花色苷正交试验设计及结果Table 1 Orthogonal array design and corresponding experimental results for optimizing enzymatic extraction of purple sweet potato anthocyanins
由表1可知,紫甘薯花色苷最佳提取条件为α-淀粉酶用量0.25%、果胶酶用量0.1%、酶解pH5.5、酶解温度55℃。其中最大影响因素为酶解温度,其次是果胶酶,再次是α-淀粉酶,pH值影响相对较小。
通过SPSS 10.0对正交试验结果进行方差分析,结果见表2。

表2 正交试验方差分析Table 2 Variance analysis of the experimental results of orthogonal array design
由表2可见,4因素对试验均有显著影响,影响顺序与表1相同。结合Duncan多重比较发现,酶解温度50℃和55℃条件下,花色苷提取率无显著性差异。考虑到过高温度对花色苷有一定的破坏作用,最终确定酶解温度50℃(D2)为最佳提取温度,即最佳提取工艺为A2B2C3D2。该提取工艺得到的花色苷得率理论值为2.58mg/g,95%置信区间为(2.58±0.13)mg/g。取250g紫甘薯用最佳提取工艺进行3次平行实验,花色苷得率平均值为2.49mg/g,经验证实验最终确定提取工艺为A2B2C3D2。
2.3 花色苷粗提液的纯化
在最佳工艺条件下提取的花色苷粗提液,花色苷得率为2.49mg/g,总糖含量为8.60g/100g,还原糖含量为5.71g/100g;Daravingas在研究中发现糖及其降解产物均能引起花色苷的降解[16],通过最佳纯化工艺纯化后,糖含量显著降低,总糖含量为0.18g/100g,还原糖含量为0.07g/100g,保证了花色苷的品质。纯化后花色苷得率为2.71mg/g,色价达到43.2。
3 结 论
通过双酶法提取的紫甘薯花色苷含量比韩永斌等[6]利用果胶酶和α-淀粉酶单一酶法提取的紫甘薯花色苷含量明显高。双酶法可提高花色苷的提取率,且操作简单,经济高效,对多种酶提取紫甘薯花色苷提供了一定的理论基础。本实验利用两种酶提取紫甘薯花色苷,得到最佳工艺为温度50℃、pH5.5、料液比1:15、α-淀粉酶用量0.25%、果胶酶用量0.10%。有关两种酶之间相互作用和影响及其机理,有待于进一步深入研究。
[1] 陆国权, 邱永军. 紫心甘薯红色素提取技术研究[J]. 天然产物研究与开发, 1997, 23(1): 105-107.
[2] CLIFFORD M N. Anthocyanins-nature occurrence and dietary burden[J]. Journal of the Science of Food and Agriculture, 2000, 80(7): 1063-1072.
[3] 陆国权, 史峰, 邬建敏, 等. 紫心甘薯花青苷的提取和纯化及其组分分析[J]. 天然产物研究与开发, 1997, 9(3): 48-51.
[4] 吴巧玲. 紫心甘薯紫红色素的提取工艺研究进展[J]. 今日科技, 2003(6): 43-44.
[5] 李金林, 刘林勇, 徐宗财, 等. 生物酶法提取紫甘薯花色苷的研究[J].江西食品工业, 2009(4): 25-27.
[6] 韩永斌. 紫甘薯花色苷提取工艺与组分分析及其稳定性和抗氧化性研究[D]. 南京: 南京农业大学, 2007.
[7] LEE L S, RHIM J W, KIM S J, et al. Study on the stability of anthocyanin pigment extracted from purple sweet potato[J]. Korean Journal of Science and Technology, 1996, 28(2): 352-359
[8] 岳静. 紫甘薯红色素的制备及生物学活性研究[D]. 大连: 辽宁师范大学, 2004.
[9] 王智勇. 紫甘薯色素提取纯化工艺及性质研究[D]. 重庆: 西南大学,2008.
[10] MATSUI Y, EBUCHI S, FUKUI K, et al. Anti-hyperglycemic effect of diacylated anthocyanin derived fromIpomoea batatasL. cultivar Ayamurasaki can be achieved through the alpha-glucosidase inhibitory action[J]. Agric Food Chem, 2002, 50(25): 7244-7248.
[11] 赵晟锌, 徐雅琴, 李兴国, 等. 大孔吸附树脂纯化黑穗醋栗花色苷研究[J]. 东北农业大学学报, 2010(8): 37-40.
[12] 杨朝霞. 紫甘薯花色苷提取纯化工艺研究及组分分析[D]. 青岛: 青岛大学, 2004.
[13] 连喜军, 陈良笛, 王咙, 等. 酶法水解甘薯提取三种紫甘薯色素[J].粮食与油脂, 2008(1): 19-23.
[14] 李金林. 紫甘薯花色苷提取、膜分离及加工稳定性研究[D]. 南昌:南昌大学, 2007.
[15] 花色苷的结构稳定性与降解机制研究进展[J]. 中国农业科学, 2009,43(1): 996-1008.
[16] DARAVINGAS G, CAIN R F. Thermal degradation of black raspberry anthocyanin pigments in model systems[J]. Journal of Food Science,1968, 33(2): 138-142.
Enzymatic Extraction and Purification of Anthocyanins from Purple Sweet Potato
BAO Cheng1,LI Ling1,TANG Hai-bin2,SHEN Jing-yu1,*
(1. School of Life Sciences, Yaitai University, Yantai 264005, China;2. Weihai Yijingyuan Fruits and Vegtables Co. Ltd., Weihai 264400, China)
The enzymatic hydrolysis of purple sweet potato was investigated for anthocyanin extraction. The effects of extraction temperature, pH, solid-to-solvent ratio, and enzyme amount on extraction rate of anthocyanins were explored by onefactor-at-a-time and orthogonal array design methods. The best extraction results were achieved by adding 0.25%α-amylase and 0.1% pectinase for hydrolysis at pH 5.5, 50 ℃, and a solid-to-solvent ratio of 1:15. The extract was adjusted to pH 2 and a concentration of 26.57 mg/100 mL for adsorption by AB-8 macro-porous resin at a flow rate of 1 mL/min and subsequent desoroption with 60% acidic ethanol solution at pH 3. Under these conditions, the extraction rate of anthocyanins was 2.71 mg/g, and the color value of the purified anthocyanins was 43.2.
purple sweet potato anthocyanins;enzymatic extraction;α-amylase;pectinase;macro-porous resins;purification
TS246.4
A
1002-6630(2012)16-0059-04
2011-07-03
鲍诚(1986—),女,硕士研究生,研究方向为食品加工与安全。E-mail:zihencc1319@163.com
*通信作者:申京宇(1965—),男,副教授,博士,研究方向为功能食品加工、食品安全。E-mail:jyshen119@163.com
