不同无机盐对二醇型人参皂苷分纯效果的影响
2012-10-26邓小莉常景玲宁晓明吴羽晨
邓小莉,常景玲,宁晓明,吴羽晨
(1.河南科技学院,河南新乡 453003;2.新乡学院,河南新乡 453003)
不同无机盐对二醇型人参皂苷分纯效果的影响
邓小莉2,常景玲1,*,宁晓明1,吴羽晨1
(1.河南科技学院,河南新乡 453003;2.新乡学院,河南新乡 453003)
研究了二醇型人参皂苷在NaCl、KCl、CaCl2、MgCl2等不同无机盐溶液中的溶解度,采用萃取方法分离二醇型人参皂苷,经高效液相色谱检测,确定了二醇型人参皂苷提纯所需的最佳无机盐及浓度。结果显示采用丙酮-5%CaCl2盐溶液(体积比6∶1)溶剂系统,萃取分离效果最好,其最高得率可达93%。
二醇型人参皂苷,无机盐,高效液相色谱检测
人参皂苷(Ginsenoside)是人参的主要有效成分[1-4],是固醇类化合物的一种。依据皂苷元的不同,可将皂苷分为二醇型和三醇型人参皂苷。两类皂苷经加工可以转化为稀有皂苷。如Ra1、Ra2、Rb1、Rb2、Rc、Rd、Rg3和Rh2等属于二醇型稀有皂苷;Re、Rf、Rg1、Rg2和Rh1等属于三醇型稀有皂苷。稀有皂苷的药用价值远高于普通皂苷[1,5]。研究证明[6-8],人参皂苷Rg3具有抑制肿瘤细胞增殖浸润、对抗肿瘤细胞转移、促进肿瘤细胞凋亡、提高机体免疫力等作用;人参皂苷Rh1、Rh2具有较强的抗癌作用,其中Rh2抗肿瘤作用最强。由于在自然界中稀有皂苷的含量甚微,从天然人参中提取又非常困难[9-12]。因此有必要分离总人参皂苷中的二醇型和三醇型皂苷单体,以提高稀有皂苷的转化和利用[13-15]。目前,已有的皂苷分离方法均存在操作复杂、成本较高、分离不彻底等缺陷。由于无机盐溶液能够改变二醇型人参皂苷各单体在水相中的溶解度。因此,本实验根据二醇型人参皂苷在不同无机盐溶液中的溶解度,采用相关溶剂系统研究其萃取方法,确定了二醇型人参皂苷提纯所需的最佳无机盐及浓度。
1 材料与方法
1.1 材料与仪器
二醇型人参皂苷标准品Rb1、Rc、Rd、Rg3、Rh2由成都曼斯特公司提供;甲醇、乙醇、氯化钙、丙酮、正丙醇、异丙醇、异戊醇 均为分析纯,北京化工厂;乙腈、磷酸、甲醇 均为色谱纯,上海陆忠化工试剂厂;人参总皂苷 中国药品生物制品检定所提供。
LC-2010C型高效液相色谱仪 日本岛津;BL610电子精密天平 Sartorius;HH.W 21.600型电热恒温水温箱 北京市光明医疗器械厂;SHZ-III循环水真空泵 上海亚荣生化仪器厂;KQ-600E型超声波破碎仪 昆山市超声仪器有限公司。
1.2 实验方法
1.2.1 标准曲线的制作 精确量取适量Rb1、Rc、Rd、Rg3、CK和Rh2标准品溶液,混合后依次梯度稀释。稀释后的Rb1、Rc、Rd、Rg3、CK和Rh2浓度见表1。
1.2.2 溶液的配制
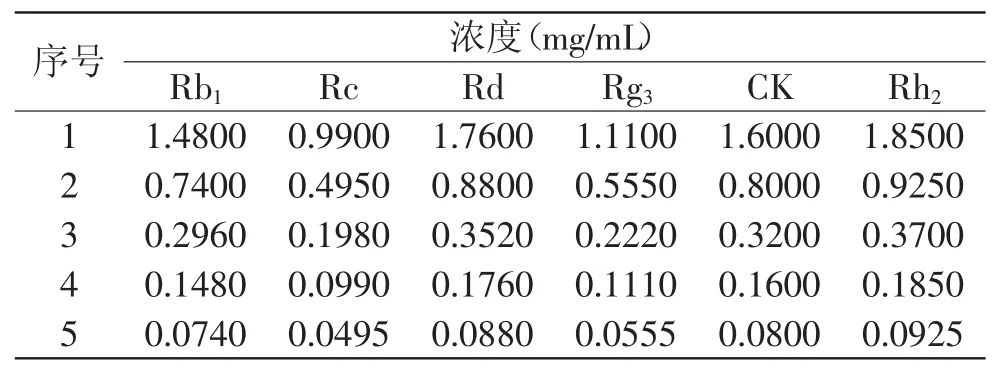
表1 人参皂苷不同稀释浓度Table 1 Different dilution concentration of six ginsenosides
1.2.2.1 无机盐溶液的配制[10]将无机盐NaCl、KCl、CaCl2、MgCl2由最低浓度至饱和浓度配制出均匀的5个梯度,每种标准量为10m L。现用现配或密封保存,防止发生吸水导致浓度变化。
1.2.2.2 皂苷溶液的制备 分别取1.2.2.1配制好的各浓度盐溶液5m L在40℃恒温水浴锅中加热,5m in后,将称好的4g皂苷加入盐溶液中搅拌至完全溶解待用。
1.2.2.3 95%色谱级甲醇的预处理 大于99%的色谱级甲醇和双蒸水分别经0.45μm纤维过滤膜过滤,取5m L双蒸水于容量瓶用甲醇定容至100m L。
1.2.3 分离过程
1.2.3.1 萃取 将1.2.2.2处理好的皂苷溶液稍冷却后加入丙酮35m L,在超声辅助下萃取,静置分层。
1.2.3.2 重复萃取 根据二醇型、三醇型皂苷的性质,上层有机相含三醇型皂苷,收集备用,下层水相含二醇型皂苷。在含二醇型皂苷的水相中加入2.5m L无机盐溶液搅拌溶解后,再加入丙酮15m L搅拌,静置分层。重复上述操作5次,合并下层水相,合并上层有机相。
1.2.3.3 干燥 将萃取分离的二醇型皂苷60℃烘干,称量。
1.2.3.4 二醇型皂苷脱盐 取干燥好的二醇型皂苷样品溶解于20m L乙醇中,0.22μm膜过滤除盐,60℃烘干,称量。
1.2.4 高效液相色谱(HPLC)检测
1.2.4.1 样品液制备 取分离得到的二醇型皂苷样品0.01g,精密称定,于1m L 95%的甲醇中超声溶解,经0.22μm膜过滤于样品瓶中待测。
1.2.4.2 标准品溶液的配制 准确称取0.05g二醇型人参皂苷单体Rg3、Rb1、Rc、Rd、Rh2,分别于10m L容量瓶蒸馏水定容,准确吸取0.1m L上述皂苷单体溶液,于2m L容量瓶无水甲醇定容,0.45μm脂膜过滤。
1.2.4.3 高效液相色谱分析条件 色谱柱C184.6mm× 150mm,检测波长为203nm,进样量10μL,柱温35℃,流速1m L/m in。流动相梯度如下:0~22m in,乙腈(A)∶磷酸水(B)=34∶66;22.01~100min,乙腈(A)∶磷酸水(B)=43∶57,磷酸水浓度为5.88‰[12]。
2 结果与分析
2.1 人参皂苷Rb1、Rc、Rd、Rg3、CK和Rh2标准曲线HPLC检测色谱峰
根据图1结果,利用LC-Solution软件以测得的人参皂苷峰面积(Area)为横坐标X,浓度(Conc)为纵坐标Y,进行回归处理,得上述皂苷的回归方程。Rb1:Y= 3.295583e-007X,相关系数r=0.9996;Rc:Y=4.380841e-007X,r=0.9994;Rd:Y=3.105281e-007X,r=0.9991;Rg3:Y=2.235923e-007X,r=0.9994743;CK:Y=2.153659e-007X,r=0.9992;Rh2:Y=2.081828e-007X,r=0.9997。结果表明上述皂苷在相关范围内具有良好的线性关系。
利用LC-Solution软件制得上述六种人参皂苷的标准曲线,如图2所示。
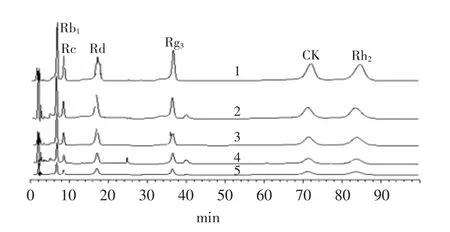
图1 人参皂苷不同稀释浓度的色谱图Fig.1 Chromatogram of different dilution concentration of six ginsenosides
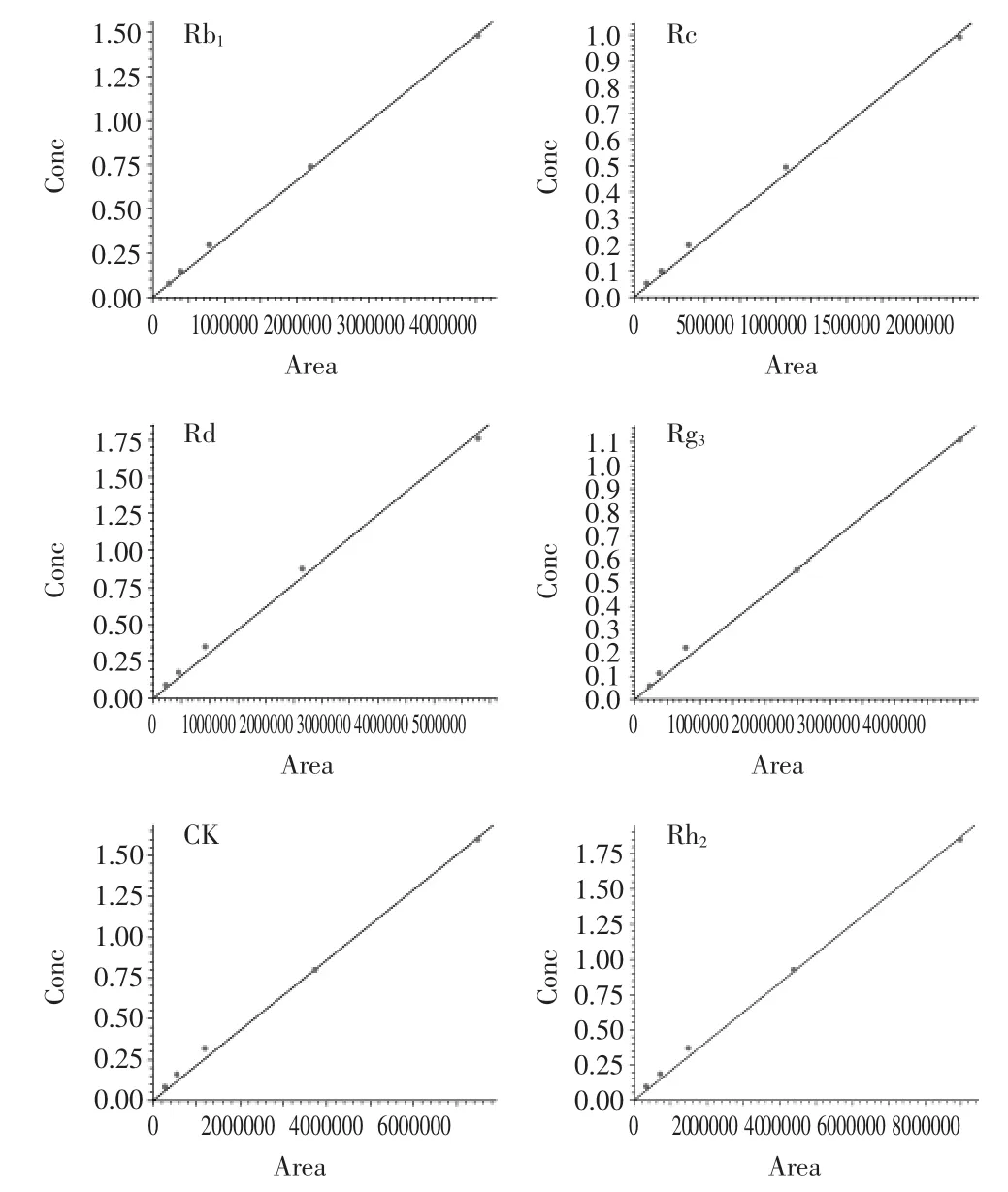
图2 人参皂苷Rb1、Rc、Rd、Rg3、CK、Rh2标准曲线Fig.2 The standard curves of ginsenoside Rb1,Rc,Rd,Rg3,CK and Rh2
2.2 不同无机盐分离效果的比较
NaCl、KCl、CaCl2、MgCl2各浓度分离二醇型人参皂苷单体的HPLC检测出峰时间见表2。无机盐分离效果最优浓度HPLC见图3。
由表2数据与标准品人参皂苷单体出峰时间对比可以看出:15%NaCl、25%KCl、40%MgCl2、5%CaCl2出峰时间与标准品人参皂苷单体的出峰时间相接近,依此可确定此浓度为各无机盐的最优浓度。由图3结果通过各峰值位置比较,四种无机盐中5% CaCl2的出峰时间与标准品最相近,且与标准品一样无杂峰。
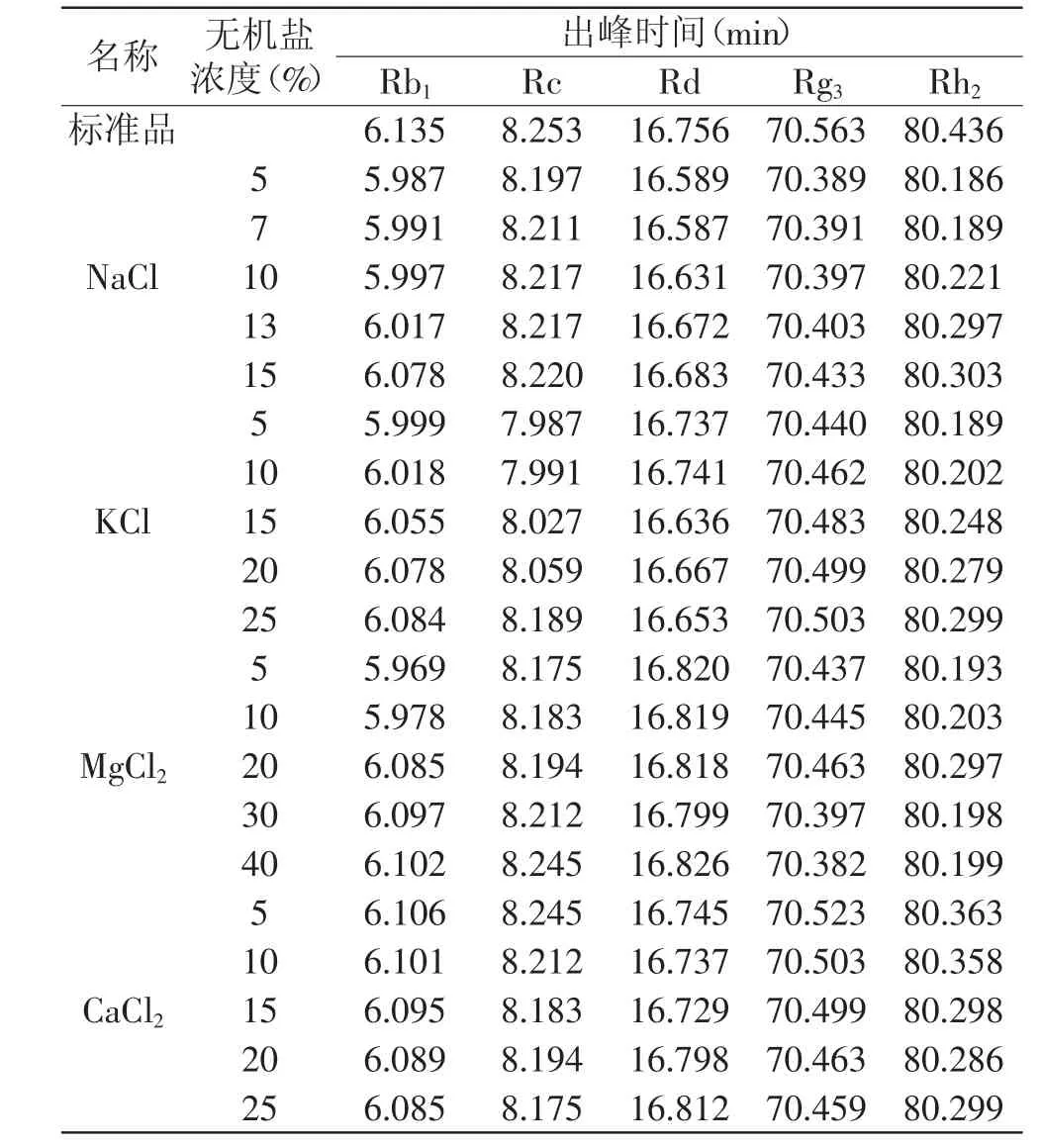
表2 不同无机盐分离得到的二醇型单体的出峰时间Table 2 Appearance time of panoxadiol type ginsenoside by separating different inorganic salts
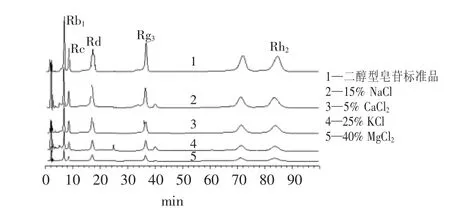
图3 不同无机盐最优浓度分离二醇型人参皂苷HPLC图Fig.3 HPLC of separating panoxadiol type ginsenoside by different inorganic salts
2.3 丙酮、5%CaCl2萃取二醇型人参皂苷HPLC
按丙酮∶5%CaCl2溶液=6∶1萃取二醇型人参皂苷粗品并进行HPLC检测,色谱图见图4。

图4 丙酮-5%CaCl2溶液萃取二醇型人参皂苷HPLC图Fig.4 The HPLC of purifying panoxadiol type ginsenoside by organic solvents 5%CaCl2 salt solution
由图4与标准品对比可知,5m in之前为杂峰。各主峰与标准品出峰时间基本一致,二醇型皂苷得到了很好分离。
根据LC-Solution软件制得的上述六种人参皂苷的标准曲线得二醇型皂苷含量见表3。
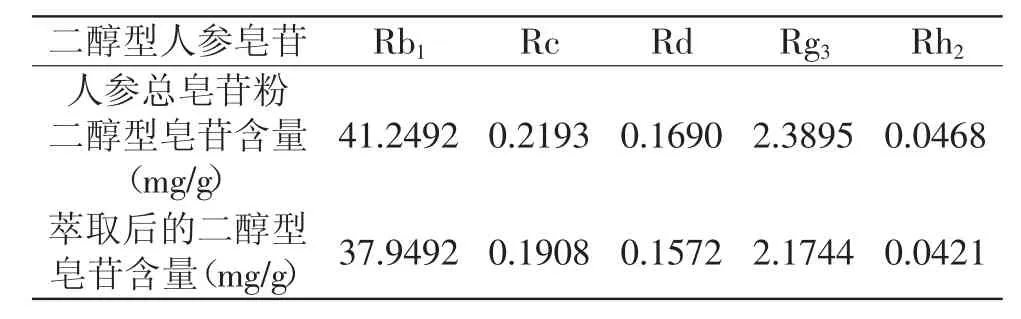
表3 丙酮-5%CaCl2溶液萃取二醇型人参皂苷含量Table 3 Different dilution concentration of five ginsenosides
由表3可知,丙酮-5%CaCl2溶液萃取的各单体含量与人参总皂苷粉各单体的含量接近,得率为87%~98%,最高得率可达98%。
3 结论与讨论
国内外对人参皂苷的功能研究非常多,分离提取总皂苷的方法也有大量研究,但分离纯化二醇型、三醇型人参皂苷的研究较少。由于稀有皂苷的药用价值和生理活性较高,稀有皂苷是从二醇型、三醇型皂苷加工转化获得的,因此对二醇型、三醇型人参皂苷的分离转化已成为当今研究热点。本研究通过对二醇型人参皂苷在NaCl、KCl、CaCl2、MgCl2不同盐浓度中的丙酮有机溶剂溶液萃取,确定了CaCl2盐溶液分离二醇型人参皂苷的用量和方法。
[1]医科院北京药物所.中药志[M].北京:人民卫生出版社,1997:20-23.
[2]张丹,鱼红闪,奥大介,等.高产人参皂苷β-葡萄糖苷酶菌种的筛选[J].大连轻工业学院学报,2000,19(3):195-198.
[3]王铁生.中国人参[M].沈阳:辽宁科学技术出版社,2001:671-695.
[4]J萨姆布鲁克,DW拉塞尔.分子克隆实验指南[M].黄培堂,译.第三版.北京:科学出版社,2002.
[5]杨其蕴.天然药物化学[M].北京:中国医药科技出版社,1996:180-184.
[6]薛丽莉,周海彤,李龙华,等.酶转化人参皂苷中间品Rg3皂苷的分析[J].大连轻工业学院学报,2007,26(1):1-4.
[7]Zhao Y.Advance in studies on anticarcinogenic effects of 20(R)-ginsenoside Rg3[J].Chin C lin Oncology,2001,6(1):812-821.
[8]李粱,卢明春,鱼红闪,等.从一种新筛选的菌中找出人参皂苷酶[J].大连轻工业学院学报,2003,22(3):164-166.
[9]沈萍,范秀容,李广武.微生物学实验[M].第三版.北京:高等教育出版社,2005:215.
[10]王秀奇,秦淑媛,高天慧,等.基础生物化学实验[M].第二版.北京:高等教育出版社,2005:18-277.
[11]发酵工程教研室.生物工程专业实验、实习指导[M].第三版.河南科技学院内部资料,2007:6-16.
[12]刘欣,崔昱,杨凌,等.蜗牛酶中一种人参皂苷Rb1水解酶的分离纯化[J].生物工程学报,2005,21(6):929-932.
[13]SyuichiS,Noriko K,Junzo S,etal.Studies in the ginsenoside of ginsengⅠ structures of ginsenoside Ro,Rb1,Rc,Rd[J].Chem Pharm Bull,1974,22(2):421-428.
[14]张丹.人参皂苷β-葡萄糖苷酶的分离纯化及其酶学特性[J].应用与环境生物学报,2003,9(3):259-262.
[15]Zhang C Z,Yu H S,Bao Y M,et al.Purification and characterization ofginsenoside-glucosidase from ginseng[J].Chem Pharm Bull,2001,49:795-798.
Effect of different inorganic salts on the purification of panoxadiol type ginsenoside
DENG Xiao-li2,CHANG Jing-ling1,*,NING Xiao-m ing1,WU Yu-chen1
(1.Henan Institute of Science and Technology,Xinxiang 453003,China;2.Xinxiang University,Xinxiang 453003,China)
The ob jectwas to determ ine the best inorganic salt and its concentration in purifying panoxad iol type ginsenoside.Different solubilities of panoxad iol type ginsenoside in different inorganic salt solutions were stud ied,inc lud ing NaCl,KCl,CaCl2and MgCl2.Panoxad iol type ginsenoside was separated through extraction. By using the high performance liquid chromatography test,best inorganic salt solution and its concentration were determ ined.The results showed that the best cond ition for extrac ting and separating panoxad iol type ginsenoside was the organic solvents acetone-5%CaCl2salt solution(v/v,6∶1).The highest yield was 93%.
panoxad iol type ginsenoside;inorganic salt;HPLC
TS201.1
B
1002-0306(2012)09-0260-04
2011-07-26 *通讯联系人
邓小莉(1962-),女,本科,副教授,研究方向:生物工程和生物活性物质。
河南省重点科技攻关项目(082102220001)。
