方波伏安法检测酱油和食盐中乙二胺四乙酸铁钠
2012-10-25霍军生
魏 峰,霍军生,狄 蕊,孙 静,*,黄 建
(1.黄山学院现代教育技术中心,安徽 黄山 245041;2.中国疾病预防控制中心营养与食品安全所,北京 100050)
方波伏安法检测酱油和食盐中乙二胺四乙酸铁钠
魏 峰1,霍军生2,狄 蕊1,孙 静2,*,黄 建2
(1.黄山学院现代教育技术中心,安徽 黄山 245041;2.中国疾病预防控制中心营养与食品安全所,北京 100050)
采用方波伏安法建立乙二胺四乙酸铁钠(NaFeEDTA)的检测方法。用pH值为3.0的磷酸缓冲溶液作为底液;电化学条件为扫描增量10mV、方波频率2.5kHz、方波振幅100mV,可实现对NaFeEDTA的检测。试液中NaFeEDTA的质量浓度在10~200mg/L范围内,标准曲线相关系数为0.9997,检出限为4mg/L。对铁强化酱油和食盐中的NaFeEDTA检测的回收率为(93.5±2.1)%和(96.8±2.8)%。
乙二胺四乙酸铁钠(NaFeEDTA);方波伏安法;铁强化酱油;铁强化食盐
乙二胺四乙酸铁钠(NaFeEDTA)作为一种络合型铁营养强化剂具有生物利用率高,食物感官影响小等特点[1],在我国食品行业应用已有十多年[2]。强化食品中NaFeEDTA的检测方法,是生产质量控制和强化食品推广、应用和质量监督的必要手段。检测食品中铁元素总量的如原子吸收法、溶出伏安法等,无法对NaFeEDTA和焦磷酸铁、硫酸亚铁等各种铁强化剂进行区分,无法用于对食品中NaFeEDTA的直接检测。目前,测定食品中NaFeEDTA含量的方法有直接紫外分光光度法[3-4]、可见分光光度法[5-7]、毛细管区带电泳法[7]、HPLC法[9-11]等仪器分析方法。其中,毛细管区带电泳法由于仪器较少而难以普及;HPLC法相对准确,但操作比较繁琐,速度较慢;而分光光度法容易受酱油等食品本底颜色的影响。
电化学分析法具有仪器装置简单、操作方便和选择性好等特点。Gonzalez[12]和Kenichi[13]等通过电化学方法对FeEDTA络合物的电化学性质进行了研究。Ugo1等[14]使用方波伏安法对在络合剂存在条件下的痕量铁进行了分析。李彦等[15]报道了用单扫示波极谱法测定酱油中NaFeEDTA的方法,该方法回收率为88.8%~112.0%,但使用的滴汞电极对环境严重污染。方波伏安法的灵敏度和分辨率比线性扫描方法都有进一步的提高[16],可在较低的电解质浓度和反应物浓度条件下进行峰电位、峰电流测量。本实验对NaFeEDTA的电化学行为进行考察,并以无污染的玻碳电极为检测电极,通过对电化学条件、底液条件和样品处理方法的考察,拟建立酱油、食盐等食品中NaFeEDTA的方波伏安检测方法。
1 材料与方法
1.1 材料、试剂与仪器
加碘食盐、酱油 市售。
NaFeEDTA·3H2O标准物 美国Sigma公司;铁标准储备液(1000mg/L) 国家钢铁研究总院分析测试研究所;硝酸、高氯酸为优级纯;其他试剂均为分析纯。实验用水为超纯水(电阻率18.2MΩ·cm)。
LK2006A型电化学工作站及电极 天津市兰力科化学电子公司;WFX-210型原子吸收光谱仪 北京瑞利公司;TGL-16C飞鸽牌离心机 上海安亭科学仪器厂;PHS-3C精密酸度计 上海精密科学仪器公司;固相萃取装置及3mL C18固相萃取柱 美国Waters公司。
1.2 方法
1.2.1 标准溶液的配制
向6支50mL容量瓶中分别加入0、0.5、1、2、5、10mL的质量浓度为1.00g/L的NaFeEDTA标准储备溶液,再向容量瓶中分别加入2mL pH3.0的0.5mol/L磷酸缓冲溶液和3mL的0.5mol/L的氯化钠溶液,定容到刻度,制成标准系列,备用。
1.2.2 酱油样品试液的制备
在酱油中加入NaFeEDTA,溶解,制成NaFeEDTA含量为2.00g/kg(铁含量为0.27g/kg)的铁强化酱油样品。将2mL上述铁强化酱油与2mL pH3.0 0.5mol/L磷酸缓冲溶液混合后,以10000r/min离心10min。取上清液进固相萃取柱(事先用3mL甲醇进行活化,再以5mL水冲洗),然后用5mL蒸馏水对萃取柱进行洗涤,将滤液与清洗液合并,移至5 0 m L容量瓶,定容,摇匀备用。
1.2.3 食盐样品试液的制备
在加碘食盐中加入N a F e E D T A混匀,制成含NaFeEDTA 7.54g/kg(铁含量为1.00g/kg)的铁强化食盐样品[4]。对该样品进行原子吸收实验测定总铁含量,显示其混合均匀度的变异系数小于2.0%(n=6)。准确称取0.5g上述铁强化食盐样品,加入50mL容量瓶中,再向容量瓶中加入2mL的pH值为3.0的0.5mol/L磷酸缓冲溶液,定容到刻度,备用。
1.2.4 方波伏安法检测
用玻碳电极作为工作电极,铂柱电极作为辅助电极,甘汞电极作为参比电极的三电极系统,进行方波伏安法检测。为保证每次实验的重复性,玻碳电极在使用前应先用0.05μm氧化铝粉末打磨抛光,然后依次在丙酮、100g/L NaOH溶液、1:1的HNO3溶液超声清洗3min,再用水超声清洗5min。在电解池中,加入测试液,通氮气除氧,并保持氮气气氛,扫描电位为0.4~-0.4V,扫描增量10mV,方波频率2.5kHz,方波振幅100mV,进行扫描,根据峰电流计算试样中NaFeEDTA的含量。
2 结果与分析
2.1 NaFeEDTA在玻碳电极上的电化学行为
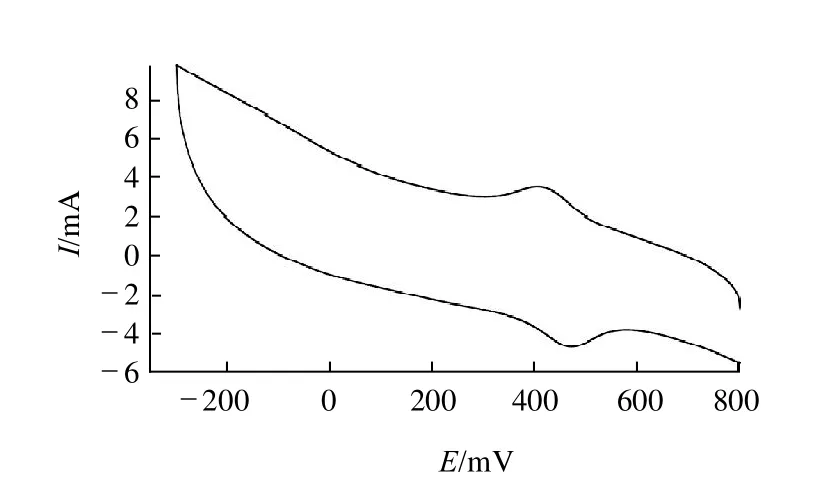
图1 NaFeEDTA的循环伏安谱图Fig.1 Cyclic voltammogram of NaFeEDTA
图1为200mg/L的NaFeEDTA标准溶液的循环伏安图,扫描速度为50mV/s。在pH3的溶液中,络合物主要以FeEDTA-形式存在。可以看出循环伏安曲线中,上部的曲线是由FeEDTA-反应生成FeEDTA2-时的还原峰,下部的曲线为氧化峰,两者的峰高基本相等。还原峰的峰电位为408mV,氧化峰的峰电位为468mV,两者之差为60mV。因此可以认为FeEDTA-在该条件下的氧化还原反应为可逆反应。Kenichi等[13]以pH2.2的氯乙酸缓冲溶液和pH4.5的乙酸缓冲溶液作为底液,进行循环伏安扫描,同样证实了此反应为可逆反应。
2.2 电化学检测条件的选择
方波伏安法电化学条件的频率和振幅均会影响方波峰电流的大小和形状。通过实验可以观察出,扫描过程施加的电压的方波频率对峰高影响明显。当其他条件不变时,改变方波频率分别为1、2.5、5kHz时,峰高分别为6.2、7.3、8.3mA,但方波频率为5kHz时基线发生严重倾斜,不便于准确读数。因此本实验选择方波频率为2.5kHz。
方波振幅是施加的方波电压的波动幅度,增大方波振幅时,峰的宽度和高度都变大。为提高检测灵敏度,本实验设置方波幅度为100mV。此时NaFeEDTA的峰宽约为400mV。
扫描增量所控制的是扫描过程中采样点的多少。扫描增量小,会使采样点增加,但所需的时间较长。如果设置较大的扫描增量,则采样点较少,曲线绘制不准确。本研究将其设置为10mV,整个峰形有40个左右的数据点,扫描过程可以在1min内完成。
图2为方波频率2.5kHz、方波幅度100mV、扫描增量10mV时,100mg/L的NaFeEDTA标准溶液的循环方波伏安曲线。可知还原峰和氧化峰的峰电压均在20~-20mV范围内,且二者峰电流接近1:1,峰形对称,且基线较平,在附近没有其他干扰。还原曲线的基线比较平缓,因此本研究采用还原峰的峰电流进行NaFeEDTA的定量分析。
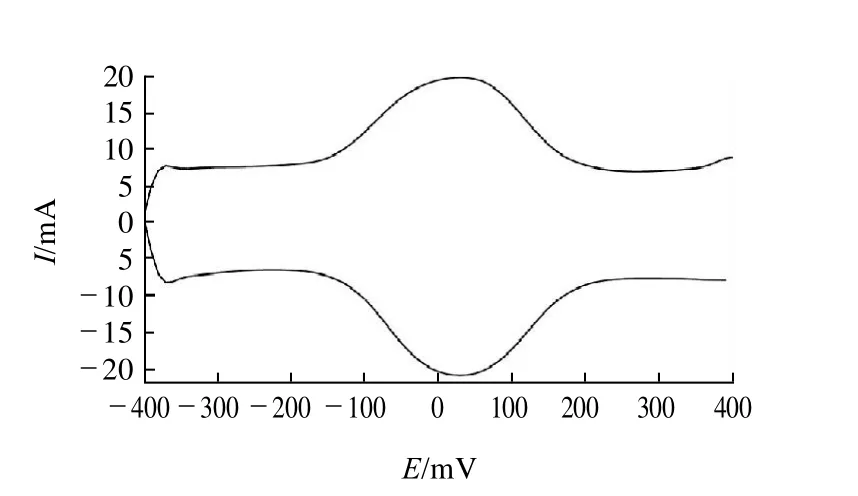
图2 NaFeEDTA的循环方波伏安谱图Fig.2 Cyclic square wave voltammogram of NaFeEDTA
2.3 底液条件的选择
2.3.1 pH值的选择将不同pH值的0.5mol/L的磷酸缓冲溶液2mL,加入50mL的容量瓶中再分别加入氯化钠溶液和10mL 1g/L

表1 不同p H值溶液中的NaFeEDTA峰电流Table 1 Ip of NaFeEDTA in solutions with different pH values
的NaFeEDTA溶液,定容到50mL,进行方波扫描,测出的峰电流结果见表1。可以看出,当pH值为3.0时的峰电流最大。同时发现在不同pH值溶液中,峰电位均为20mV左右,pH值对峰电位没有影响。故选择实验缓冲溶液的pH值为3.0。
2.3.2 缓冲组分的选择

表2 不同缓冲溶液组分中NaFeEDTA的峰电流Table 2 Ip of NaFeEDTA in different buffers
分别取pH 3.0的0.5mol/L的酒石酸溶液、三氯乙酸溶液、冰醋酸溶液、磷酸溶液2mL,加入50mL的容量瓶中再分别加入氯化钠溶液和10mL 1g/L的NaFeEDTA溶液,定容到50mL。由表2可以看出,磷酸作为缓冲液组分时峰电流最大,故选择磷酸作为缓冲溶液。
2.3.3 缓冲液浓度的选择

表3 在不同浓度缓冲溶液中扫描NaFeEDTA的峰电流Table 3 Ip of NaFeEDTA in buffers with different concentrations
由表3可以看出,当缓冲液浓度为0.02mol/L时测出的峰电流最高,因此选择此浓度为最佳的缓冲液浓度。
2.4 干扰实验
2.4.1 食品添加剂的影响
硫酸亚铁和三氯化铁为常用的铁强化剂,苯甲酸钠、山梨酸钾为食品中常用的防腐剂,柠檬酸为酱油中常见的有机酸,而亚铁氰化钾为食盐中使用的抗结剂。本研究在实验条件下对,这些物质对NaFeEDTA的检测产生干扰进行实验。200mg/L的铁氰化钾、亚铁氰化钾、三氯化铁、硫酸亚铁、柠檬酸、苯甲酸钠、山梨酸钾和NaFeEDTA溶液,在实验条件下的方波伏安曲线见图3。结果发现,铁氰化钾、亚铁氰化钾的伏安曲线峰电流比较明显,但峰电压与NaFeEDTA有300mV以上的差异,而其他添加剂没有明显的还原峰。因此使用方波伏安法可以对上述离子进行区分,对NaFeEDTA进行定性分析,食品中的其他添加剂不会产生干扰。
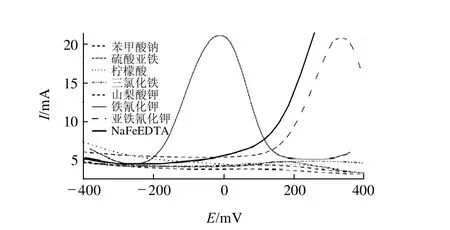
图3 NaFeEDTA和其他食品添加剂的方波伏安谱图Fig.3 Square wave voltammogram of NaFeEDTA and other food additives
2.4.2 氯化钠浓度的影响
实验发现试液中的氯化钠浓度对峰电流会产生较大影响,表4是在不同浓度的氯化钠溶液中,200mg/L的NaFeEDTA溶液的峰电流值。由表4可以看出,试液中氯化钠浓度为0.030mol/L时峰电流最高,氯化钠浓度过大会使峰电流降低。酱油、食盐等食品中氯化钠含量较高因此对这类样品进行测定时,应采用标准加入法进行检测,以消除氯化钠浓度差异的影响。

表4 不同浓度氯化钠溶液中NaFeEDTA的峰电流Table 4 Ip of NaFeEDTA in sodium chloride solutions with different concentrations
2.5 标准曲线
在优化的实验条件下,质量浓度为10~200mg/L的NaFeEDTA标准系列溶液的方波扫描曲线见图4。峰电流(Ipc)/mA与质量浓度(C)/(mg/L)的线性关系良好,其线性回归方程为Ipc=0.0769C-0.3025,相关系数r=0.9997。试液中NaFeEDTA的检出限为4mg/L(RSN=3)。
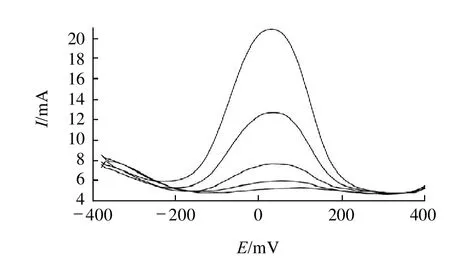
图4 NaFeEDTA标准系列溶液的方波伏安图Fig.4 Square wave voltammograms of NaFeEDTA standard series
2.6 样品处理与检测
NaFeEDTA强化酱油为我国销售范围最广的含有NaFeEDTA的食品。酱油的成分十分复杂,其中的氨基酸、蛋白质、有机酸等干扰物较多。实验发现,如不经处理,直接将酱油样品加入底液中进行检测,则基线会产生很大波动无法准确定量,因此需要对酱油进行净化。固相萃取法为复杂样品净化的常用方法,而酱油先经过离心可去除蛋白质等大分子质量的杂质,这样可以避免固相萃取柱因吸附样品杂质过多而过载[17]。实验发现,酱油样品在酸性条件下离心,得到的沉淀量较大,因此本实验选择在pH3.0的磷酸溶液中进行离心。样品经离心后取上清液进萃取柱,样品中大分子和非极性物质均可被固相萃取柱吸附,而FeEDTA-则不被保留直接流出,再用5mL水对萃取柱进行冲洗将FeEDTA-完全冲出。根据GB 2760—1996《食品添加剂使用卫生标准》,NaFeEDTA在铁强化酱油中的添加量为1.75~2.10g/L。取2mL酱油样品经处理后,试液中NaFeEDTA溶液质量浓度为70~84mg/L,处于本方法的线性范围以内。
在实验条件下,对NaFeEDTA添加量为2.00g/L的铁强化酱油样品重复测定6次,其峰电流的相对标准偏差为2.1%,平均回收率为93.5%。食盐可不用进行预处理,将样品溶解于底液中直接测量,在实验条件下,对NaFeEDTA添加量7.54g/kg的铁强化食盐样品重复测定6次,其峰电流的相对标准偏差为2.8%,平均回收率为96.8%。
NaFeEDTA在奶粉中的允许添加量为460~760mg/kg[6],在面粉中的允许添加量为180~360mg/kg[11],含量要比在酱油和食盐中小,而干扰成分众多。直接用该方法检测奶粉和面粉,灵敏度较低而干扰太严重,因此对于上述两种食品的电化学检测方法还需要进一步的研究。
3 结 论
在pH值为3的磷酸溶液中,通过循环伏安曲线,可判断FeEDTA-在该条件下的氧化还原反应为可逆反应。利用方波伏安法可实现对NaFeEDTA的准确检测。铁强化酱油经离心、固相萃取过滤后即可进行测定,铁强化食盐可溶解后直接测量。本方法具有操作简便、选择性强的特点,可用于酱油和食盐中NaFeEDTA的测定。
[1] 王波, 詹思延, 夏愔愔, 等. 乙二胺四乙酸铁钠与硫酸亚铁改善铁缺乏的效果比较: 对照试验的系统评价[J]. 现代预防医学, 2011, 38(7): 1240-1243.
[2] 刘鲁林, 许中敏, 常欣, 等. 乙二胺四乙酸铁钠(NaFeEDTA)在改善铁营养状况和预防铁缺乏性贫血方面的研究[J]. 中国食品添加剂, 2010(2): 119-123.
[3] 苗虹, 于波, 霍军生, 等. 食品添加剂NaFeEDTA测定方法研究[J].食品科学, 2000, 21(8): 48-50.
[4] 魏峰, 霍军生, 孙静, 等. 两种铁强化食盐中乙二胺四乙酸铁钠的检测方法研究[J]. 中国调味品, 2009, 34(4): 94-96; 105.
[5] 苏文斌,兰瑞家. 铁强化酱油中NaFeEDTA含量的测定[J]. 食品科学, 2008, 29(6): 308-311.
[6] 魏峰, 霍军生, 狄蕊, 等. 奶粉中乙二胺四乙酸铁钠的检测方法及其稳定性研究[J]. 食品工业科技, 2011(4): 379-382.
[7] JENNIFER S K, ANDREW C Y, ANA I G, et al. A rapid method for iron determination in fortified foods[J]. Food Chemistry, 2001, 75(3): 371-376.
[8] 魏峰, 霍军生, 黄建, 等. 毛细管区带电泳法分离测定铁强化酱油中乙二胺四乙酸铁钠[J]. 卫生研究, 2006, 35(1): 103-106.
[9] KARI F G, HILGER S U, CANONICA S. Determination of the reaction quantum yield for the photochemical degradation of Fe-(Ⅲ) EDTA:implications for the environmental fate of EDTA in surface waters[J].Environ Sci Technol, 1995, 29(4): 1008-1017.
[10] LUCENA J J, BARAK P, HERNANDEZ A L. Isocratic ion-pair highperformance liquid chromatographic method for the determination of various iron(Ⅲ) chelates[J]. Journal of Chromatography A, 1996, 727(2): 253-264.
[11] 魏峰, 狄蕊, 李文仙, 等. 面粉中NaFeEDTA的HPLC检测方法[J].粮油食品科技, 2007, 15(4): 56-57.
[13] KENICHI S, RYAN H, MARK D E, et al. Cyclic voltammetric and aqueous equilibria model study of the pH dependant iron(Ⅱ/Ⅲ)ethylenediamminetetraacetate complex reduction potential[J]. Journal of Electroanalytical Chemistry, 2007, 603(1): 44-50.
[14] UGO P, MORETTO L M, RUDELLO D, et al. Trace iron determination by cyclic and multiple square-wave voltammetry at nafion coated electrodes. applicationto pore-water analysis[J]. Electroanalysis, 2001,13(8/9): 661-668.
[15] 李彦, 张文德. 单扫极谱法测定强化酱油中NaFeEDTA含量与标准方法的比较[J]. 中国卫生检验杂志, 2008, 18(6): 1067-1068; 1090.
[16] GONZALEZ J, SOTO C M, MOLINA A. Square wave voltammetry and voltcoulometry applied to electrocatalytic reactions. oxidation of ferrocyanide at a ferrocene modified gold electrode[J]. Journal of Electroanalytical Chemistry, 2009, 634(2): 90-97.
[17] 魏峰, 李文仙, 黄建, 等. 反相离子对高效液相色谱法测定铁强化酱油中的乙二胺四乙酸铁钠[J]. 色谱, 2006, 24(14): 58-61.
Determination of NaFeEDTA by Square Wave Voltammetry
WEI Feng1,HUO Jun-sheng2,DI Rui1,SUN Jing2,*,HUANG Jian2
(1. Modern Educational Technology Center, Huangshan University, Huangshan 245041, China;2. Institute of Nutrition and Food Safety, Chinese Center for Disease Control and Prevention, Beijing 100050, China)
Square wave voltammetry was established to determine sodium iron EDTA (NaFeEDTA). In the square wave voltammetry, the phosphate buffer solution (pH 3.0) was set as the base solution, scan increment was set for 10 mV, square wave frequency was set at 2.5 kHz, and square wave amplitude was set at 100 mV. The linear range for the determination of NaFeEDTA was 10-200 mg/L with the correlation coefficient of 0.9997. The limit of detection of NaFeEDTA was 4 mg/L.In iron fortified soy sauce and salt samples, the recoveries were (93.5 ± 2.1)% and (96.8 ± 2.8)%.
sodium iron EDTA (NaFeEDTA);square wave voltammetry;iron fortified soy sauce;iron fortified salt
TS207.3;O657 .1
A
1002-6630(2012)10-0274-04
2012-01-05
国家“863”计划项目(2010AA023004)
魏峰(1979—),男,讲师,硕士,研究方向为食品分析。E-mail:keania@126.com
*通信作者:孙静(1963—),女,副研究员,本科,研究方向为食品营养。E-mail:jhuang@263.net
