蒲地蓝消炎口服液质量控制方法的研究
2012-10-25孟祥松马欣羽
蒋 磊,孟祥松,李 军,益 磊,马欣羽
(1.亳州市食品药品检验所,安徽亳州236800;2.安徽中医学院,安徽合肥230031)
蒲地蓝消炎口服液是由蒲公英、黄芩、板蓝根、苦地丁四味中药组成,具有清热解毒、抗炎消肿的功能。可用于疖肿、腮腺炎、咽炎、淋巴结炎、扁桃体炎等疾病的治疗[1]。蒲公英是蒲地蓝消炎口服液的主药之一,现代药理研究表明,蒲公英的药理作用主要有以下几点:抗菌及抗病毒作用、提高免疫功能的作用、抗胃损伤作用、保肝胆作用、抗肿瘤作用[2]。此外,蒲公英还是一味治疗妇科疾病的良药,单用即有可靠的效果,若以其为主组方辨证论治疗效更佳。可用于回乳,更年期综合征,女性腹痛等[3]。蒲地蓝消炎口服液现行国家标准收载的质控项目中未对蒲公英有效成分进行质量控制,因此作者拟对处方中蒲公英的有效成分咖啡酸进行定性定量控制研究。首先采用薄层色谱法作定性鉴别,并以口服液中特异性较强的咖啡酸为指标,为了有效地控制制剂质量,采用RP-HPLC法对处方中蒲公英的咖啡酸进行含量测定,考察蒲地蓝消炎口服液中咖啡酸的线性范围、专属性试验、精密度考察、重复性试验、稳定性试验、回收率试验,为蒲地蓝消炎口服液的质量控制提供简便可行,重现性好的方法,从而建立蒲地蓝消炎口服液的质量控制标准。
1 仪器、试剂与试药
1.1 仪器 高效液相色谱仪:型号:Agilent 1200,Hypersil ODS(4.6 mm ×250 mm,2.5 μm)色谱柱,G1329A 自动进样器,G1316A柱温箱,G1315D检测器(上海禾工科学仪器有限公司),超声仪:型号:JL360DT(上海吉理超声仪器有限公司),三用紫外分析仪:型号:UV-8(无锡科达仪器厂),离心沉淀机:型号:80-2(上海手术器械厂),分析天平:型号:ES-180J(沈阳龙腾电子称量责任有限公司),分析天平:型号:AB135-S(瑞士梅特勒-托利多),数显恒温水浴锅:型号:HH-S6(江苏省金坛市金城国胜实验仪器厂),酸度计:型号:PHS-25(上海第二分析仪器厂)。
1.2 试剂与试药 咖啡酸对照品(中国药品生物制品检定所,批号:110885-200102);水(娃哈哈纯净水,杭州娃哈哈集团有限公司,批号:20110409);乙腈(色谱纯,国药集团化学试剂有限公司,批号:20110209);甲醇(色谱纯,国药集团化学试剂有限公司,批号:20110209);其他试剂均为分析纯。
1.3 药品 蒲地蓝消炎口服液(市售)。
2 方法与结果
2.1 薄层色谱分析
2.1.1 供试品溶液的制备 取本品10 mL,用乙酸乙酯振摇提取2次,每次20 mL,合并乙酸乙酯液,蒸干,残渣加甲醇1 mL使溶解,作为供试品溶液[6]。
2.1.2 阴性对照溶液的制备 取除蒲公英以外的其他3味药材按处方制备成缺蒲公英的样品,同2.1.1法制成阴性对照溶液。
2.1.3 对照品溶液的制备 取咖啡酸对照品,加甲醇制成每1 mL含0.5 mg的溶液,作为对照品溶液。
2.1.4 薄层色谱分析 展开剂:三氯甲烷-甲醇-甲酸(9∶1∶0.5),方法:吸取上述三种溶液各 5 μL,分别点于同一硅胶G板上,放入展开缸中展开,取出,晾干。置紫外光灯(365 nm)下检视。供试品与对照品药材在相同的位置上显相同颜色的斑点,阴性对照则不显斑点,见图1。

图1 蒲地蓝消炎口服液的薄层鉴别
2.2 高效液相色谱分析
2.2.1 色谱条件 Hypersil ODS(4.6 mm × 250 mm,2.5 μm)色谱柱;流动相:甲醇-磷酸盐缓冲液(取磷酸二氢钠1.56 g,加水溶解为1 000 mL,再加1%磷酸溶液调节pH值至3.8 ~4.0);检测波长 323 nm;流速 1.0 mL·min-1;柱温40℃。理论板数:以咖啡酸计算应不低于3 000[4]。
2.2.2 溶液的制备
2.2.2.1 对照品溶液[5]精密称取经五氧化二磷减压干燥24 h的咖啡酸对照品8.95 mg,置100 mL量瓶中,加甲醇溶解并定容至刻度,摇匀,即得。
2.2.2.2 供试品溶液 取本品2 mL,置10 mL量瓶中,加5%甲酸的甲醇溶液至刻度,摇匀,离心,取上清液,置棕色瓶中,即得。
2.2.2.3 阴性对照液 取除蒲公英以外的其他3味药材按处方制备成缺蒲公英的样品,再按供试品溶液方法制备,即得。
2.2.3 标准曲线的制备 取按2.2.2.1项下制备的对照品溶液,分别取1.0、2.0、3.0、4.0、5.0、6.0 mL 置于 10 mL 量瓶中,加甲醇定容至刻度,摇匀,即得。分别进样10 μL,记录色谱图,由峰面积(Y)对相应的浓度(X)直线回归,得咖啡酸回归方程为:Y=33.402X+16.38,r=0.999,表明咖啡酸在 8.95 ~53.7 μg·mL-1的浓度范围内线性相关(见表 2、图2)。

表2 咖啡酸标准曲线
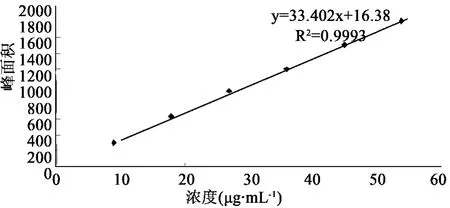
图2 咖啡酸标准曲线
2.2.4 专属性试验 分别取对照品溶液、样品溶液、阴性对照液注入色谱仪,记录色谱图,从图3、4、5中可以看出,咖啡酸与其相邻峰完全分离,阴性对照色谱图在对应的咖啡酸峰位置处无干扰峰,即表明其他组分对测定无干扰。咖啡酸峰与其他组分峰的分离度都大于1.5。对照品液相色谱图(见图 3、4、5)。
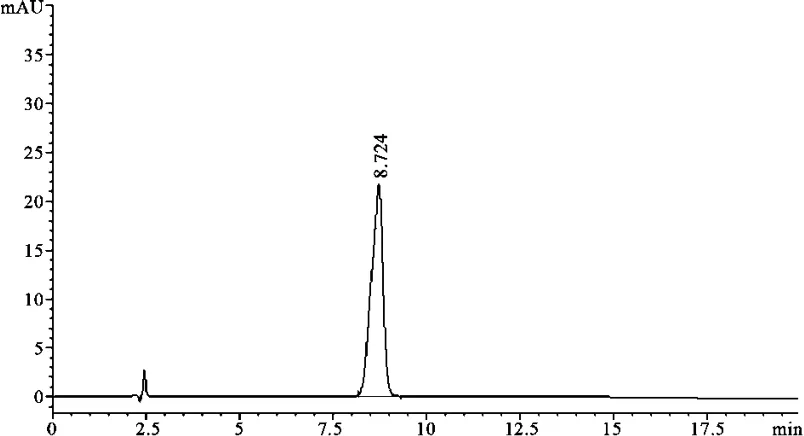
图3 对照品色谱图
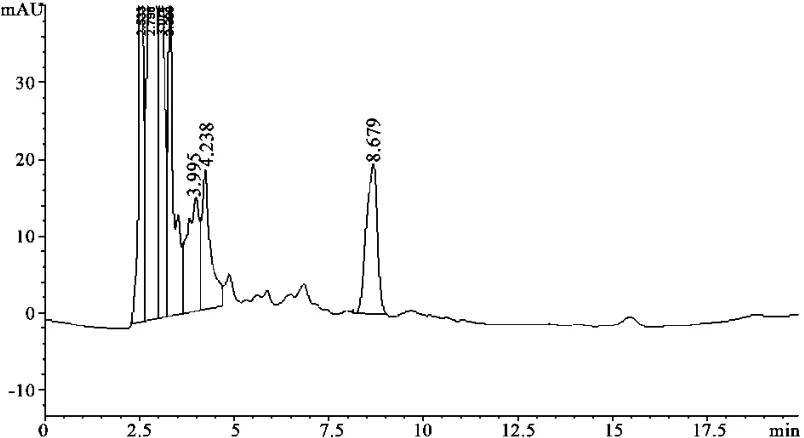
图4 样品色谱图
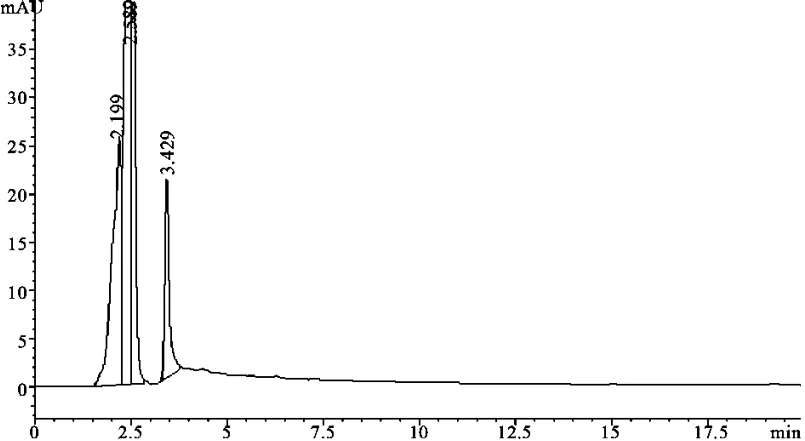
图5 阴性对照色谱图
2.2.5 精密度考察 取同一对照品溶液连续进样5次,进样量10 μL,测定峰面积,计算RSD为0.26%。表明仪器与色谱条件具有良好的精密度。
2.2.6 重复性试验 取同一批号的样品5份,按2.2.2.2项制备供试品溶液,分别精密吸取各供试品溶液10 μL注入高效液相色谱仪。测定峰面积,结果连续5针供试品峰面积的RSD为0.30%,表明含量测定方法的重复性良好。
2.2.7 稳定性试验 取同一样品溶液,在 0、2、4、6、8、10 h分别进样10 μL,依法测定峰面积,结果6次测定的咖啡酸峰面积RSD为0.01%,表明样品溶液在10 h内相对稳定。
2.2.8 回收率试验[7]精密量取同一批已知含量的供试品(含咖啡酸浓度为91.94 μg·mL-1)2 mL 6 份,分成 3 组,每组2份,分别置5 mL量瓶中,分别加入咖啡酸对照品(含咖啡酸浓度为 89.5 μg·mL-1)1.8、2.1、2.4 mL,加甲醇定容,按2.2.2.2 方法制备,按 2.2.1 项下分别进样 10 μL,记录色谱图,计算咖啡酸的回收率(见表3)。

表3 咖啡酸回收率计算结果
2.2.9 样品含量测定 将4批不同批号的蒲地蓝消炎口服液按 2.2.3方法制备,进样10 μL,测定峰面积,按外标法计算含量(见表4)。

表4 咖啡酸含量测定结果
3 讨论
本实验采用硅胶G板,以三氯甲烷-甲醇-甲酸(9∶1∶0.5)为展开剂,置紫外光灯(365 nm)下检视,斑点清晰。RP-HPLC在选择检测波长时,经紫外-可见分光光度计扫描,咖啡酸在323.2 nm处有最大吸收,故选323 nm作为检测波长。
4 结论
本方法可通过简单有效的方法首先对蒲地蓝消炎口服液中咖啡酸进行薄层色谱定性鉴别,确定其中含有咖啡酸,之后采用高效液相色谱法进行定量检测,从而有效地控制蒲地蓝消炎口服液中蒲公英的投药量,为蒲地蓝消炎口服液质量控制提供了准确、简便、可行的方法。
[1]曹兵,胡春雪,熊叶红,等.蒲地蓝消炎片质量控制方法研究[J].大理学院学报,2008,7(8):4 -6.
[2]王柏清,郭青竹,董玉旺.蒲公英的药理作用[J].兽医导刊,2010,10(12):43.
[3]桂风云.蒲公英在妇科的临床应用[J].甘肃中医,2010,23(7):33 -34.
[4]国家药典委员会.中华人民共和国药典2010年版(一部)[S].北京:中国医药科技出版社,2010:331.
[5]晏嫒,刘世霆,许重远,等.高效液相色谱法同时测定蒲公英中咖啡酸和阿魏酸的含量[J].中国现代应用药学,2006,23(3):229 -231.
[6]刘广川,吕剑,杨小孟.蒲地蓝消炎片质量标准研究[J].首都医药,2007,14(6):49.
[7]刘文英.药物分析[M].北京:人民卫生出版社,1998:72-73.
