在物理化学实验中引入纳米光催化综合实验*
2012-09-25周爱秋马跃宁许效红
周爱秋 马跃宁 许效红
(山东大学化学与化工学院 山东济南 250100)
物理化学实验是综合性、技术性较强的化学基础实验。大多数物理化学实验多年来一直沿用传统的教学内容,没有大的更新。为了使学生能更好地适应现代科学技术的发展,必须改革现有的实验教学内容及实验技术,将高科技实用型的综合性实验引入其中。
纳米半导体光催化技术在环境治理以及光照分解水制氢、太阳能电池等方面均具有巨大潜在应用前景,近年来得到广泛的研究[1-4]。半导体光催化的研究涵盖纳米材料、催化化学、半导体物理、环境科学以及能源科学等学科,是典型的交叉学科。在化学本源上,光催化属于物理化学范畴。因此,将光催化引入物理化学实验,使科学研究的前沿和热点与传统的物理化学教学内容紧密结合,使学生通过实验了解科学研究的最新进展,将大大开拓学生的视野,激发学生的学习兴趣,提高学生的创新能力和科研能力。
尽管纳米二氧化钛是目前被研究和应用最广泛的光催化剂,但是为了提高可见光的利用率及光量子效率,研究工作者近年来一直在努力合成和研究新型光催化材料。Bi4Ti3O12是一种典型的Aurivillius层状化合物,由于具有高的居里温度(675℃)和电光开关效应,其在高温压电、信息存储以及光学显示等领域的潜在应用一直广受关注并被广泛研究。最近的研究发现,Bi4Ti3O12具有良好的半导体光催化剂的特性,在紫外光照射下可有效地催化有机污染物的降解[5-8]。
本实验设计采用化学溶液分解法制备纳米钛酸铋Bi4Ti3O12,并对其进行酸化处理,以改变其尺寸、形貌、表面化学组成与微结构;采用典型偶氮染料甲基橙作为模型有机污染物,研究其光催化性能。通过本实验,可使学生了解和掌握纳米材料的制备、表征,光催化性能研究的方法及相关的基本概念和理论,并使学生对材料、环境、能源等热点领域与化学的相关性有所了解,培养学生查阅资料、设计实验方案、综合分析问题和解决问题的能力以及创新精神。
1 实验部分
1.1 实验仪器和药品
管式炉,自制光催化装置,恒温水浴,恒温干燥箱等。
硝酸铋(Bi(NO3)3·5H2O),钛酸四丁酯(Ti(OC4H9)4),冰醋酸(CH3COOH),乙酰丙酮 (C5H8O2)。实验所用试剂均为分析纯,使用之前未进行纯化处理。
1.2 材料制备
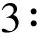
将1.0g Bi4Ti3O12源样品(BTO-0)加入到20mL浓硝酸中,恒温70℃搅拌酸化处理20min,倾倒掉上层清液,然后用去离子水将酸化样品洗至中性并离心抽滤,最后将样品置于烘箱中,于100℃烘干24h,得到白色粉末产物(标记为BTO-1)。
1.3 材料表征
利用粉末X射线衍射(XRD)表征样品的物相结构,在Bruker D8 Advanced Solution X射线衍射仪上进行。仪器使用CuKα靶,衍射波长为1.5418Å,扫描速度0.04°/s,扫描范围10°~80°。采用JEOL JSM-6700F型场发射扫描电镜(FE-SEM)观察产物的形貌及尺寸。在带积分球的Shimadzu UV-3100型紫外可见分光光度计上测定样品的UV-Vis漫反射光谱,采用无吸收参比BaSO4,扫描波长范围为200~800nm。比表面积的测定采用液氮温度(77K)下N2吸附法在Quadrasorb SI比表面及孔隙度分析仪上完成,测试前先将样品于200℃、1.333Pa条件下脱气处理2h。
1.4 光催化性能测定
利用悬浮液体系中紫外光照射下对偶氮染料甲基橙的降解评价所制备材料的光催化性能:称取0.3g光催化剂样品,放入100mL甲基橙溶液(10mg/L)中,在黑暗条件下电磁搅拌0.5小时,使光催化剂和甲基橙达到吸附平衡后取样;然后开启紫外灯光源,在恒温25℃下进行反应,直至溶液接近无色。在反应过程中按15min间隔取样,经0.45μm微孔滤膜滤去取样溶液中残留的催化剂颗粒。采用Shimadzu UV-3100型紫外可见分光光度计监测滤液在200~800 nm范围的吸收光谱变化及波长464nm处的吸光度,以确定甲基橙的降解程度及浓度。
2 结果与讨论
2.1 材料制备和表征
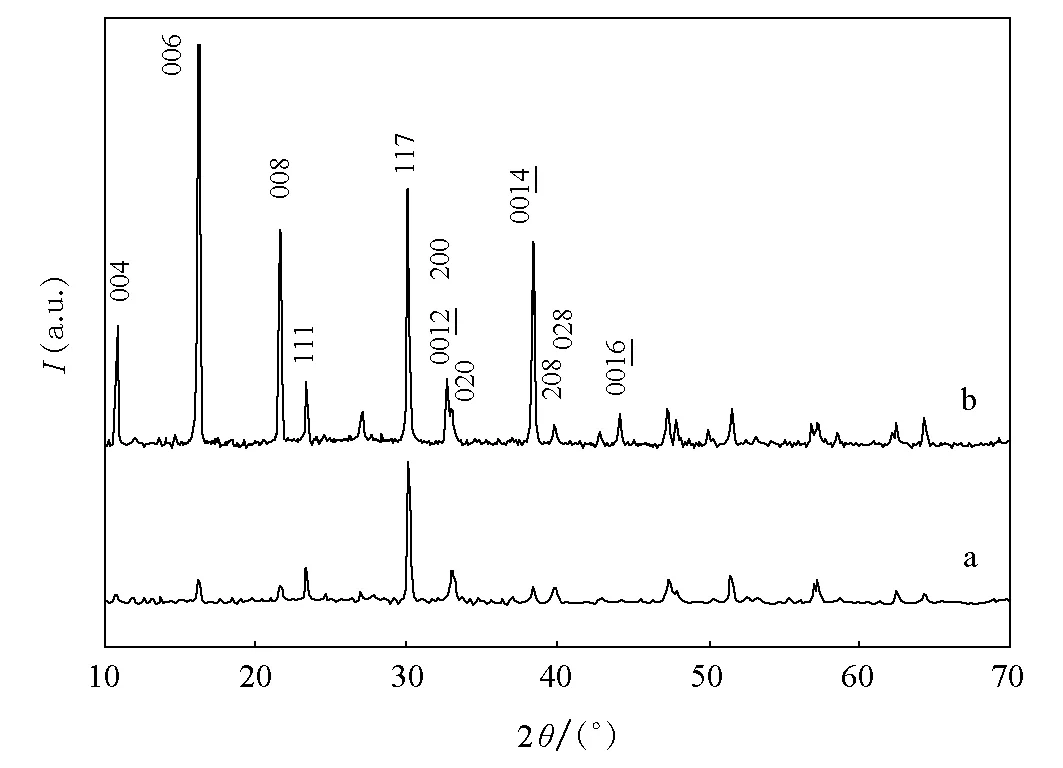
图1 酸化前后样品的XRD谱(a) BTO-0;(b) BTO-1

与Bi4Ti3O12源样品相比,在酸化产物的XRD谱中,出现了极强的(00l)衍射峰,表明酸化产物BTO-1的晶粒沿c轴方向高择优取向。其衍射峰(006)与(117)的强度之比(I(006)/I(117))大约为Bi4Ti3O12源样品的15倍,这意味着酸化产物具有盘片状形貌。从图2的SEM图片可以看出:经过酸化处理后,Bi4Ti3O12颗粒的尺寸从大约0.1~ 3μm剥离为150nm×80nm~80nm×30nm的纳米片层。与此相应,采用N2吸附法(BET)测定的结果表明,酸化处理使Bi4Ti3O12的比表面积从1.737m2·g-1提高到46.907m2·g-1。

图2 酸化前后样品的SEM图(a) BTO-0;(b) BTO-1
必须指出的是,对酸化后的产物没有观察到任何衍射峰位置的偏移,特别是分裂(208)和(028)衍射峰(2θ≈32.872°和33.120°)出现在与源样品完全相同的位置。上述结果表明酸化产物保留了Bi4Ti3O12源样品的正交晶相结构,其晶格没有任何膨胀与收缩。根据XRD曲线可计算出其晶格参数分别为a=0.5445nm,b=0.54065nm,c=3.2778nm。
光催化剂的光吸收特性一般采用UV-Vis漫反射谱来确定。图3为CSD法制备的Bi4Ti3O12源样品BTO-0与其酸化产物BTO-1的UV-Vis漫反射谱。源样品BTO-0的反射谱图分为两个区域,没有清晰的吸收边缘并且延伸到可见光区,这与其淡黄色的颜色相吻合。酸化产物BTO-1的漫反射谱是陡立的曲线,其吸收边蓝移至约400nm处,这与酸化处理后的样品脱色为白色粉末相一致。造成这种现象的原因之一可能是量子尺寸效应,即酸化处理导致颗粒尺寸减小,特别是沿c轴方向的尺度大大降低所致;其二是酸化处理使Bi4Ti3O12颗粒表面的微结构发生变化,从而引起其电子结构改变。根据文献报道,Bi4Ti3O12为间接带隙半导体[10],因此可取Kubelka-Munk函数(F(R))1/2对照射光能E作图计算其禁带宽度。如图4所示,将曲线的线性部分延伸至与坐标横轴(光能)相交,求出酸化前后的样品BTO-0和BTO-1的禁带宽度分别为2.95和3.10eV。
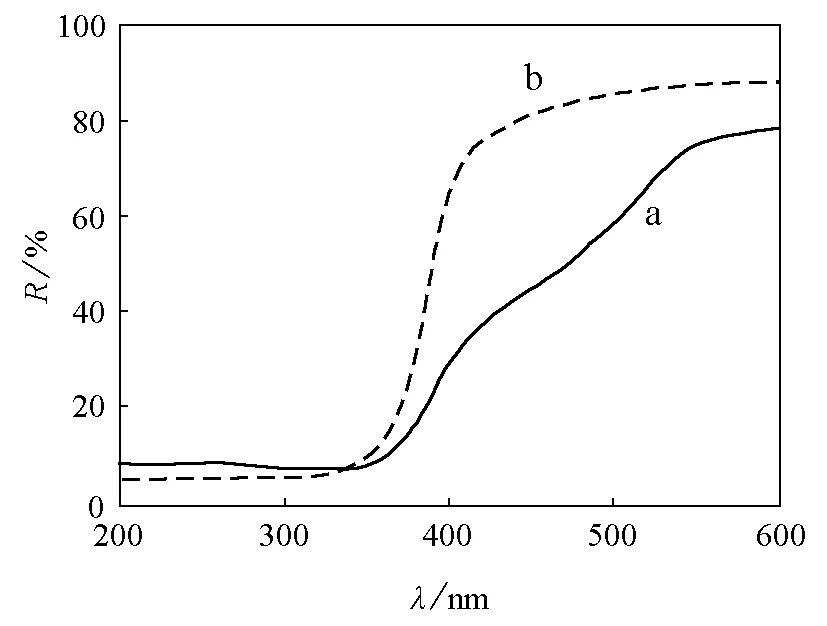
图3 酸化前后样品的UV-Vis漫反射谱图(a) BTO-0;(b) BTO-1
图4 酸化前后样品的Kubelka-Munk函数与照射光能的关系(a) BTO-0;(b) BTO-1
2.2 材料的光催化性能
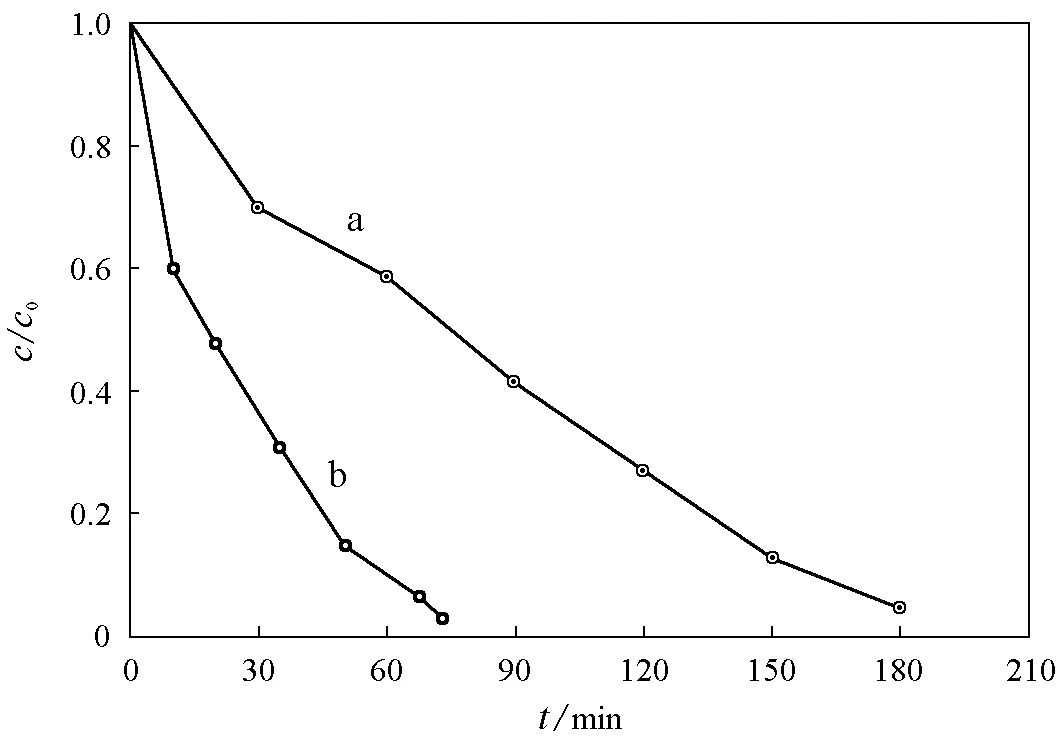
图5 紫外光照下酸化前后样品对甲基橙的光催化降解反应(a) BTO-0;(b) BTO-1
作为一种典型的Aurivillius化合物,Bi4Ti3O12被发现在紫外光照下可有效地光催化降解偶氮染料甲基橙[5-8]。因此,我们设计了在悬浮水溶液体系中,利用紫外光照射下对偶氮染料甲基橙的降解评价所制备的Bi4Ti3O12及酸化产物的光催化性能。图5为酸化前后的Bi4Ti3O12在紫外光照下光催化降解甲基橙溶液的浓度-时间曲线。很明显,酸化产物显示出比源样品高得多的光催化活性。根据文献报道,纳米半导体对水溶液中甲基橙的光催化降解可采用由Langmuir-Hinshelwood模型简化得到的准一级反应动力学模型描述[11],即:
-ln(c/c0)=Kt
由此可以计算出上述光催化反应的速率常数。对应于Bi4Ti3O12源样品BTO-0和酸化产物BTO-1,计算得到的光催化反应速率常数分别为0.01411和0.04307min-1。显然,酸化处理可大大提高Bi4Ti3O12催化甲基橙降解的速率,酸化产物的光催化活性比源样品大大提高。根据XRD分析,在酸化处理前后,Bi4Ti3O12的物相结构维持不变。因此酸化产物光催化活性的提高,一方面可归因于颗粒尺寸减小和形貌改变引起的比表面积增加,另一方面是由于酸化处理会导致颗粒表面的微结构发生改变,从而导致其表面物理化学性能变化。的确,根据UV-Vis漫反射谱测定,酸化处理明显改变了Bi4Ti3O12的光吸收特性,显示其表面的微结构发生了变化,其在甲基橙水溶液中的表面物理化学性质也相应有所变化(例如表面吸附OH的数量和分布),这可以影响光催化剂表面的化学反应速率及其光催化活性。
3 实验运行模式与内容的建议
本实验可以采取综合开放式模式。目的是将纳米材料制备、表征、光催化性能测试、光催化反应动力学融为一体,在“纳米材料光催化”的题目下,让学生通过查阅文献资料,了解相关科研领域的最新进展,自主确定具体研究内容并设计实验方案;然后在教师的指导下,独立完成实验。也可以设计成物理化学光催化动力学基础实验,将科学研究的前沿和热点与传统的物理化学反应动力学的教学内容紧密结合,这样不仅能加深学生对基础化学反应动力学理论的理解和掌握,而且能使学生通过实验系统地了解和掌握光催化性能的一些基本概念、方法和理论。另外,将光催化动力学引入物理化学实验是物理化学实验教学的全新内容,填补了物理化学实验中光化学实验的空白。
本文主要描述纳米半导体光催化剂Bi4Ti3O12的制备,通过酸化处理改变其尺寸、形貌、表面组成和微结构,并研究上述因素对光催化活性的影响。在实际开设实验时,可对具体内容进一步拓展,根据学生的兴趣和学时在以下范围内灵活选择:
(1) 采用不同纳米光催化剂,如TiO2、AgCl等。
(2) 采用不同的纳米光催化剂的制备方法,如水热法、溶胶-凝胶法等。
(3) 采用其他的模型有机污染物,如四氯苯酚、硝基苯酚、甲醛等。
(4) 水溶液中有机物浓度、pH、催化剂投加量等对光催化降解速率的影响。
[1] Fujishima A,Honda K.Nature,1972,238:37
[2] Hoffmann M R,Martin S T,Choi W,etal.ChemRew,1995,95(1):69
[3] Linsebigler A L,Lu G,Yates J T.ChemRev,1995:95(3):735
[4] 桥本和仁,藤岛昭.图解光催化技术大全.北京:科学出版社,2007
[5] Yao W F,Wang H,Xu X H,etal.MaterLett,2003,57(13-14):1899
[6] Yao W F,Xu X H,Wang H,etal.ApplCatalB:Environ,2004,52(2):109
[7] 许效红,姚伟峰,张寅,等.化学学报,2005,63(1):5
[8] Zhang H P,Lü M K,Liu S W,etal.MaterChemPhys,2009,114(2-3):716
[9] Cummins S E,Cross L E.JApplPhys,1968,39(5):2268
[10] Cai M Q,Yin Z,Zhang M S,etal.ChemPhysLett,2005,401(4-6):405
[11] Rajeshwar K,Osugi M E,Chanmanee W,etal.JPhotochemPhotobiolC:PhotochemRev,2008,9(4):171
