儿茶素及茶黄素单体间清除羟自由基能力研究
2012-09-15涂云飞杨秀芳孔俊豪张士康朱跃进王盈峰
涂云飞,杨秀芳,孔俊豪,张士康,朱跃进,王盈峰
中华全国供销合作总社杭州茶叶研究院,杭州 310016
儿茶素及茶黄素单体间清除羟自由基能力研究
涂云飞*,杨秀芳,孔俊豪,张士康,朱跃进,王盈峰
中华全国供销合作总社杭州茶叶研究院,杭州 310016
本文通过二次通用旋转回归设计考察儿茶素体系和酯型儿茶素-茶黄素体系中各成分间的抗氧化能力强弱及相互间协同清除羟自由基能力。结果表明:儿茶素与茶黄素中的各成分随含量增加,清除能力亦随之增加,其中TF-D-G增加至一定浓度后,其效率有降低的趋势。儿茶素体系中各成分清除羟自由基能力为:ECG>EC>EGCG,其中ECG的贡献率达到了43%以上,而EGC在该体系中贡献不明显;酯型儿茶素-茶黄素体系中的羟自由基清除能力主要表现为:TF-D-G>TF-M-G>ECG>EGCG>TF,其中TF-D-G占对优势(贡献率为51.91%),而儿茶素清除自由基能力却未能有效发挥,每组中各成分之间的协同作用微弱。
儿茶素;茶黄素;羟自由基;化学发光;流动注射

图1 表儿茶素与茶黄素结构Fig.1 Structure of Epi-catechins and theaflavins
茶鲜叶按不同的加工工艺[1],可被制成绿茶,乌龙茶及红茶。其中乌龙茶及红茶中不仅含有儿茶素,还有一定量的儿茶素经酶促氧化聚合形成的茶黄素(结构如图1所示),这些成分不仅构成了茶叶的特征性品质成分,而且对人类健康的保护方面发挥了重要作用[2-5]。
通常,绿茶中酯型儿茶素比简单儿茶素的摩而数高出约3~5倍[2,6,7],而经酶促反应后,表型简单儿茶素(EC和EGC)则会消耗怠尽,酯型儿茶素(EGCG和ECG)会有一定量的残存。传统工艺条件下,儿茶素的消耗与茶黄素的生成不成比例。有研究表明[8],儿茶素的消耗可能是因为酚类酶促同时生成的双氧水被过氧化物酶利用而产生的羟自由基攻击儿茶素,降低了茶黄素的生物合成。然而至今未有实验数据证实。因此本文模拟过氧化物酶分解过氧化氢,利用芬顿反应产生的羟自由基攻击多酚类物质,目的是通过二次通用旋转回设计探索儿茶素和茶黄素单体对羟自由基清除能力及其协同清除效果,从而有望为红茶中儿茶素大量消除,而茶黄素未能成比例生成这一机理提供一些前期性的基础研究结果,为提高红茶中茶黄素含量作一些铺垫性的工作。
1 材料与方法
1.1 试剂
儿茶素单体(上海友思生物技术有限公司);茶黄素单体自制[12];硅胶(60~200目,岛海洋化工厂);Sephadex LH-20(安玛西亚有限公司);鲁米诺(≥98%,苏州工业园区亚科化学试剂有限公司),其它试剂均为分析纯。
1.2 仪器
IFFM-E型流动注射化学发光分析仪(西安瑞迈分析仪器有限公司);分析天平(梅特勒 AL-204);定量加样器(上海化科实验器材有限公司)。
1.3 羟自由基清除能力测定
羟自由清除能力测定采用流动注射化学发光法[9]。即将双氧水(8.4%,v/v)通过六通阀注射进入约100 μL定量环,再与含有鲁米诺(2.0×10-4mol/L)、Fe2+-EDTA(6.0×10-2mol/L)及含儿茶素或茶黄素的磷酸盐缓冲溶液(pH 7.4,0.05 mol/L)载流相混合后进入光电倍增管,记录化学发光信号。空白样以水取代儿茶素或茶黄素进行实验。其清除能力通过抑制发光体系(Fe2+-H2O2-鲁米诺体系)[10]来衡量。清除率=(1-Si/S0)×100%,Si为实际发光面积,S0为空白发光面积。.
1.4 实验设计
试验在单因素的基础上分两组,组ⅰ为四个表儿茶素单体,组ⅱ为茶黄素单体与酯型表儿茶素间的羟自由基清除能力比较。实验实施以二次通用旋转回归设计[11]为基础,每一独立变量的变化在5个无量纲编码水平(-r,-1,0,+1,+r),并确定了儿茶素与茶黄素单体因素的体积浓度变化范围(见表1)。
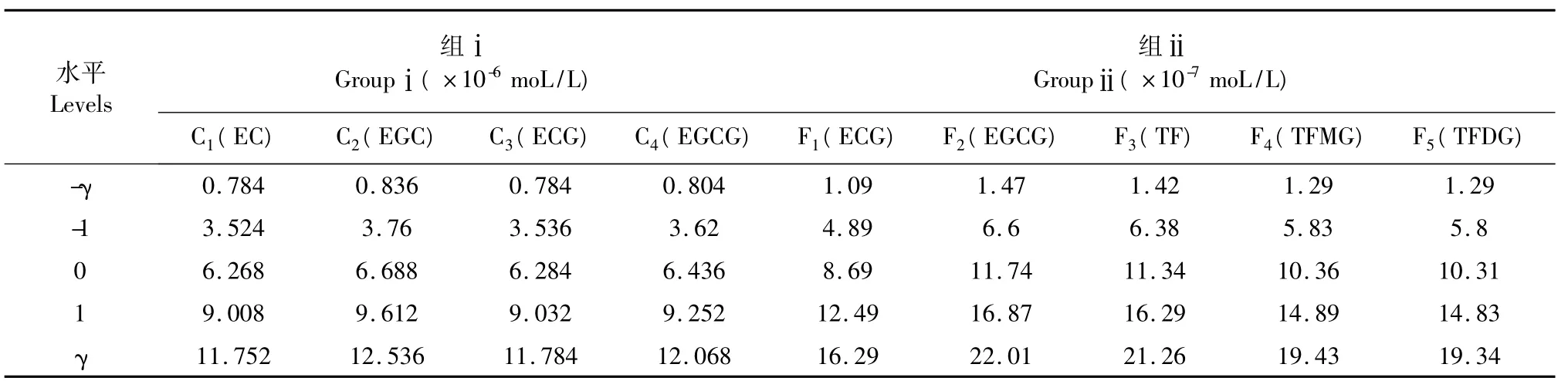
表1 二次通用旋转试验水平编码表Table 1 Coded levels of variables of the central composite experimental design
组ⅰ为31次实验实施,包括16次因子设计实施,8次坐标轴点实施,和7次重复中心设计实施;组ⅱ为32次实验实施,包括16次因子设计实施,10次坐标轴点实施,和6次重复中心设计实施,其实施结果见表2。

表2 二次通用回归旋转模型试验设计方案及结果Table 2 General quadratic regression central composition design experiment and experimental result employed for evaluating the antioxidant ability

2 1 1 1 -1 1 1 1 -1 -1 80.01 66.88 3 1 1 -1 1 1 1 -1 1 -1 78.16 71.75 4 1 1 -1 -1 1 1 -1 -1 1 71.76 74.08 5 1 -1 1 1 1 -1 1 1 -1 81.16 70.93 6 1 -1 1 -1 1 -1 1 -1 1 77.70 73.39 7 1 -1 -1 1 1 -1 -1 1 1 75.50 73.76 8 1 -1 -1 -1 1 -1 -1 -1 -1 68.06 60.56 9 -1 1 1 1 -1 1 1 1 -1 77.19 69.77 10 -1 1 1 -1 -1 1 1 -1 1 72.69 70.49 11 -1 1 -1 1 -1 1 -1 1 1 68.72 74.66 12 -1 1 -1 -1 -1 1 -1 -1 -1 60.55 60.22 13 -1 -1 1 1 -1 -1 1 1 1 75.93 73.47 14 -1 -1 1 -1 -1 -1 1 -1 -1 71.51 62.84 15 -1 -1 -1 1 -1 -1 -1 1 -1 68.84 64.70 16 -1 -1 -1 -1 -1 -1 -1 -1 1 58.02 68.97 17 2 0 0 0 2 0 0 0 0 77.07 74.98 18 -2 0 0 0 -2 0 0 0 0 66.48 67.46 19 0 2 0 0 0 2 0 0 0 74.61 71.15 20 0 -2 0 0 0 -2 0 0 0 72.62 67.13 21 0 0 2 0 0 0 2 0 0 80.29 72.93 22 0 0 -2 0 0 0 -2 0 0 62.65 70.39 23 0 0 0 2 0 0 0 2 0 77.59 70.74 24 0 0 0 -2 0 0 0 -2 0 67.78 66.31 25 0 0 0 0 0 0 0 0 2 73.06 74.31 26 0 0 0 0 0 0 0 0 -2 73.37 61.39 27 0 0 0 0 0 0 0 0 0 72.85 69.98 28 0 0 0 0 0 0 0 0 0 75.21 69.40 29 0 0 0 0 0 0 0 0 0 74.09 70.07 30 0 0 0 0 0 0 0 0 0 73.21 68.91 31 0 0 0 0 0 0 0 0 0 73.19 71.32 3200 0 0 0 78.24 69.48
1.5 试验数据处理
数据的统计及响应面分析采用统计软件Matlab6.0进行。并利用ANOVA评价各统计参数(P<0.05表示差异显著)。
2 结果
2.1 回归模型的系数建立与检验
利用统计软件对表2中的实施过程所取得的羟自由基清除率进行系数回归与方差分析,结果如表3和表4所示。两组体系中方程的回归均显著,组ⅰ与组ⅱ的P值均小于0.01,并且两组数据的回归方程的失拟性的概率P均大于0.05,说明方程能够拟合真实值。

表3 次响应回归模型方差分析Table 3 Analysis of variance for fitted mathematical model to an experimental data set using multiple regression
考虑到因子间存在交互作用,因此,各因素的一次,交互及二次项的回归系数以P值与各因素的贡献率综合考虑,忽略各因素的P<0.05,得到组ⅰ与组ⅱ的回归方程为:

组ⅰ中,各因子的二次项均不显著,同时交互项亦只有C1×3和C3×4项达到显著水平,一次项中,除C2不显著外,其余三因素均达到显著水平,并且三因子的单因素水平的贡献率超过80%。对于组ⅱ来说,各单因子均达到显著性水平,二次项中,F1、F3、F5达到显著水平,与组ⅰ相似,各因子的交互作用很微弱,并且ECG与TFDG分别为两组中对于羟自由基的清除率具有绝对的优势。
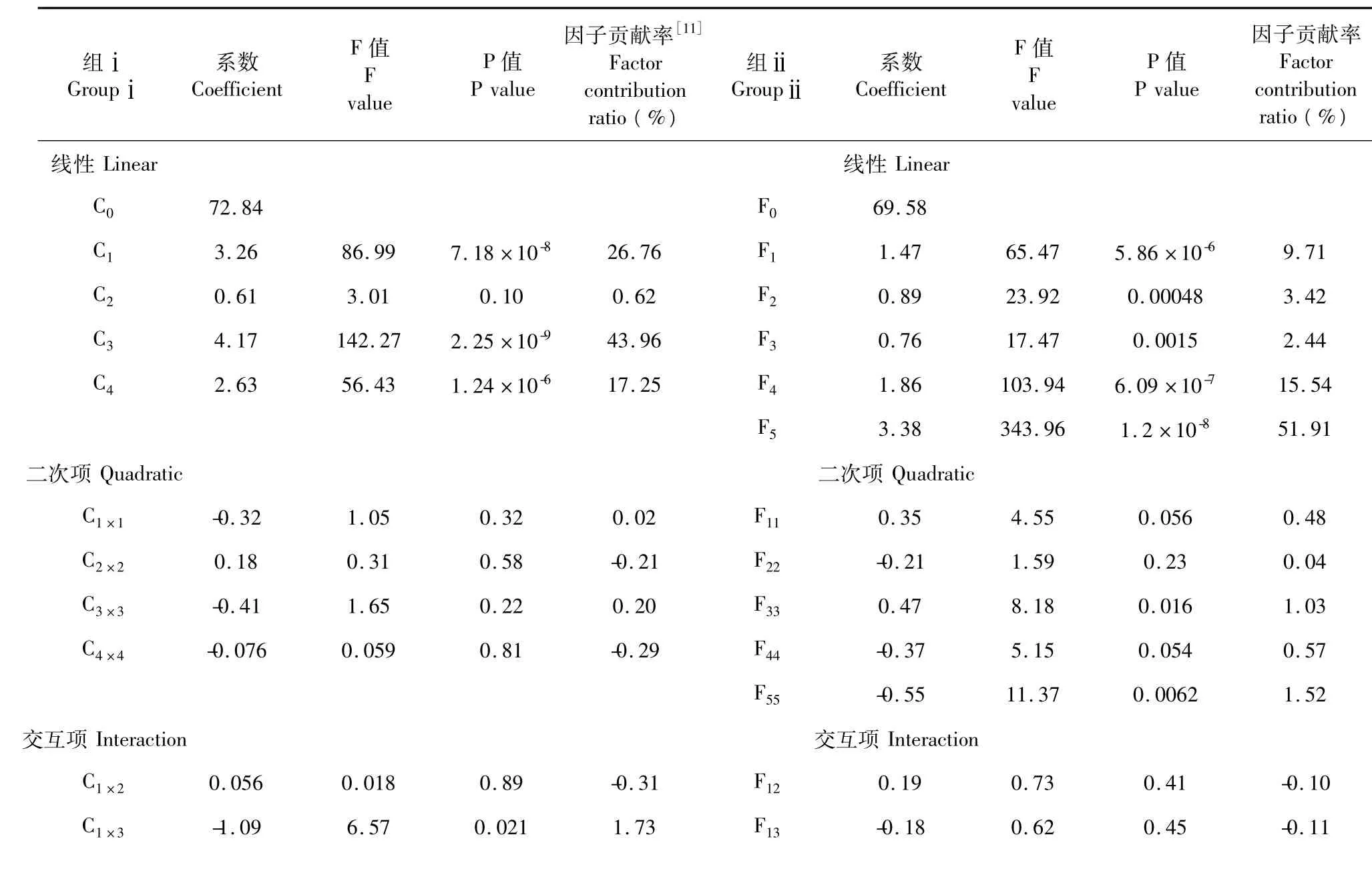
表4 二次通用旋转回归模型因子系数及清除能力贡献率Table 4 Regression coefficients of the fitted quadratic equation and factor contribution ratio for the yield of antioxidant ability

C1×4-0.77 3.26 0.089 0.70 F14-0.28 1.52 0.24 0.02 C2×3-0.43 1.02 0.33 0.01 F15-0.30 1.80 0.21 0.07 C2×4-0.55 1.67 0.21 0.21 F23-0.75 11.39 0.0062 1.52 C3×4-1.39 10.51 0.0051 2.96 F240.097 0.19 0.67 -0.18 F25-0.36 2.64 0.13 0.19 F34-0.39 3.17 0.10 0.28 F35-0.82 13.51 0.0037 1.84 F45-1.09 24.12 0.00046 3.45
2.2 数学模型分析
2.2.1 主效应分析
各因素处理均经无量纲线性编码代换,偏回归系数已经不受因素取值的大小及单位的影响,其绝对值的大小直接反映了变量对响应值的影响程度。但是由于实验因子存在交互作用,因此各因子对羟自由基的清除率的贡献大小需进一步转化成贡献率来衡量。由表4可知,各组中因素间的清除能力按从强至弱的顺序依次为:C3(43.96%)>C1(26.76%)>C4(17.25%);F5(51.91%)>F4(15.54%)>F1(9.71%)>F2(3.42%)>F3(2.44%)。比较两组结果,虽然儿茶素组中的ECG在该体系中抗氧化能力较强,但是当与茶黄素混合后的新体系中,酯型儿茶素ECG发挥清除羟自由基的能力明显降低,取而代之的是酯型茶黄素。
2.2.2 单因素效应分析
将回归模型中三个固定在零水平,得到的单因素模型分别为:
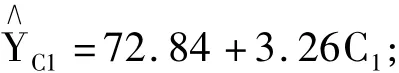

将4个因素固定在γ、1、0、-1、-γ水平,得到各因子的单因素效果图2。从图中可以明显看出,组ⅰ(图2-A)中各因素的效应随着自变量的变化直线走向,并且C3的斜率最大,其余次之。而组ⅱ(图2-B)中,茶黄素双没食子酸酯呈现出抛物线状,从左至右呈现出先快速增长后趋缓的态势。而F3呈现出开口向上的抛物线状说明有最小值点。其余成分变化趋于线性,即在实验范围内,每组中的成分对羟自由基的影响主要表现为含量越高,清除能力越大。
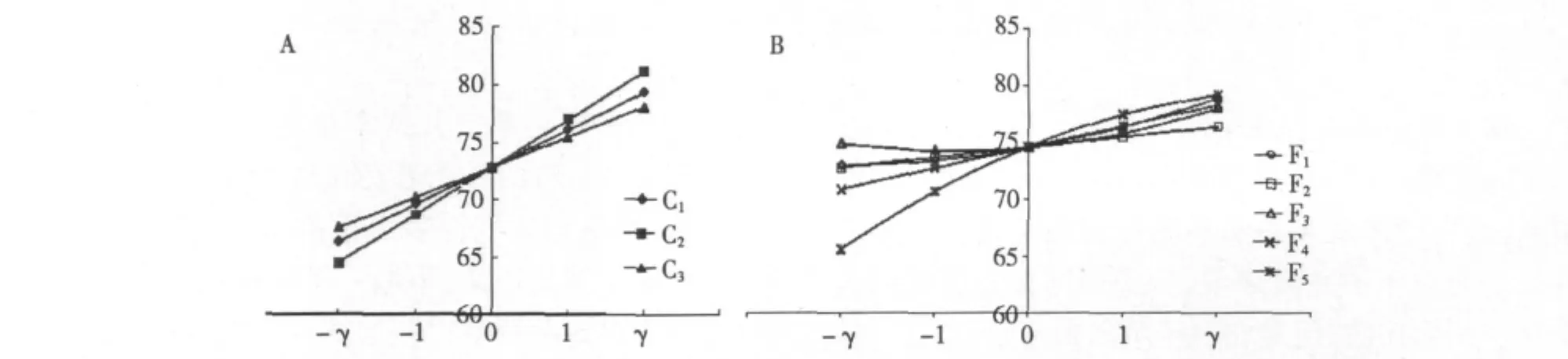
图2 各单因素水平与清除率的回归曲线Fig.2 Regression curve of scavenge and the levels of each component
2.2.3 单因素边际效应分析
单因素边际效应在二级响应面交互作用条件下,主要反应清除率随各因子水平的变化而变化的速率。为了确定各因素的边际效应,将上述所得方程进行单因素求导,各方程如下:
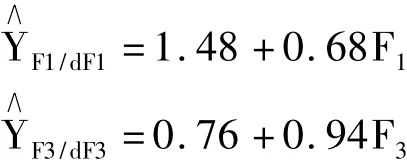
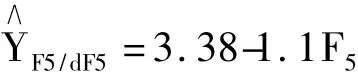
从上图中可以看出,茶黄素及茶黄素单没食子酸酯随着编码值的增加,清除速率快速上升,同时茶黄素双没食子酸酯(F5)的清除速率主要表现为随编码值的增加而急剧下降,这亦间接说明,虽然茶黄素双没食子酸酯(F5)的浓度增加可以增强羟自由基的清除率,但低浓度时清除自由基的效率更高,而对于茶黄素(F3)及单没食子酸酯(F4)则表现出随浓度的增加,清除羟自由基的效果呈现出上升的趋势。
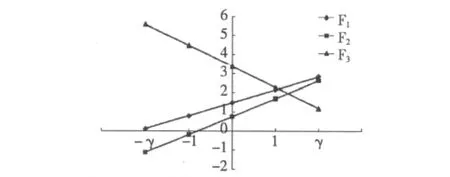
图3 各单因素边际效应Fig.3 Marginal utility of scavenge of each component
2.2.4 两因素互作效应分析
在组1中,分别将两个因素固定在零水平,得到另外两个因素的模型。分别为,根据模型做出的响应面和等高线图。

图4-C说明儿茶素(组ⅰ)中除了C1×3与C3×4因子间的微作用外,主要表现为相互间的交互作用很弱,这主要体现在各水平的等高线呈现出平等的直线。而对于图4-D来说,响应面则被双因素间的交互作用而扭曲,但是相对于单因素来说,交互作用依然较弱,其总贡献率不足7%。
3 讨论
儿茶素单体在清除自由基或抑制脂质过氧化能力方面,不同的研究体系结果表明酯型儿茶素强于简单儿茶素,并且酯型或简单儿茶素中存在着表没食子型与表儿茶素型强弱顺序不定的差异[12-14],然而这些结果都是基于儿茶素单体独立的抗氧化效果。笔者通过将四种儿茶素同时暴露于活性氧羟自由基时,则主要表现为表儿茶素型(ECG和EC)强于表没食子型儿茶素(EGCG和EGC),这可能是由于儿茶素在清除羟自由基时,有着两种类型相互间自修复作用[15,16],达到重复利用的可能,从而增强表型儿茶素的抗氧化能力。另一方面,表型与表没食子型儿茶素的B环4位酚羟基发生抽氢后,表型儿茶素B环上的2位苄氢比表没食子型儿茶素B环上的3或5位酚羟基更易于发生抽氢反应[17],从而导致表型儿茶素在清除自由时处于优势地位。
对于酯型儿茶素-茶黄素体系,茶黄素单或双没食子酸酯>酯型儿茶素>茶黄素。在该体系中,茶黄素双没食子酸酯对于羟自由清除的贡献率高于50%,这与儿茶素及茶黄素结构中的没食子基具有稳定儿茶醌或茶黄醌的作用相符合[18]。同时,这也可以间接说明高茶黄素与儿茶素提取物可更好的改善心脑血管疾病的性状[4],因为茶黄素与儿茶素的联用增强了酯型茶黄素的清除羟自由基能力而发挥作用。
另有研究表明[6,19]在茶鲜叶酶促发酵中表儿茶素在氧化的同时,会降低生成的茶黄素及茶黄素单没食子酸酯,而对茶黄素双没食子酸酯的影响较小,同时简单儿茶素则消耗较小,说明茶黄素与儿茶素在同一体系中共同清除自由基时,相对弱的儿茶素或茶黄素充当修复剂的作用,而保护了先被自由基攻击的抗氧化物质。
4 结论
儿茶素与茶黄素的抗氧化能力主要表现为单因子独立效应,并且各组中ECG或TF-DG在该体系清除自由基中发挥了将近一半的作用,而其余成分则是发挥着补充修复的作用。两组中各因素的交互作用相对来说弱很多。另外,虽然大量关于儿茶素及茶黄素的抗氧化能力的强弱研究,但是对于茶鲜叶中的茶黄素含量偏低于理论含量,至今仍然不清。更好的基础性的理解涉及到关于儿茶素在氧化过程中的自由基的生成,所以需要研究清楚。至此,更进一步的研究关于儿茶素的酶促氧化及茶黄素合成仍需要进行详细的研究,这不仅关系到茶叶的品质,更重要的是让茶叶发挥应有的保健功效,其意义深远。
1 College of anhui agronomy(安徽农学院主编).Manufacture of Tea(制茶学),2edEd.Beijing:China Agriculture Press,1979.1-25.
2 Wan XC(宛晓春).Tea Biochemistry(茶叶生物化学),1stEd.Beijing:China Agriculture Press,1987.319-358.
3 Joshua DL,Yang CS.Mechanisms of cancer prevention by tea constituents.J Nutr,2003,133:3262s-3267s.
4 David JM,Lu GP,Nai SC,et al.Cholesterol-lowering effect of a theaflavin-enriched green tea extract.Arch Intern Med,2003,163:1448-1453.
5 Sabu MC,Priya TT,Ramadasan K,et al.Beneficial effects of green tea:a literature review.Chin Med(中国医药),2010,5:13.
6 Shen DY(沈丹玉).Studies on Reaction Characteristics and Optimization of liquid-state fermentation for the production of black tea beverage by flesh leaves.Beijing:Chinese Academy of Agircultural Sciences(中国农业科学院),MSc.2009.
7 Lin XR(林小端).Analysis of the variation of catechins content in oolong tea germplasm resources.Fuzhou:Fujian Agriculture and Forest University(福建农林大学),Msc.2009.
8 Subramanian N,Venkatesh P,Ganguli SY,et al.Role of polyphenol oxidase and peroxidase in the generation of black tea theaflavins.J Agric Food Chem,1999,47:2571-2578.
9 Tu YF(涂云飞),Mao ZF(毛志芳),Yang XF(杨秀芳).Mobile injection and chemical illumination for determining the antioxidation capacity of tea.Chin Tea Proc(中国茶叶加工),2009,1:42-45.
10 Cheng ZY,Yan GT,Li YZ,et al.Determination of antioxidant activity of phenolic antioxidants in a Fenton-type reaction system by chemiluminescence assay.Anal Bioanal Chem,2003,375:376-380.
11 Yuan ZF(袁志发),Zhou JQ(周静芉).Design of Experiment and Analysis(试验设计与分析),2ed.Beijing:Higher Education Press,2000.381.
12 Lai KL,Su YL,Chen RY,et al.Theaflavins in black tea and catechins in green tea are equally effective antioxidants.J Nutr,2001,131:2248-2251.
13 Salah N,Miller NJ,Paganga G,et al.Polyphenolic flavanols as scavengers of aqueous phase radicals and as chain-breaking antioxidants.Arch biochem Biophys,1995,22:339-346.
14 Chen CW,Ho CT.Antioxidant properties of polyphenols extracted from green and black teas.J Food Lipids,1995,2:35-46.
15 Shen SR(沈生荣),Yang XQ(杨贤强),Yang FJ(杨法军),et al.Coordinatingly synergic effect of catechins during their antioxidation.Tea Sci(茶叶科学),2003,2:141-146.
16 Chen LJ(陈留记),Yang XQ(杨贤强),Shen SR(沈生荣),et al.Mechanismof Scavenging Reactive Oxygen Radicals of Tea catechins.J Zhejiang Univer,Agri&Life Sci(浙江大学学报,农业与生命科学版),2002,28:573-574.
17 Zhang HY(张红雨),Wang LF(王兰芬).Quantum chemical study of molecular mechanism for green tea poly phenols to scavenge peroxyl radicals.J Zibo Univ(Nat Sci Ed)(淄博学院学报,自科与工程版),2002,3:5-10.
18 Sobodan VJ,Yukihiko H,Steen S,et al.Antioxidant potential of theaflavins.A pulse radiolysis study.J Am Chem Soc,1997,119:5337-5343.
19 Krishan LB,Toyomasa A,Tojiro T,et al.Effects of(-)-epicatechin on oxidation of theaflavins by polyphenol oxidase from tea leaves.Agric Biol Chem,1987,7:1767-1772.
Antioxidant Capability of Epi-catechins and Theaflavins In Vitro by Scavenging Hydroxyl Free Radical
TU Yun-fei*,YANG Xiu-fang,KONG Jun-hao,ZHANG Shi-kang,ZHU Yue-jin,WANG Yin-feng
Hangzhou Tea research institute,All-China Federation of Supply and Marketing Co-operatives,Hangzhou 310016,China
In this paper,the scavenge ability of hydrogen free radical for both catechins(groupⅰ)and gallate catechintheaflavins(groupⅱ)was investigated by the method of quadratic general rotate regression design.The results indicated that the scavenge ability of each group increased along with the increasing content of each component in the system,except for TF-D-G which mainly played important role at the low concentration.In groupⅰ,the scavenge ability of of each component was in order of ECG>EC>EGCG,and the contribution ratio of ECG in this system was more than 43%,which in sharp contrast to negligible component of EGC.As for groupⅱ,the order of each component in the scavenge ability was TF-D-G>TF-M-G>ECG>EGCG>TF,and the contribution ratio of TF-D-G exceeded 50%.Interestingly,the gallate catechins could not effectively play the role of scavenging the hydrogen free radicals when they mixed with theaflavins.And the synergy effect of components in corresponding group was weak.
catechins;theaflavins;hydrogen free radical;chemiluminescence;flow injection analysis
Q599.5
A
1001-6880(2012)05-0653-07
2011-06-07 接受日期:2011-10-31
浙江省自然科学基金项目(Y3100683)
*通讯作者 Tel:86-571-86032092;E-mail:tyfaf@sohu.com
