多巴胺检测新方法的研究
2012-09-14陈德志陈巧辉甘惠贞杨昌云
陈德志,陈巧辉,甘惠贞,杨昌云
(中国人民解放军第一八零医院静脉药物配液中心,福建 泉州 362000)
多巴胺(DA)是体内合成肾上腺素的前体,用于各种类型休克,目前其检测方法主要有流动注射化学发光法[1-4]、高效液相色谱法[5]及荧光法[6]。这些方法都需要复杂的前处理过程,灵敏度较低,不便于快速、灵敏检测DA。笔者利用循环伏安法电聚合研制了溴百里香酚蓝聚合膜修饰电极,研究DA[7]在修饰电极上的伏安行为,建立了抗环血酸(AA)和尿酸(UA)同时存在时DA定量检测的电化学新方法,并将该法用于实际样品盐酸多巴胺注射液的含量检测,结果令人满意。
1 材料与方法
1.1 仪器与试药
CHI660C型电化学分析仪(上海辰华仪器有限公司);三电极系统:工作电极为玻碳电极,对电极为铂丝电极,Ag/AgCl电极为参比电极。溴百里香酚蓝(BTB,国药集团上海化学试剂公司)用稀碱配制成1mmol/L的溶液;多巴胺用稀盐酸配制成1×10-2mol/L的溶液,抗坏血酸配制成1×10-1mol/L的水溶液,尿酸用稀碱配制成1×10-2mol/L的溶液,以上试剂均由中国药品生物制品检定所提供;配制 0.1mol/L 磷酸盐缓冲体系 (PBS,pH=5.0,50mmol/L磷酸二氢钠-磷酸氢二钠和20mmol/L的氯化钠);盐酸多巴胺注射液(广州白云山明兴制药有限公司,浓度10 g/L,批号071101);维生素C注射液(福州海王福药制药有限公司,浓度0.25 g/L,批号080107);其他试剂均为分析纯,全部溶液均用二次蒸馏水配制。
1.2 试验方法
BTB膜修饰电极的制备:电聚合前将玻碳电极0.05μm氧化铝粉末和水的混合物在麂皮上抛光,再依次经1∶1 HNO3和水、无水乙醇和二蒸水超声清洗。然后将电极置于铁氰化钾溶液中表征,在-0.2~+0.8 V电位区间扫描循环伏安曲线CV图至电位差小于0.080 V为止。将处理好的电极置于含0.3mmol/L BTB的 PBS缓冲液(pH=5.0)中,于 -0.8 ~ +1.8 V 电位区间内,以100mV/s的扫描速率聚合30圈。将聚合好的电极用蒸馏水清洗干净后,放在磷酸盐缓冲液中保存备用。
聚合膜电催化性质:以BTB修饰玻碳电极作为工作电极,在-0.2~+0.8 V电位区间内由循环伏安法研究扫描速率、聚合圈数及溶液pH值等对DA电催化过程的影响。
差示脉冲伏安法测定:以磷酸盐缓冲液(pH=5.0)作为测定底液,在-0.2~+0.8 V电位区间内,测定DA的差示脉冲伏安曲线,以空白溶液测定曲线进行背景校正,测量其氧化峰电流,研究其性质。每次扫描结束后,将电极置PBS缓冲液中循环扫至稳定,即可更新电极表面,使电极有良好的重现性。
干扰试验:配置不同浓度的多巴胺溶液,在一定浓度的AA和UA存在情况下,用差示脉冲伏安法(DPV)考察BTB膜修饰电极测定DA时,AA和UA的干扰情况。
2 结果
2.1 聚BTB膜的电聚合和电化学特征
在含1 mmol/L BTB的PBS电解质溶液中,随着聚合的进行,在1.34 V处BTB单体氧化电流不断上升,显示聚PAR膜在玻碳电极上逐渐生长,见图1。

图1 电聚BTB的循环伏安图(扫描速率为100mV/s,30圈)
在0.05mol/L的硫酸中考察了BTB膜修饰电极的性质。在-0.2~+0.8 V电位内扫描出现了一对氧化还原峰(图 2 A,Epa=0.350 V,Epc=0.250 V),由 ΔEp=Epa- Epc=2.3 RT/nF(59/n mV,25℃)可推算出 n≈1,并且峰电流随着扫描速率增加而增加,峰电流和扫描速率呈现良好的线性关系(Ipa=1.541+8.044 2 υ,r=0.997 3),BTB 在电极表面反应受吸附反应动力学控制。如图2 B所示,试验考察了在pH 2.0~7.0范围内酸度对应BTB膜的电位关系,BTB膜电位与pH呈良好的线性关系(Epa=0.296 4 -0.050 21 pH,r=0.997 2),斜率(k= -0.050 21)等于 0.059 m/n(n为电子转移数),由 n=1,从而有 m≈1。说明该膜在电极表面发生单电子转移单质子转移反应。
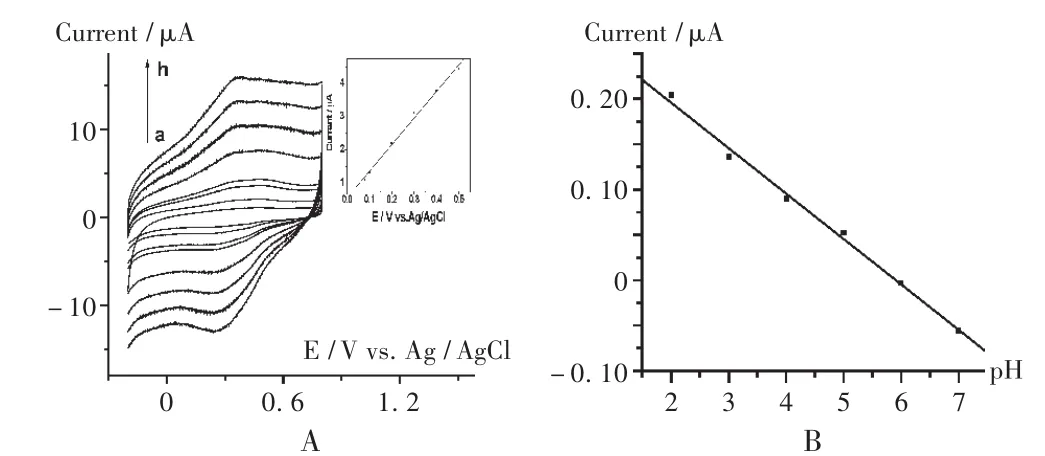
图2 聚BTB膜修饰电极不同扫描速率的CV图与变化曲线图(A)和pH对应BTB膜的电位关系(B)(扫描速率100mV/s)
2.2 DA在修饰电极上循环伏安特性
在pH=5.0的磷酸盐缓冲液中,DA分别在裸玻碳电极(a)和聚BTB修饰电极(b)上的循环伏安曲线(图3 A)。从图3 A(a)可见,在裸玻碳电极上DA应相对较弱,聚合后信号显著增强。由图3 B(a)可见,没有聚合之前,AA和DA的信号无法分离出来,聚上BTB膜后,AA、DA的信号能很好地分离开来。

图3 DA于裸电极(a)和聚BTB修饰电极 (b)的CV图与DPV图(扫描速率100mV/s)
2.3 DA测定条件的选择
聚BTB膜厚度:在pH=5.0磷酸盐缓冲液中,分别聚合10,20,30,40圈,观察多巴胺电位的影响,见图4。在聚合30圈时,DA的信号达到最大值,圈数增加,膜厚度增加,导致电极表面电子的传输受阻,信号反而下降,综合考虑选择聚合30圈进行试验。
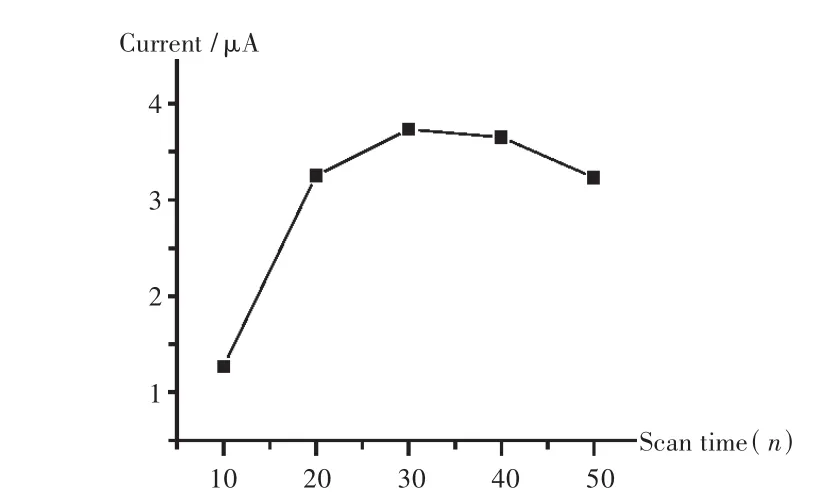
图4 BTB在玻碳电极上的不同聚合圈数对AA(200μmol/L)、DA(10μmol/L)和UA(10μmol/L)催化电流影响图(扫描速率100mV/s)
溶液pH:在聚合30圈的条件下,考察聚BTB膜修饰电极于不同酸度中对AA,DA,UA的电催化活性的影响。将AA,DA,UA在各种不同pH的磷酸盐缓冲液中进行测定,当pH=5.0时,AA,DA,UA的信号较显著,综合考虑选择pH=5.0的磷酸盐缓冲液作为底液。
2.4 工作曲线绘制
当存在一定浓度的0.2mmol/LAA和0.01mmol/LUA时,往电解池中添加不同浓度的DA时的差示脉冲伏安曲线(图5)。可见,DA 氧化峰电流与其浓度在 1.0×10-6~1.5 ×10-4mol/L范围内呈良好的线性关系(Ipa=2.38832+0.18819C,r=0.9980)。

图5 不同浓度的DA在200μmol/LAA和10μmol/LUA同时存在下的DPV曲线图及峰电流与浓度变化的工作曲线(扫描速率100mV/s)
2.5 样品及回收率的测定
准确移取10 L多巴胺注射液于10mLPBS(pH=5.0)的电解池中,按差示脉冲伏安法测定。结果注射液中多巴胺浓度为5.453 4 ×10-5mol/L,即 10.34 g/L,见表 1。符合药典标准。
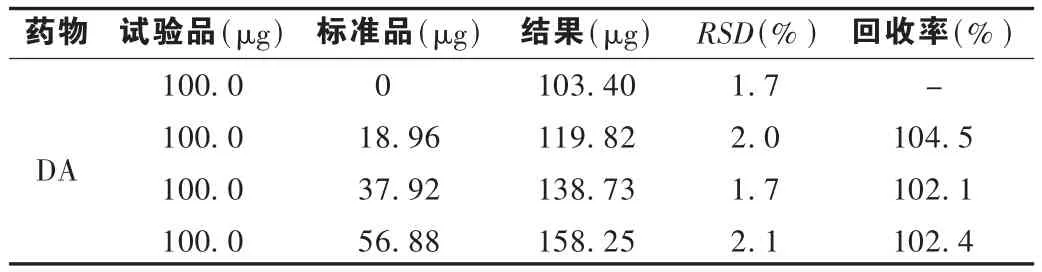
表1 多巴胺注射液测定结果
3 讨论
在此研制的聚溴百里香酚蓝导电聚合膜修饰电极对多巴胺有很强的电催化活性,其反应受吸附控制。抗坏血酸和尿酸在此聚合膜修饰电极上的响应与DA互不干扰。并且在模拟体内环境,即在存有一定浓度的AA和UA的情况下,DA氧化电流与其浓度的工作曲线线性关系良好,结果的准确度和精密度高,方法快速、简便,可为多巴胺药物质量的控制和检测提供一种快速、简便的方法。
[1]李利军,钟招亨,冯 军,等.流动注射化学发光法测定盐酸多巴胺[J].分析测试学报,2007,26(1):125 -127.
[2]于春玲,唐玉海,韩小年,等.流动注射化学发光法测定制剂和血浆中的盐酸多巴胺[J].分析测试学报,2006,25(1):119-121.
[3]王术皓,杜凌云,魏新庭,等.反相流动注射-化学发光法测定盐酸多巴胺[J].光谱学与光谱分析,2005,25(5):678-679.
[4]杜凌云,王术皓,林世蕾.流动注射协同化学发光法测定盐酸多巴胺[J].分析实验室,2005,24(7):88 -89.
[5]乔坤云,高继玲.高效液相色谱法测定尿液中儿茶酚胺类物质[J].分析科学学报,2005,21(2):219 -220.
[6]汪丛莹,庞志功,汪宝琪,等.荧光法测定SD大白鼠不同脑区的单胺类神经递质[J].分析化学,1999,27(1):102-104.
[7]陈 伟,黄丽英,林新华.聚溴酚蓝膜电极对儿茶酚的电催化性能及其应用[J].分析测试学报,2005,24(3):72 -74.
