灰毡毛忍冬芽的毒理学评价
2012-09-06李金玲徐晓玉
李金玲,张 辉,陈 刚,王 琴,徐晓玉,*
(1.西南大学药学院,重庆400716;2.重庆九龙坡区第五人民医院,重庆401329;3.重庆工商大学药物研究中心,重庆400067)
灰毡毛忍冬(Lonicera macranthoides Hand-Mazz)俗称大花忍冬,是中国药典规定的山银花项下的品种之一。灰毡毛忍冬的花蕾具有清热解毒、凉散风热的功效,现代药理研究发现其有抗炎、抗菌、抗病毒、保肝、免疫调节、降血脂等作用[1]。灰毡毛忍冬的藤[2-3]也具有药用价值,有祛风除湿,通络止痛的功效,用于治疗肢体关节风湿痹痛。重庆灰毡毛忍冬产量大、发展快[4],为当地山区农民带来了良好的经济效益。但是,目前国内外对灰毡毛忍冬的利用[5]主要集中在花、茎、叶、藤上,对于灰毡毛忍冬芽的利用还未见报道。课题组为了进一步拓展灰毡毛忍冬的药用价值,充分利用药材资源,增加药农的收入,对灰毡毛忍冬芽进行了系列研究,拟开发成为新的药用部位或者茶叶原料,相关论文已有发表[6]。本文按照2005年颁布的《新药(中药)研究指导原则》[7-9]对灰毡毛忍冬芽进行了急性毒性、亚急性毒性等系列研究,旨在对灰毡毛忍冬芽的毒理学做出初步的客观评价。
1 材料与方法
1.1 材料与仪器
灰毡毛忍冬芽 采自重庆秀山坝芒基地,批号:110510;本研究所用的各种血液生理生化试剂盒 南京建成生物工程研究所;灌胃用的灰毡毛忍冬芽提取物供试液 按干燥灰毡毛忍冬芽(g)∶蒸馏水(mL)=1∶10煮沸提取3次,每次45min,合并提取液并真空加热干燥,配制1000mL浓度为1500、750、375mg·mL-1的灰毡毛忍冬芽提取物供试液,4℃保存备用;SPF级昆明种小鼠 体重18~22g;SPF级 SD大鼠 体重180~220g;均为雄性,购于重庆医科大学实验动物中心,生产许可证号:SCXK(渝)2007-0001,饲养于西南大学药学院SPF级实验动物中心,使用许可证号:SCXK(渝)2009-0002。
Eos-Bravo自动生化分析仪 意大利HOSPITEX DIAGNOSTICS s.r.l公司;CM1900冰冻切片机德国徕卡仪器有限公司;BI-2000医学图像分析系统 成都泰盟科技有限公司。
1.2 实验方法
1.2.1 急性毒性实验
表1 灰毡毛忍冬芽对小鼠体重的影响±s,n=10)Table 1The effect of Lonicera bud on weight of mice(±s,n=10)

表1 灰毡毛忍冬芽对小鼠体重的影响±s,n=10)Table 1The effect of Lonicera bud on weight of mice(±s,n=10)
?
表2 灰毡毛忍冬芽对大鼠体重及体重增长的影响(单位:g;±s,n=10)Table 2Effect of Lonicera bud on weight and weight gain of rats(unit:g;±s,n=10)
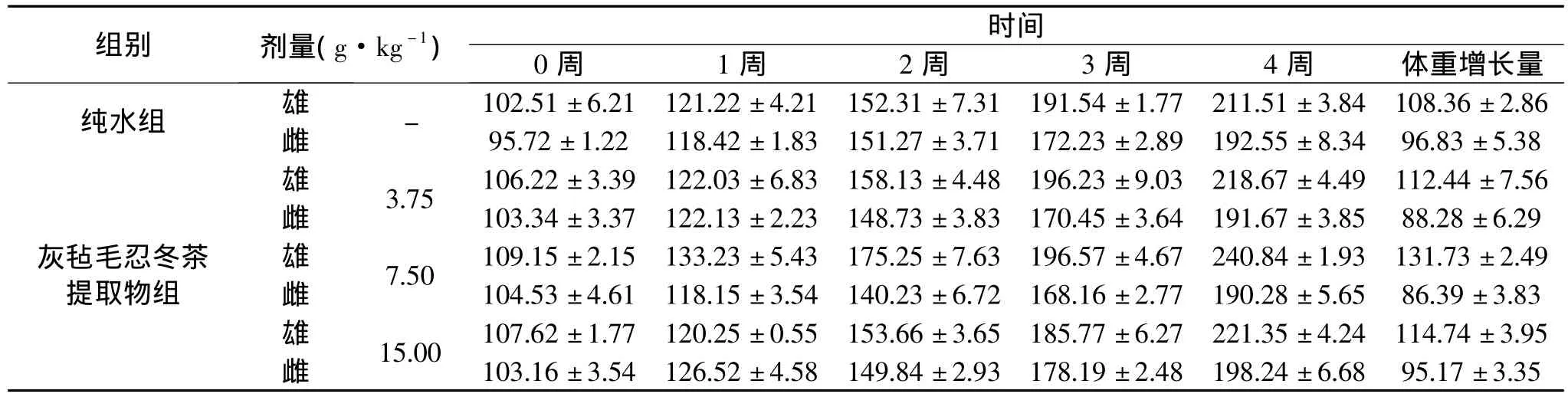
表2 灰毡毛忍冬芽对大鼠体重及体重增长的影响(单位:g;±s,n=10)Table 2Effect of Lonicera bud on weight and weight gain of rats(unit:g;±s,n=10)
?
1.2.1.1 预实验 取昆明种小鼠16只,雌雄各半,分成4组,每组2只,分别按1、5、15g·kg-1(最大耐受量)给药,若在某个剂量上给药后动物死亡,则从低一级剂量(例如5g·kg-1)开始给药,每组增加剂量5g·kg-1,直到出现动物死亡为止[10-11],得到 Dmax,对所有死亡动物进行尸检。
1.2.1.2 正式实验 选用健康、成熟,体重18~22gKM小鼠20只,雌雄各半。按实验的最大给药剂量给药一次,连续观察14d,并称量小鼠给药前、给药后第3、7、14d的体重。小鼠的一般症状(皮肤、毛发,行为活动,呼吸,心跳,眼泪、瞳孔和饮食等)和死亡情况,对死亡动物进行尸检并记录死亡原因,必要时做病理检查。
1.2.2 亚急性毒性实验 SD大鼠,180~220g,雌雄各半,80只随机分为4组,每组20只,对照组给予纯水,忍冬芽提取物三个剂量组,按高中低剂量分别给1500、750、375mg·mL-1浓度的供试药液 2mL,折合生药量为15、7.5、3.75g·kg-1。各组灌胃给药,每天一次,给药前4h,给药后2h动物禁食不禁水,其他时间自由饮食。实验期间观察动物的一般症状,每周称重。喂养30d后,股动脉取血做生化指标及血常规测定,对肾、肝、脾等称重,并做相应的病理学检查[12-13]。观察的指标主要有:
a.一般情况观察:记录动物的一般症状(皮肤、毛发,行为活动,呼吸,心跳,瞳孔、眼泪和饮食等)、死亡情况和每周体重等。
b.血液学指标:血红蛋白、血小板数、红细胞计数、白细胞计数。
c.血液生化指标:谷丙转氨酶(ALT)、谷草转氨酶(AST)、尿素氮(BUN)、血糖(GLU)、白蛋白(ALB)、肌酐(CR)、甘油三酯(TG)、总蛋白(TP)和总胆固醇(TCH)。
d.病理检查:脏体比(脏器系数)、大体观察及病理组织检查。
1.2.3 数据处理 用SPSS 18.0对相关数据进行t检验或单因素方差分析。
2 结果与分析
2.1 急性毒性实验结果
2.1.1 预实验结果 当剂量达到15g·kg-1时小鼠仍未死亡,因此未能测出LD50,初步确定了最大耐受量为 15g·kg-1。
2.1.2 正式实验结果 给药2h内,小鼠活动减少、食量减少,12h后症状基本消失,24h后症状完全消失。13d实验恢复期间,20只小鼠无死亡,其毛色、活动和饮食均正常。在给药前,给药后3d、7d、14d动物称重(表1),显示体重随周龄而增长,且雌雄各组间无显著性差异。确定了灰毡毛忍冬芽对小鼠经口的最大给药量为15g·kg-1·BW,说明灰毡毛忍冬芽对小鼠正常生长影响小,安全性高。
2.2 亚急性毒性实验结果
2.2.1 一般体征观察 实验期间各组的雌、雄大鼠均正常生长,各组动物皮毛光滑、毛色正常,无死亡[14-16]。给药30d后,各剂量组雌、雄大鼠的体重增长情况良好,雄性大鼠体重增长都略高于雌性大鼠,但各剂量组的体重和体重增重与纯水组相比无显著性差异(p>0.05),大鼠体重及体重增长变化值见表2。
2.2.2 血液学指标 见表3。大鼠给药30d后,在血液学各项指标中,各剂量组与纯水组比较无显著性差异(p>0.05),均在正常值范围内。
2.2.3 血液生化指标 见表4。大鼠给药30d后,各剂量组的血液生化指标与纯水组比较无显著性差异性(p>0.05),均在正常值范围内。
2.2.4 病理组织检查 见表5。解剖后经切片、染色、镜检检查,大体标本未发现明显病变。取各脏器称重比较知各组脏器系数与纯水组相比差异无显著性(p>0.05。
3 讨论
通过急性毒性实验确定了灰毡毛忍冬芽对KM小鼠的最大给药量为15g·kg-1·BW,据此可以得出结论,灰毡毛忍冬芽的急性毒性很小,在常规剂量下服用是安全可靠的。从急性毒性来看,饮用灰毡毛忍冬芽具有很高的安全性,但是任何事物都有一个合理的使用范围,超过这个限量就不可能发挥好的作用,据研究大鼠在摄入过高量的蒸馏水也会致死,因此科学地饮用灰毡毛忍冬芽则是饮茶健身的必然要求。
表3 灰毡毛忍冬芽灌胃给药30天对大鼠血液的影响(±s,n=10)Table 3Effects of Lonicera bud on rats’blood by ig in 30 days(±s,n=10)
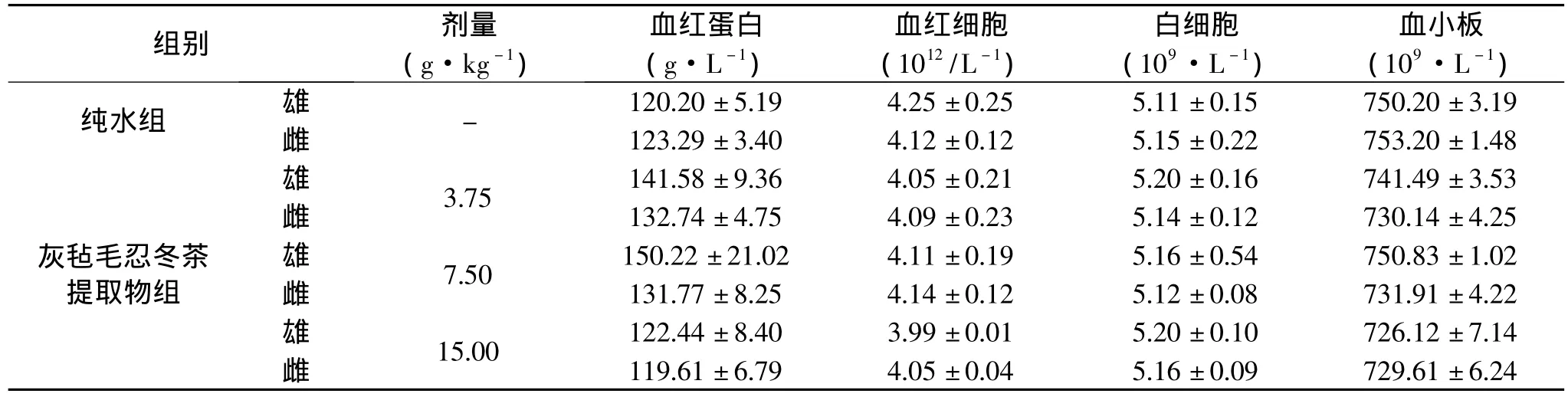
表3 灰毡毛忍冬芽灌胃给药30天对大鼠血液的影响(±s,n=10)Table 3Effects of Lonicera bud on rats’blood by ig in 30 days(±s,n=10)
?
表4 灰毡毛忍冬芽灌胃给药30天对大鼠血液生化指标的影响(±s,n=7)Table 4Effect of Lonicera bud on biochemical indexes of rat blood by ig in 30 days(±s,n=7)
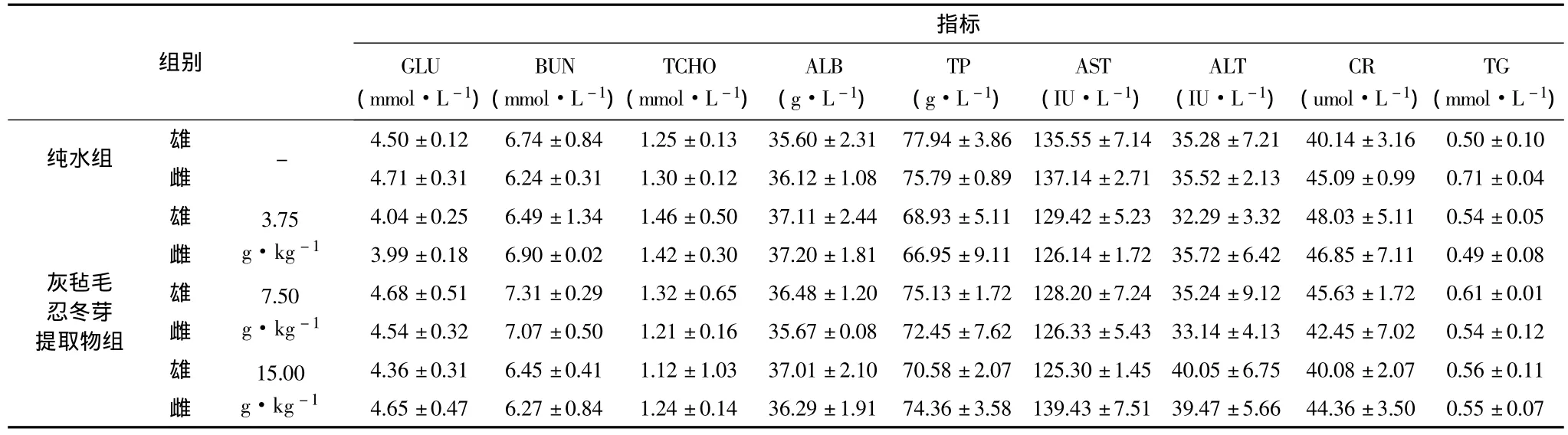
表4 灰毡毛忍冬芽灌胃给药30天对大鼠血液生化指标的影响(±s,n=7)Table 4Effect of Lonicera bud on biochemical indexes of rat blood by ig in 30 days(±s,n=7)
?
表5 灰毡毛忍冬芽灌胃给药30天对大鼠脏器系数的影响(g/100g,±s,n=10)Table 5Effect of Lonicera bud on organ index of rat by ig in 30 days(g/100g,±s,n=10)
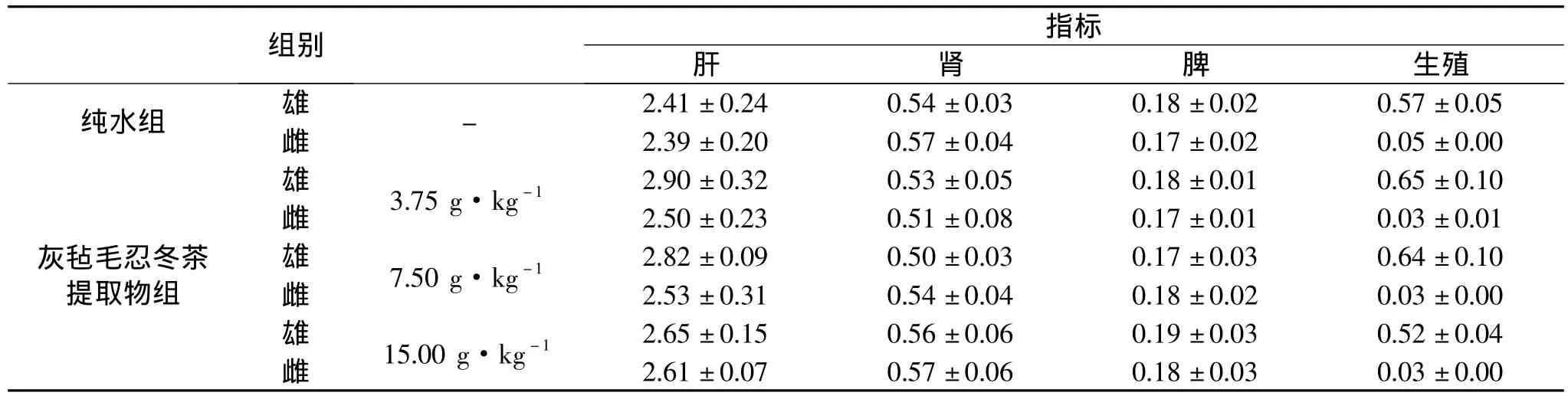
表5 灰毡毛忍冬芽灌胃给药30天对大鼠脏器系数的影响(g/100g,±s,n=10)Table 5Effect of Lonicera bud on organ index of rat by ig in 30 days(g/100g,±s,n=10)
?
通过慢性毒性实验得到灰毡毛忍冬芽对SD大鼠生长发育无不良影响,血常规、血液生化指标和脏器指数均在正常值范围内,皆无潜在的毒性作用[17-18],病理学检查未见明显病变。表明灰毡毛忍冬芽无明显毒性,可为其应用推广的安全性提供相关实验依据。
综上所述,灰毡毛忍冬芽具有丰富的营养价值,经过一定的卫生处理和加工后,对人体健康不会造成危害,可作为新食品资源进行开发利用。
[1]贾晓东,冯煦,董云发.灰毡毛忍冬中皂苷类成分的研究[J].中草药,2007,38(10):145-149.
[2]Yu C,Feng X,Xiaodong J,et al.Triterpene glycosides from Lonicera Isolation and structural determination of seven glycosides from flower buds of Lonicera macranthoides[J].Chemistry of Natural Compounds,2008,44(1):392-431.
[3]陈 敏,吴威巍,沈国强,等.灰毡毛忍冬化学成分研究[J].药学学报,1994,29(8):6172-6201.
[4]陈君,许小方,柴兴云,等.灰毡毛忍冬花蕾的化学成分[J].中国天然药物,2006,4(5):347-351.
[5]茅青,曹东,贾宪生.灰毡毛忍冬化学成分的研究[J].药学学报,1993,28(4):2732-2811.
[6]李金玲,王永胜,马强,等.忍冬茶及其加工过程中氨基酸和微量元素分析[J].食品工业科技,2012,33(12):75-78.
[7]中华人民共和国卫生部(GB/T15193,3-2003).急性毒性实验标准[S].中国国家标准化管理委会,2003:9.
[8]中华人民共和国卫生部(GB/T15193,13-2003).30天和90天喂养实验[S].中国国家标准化管理委会,2003:9.
[9]国家食品药品监督管理局.中药、天然药物研究技术指导原则[M].2005:27-34.
[10]CHEN D,MILACIC V,CHEN M S,et al.Tea polyphenols,their biological effects and potential molecular targets[J].Histol Histopathol,2008,23(4):487-496.
[11]PETER J R,JESSICA E S,SUSAN V.Time for tea mood,blood pressure and cognitive performance effects of caffeine and theanine administered alone and together[J].Psychopharmacology,2008,195(4):569-577.
[12]MANDEL S A,AMIT T,KALFON L,et al.Targeting multiple neurodegenerative diseases etiologies with multimodal-acting green tea catechins[J].J Nutr,2008,138(8):1578-1583.
[13]王冬平,隋丽华,尚世臣,等.清洁级SD大鼠血液生理生化指标的测定[J].中国比较医学杂志,2009,19(9):44-46.
[14]杨锋,王红星,何永亮,等.清洁级、SPF级SD大鼠血液生理、生化测定与比较[J].四川动物,2008,27(4):648-650.
[15]王菌,楼正清,来伟旗.SD大鼠血液生化指标正常参考值探讨[J].卫生毒理学杂志,2001,15:122.
[16]YE Pian,ZHANG Shuling,ZHAO Lei,et al.Tea polyphenols exerts anti-hepatitis B virus effects in a stably HBV-transfected cell line[J].Journal of Huazhong University of Science and Technology:Medical Sciences,2009,29(2):169-172.
[17]付立杰.现代毒理学及其应用[M].上海:上海科学技术出版社,2001:134-136.
[18]沈建忠.动物毒理学[M].北京:中国农业出版社,2002:256-258.
