米格列奈钙分散片溶出度测定
2012-08-24黄牧童曹建英宋劲燕戚可人
黄牧童 曹建英 宋劲燕 戚可人 程 琳
1.天津南开允公医药科技有限公司,天津 300384;2.天津天士力现代中药资源有限公司,天津 300410
米格列奈钙分散片溶出度测定
黄牧童1曹建英1宋劲燕1戚可人2程 琳2
1.天津南开允公医药科技有限公司,天津 300384;2.天津天士力现代中药资源有限公司,天津 300410
目的建立米格列奈钙分散片溶出度的测定方法方法以水900 mL为溶剂,桨法,转速为50 r/min,溶出度的测定采用高效液相色谱法结果米格列奈钙在7.15~11.55 μg/mL范围内,线性关系良好(r=0.999 9),平均回收率为100.03%。 结论 建立的米格列奈分散片溶出度测定方法简便、准确、可靠,可较好地控制该片质量。
米格列奈钙分散片;溶出度;高校液相色谱;测定
当今,糖尿病的发病率日益增高,米格列奈是一种新型的促进胰岛素分泌的降糖药物,化学名为(-)-2(S)-苄基-4-(顺式-全氢化异吲哚-2-基)丁酸,常以钙盐米格列奈钙存在[1-3]。米格列奈钙是用以恢复或替代早期相胰岛素分泌的抗高血糖新药。它可使胰岛细胞膜上的K+-ATP通道关闭,使细胞内Ca2+浓度增加而使细胞外含胰岛素的囊泡脱粒[4-5]。米格列奈钙促进餐时胰岛素分泌起效快,作用时间短,引起低血糖的危险性较小,在摸拟餐时正常胰岛素分泌模式、降低餐后血糖水平方面有着杰出表现[6-7]。本文考察了米格列奈钙分散片的体外溶出行为,建立了其溶出度的测定方法。
1 仪器与试剂
1.1 仪器
BP211D电子天平(德国赛多利斯股份公司);ZRS-8G型智能溶出试验仪(天津大学无线电厂);Aglient 1260系列高效液相色谱仪(美国安捷伦科技有限公司);DELTA 320S pH计(梅特勒-托利多仪器(上海)有限公司)。
1.2 试剂
米格列奈钙分散片(10 mg/片,南开允公医药科技有限公司,批号:110824,110825,110826);米格列奈钙对照品(纯度99.92%,南开允公医药科技有限公司),磷酸、乙腈均为色谱纯,水为纯化水。
2 实验方法与结果
2.1 米格列奈钙分散片的制备
按处方量比例将乳糖、微晶纤维素、预胶化淀粉、低取代羟丙纤维素、阿司帕坦分别粉碎,过100目筛,按等量递增法充分混匀,同法与已过120目筛的米格列奈钙混合。用2%羟丙甲纤维素水溶液,24目筛制粒,于50℃干燥,24目筛整粒;加入硬脂酸镁、滑石粉混匀,测定半成品含量,压片,包装,即得。
2.2 测定方法的确定
2.2.1 溶出条件的确定 参照中国药典2010年版二部附录XC第二法[8]。以水900 mL为溶剂,桨法,转速为50 r/min,温度调至(37.0±0.5)℃。
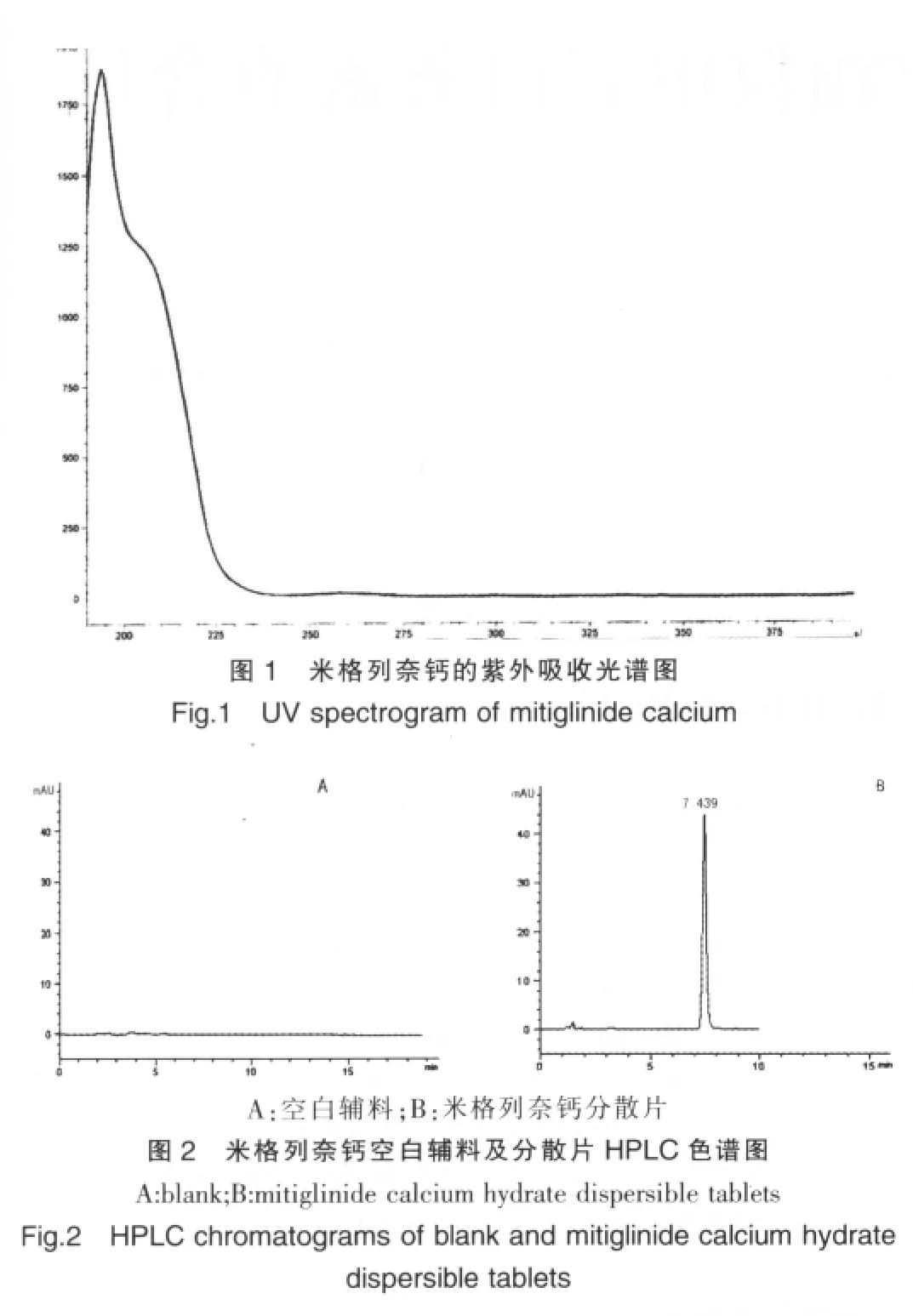
2.2.2 检测波长的确定 称取米格列奈钙对照品适量,用水溶解并稀释制成1 mL中约含米格列奈钙11 μg的溶液,精密量取20 μL注入液相色谱仪,用二极管阵列检测器检查其紫外图谱(图1)。由图1可知,米格列奈钙在193 nm处有最大吸收峰,在205 nm处有一肩峰。由于193 nm作为检测波长,其基线噪音过大,会影响测定结果,而在205 nm处吸收度较大,为兼顾各杂质的吸收灵敏度及紫外检测的基线噪音,选择210 nm作为检测波长。
2.2.3 色谱条件 色谱柱:Agilent SB-C18柱(250 mm×4.6 mm,5 μm);流动相:水溶液(用磷酸调节 pH 值为 2.4)-乙腈(55∶45);检测波长:210 nm;流速:1 mL/min;柱温:30℃;进样量:20 μL;理论塔板数大于2 000。在本色谱条件下,米格列奈钙保留时间为7.439 min,色谱图见图2。
2.3 方法学研究
2.3.1 溶液的精密度考察 取米格列奈钙对照品适量,精密称定,用水溶解并稀释制成1 mL中约含米格列奈钙11 μg的溶液,精密量取20 μL注入液相色谱仪,记录色谱图,量取峰面积,重复6次,结果RSD为0.19%。
2.3.2 溶液的稳定性考察 取本品,以水900 mL为溶剂,转速为50 r/min,依法操作,经15 min时,取溶液10 mL,滤过,取续滤液作为供试品溶液,于不同时间分别精密量取20 μL注入液相色谱仪,记录色谱图,量取峰面积,结果见表1。

表1 溶液稳定性试验结果Tab.1 The results of Stability test for mitiglinide calcium solution
2.3.3 线性范围的测定 精密称取米格列奈钙对照品约11 mg,置100 mL量瓶中,用水溶解并稀释至刻度,摇匀,精密量取6.5、7.5、8.5、9.5、10.5 mL,分别置于 100 mL 量瓶中,用水稀释至刻度,摇匀,精密量取20 μL,注入液相色谱仪,记录色谱图,量取峰面积,以浓度C(μg/mL)对峰面积A进行线性回归,得回归方程为:A=41.52 C+67.732,r= 0.999 9。结果表明,米格列奈钙的浓度在7.15~11.55 μg/mL范围内,线性关系良好。
2.3.4 回收试验 分别取米格列奈钙约7.15、9.35、11.55 mg,精密称定,分别置于100 mL量瓶中,按处方量比例加入空白辅料,加水溶解并稀释至刻度,摇匀,滤过,精密量取续滤液1 mL,分别置于10 mL量瓶中,用水稀释至刻度,摇匀,作为供试品溶液,精密量取20 μL,注入液相色谱仪,记录色谱图,量取峰面积,计算回收率,结果见表2。
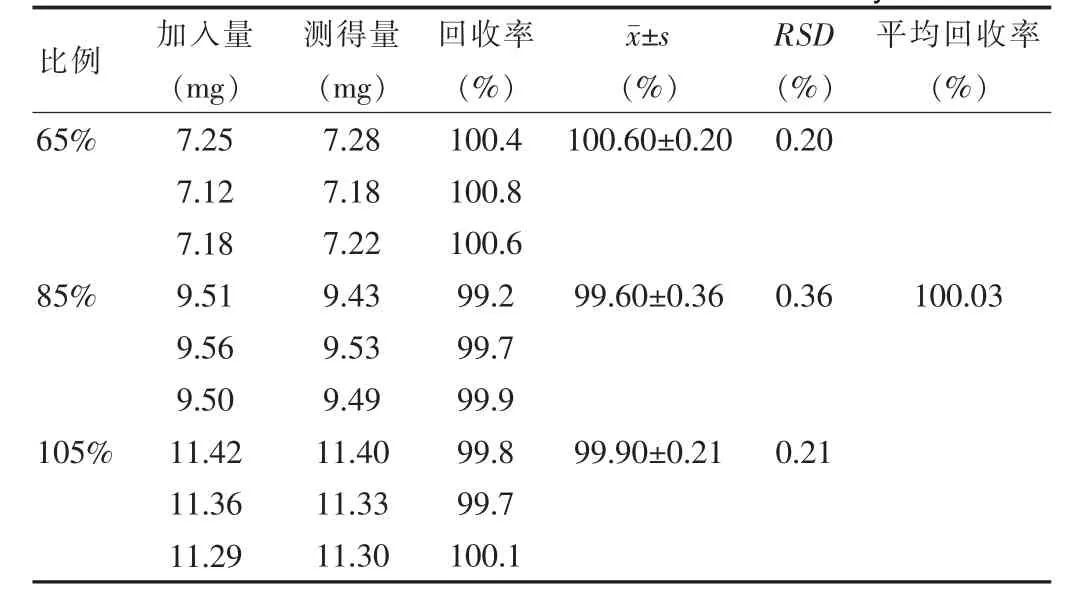
表2 回收试验结果Tab.2 The results of determination of recovery
2.4 溶出度的测定
2.4.1 溶出度的测定方法 取本品,以水900 mL为溶剂,转速为50 r/min,依法操作,经15 min时,取溶液10 mL,滤过,取续滤液作为供试品溶液;另取米格列奈钙对照品适量,精密称定,用水溶解并稀释制成每1毫升中约含11 μg的溶液作为对照品溶液。照2.2.3项下色谱条件,取上述两种溶液各20 μL注入液相色谱仪,记录色谱图。按外标法以峰面积计算出每片的溶出量,限度为标示量的85%。
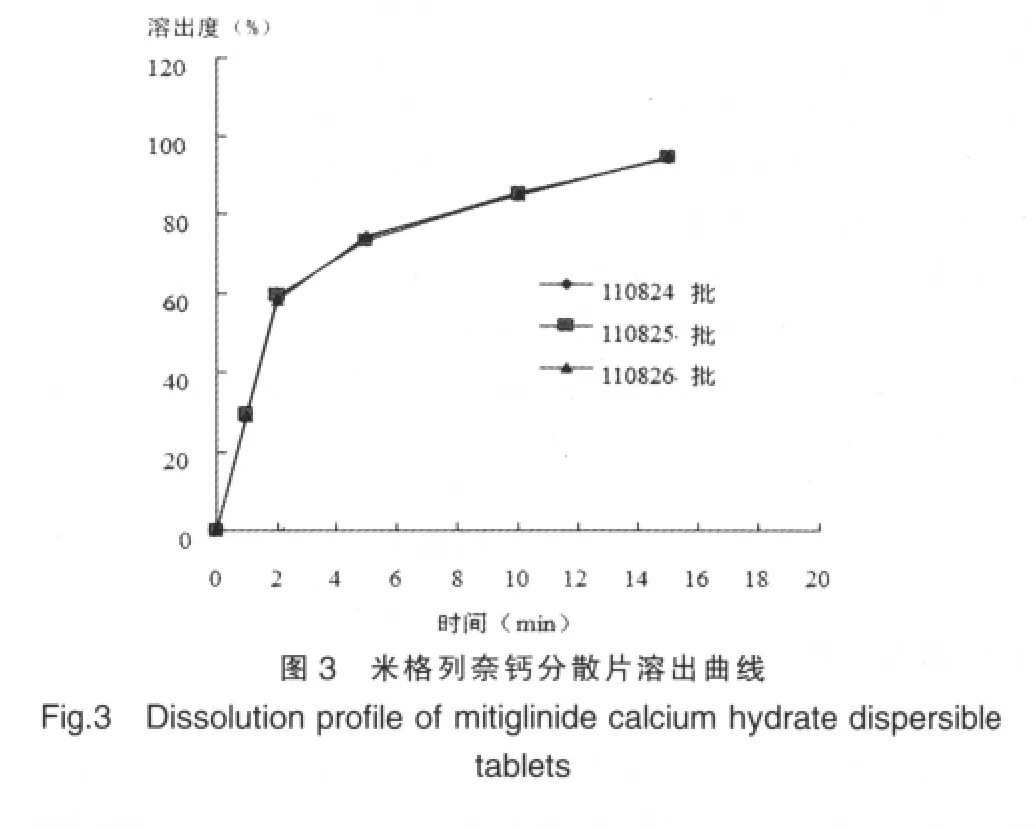
2.4.2 溶出曲线的绘制 取本品3批,依法操作,分别于1、2、5、10、15 min取样(并立即补充等体积新鲜溶出介质),滤过,取续滤液作为供试品溶液,依法测定,计算,即得。溶出曲线见图3。
2.4.3 溶出度测定结果 用本法测定了3批米格利奈钙分散片15 min时的溶出度,溶出度测定结果见表3。
3 结论
本实验采用HPLC法测定米格列奈钙分散片的体外溶出结果,色谱峰形好,辅料不干扰测定,方法简便、快捷,线性关系良好,回收率高,重现性好。
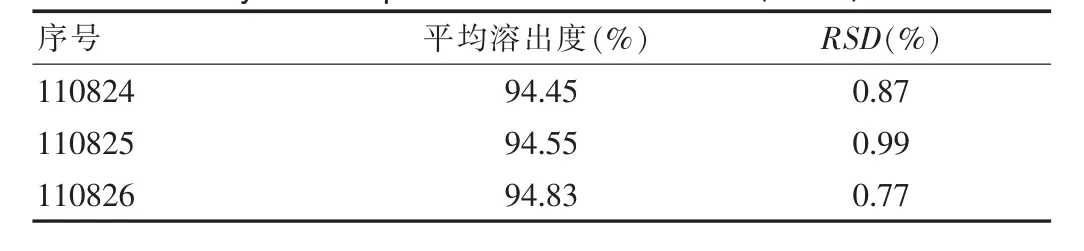
表3 15 min时米格列奈钙分散片溶出度测定结果(n=6)Tab.3 The results of dissolution of mitiglinide calcium hydrate dispersible tablets at 15 min(n=6)
从米格列奈钙分散片溶出曲线可以看出米格列奈钙分散片3批样品,在10 min时,溶出量均可达到标示量的80%以上,在15 min时,则可溶出标示量的94%以上。
通过米格利奈钙分散片的溶出度测定结果,可知3批米格利奈钙分散片15 min时的溶出度为94.45%、94.55%、94.83%,RSD为 0.87%、0.99%、0.77%,均符合规定。
综上所述,本文建立了一个可行的溶出度测定方法,用此法可较好地控制本片质量。
[1]梁海霞,郝光涛,权苗苗,等.HPLC-MS/MS测定人血浆中米格列奈钙的浓度[J].药物分析杂志,2010,30(4):596-599.
[2]高凤英,赵铁耘,李芳,等.国产米格列奈钙片治疗2型糖尿病的多中心临床研究[J].四川大学学报(医学版),2011,42(4):580-582.
[3]刘伦德,聂丽华,周亚球.HPLC测定米格列奈钙原料药的含量及有关物质[J].安徽医药,2010,14(3):291-293.
[4]李娜,康后生,陈玉华,等.米格列奈钙治疗初诊2型糖尿病的临床疗效观察[J].医学理论与实践,2011,24(15):1768.
[5]张俊,张啟智,彭文兴,等.UPLC-MS/MS法测定米格列奈钙片血药浓度及其药动学研究[J].中南药学,2010,8(10):126-128.
[6]滕香宇.格列奈类促胰岛素分泌剂治疗2型糖尿病[J].世界临床药物,2005,26 (12):722-725.
[7]吉同琴,唐燕平.HPLC法测定米格列奈钙中的R-异构体含量[J].药学与临床研究,2007,15(4):336-338.
[8]国家药典委员会.中华人民共和国药典[S].二部.北京:中国医药科技出版社,2010:附录85-87.
Dissolution determination of mitiglinide calcium hydrate dispersible tablets
HUANG Mutong1CAO Jianying1SONG Jinyan1QI Keren2CHENG Lin2
1.Tianjin Nankai Share Pharmaceutical Science and Technology Co.,Ltd.,Tianjin 300384,China;2.Tianjin Tasly Mordern TCM Resources Co,Ltd.,Tianjin 300410,China
ObjectiveTo develop a method for dissolution determination of mitiglinide calcium hydrate dispersible tablets.MethodsThe dissolution was determined with paddle method(50 r/min)in 900 mL water.Mitiglinide calcium was detected by high performance liquid chromatography(HPLC).ResultsThere was a good linearity over the range of 7.15 to 11.55 μg/mL with a correlation coefficient r=0.999 9.And average recovery was 100.03%.ConclusionThe method is simple,accurate,reliable and the quality of the mitiglinide calcium hydrate dispersible tablets can be well controlled by this method.
Mitiglinide calcium hydrate dispersible tablets;Dissolution;High performance liquid chromatography;Determination
R969.1
A
1674-4721(2012)10(c)-0064-03
2012-06-13 本文编辑:郭静娟)
