Cu2+/Zn2+对牛血清白蛋白-盐酸小檗碱结合过程的变构效应
2012-07-28徐列兵陈世云赵英杰
李 磊,徐列兵,陈世云,赵英杰
(1.中国石油集团石油职业卫生技术服务中心,河北 廊坊 065000;2.中国石油管道公司济南输油分公司,山东 济南 250014;3.廊坊师范学院管理学院,河北 廊坊 065000)
多种小分子(离子)物质同时与生物大分子结合及彼此间的影响已经引起研究者的关注[1~5]。Chen等[6]利用生物作用色谱(Biointeraction chromatography)技术以血清白蛋白为固定相考察了一种药物(变构剂)对另一种药物与蛋白质结合所产生的变构效应(Allosteric effect)[6~8],报道了蛋白质-药物结合的定量变构系数,为探讨多种药物分子在结合蛋白质过程中的竞争作用提供了新的思路。目前,大部分报道仅局限于金属离子对蛋白质-药物分子结合过程的影响研究[1~5],而关于金属离子对蛋白质-药物分子结合过程的变构效应少有报道。
考虑到在色谱技术中蛋白质作为固定相其原有性质可能改变以及蛋白质随流动相的洗脱损失,采用光谱技术研究药物分子对牛血清白蛋白(Bovine serum albumin,BSA)-金属离子结合过程的变构效应已有报道[9]。作者选取金属离子Cu2+、Zn2+作为变构剂,分别采用荧光光谱(FS)、紫外可见吸收光谱(UV-Vis)以及圆二色谱(CD)考察了Cu2+/Zn2+对中药有效成分盐酸小檗碱(Berberine chloride,BC)与BSA结合过程的变构效应,并从BSA分子构象转变角度对变构效应产生的可能机制进行了探讨,以期为金属离子对血浆中外源药物的储存和分布的影响以及后续生物效应的研究提供有用信息。
1 实验
1.1 试剂与仪器
牛血清白蛋白(>98%,BSA Fraction Ⅴ),上海华美生物工程公司;盐酸小檗碱,自制[10];Tris(生化试剂)、ZnCl2(分析纯)、CuCl2·2H2O(分析纯),国药集团化学试剂有限公司;其它试剂均为分析纯。
RF-5301PC型荧光光度计,日本岛津公司;TU-1901型紫外可见分光光度计,北京普析通用仪器有限责任公司;J-715型圆二色光谱仪,日本JASCO公司。
1.2 方法
分别以Cu2+/Zn2+浓度(×10-5mol·L-1)为0.2、0.4、0.6、0.8、1.0的Tris-HCl缓冲溶液(37 ℃下pH=7.4,内含0.15 mol·L-1NaCl以维持溶液离子强度)为溶剂配制1.0×10-5mol·L-1的BSA标准溶液,备用。在三角瓶中精确移入一定量1.5×10-2mol·L-1的BC甲醇标准溶液,迅速吹干溶剂,准确移入BSA标准溶液10 mL,超声分散3 min,在(37±0.1) ℃下恒温3 h至结合平衡。激发波长为295 nm,激发光栅和发射光栅狭缝宽度均为3 nm,恒温测定上述样品在300~500 nm的荧光发射光谱。
分别以Cu2+/Zn2+浓度(×10-5mol·L-1)为0.2、0.4、0.6、0.8、1.0的Tris-HCl缓冲溶液为溶剂配制1.0×10-5mol·L-1的BC溶液,测定其在300~500 nm的紫外可见吸收光谱,以相应的Tris-HCl缓冲溶液为参比。
以2.0×10-6mol·L-1的BSA的Tris-HCl溶液为溶剂配制BC与Cu2+/Zn2+成一定浓度比的Cu2+/Zn2+-BSA-BC溶液,测定其在190~250 nm 的圆二色谱(色谱条件参照文献[11,12])。
2 结果与讨论
2.1 Cu2+/Zn2+对BC猝灭BSA内源性荧光的变构效应
BSA分子中含有荧光性氨基酸残基(色氨酸、酪氨酸和苯丙氨酸),为内源性荧光物质。在Cu2+存在下,BC对BSA内源性荧光的猝灭作用见图1。
由图1可知,当激发波长为295 nm时,BSA的荧光发射峰在343 nm附近,与BSA-BC二元体系类似[10]。当BC浓度低于1.0×10-5mol·L-1时,BSA在343 nm处的荧光发射峰强度随BC浓度的增大而降低,但峰形和出峰位置基本不变;当BC浓度超过1.0×10-5mol·L-1时,BSA的荧光发射峰强度不仅随BC浓度的增大而降低,并且出现峰裂分[10]。
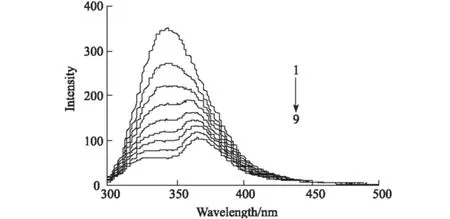
cCu2+=cBSA=1.0×10-5 mol·L-1 1~9,cBC(×10-5 mol·L-1):0,0.525,1.0,1.5,2.025,2.55,3.0,3.525,4.05
考虑到峰裂分,以荧光发射峰峰面积S代替荧光发射峰强度,按照Stern-Volmer方程和Perrin方程[即式S0/S=1+KSVcBC和式ln(S0/S)=KPcBC,式中:S和S0分别为有、无BC时BSA的荧光发射峰面积;KSV、KP为荧光猝灭常数;cBC为BC浓度][10]对0.2×10-5mol·L-1Cu2+/Zn2+存在下BC对BSA的荧光猝灭数据进行处理,结果见图2。
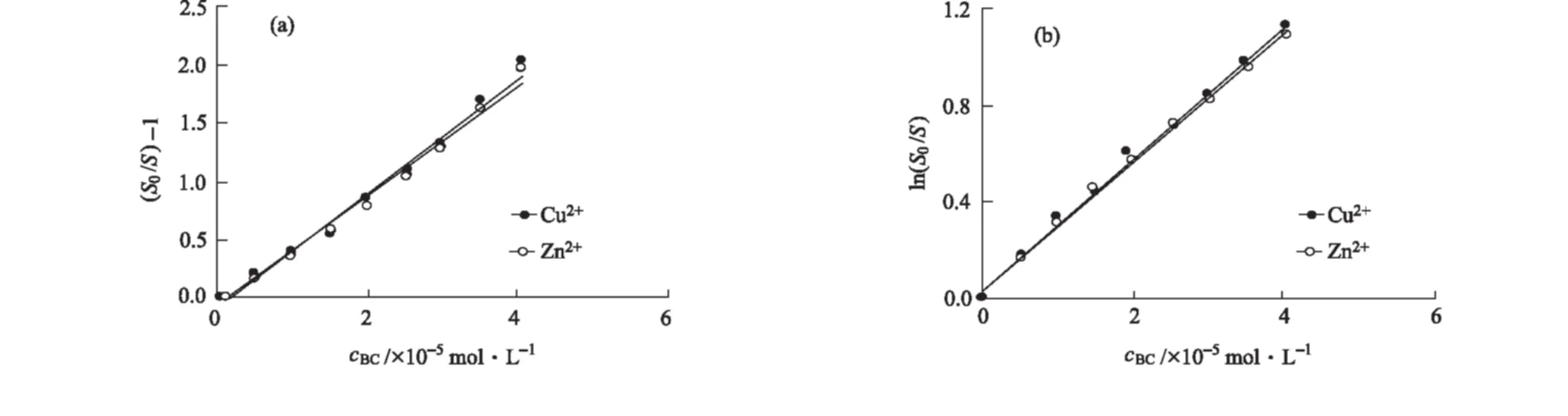
图2 Cu2+/Zn2+存在下,BSA-BC体系的Stern-Volmer(a)和Perrin(b)曲线
线性拟合得到BSA-BC体系的Stern-Volmer方程和Perrin方程,计算猝灭常数KSV、KP,结果见表1。
由表1可见,在BSA-BC体系中分别加入Cu2+、Zn2+后,各体系线性拟合后所得KSV为104数量级,由KSV=kqτ0[13][kq为扩散过程控制的双分子动态猝灭速率常数(L·mol-1·s-1),τ0为生物大分子内源性荧光寿命,对于BSA一般取6.3 ns[14]]求得双分子kq大于各种猝灭体对生物大分子的最大扩散猝灭速率常数2×1010L·mol-1·s-1 [15],可以初步判定Cu2+/Zn2+存在下,BC对BSA的荧光猝灭并非由于分子扩散和动态碰撞引起的动态猝灭,而是由于BC与BSA形成复合物而引起的静态猝灭。
参照文献[9],定义猝灭变构系数βQ=KP/KP,0,其中KP和KP,0分别为有、无Cu2+/Zn2+时BC对BSA荧光的猝灭常数,结果见表1。以βQ对金属离子浓度作图,如图3所示。
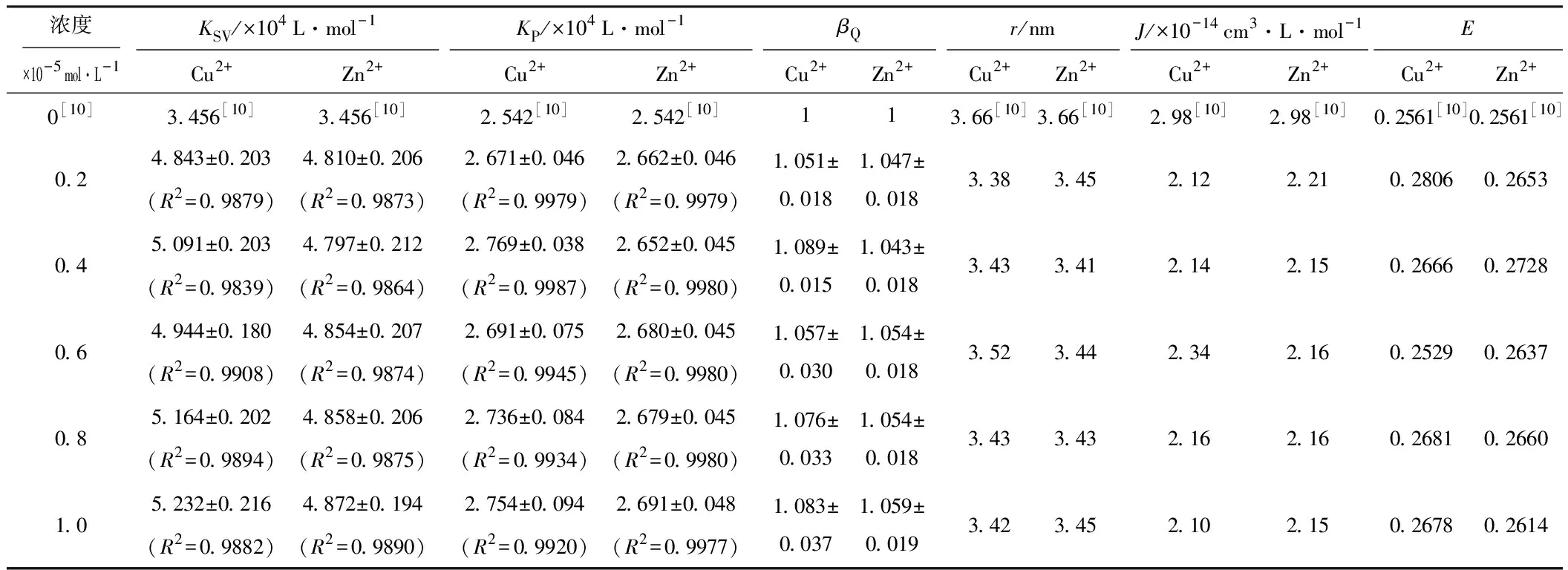
表1 Cu2+/Zn2+存在下,BSA-BC体系的KSV、KP、βQ、r、J、E
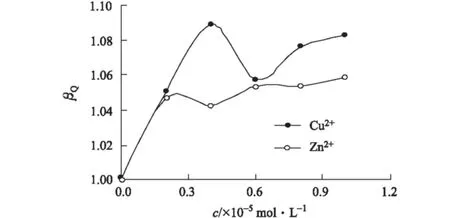
图3 βQ随金属离子浓度的变化关系
由图3可知,与BSA-BC二元体系比较,金属离子存在下BSA-BC体系的KP有所增大(即βQ>1),变构剂Cu2+/Zn2+对BC猝灭BSA内源性荧光的过程产生正变构效应,且在低浓度(<0.2×10-5mol·L-1)情况下,变构效应比较明显;随着金属离子浓度的增大,变构效应趋于平缓。与BC作为变构剂不同[9],Cu2+/Zn2+作为变构剂时,其变构效率存在饱和性,即趋于一定值,其原因可能为Cu2+对BSA内源性荧光猝灭效率远小于BC[10,16],BC一定程度“掩盖”了Cu2+的变构效应,而Zn2+本身对BSA的内源性荧光不产生猝灭效应[16]。
根据Förster无辐射的能量转移理论[17]和变构剂Cu2+/Zn2+存在下BC的紫外可见吸收光谱与BSA的荧光光谱的重叠(图4),计算变构剂Cu2+/Zn2+存在下BC与BSA荧光性氨基酸残基之间的空间距离r(K2=2/3,N=1.336,Φ=0.15[10]),结果见表1。
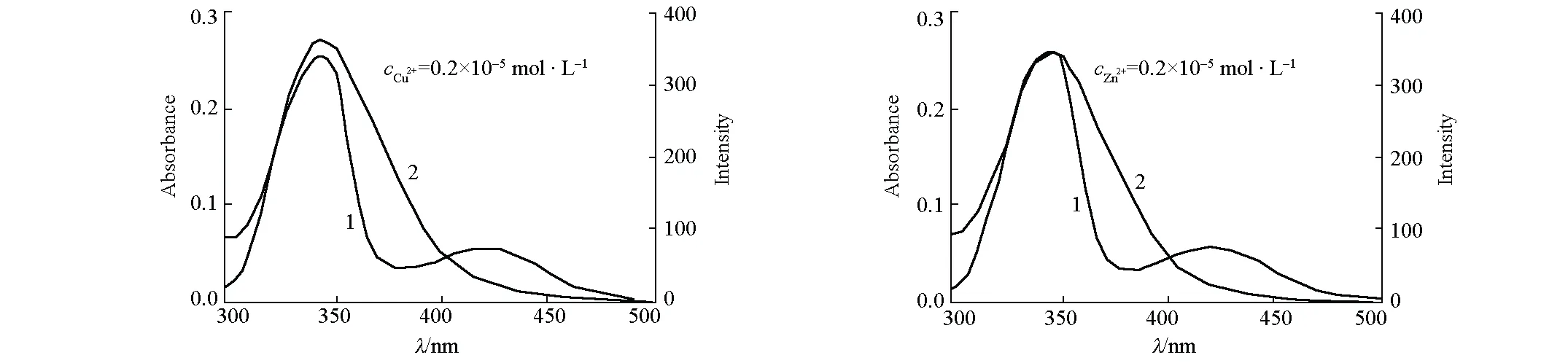
1.UV-Vis of BC 2.FS of BSA cBC=1.0×10-5 mol·L-1 cBSA=1.0×10-5 mol·L-1
由表1可知,有、无Cu2+/Zn2+存在时,r都小于7 nm,表明BC与BSA之间存在非辐射能量转移,这是发生荧光猝灭的原因之一[17]。与BSA-BC二元体系比较,Cu2+/Zn2+使BSA-BC分子间空间距离r减小,必然导致BC对BSA内源性荧光猝灭能力增强,这可能是Cu2+/Zn2+对BC猝灭BSA内源性荧光过程具有正变构效应的直接原因。此外,与BSA-BC二元体系比较,Cu2+/Zn2+存在下BSA荧光发射光谱与BC紫外可见吸收光谱的重叠积分J有所下降、能量转移效率E略有上升(表1),说明Cu2+/Zn2+对BC与BSA之间的能量转移产生了影响。
2.2 Cu2+/Zn2+对BSA-BC复合物稳定性和结合位点数的变构效应
按照式S0/S=KAcBCS0/(S0-S)-nKAcBSA[10],对0.2×10-5mol·L-1Cu2+/Zn2+存在下BSA-BC体系的实验数据进行处理,得到图5。
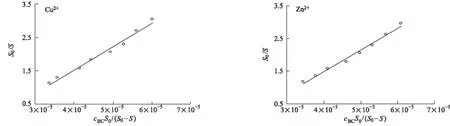
图5 Cu2+/Zn2+存在下,BSA-BC体系cBCS0/(S0-S)~S0/S的关系曲线
拟合得到线性方程,再由方程的斜率和截距得到表观结合常数KA和结合位点数n,并定义结合变构系数βA=KA/KA,0、βn=n/n0(其中KA,0、KA和n0、n分别为加入Cu2+/Zn2+前后BSA-BC结合的表观结合常数和结合位点数)[9],结果见表2。
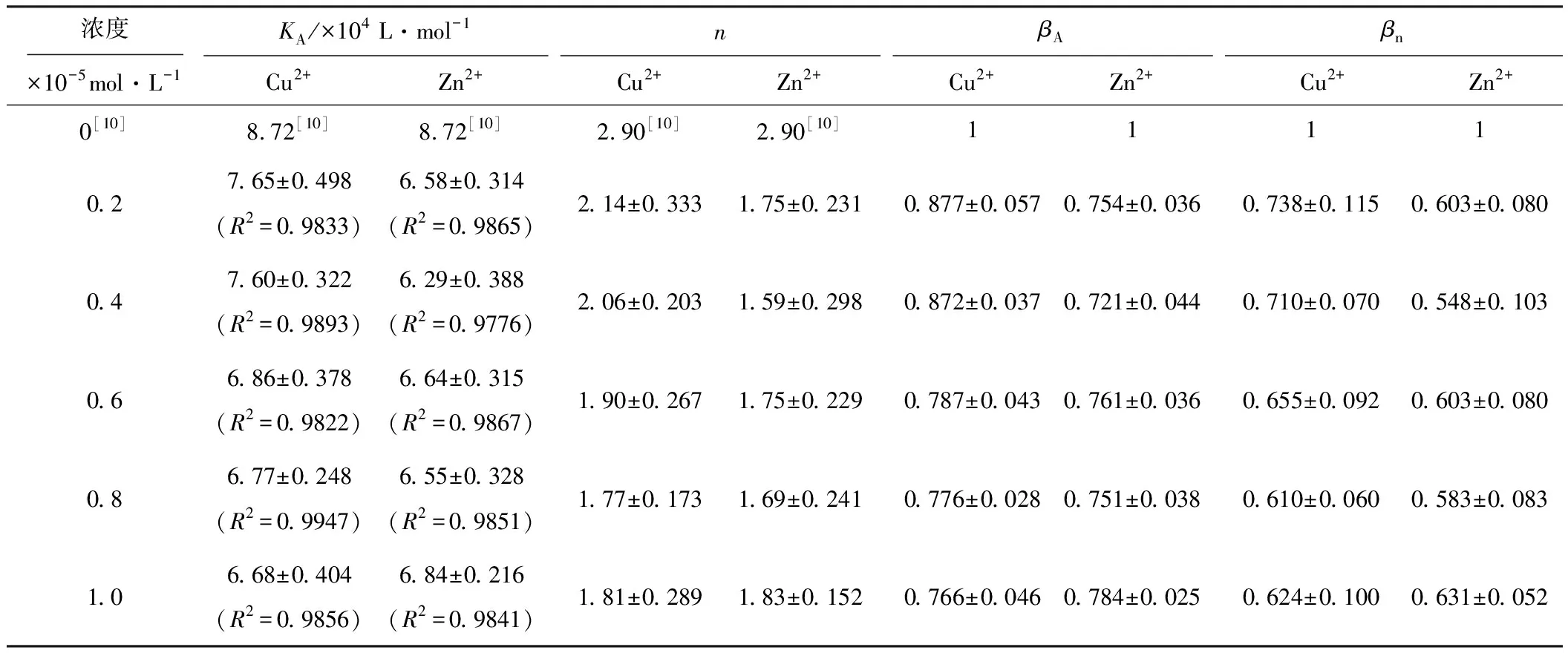
表2 Cu2+/Zn2+存在下,BSA-BC结合过程的表观结合常数KA、结合位点数n、变构系数βA和βn
由表2可知,0<βA<1和0<βn<1表明Cu2+/Zn2+对BSA-BC复合物稳定性和结合位点数都具有负变构效应,说明Cu2+/Zn2+存在时使BSA-BC复合物稳定性下降,进而使BC在血液中的存储时间缩短,释放速度加快,同时其游离浓度增大。KA较BSA-BC二元体系减小,说明加入Cu2+/Zn2+后BC、BSA与金属离子所形成的三元复合物比BC与BSA形成的二元复合物的稳定性低。
以变构系数βA和βn的数值对所加入Cu2+/Zn2+的浓度作图,结果见图6。
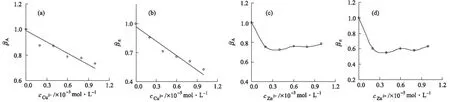
图6 βA~cCu2+(a)、βn~cCu2+(b)、βA~cZn2+(c)、βn~cZn2+(d)的关系曲线
由图6可知,变构效应随两种变构剂Cu2+、Zn2+浓度的增大呈现不同的变化趋势:变构剂Cu2+的结合变构系数βA和βn与其浓度总体呈线性关系;而变构剂Zn2+的变构效应呈现饱和性。这可能与两者在BSA分子上的结合部位不同有关,Cu2+的结合位点为BSA分子中含N、O的氨基酸残基[18],而Zn2+的结合位点位于BSA分子domain Ⅰ和domain Ⅱ的交界处[19],这可能导致BC的进一步结合受到不同的影响。
通过拟合方程βA=-2.96×104cCu2++0.99(R2=0.9602)、βn=-4.96×104cCu2++0.97(R2=0.9318),计算变构剂Cu2+的变构效率系数[9]γA=(-2.96±0.426)×104L·mol-1、γn=(-4.96±0.950)×104L·mol-1。
可见,γA和γn均为104数量级,且|γn|>|γA|,说明Cu2+对BSA-BC复合物稳定性的变构效率低于其对结合位点数的变构效率;总体呈线性关系说明BSA-BC复合物稳定程度随Cu2+浓度增大而减弱,此结果与BC作为变构剂时相反[9]。
2.3 变构效应的可能机制
Cu2+/Zn2+存在下,BSA-BC的CD图谱见图7,由图7计算得到的BSA-BC二级结构含量见表3。

cBSA=2.0×10-6 mol·L-1 1~5,nCu2+∶nBSA∶nBC:0∶1∶0,0∶1∶1,1∶1∶1,0.4∶1∶1,0.8∶1∶1 6~10,nZn2+∶nBSA∶nBC:0∶1∶0,0∶1∶1,0.8∶1∶1,0.4∶1∶1,1∶1∶1
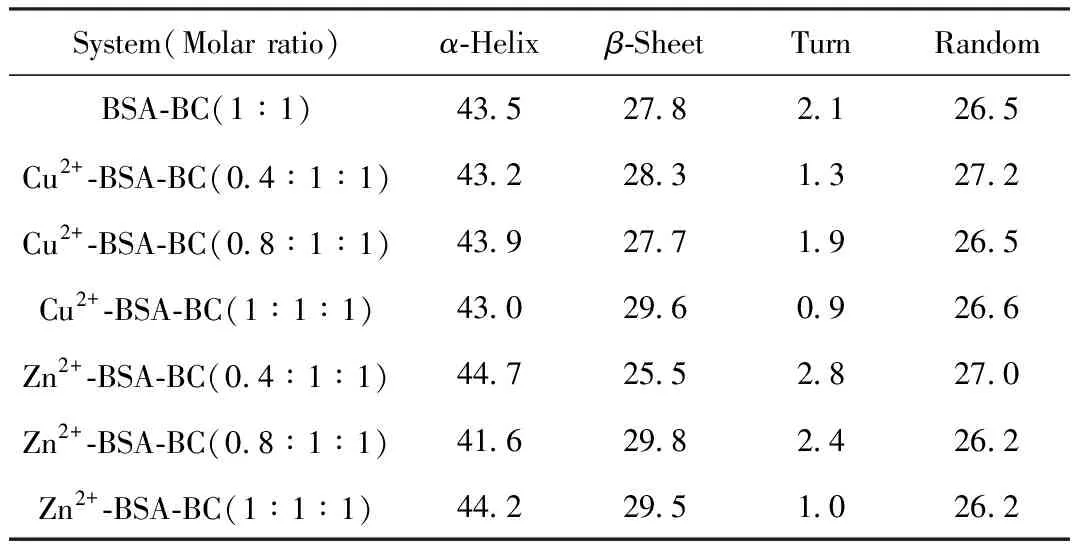
表3 Cu2+/Zn2+存在下,BSA-BC体系二级结构的含量/%
由表3可知,变构剂Cu2+/Zn2+使BSA-BC分子构象中4种二级结构(α-Helix、β-Sheet、Turn和Random)含量均有不同程度的改变,说明与BC类似,Cu2+/Zn2+的变构效应同样是通过Cu2+/Zn2+与BSA结合进而使BSA构象改变得以实现的。
与BC为变构剂时有所不同,Cu2+-BSA-BC三元体系中BSA分子的β-Sheet含量随Cu2+浓度增大呈现不规律变化,而Turn结构减少,BSA分子结构一定程度趋于松散,这种构象改变可能是导致BC与BSA分子中荧光性氨基酸残基间的空间距离r缩小的主要原因,进而使直接荧光猝灭和非辐射能量转移过程变得相对容易,导致Cu2+对BSA-BC荧光猝灭过程呈正变构效应。而Zn2+-BSA-BC三元体系中,BSA分子构象中4种二级结构含量同样有不同程度的改变,当Zn2+浓度小于1×10-5mol·L-1时,Turn含量较BSA-BC二元体系略有增加,α-Helix、β-Sheet和Random含量呈现不规律变化;当Zn2+浓度为1×10-5mol·L-1时,Turn含量较BSA-BC二元体系明显减少,α-Helix、β-Sheet含量增加,这种不规律变化可能是由于Zn2+和BC在BSA分子中的结合位置比较接近(位于domain Ⅰ和domain Ⅱ的交界处)[19],而Zn2+结合后对BSA构象的改变同样可能导致BC对BSA的直接荧光猝灭和非辐射能量转移过程变得相对容易,呈现正变构效应。
Cu2+/Zn2+对KA和n呈负变构效应的原因可能也源于BSA分子构象的转变。因为Cu2+/Zn2+与BSA分子结合后,BSA分子构象发生局部应激改变,使BSA分子中容易与BC结合的疏水空腔受到一定程度的破坏,导致BC与BSA分子的结合变得困难(0<βA<1)、可结合的位点数也有所减少(0<βn<1)。
3 结论
Cu2+/Zn2+对BC猝灭BSA内源荧光呈正变构效应(βQ>1),Cu2+/Zn2+存在下,BC与BSA分子空间距离r的缩小可能是产生正变构效应的直接原因,变构效应随Cu2+/Zn2+浓度的增大呈现一定的饱和性。Cu2+/Zn2+对BSA-BC复合物稳定性以及BC在BSA分子上的结合位点数呈负变构效应(0<βA<1,0<βn<1),变构效应随Cu2+/Zn2+浓度的增大呈现不同变化趋势:其中Zn2+对BSA-BC复合物稳定性以及BC在BSA分子上的结合位点数的变构效应随Zn2+浓度的增大呈现饱和性,而Cu2+的两种变构效应总体呈线性关系,且对BSA-BC复合物稳定性的变构效率低于其对结合位点数的变构效率。BSA分子构象转变可能是产生变构效应的主要原因。
参考文献:
[1] Chen T T,Cao H,Zhu S J,et al.Investigation of the binding of Salvianolic acid B to human serum albumin and the effect of metal ions on the binding[J].Spectrochimica Acta Part A:Molecular and Biomolecular Spectroscopy,2011,81(1):645-652.
[2] Peng M J,Shi S Y,Zhang Y P.The influence of Cd2+,Hg2+and Pb2+on taxifolin binding to bovine serum albumin by spectroscopic methods:With the viewpoint of toxic ions/drug interference[J].Environmental Toxicology and Pharmacology,2012,33(2):327-333.
[3] Shaikh S M T,Seetharamappa J,Kandagal P B,et al.Invitrostudy on the binding of anti-coagulant vitamin to bovine serum albumin and the influence of toxic ions and common ions on binding[J].International Journal of Biological Macromolecules,2007,41(1):81-86.
[4] 余燕敏,冯金朝,刘颖.Fe3+存在下磺胺甲恶唑与牛血清白蛋白相互作用的光谱学研究[J].化学学报,2011,69(2):190-198.
[5] 王腾,何晓囡,董颖,等.布南色林与人血清白蛋白相互作用的光谱学研究[J].分析试验室,2012,31(1):105-109.
[6] Chen J Z,Hage D S.Quantitative analysis of allosteric drug-protein binding by biointeraction chromatography[J].Nature Biotechnology,2004,22(11):1445-1448.
[7] Wainer I W.Finding time for allosteric interactions[J].Nature Biotechnology,2004,22(11):1376-1377.
[8] Chen J Z,Fitos I,Hage D S.Chromatographic analysis of allosteric effects between ibuprofen and benzodiazepines on human serum albumin[J].Chirality,2006,18(1):24-36.
[9] 刘雪锋,李磊,方云.牛血清白蛋白-Cu2+结合过程中盐酸小檗碱的变构效应[J].化学学报,2008,66(17):1967-1973.
[10] Liu X F,Xia Y M,Fang Y.Effect of metal ions on the interaction between bovine serum albumin and berberine chloride extracted from a traditional Chinese Herb coptis chinensis franch[J].Journal of Inorganic Biochemistry,2005,99(7):1449-1457.
[11] Kandagal P B,Ashoka S,Seetharamappa J,et al.Study of the interaction of an anticancer drug with human and bovine serum albumin:Spectroscopic approach[J].Journal of Pharmaceutical and Biomedical Analysis,2006,41(2):393-399.
[12] Kandagal P B,Seetharamappa J,Shaikh S M T,et al.Binding of trazodone hydrochloride with human serum albumin:A spectroscopic study[J].Journal of Photochemistry and Photobiology A:Chemistry,2007,185(2-3):239-244.
[13] 王洋,陈艳萍,张业中.2,4-二氯苯酚与人血清白蛋白相互作用的研究[J].化学与生物工程,2011,28(5):28-33.
[14] Gelamo E L,Tabak M.Spectroscopic studies on the interaction of bovine(BSA) and human serum albumins(HSA) with ionic surfactants[J].Spectrochimica Acta Part A,2000,56(11):2255-2271.
[15] Jiang C Q,Gao M X,Meng X Z.Study of the interaction between daunorubicin and human serum albumin,and the determination of daunorubicin in blood serum samples[J].Spectrochimica Acta Part A,2003,59(7):1605-1610.
[16] 宋琤,梁宏.荧光猝灭法研究Cu(Ⅱ)和Zn(Ⅱ)离子与牛血清白蛋白结合竞争[J].光谱学与光谱分析,2003,23(5):892-894.
[17] Messina P V,Prieto G,Ruso J M,et al.Conformational changes in human serum albumin induced by sodium perfluorooctanoate in aqueous solutions[J].Journal of Physical Chemistry B,2005,109(32):15566-15573.
[18] Bal W,Christodoulou J,Sadler P J,et al.Multi-metal binding site of serum albumin[J].Journal of Inorganic Biochemistry,1998,70(1):33-39.
[19] Stewart A J,Blindauer C A,Berezenko S,et al.Interdomain zinc site on human albumin[J].Proceedings of the National Academy of Sciences of the United States of America,2003,100(7):3701-3706.
