家蚕性信息素腺体肌质网膜Ca2+-ATP酶基因的分子鉴定
2012-07-14张松斗陈丽君安世恒杜孟芳
张松斗,陈丽君,安世恒,杜孟芳
(河南农业大学植物保护学院,河南郑州450002)
肌质/内质网膜Ca2+-ATPase(Sarco/endoplasmic reticulum Ca2+-ATPase,SERCA)是普遍存在于动物肌肉组织中肌质网膜上的离子转运蛋白酶体[1].Ca2+-ATPase又称钙泵,是肌质网的主要成分,占膜蛋白总量的90%,它与Na+-K+泵和H+-K+泵的相似性较高,均属于P型ATP酶的蛋白家族.P型ATP酶转运离子是一个主动运输的过程,需要水解ATP来提供能量,且每转运2个Ca2+需要消耗1分子的ATP,因为它有自动磷酸化的特征而被称为P型ATP酶[2].当肌细胞受到外界刺激时,在Ca2+-ATP酶的作用下Ca2+由肌质网释放进入细胞质中,同时它也可以通过消耗ATP来实现钙离子的逆浓度转运,将肌细胞胞质内的钙离子泵入到内质网腔内,维持内质网内外较高的钙离子浓度差[3].因此,Ca2+-ATP酶对于细胞来说是很重要的,钙离子通常与细胞跨膜信号传导密切相关,钙离子浓度的变化会引起相应的细胞内信号途径的反应,导致一系列的生理生化变化.在大部分鳞翅目昆虫中,性信息素是两性间通讯交流的重要介质,是由位于雌虫第8和第9腹节之间的信息素腺体的上皮细胞合成,经表皮释放到体外[4].性信息素多数为长链的不饱和醇、醋酸酯、醛或酮类,在性腺内由乙酰辅酶A经过脂肪酸合成、去饱和、碳链缩短和羰基碳的还原修饰等作用合成[5].大部分鳞翅目昆虫性信息素的合成和释放由性信息素合成激活肽(Pheromone biosynthesis activating neuropeptide,PBAN)来调控的.PBAN是一类C末端为33或34个氨基酸残基的多肽类酰胺化合物[6].其作用机制被认为首先通过与性信息素腺体细胞膜上的受体(PBAN receptor,PBANR)结合,然后经过一系列的信号传递,最终导致性信息素的合成和分泌.目前对于PBAN作用机制的研究多集中在模式生物家蚕(Bombyx mori)中[7].在家蚕中,PBAN首先和PBANR结合,促进钙离子从内质网释放,内流的 Ca2+与钙调素蛋白(CaM)结合[8],直接或间接激活Ca2+/calmodulin-dependent protein kinase II(BmCaMKII),通过去磷酸化激活酰基CoA还原酶和酯酶等过程,最终成功合成蚕蛾醇[9,10].目前对SERCA基因的研究主要集中在人类、小鼠和其他一些动物,在昆虫特别是家蚕中,其在PBAN信号传导级联途径中的作用还没有相关研究[11].本试验主要运用荧光定量PCR(RT-PCR)的方法,对SERCA基因在家蚕不同发育期和不同组织中的表达情况以及断头处理和保幼激素处理后的转录情况进行研究.这些结果为进一步研究SERCA基因在PBAN调控的性信息素合成与释放信号传导途径的功能提供理论依据.
1 材料与方法
1.1 供试昆虫
家蚕品种为镇珠×春蕾,卵由河南省农业科学院内乡蚕业研究所提供,在河南农业大学昆虫实验室饲养幼虫,温度为(26±1)℃,光周期为L:D=16:8,相对湿度为75%.幼虫化蛹后区分雌雄.
1.2 主要试剂
总RNA抽提试剂RNAiso Reagent(Invitrogen,USA),PrimeScript RT reagent Kit With gDNA Eraser、2 × Power Taq PCR MasterMix、DL2000 Marker、DNA Fragment Purification Kit Ver.2,0 及荧光定量试剂盒(SYBR Primer script RT-PCR Kit)均购自TAKARA公司.其他均为国产或进口分析纯试剂.
1.3 试验方法
1.3.1 序列分析 核苷酸序列分析采用ChromasPro软件,氨基酸序列分析采用高级生物信息学在线工具 http://www.expasy.org/tools/pi_tool.html,同源性比较采用NCBI中的BLAST工具,序列多重联配采用ClustalW和Genedoc软件,进化树构建选用MAGE4.0软件.
1.3.2 引物设计 BmSERCA基因在家蚕基因组数据库(SilkDB)上的Gene ID是BGIBMGA006603-TA.利用DNAClub软件设计引物,正向引物为SERCA F1:5’-AAAGAAACGCCGAATCTGC-3’,反向引物为 SERCA R1:5’-TGATAAGGCGAATGTCAGCAG-3’.以家蚕核糖体蛋白基因49(Ribosomal protein,Rp49)作为内参基因,正向引物为RpF1:5’-CAGGCGGTTCAAGGGTCAATAC-3’,反向引物为 RpR1:5’-TGCTGGGCTCTTTCCACGA-3’.引物由上海生工生物工程有限公司合成.
1.3.3 总RNA提取 包括家蚕雌虫性信息素腺体不同发育时期和成虫不同组织的提取两部分内容.其中雌虫性信息素腺体分为-96,-72,-48,-24,0,24,48,72 h 共 8 个发育阶段;成虫取羽化当天的成虫,分别取头、体壁、卵、中肠、飞行肌、脂肪体等不同组织.将不同发育时期的腺体和不同组织分别放入经DEPC处理过的Eppendorf管中匀浆,参照Takara公司试剂说明书,用RNAiso Reagent法提取总RNA.用紫外分光光度计检测其纯度和浓度.根据反转录试剂盒说明,以家蚕不同发育时期的性信息素腺体和不同组织的总RNA为模板合成cDNA第1链备用.
1.3.4 实时荧光定量PCR Real-time PCR采用相对定量的计算方法,家蚕Rp49基因作标准化对照,在Mastercycler@ep realplex real-time PCR检测系统上进行操作,反应条件如下:95℃预变性10 min,95 ℃变性15 s,58 ℃退火15 s,68 ℃延伸20 s,共35个循环.SYBR Green PCR信号的特异性可以使用溶解曲线分析和琼脂糖凝胶电泳检测.基因的相对表达量用 2-ΔΔCT方法计算[12].
1.3.5 BmSERCA基因的时空表达 利用合成的不同发育时期该基因的cDNA第1链作为模板,以SERCA F1和 SERCA R1为引物进行 Real-time PCR扩增,以Rp49作标准化对照.相对定量计算方法同 1.3.4.
以合成的不同组织的cDNA第1链为模板,利用SERCA F1和SERCA R1引物进行PCR扩增,PCR反应条件为:94℃预变性3 min;随后35个循环的扩增,扩增条件为94℃变性1 min,58℃退火1 min,72℃延伸1 min;最后72℃延伸10 min,然后4℃保存.利用1%的琼脂糖凝胶电泳对上述PCR产物进行分析,经EB染色后使用GenDoc凝胶成像系统观察并照相.
1.3.6 断头试验 将不同发育阶段(-72,-48,-24,0 h)的家蚕雌虫断头,断头处理后 24,48,72 h分别解剖家蚕性信息素腺体.提取总RNA,反转录合成cDNA第1链后进行荧光定量分析.总RNA提取和随后反转录的方法同1.3.3,以正常发育阶段的雌虫性信息素腺体作为对照.Real-time PCR 操作和计算方法同1.3.4.
1.3.7 体外保幼激素处理 将不同发育阶段( -72,-48,-24,0 h)的家蚕雌虫断头,断头处理后24 h解剖性信息素腺体,解剖的性信息素腺体放入含有1 mL Grace’s medium昆虫培养液的组织培养板中,培养1 h后更换为新的Grace’s昆虫培养液(含有2 μmol的保幼激素).收集不同孵育间隔期(0,2,4 ,6 h)的性信息素腺体,提取总 RNA,反转录合成cDNA第1链,进行荧光定量分析.提取总 RNA和反转录的方法同 1.3.3,Real-time PCR 操作和计算方法同1.3.4.
1.3.8 统计分析 RT-PCR的试验均重复3次,平均值±标准偏差分析结果.使用t测验分析不同转录水平的RT-PCR试验结果.
2 结果与分析
2.1 BmSERCA基因的序列分析
序列分析结果表明,BmSERCA基因开放阅读框长度为2865 bp,编码954个氨基酸.利用生物信息学在线工具(http://www.expasy.org/tools/Pi_tool.html)分析氨基酸序列,结果表明,该蛋白的分子量为104.6 kD,等电点为5.40.将 12种昆虫的SERCA基因氨基酸序列进行多重联配,并构建系统进化树.结果表明BmSERCA基因的氨基酸序列与其他昆虫的SERCA基因的氨基酸序列具有较高的一致性(图1),其中与烟蚜夜蛾Heliothis virescens的一致性达到97%,与帝王斑蝶Danaus plexippus的一致性达到96%,与其他昆虫的序列一致性也都在85%以上(图2).
2.2 BmSERCA基因的时空表达情况
2.2.1 家蚕不同发育时期SERCA基因的表达情况 Real-time PCR结果显示,SERCA基因在家蚕羽化当天的表达量最高,羽化前96 h表达量最低,从羽化前96 h到羽化0 h其表达量呈上升趋势(图3).
2.2.2 家蚕不同组织中SERCA基因的表达情况
Real-time PCR结果显示,SERCA基因在性信息素腺体、头、体壁、脂肪体、飞行肌、卵中均有表达,但是在卵中的表达量相对较低,在中肠中不表达(图4).
2.3 断头处理对BmSERCA基因转录水平的影响
断头试验结果表明,该基因在-72,-48,-24 h断头处理后转录水平仍然呈显著增长的趋势,但是在0 h断头后其转录水平却显著下降.与正常发育阶段的雌虫性信息素腺体相比,断头处理明显抑制了BmSERCA基因的表达(图5).
2.4 体外保幼激素处理结果
保幼激素处理结果表明,保幼激素明显抑制了BmSERCA基因在各个阶段断头24 h后的转录水平,特别是-48 h和0 h断头后的转录水平(图6).
3 讨论
离子的跨细胞膜运输是引起生物组织中电流的主要原因[13].LEE[14]解释了 Ca2+-ATPase 和钙离子通道中的钙离子结合位点,并研究了钙离子的主动和被动运输过程.TOYOSHIMA等[15]对钙离子传输的结构基础、可能的传输通道以及抑制剂的作用进行了阐述.试验证明细胞中钙离子和镁离子、钠离子、钾离子的浓度相差数万倍的情况下,Ca2+-ATPase依然会选择性的吸收钙离子[16].肌质/内质网膜上的钙离子横跨膜运输是在钙泵作用下通过钙离子通道运输钙离子的过程,它的活性的大小可以反应出各种细胞能量代谢和功能的强弱[17].本研究中,肌质/内质网膜 Ca2+-ATPase在家蚕中的时空表达情况表明,该基因在羽化前4 d表达量相对较低,羽化前随着时间的推移其表达量一直在上升,并在羽化当天表达量达到最高.这种表达模式与性信息素合成的关键基因保持一致[18,19].家蚕的性信息素的主要成分是蚕蛾醇,其前体物质主要以Triacylglycerols(TAGs)的形式存

图1 BmSERCA和其他昆虫SERCA的氨基酸序列多重联配Fig.1 Amino acid sequence multiple alignment of BmSERCA with other insects homologs
黑色代表100%一致性;灰色代表80%一致性;白色代表小于80%一致性.BM.家蚕;DP.帝王斑蝶;HV.烟蚜夜蛾;BT.大黄蜂;AM.意大利蜜蜂;NV.丽蝇蛹集金小蜂;AP.豌豆蚜;TC.赤拟谷盗;AA.埃及伊蚊;AG.疟蚊;CQ.库蚊;DM.黑腹果蝇.下同.
The black represents 100%identity;The gray represents 80%identity;The white represents less than 80%identity.BM.Bombyx mori(NP_001157948.1);DP.Danaus plexippus(EHJ69709.1);HV.Heliothis virescens(AAD09820.1);BT.Bombus terrestris(XP_003399858.1);AM.Apis mellifera(XP_393851.3);NV.Nasonia vitripennis(XP_001603571);AP.Acyrthosiphon pisum(XP_001943129);TC.Tribolium castaneum(XP_966783.1);AA.Aedes aegypti(XP_316251.4);AG.Anopheles gambiae(XP_316251.4);CQ.Culex quinquefasciatus(XP_001868188.1);DM.Drosophila melanogaster(NP_726381.1).The same as below.

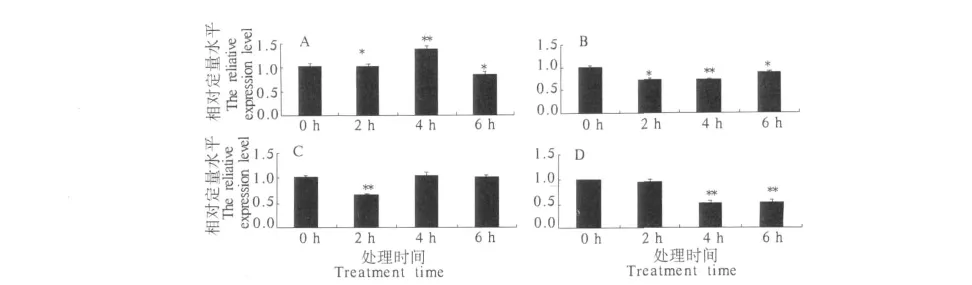
图6 保幼激素处理对BmSERCA基因转录水平的影响Fig.6 The effect of JH treatment on the transcription levels of BmSERCA gene
A.家蚕雌虫羽化前72 h断头,断头24 h后JH处理0,2,4,6 h后BmSERCA基因的转录水平;B.家蚕雌虫羽化前48 h断头,断头24 h后JH处理0,2,4,6 h后BmSERCA基因的转录水平;C.家蚕雌虫羽化前24 h断头,断头24 h后JH处理0,2,4,6 h后BmSERCA基因的转录水平;D.家蚕雌虫羽化前0 h断头,断头24 h后JH处理0,2,4,6 h后BmSERCA基因的转录水平.数据均代表3次生物学重复的平均值±标准偏差,**和**表示处理与对照(0 h)之间t-测验差异显著(*:0.01 <P <0.05 ,**:P <0.01).
A.The females at 72 h before-eclosion were decapitated.The transcription levels of BmSERCA gene after JH treatment(0,2,4 h and 6 h)after head detachment 24 h;B.The females at 48 h before-eclosion were decapitated.The transcription levels of BmSERCA gene after JH treatment(0 ,2 ,4 h and 6 h)after head detachment 24 h;C.The females at 24 h before-eclosion were decapitated.The transcription levels of BmSERCA gene after JH treatment(0,2,4 h and 6 h)after head detachment 24 h;D.The females at 0 h before-eclosion were decapitated.The transcription levels of BmSERCA gene after JH treatment(0,2,4 h and 6 h)after head detachment 24 h.The data represent the mean ± SE of three biological replicates,Significance of pairwise comparisons(treatment vs control)are marked with*or** (*:0.01 <P <0.05; **:P <0.01)as determined by the Student’s t-test.在于家蚕细胞质脂滴中.脂滴在成虫羽化前3 d或4 d开始出现,在成虫羽化当天快速积聚,达到最高值[20,21].雌成虫在羽化当天即产生大量的性信息素[22].PBAN在成虫羽化之后,从脑-咽下神经节合成,经咽侧体释放到血淋巴中,然后直接作用于性信息素腺体细胞促进性信息素生物合成的许多步骤[23,24].钙离子在 PBAN 信号转导级联途径中起着重要的作用,阻断钙离子的流入将会打断PBAN信号向下游的传导[25].而SERCA的主要功能是Ca2+的运输,是否PBAN激活Ca2+后由SERCA来运输Ca2+还需进一步的研究.
SERCA基因在性信息素腺体、头、体壁、脂肪体、飞行肌、卵中均有表达,但是在卵中的表达量相对较低,在中肠中不表达.该基因在-72,-48,-24 h断头处理后转录水平仍然呈现显著增长的趋势,但是在0 h断头后其转录水平却显著下降,这与该基因在正常发育阶段的表达趋势是一致的.但与正常发育阶段的雌虫性信息素腺体相比,断头对BmSERCA基因的表达有明显的抑制作用.体外保幼激素处理试验中,运用断头雌蛾的主要原因是排除内保幼激素的影响.RT-PCR的结果表明,保幼激素明显的抑制了该基因在各个阶段断头24 h后的转录水平,特别是-48 h和0 h断头后的转录.在家蚕从蛹到成虫的发育过程中,保幼激素的滴度也随之增加,特别是交配后,保幼激素的滴度大幅增加,交配后的家蚕不再产生性信息素.本研究为进一步研究PBAN调控性信息素合成与释放的整个信号传导途径提供理论依据.但是Ca2+-ATPase和钙离子通道在PBAN调控性信息素合成与释放信号级联途径中的具体作用机制还有待进一步阐释.
[1] PERIASAMY M,HUKE S.SERCA pump level is a critical determinant of Ca2+homeostasis and cardiac contractility[J].Mol Cell Cardiol,2001,33(6):1053-1063.
[2] 段清芬,黄海华,刘志敏.PMRl-钙离子ATP酶研究进展[J].生物技术通讯,2007,(3):501-504.
[3] PEDERSON P L.Rransport ATPase in biological systerms and relationship to human disease:a brief overview[J].J Bioenerg Biomemb,2002,34:327.
[4] KITAMURA A,NAGASAWA H,KATAOKA H,et al.Amino acid sequence of pheromone biosynthesis activating neuropeptide(PBAN)of the silkworm Bombyx mori[J].Biochemical and Biophysical Research Communications,1989,163:520-526.
[5] TILLMAN J A,SEYBOLD S J,JURENKA R A,et al.Insect pheromones overview of biosynthesis and endocrine regulation[J].Insect Biochemisty and Molecular Biology,1999,29:481-514.
[6] RAFAELI A.Pheromone biosynthesis activating neuropeptide(PBAN):regulatory role and mode of action[J].General and Comparative Endocrinology,2009,162:69-78.
[7] MATSUMOTO S,OHNISHI A,LEE J M,et al.Unraveling the pheromone biosynthesis activating neuropeptide(PBAN)signal transduction cascade that regulates sex pheromone production in moths[J].Vitamins &Hormones,2010,83:425 -445.
[8] MATSUMOTO S,MOTO K,WANG F H.Cellular events and molecular mechanisms underlying sex pheromone production in the silkmoth,Bombyx mori[J].RIKEN Review,2001,41:79-81.
[9] MATSUMOTO S,HULL J J,OHNISHI A,et al.Molecular mechanisms underlying sex pheromone production in the silkmoth,Bombyx mori:characterization of the Molecular components involved in bombykol biosynthesis[J].Journal of Insect Physiology,2007,53:752-759.
[10] MOTO K,YOSHIGA T,MATSUMOTO S,et al.Pheromone gland-specific fatty-acyl reductase of the silkmoth,Bombyx mori[J].Proceeding of the National Academy of Science,2003,100:9156-9161.
[11] SEHULTZ J J,GLASCOCK B J,WITT S A,et al.Accelerated onset of heart failure in mice during pressure overload with chronically decreased SERCA2 calcium pump activity[J].Am J Physiol Heart Circ Physiol.,286(3):1146-1153.
[12] LIVAK K J,SCHMITTGEN T D.Analysis of relative gene expression data using real-time quantitative PCR and the 2(-Delta Delta C(T))Method[J].Methods,2001,25:402-408.
[13] OSTWALD W.Elektrische Eigenschaften halbdurchlassiger Scheidewande[J].Z Phys Chem,1890,6:71 -82.
[14] LEE A.Calcium pump made visible[J].Curr Opin Struct Biol,2002,12:547 -554.
[15] TOYOSHIMA C,MIZUTANI T.Crystal structure of the calcium pump with a bound ATP analogue[J].Nature,2004,430:529-536.
[16] DRAKE S K,LEE K L,FALKE J J.Tuning the equilibrium ion affinity and selectivity of the EF-hand calcium binding motif:Substitutions at the gateway positions[J].Biochemistry,1996,35:6697 -6075.
[17] TANG Y L,ZHAO O,OIN X,et al.Paracrine action enhances the efects of autologous mesenchymal stem cell transplantation on vascular regeneration in rat model of myocardial infarction[J].Aan Thorac Surg,2005,80(1):229-236.
[18] DU M F,ZHANG S D,AN S H,et al.Identification of a diacylglycerol acyltransferase 2 gene involved in pheromone biosynthesis activating neuropeptide stimulated pheromone production in Bombyx mori[J].Journal of Insect Physiology,2012,58(5):699-703.
[19] DU M F,YIN X M,ZHANG S D,et al.Identification of lipases involved in PBAN stimulated pheromone production in bombyx mori using the DGE and RNAi approaches[J].PLoS ONE,2012,7(2):e31045.
[20] RAINA A K,JAFFE H,KEMPE T G,et al.Identification of a neuropeptide hormone that regulates sex pheromone production in female moths[J].Science,1989,244:796-798.
[21] MATSUMOTO S,FONAGY A,YAMAMOTO M,et al.Chemical characterization of cytoplasmic lipid droplets in the pheromone-producing cells of the silkmoth,Bombyx mori[J].Insect Biochemisty and Molecular Biology,2002,32:1447-1455.
[22] HULL J J,LEE J M,MATSUMOTO S.Gqalpha-linked phospholipase Cbetal and phospholipase Cgamma are essential components of the pheromone biosynthesis activating neuropeptide(PBAN)signal transduction cascade[J].Insect Molecular Biology,2010,19:553 -566.
[23] TSFADIA O,AZRIELLI A,RAFAELI A,et al.Pheromone biosynthetic pathways:PBAN-regulated rate-limiting steps and differential expression of desaturase genes in moth species[J].Insect Biochem Mol Biol,2008,38:552-567.
[24] OHNISHI A,HULL J J,MATSUMOTO S,et al.Hormone signaling linked to silkmoth sex pheromone biosynthesis involves Ca2+/Calmodulin-dependent protein kinase II-mediated phosphorylation of the insect PAT family protein bombyx mori lipid storage droplet Protein-1(BmLsd1) [J].Journal of Biological Chemistry,2011,286:24101-24112.
[25] HULL J J,LEE J M,KAJIGAYA R,MATSUMOTO S.Bombyx mori homologs of STIM1 and orail are essential components of the signal transduction cascade that regulates sex pheromone production[J].Journal of Biologiacl Chemistry,2009,284:31200-31213.
