注射用头孢替安与注射用氯诺昔康配伍稳定性考察
2012-07-11方宝霞陆连英艾学勇
方宝霞,苏 翔,陆连英* ,朱 军,艾学勇
头孢替安是半合成的第二代头孢菌素,临床用于治疗敏感菌所致的感染。氯诺昔康为新型非甾体抗炎药,通过选择性抑制环氧化酶-2 活性达到抗炎、镇痛和解热作用[1-2]。目前,临床上常将盐酸头孢替安与氯诺昔康配伍用药,用以预防术后感染与术后镇痛。然而,此方法为经验性配伍用药,其配伍液是否稳定尚未见报道,且其安全性无确切的理论依据。因此,笔者根据临床用药浓度,参考有关文献[3-9],采用高效液相梯度洗脱法考察室温下两药配伍液在0.9%氯化钠注射液中的稳定性,为临床安全、合理用药提供理论依据。
1 仪器与试药
1.1 仪器 DIONEX UltiMate 3000 高效液相色谱仪(德国戴安),包括UltiMate 3000 四元低压梯度泵、UltiMate 3000 二极管阵列检测器、Chromeleon 色谱工作站;pHs-3C 型酸度计(上海华侨仪表厂);AEU-210 电子天平(日本岛津)。
1.2 试药 注射用盐酸头孢替安(哈药集团制药总厂,批号:B201104312,规格:0.5 g/支),注射用氯诺昔康(北京利祥制药股份有限公司,批号:11070551,规格:8 mg/支),氯诺昔康对照品(中国药品生物制品检定所,批号:100663-200501),头孢替安对照品(中国药品生物制品检定所,批号:130565-200501),0.9%氯化钠注射液(四川科伦药业股份有限公司,批号:A11052308-1),磷酸二氢钾(广东汕头西陇化工有限公司,分析纯),乙腈为色谱纯,水为新制注射用水,其他试剂均为分析纯。
2 方法与结果
2.1色谱条件色谱柱:Sinochrom ODS-BP(250 mm × 4.6 mm,5 μm)。以乙腈(A)-0.05 mol/L磷酸二氢钾(B)为流动相。梯度洗脱程序:0 ~5 min,A 体积分数为12%;6 ~14 min,A体积分数为45%;15 ~21 min,A 体积分数为12%。流速:0.8 mL/min;柱温:30 ℃;进样量:20 μL;测定波长分别为261、382 nm。
2.2 对照品储备液的制备 分别精密称取头孢替安与氯诺昔康对照品适量,分别以流动相配制成浓度为520.0 μg/mL 头孢替安与212.0 μg/mL氯诺昔康对照品储备液,置4 ℃冰箱中保存备用。
2.3 测定波长的选择 在“2.1”项色谱条件下,通过二极管阵列检测器对头孢替安与氯诺昔康对照品溶液在200 ~600 nm 波长范围内进行全波长扫描,由二极管阵列检测器在200 ~600 nm 波长范围内的扫描图谱得知,头孢替安与氯诺昔康分别在261、382 nm 波长处有最大吸收。故将检测波长分别定为261、382 nm。
2.4 系统适用性试验 将上述对照品溶液等体积混合,在“2.1”项色谱条件下,进样20 μL,记录色谱图。在此条件下,头孢替安、氯诺昔康保留时间分别为6.8、12.7 min,头孢替安与氯诺昔康的色谱峰理论塔板数均>3 000,分离度>1.5,专属性良好,色谱图见图1。
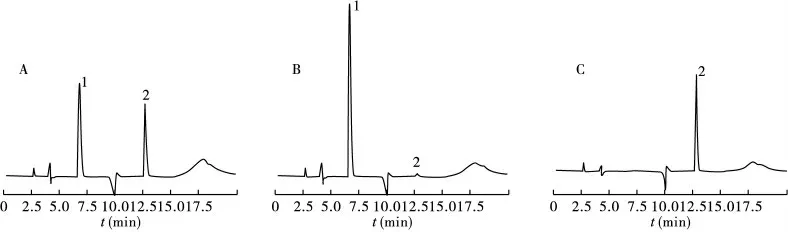
图1 HPLC 色谱图
2.5 标准曲线的绘制 分别精密吸取头孢替安与氯诺昔康对照品储备液0.5、1.0、1.5、2.0、2.5、5.0 mL 至10 mL 量瓶中,以流动相定容,混匀,制得不同浓度的头孢替安对照品溶液与氯诺昔康对照品溶液。分别取上述溶液20 μL,在“2.1”项色谱条件下进样测定。以峰面积(Y)为纵坐标、浓度(X)为横坐标绘制标准曲线,结果头孢替安回归方程为 Y头孢替安= 21.35 X头孢替安- 0.42 (r =0.999 7);氯诺昔康回归方程为Y氯诺昔康= 1.52 X氯诺昔康+0.21(r=0.999 5)。结果表明,头孢替安在26.0 ~260.0 μg/mL、氯诺昔康在10.6 ~106.0 μg/mL浓度范围内线性关系良好。
2.6 精密度试验 分别精密吸取104.0 μg/mL头孢替安对照品溶液与42.4 μg/mL 氯诺昔康对照品溶液各20 μL,重复进样6 次,测定峰面积,结果头孢替安与氯诺昔康峰面积的RSD 分别为1.15%、1.21%。
2.7 稳定性试验 配制头孢替安与氯诺昔康样品溶液,置于25 ℃下,分别于0、0.5、1.0、2.0、3.0、4.0 h,在上述色谱条件下进样20 μL,测定峰面积。结果头孢替安与氯诺昔康峰面积RSD 分别为1.35%、1.26%。说明头孢替安与氯诺昔康样品溶液在4 h 内保持稳定(n=6)。
2.8 加样回收率试验 取已知含量的注射用头孢替安与注射用氯诺昔康配伍液适量,精密加入高、中、低浓度的头孢替安与氯诺昔康对照品溶液适量,混匀,分别用纯化水分别稀释1 倍与100 倍,在“2.1”项色谱条件下测定,记录峰面积,并计算回收率,结果头孢替安与氯诺昔康的回收率分别为99.83%、99.52%,见表1。
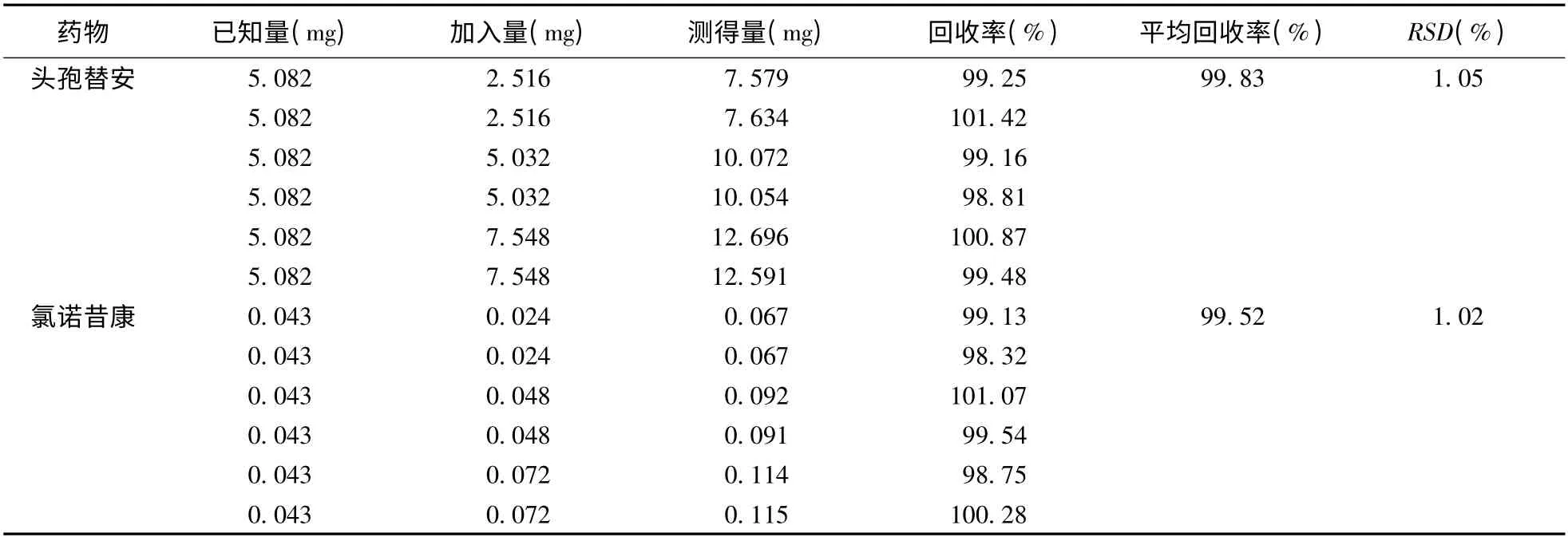
表1 回收率试验结果(n=6)
2.9 配伍稳定性试验
2.9.1 配伍液的制备 取注射用盐酸头孢替安1.0 g 与注射用氯诺昔康8 mg,以注射用水溶解后加入0.9%氯化钠注射液中,定容至100 mL,摇匀,制得配伍液置于室温条件下保存。
2.9.2 外观与pH 值变化 取上述配伍溶液适量,室温条件下,在0、1、2、3、4、6、8 h 用纳氏比色管观察颜色变化并测定溶液的pH 值。结果见表2。
2.9.3 相对百分含量变化 在上述时间间隔,取上述配伍液适量,用纯化水分别稀释100 倍与1倍,在“2.1”项色谱条件下进样测定,计算配伍液中头孢替安与氯诺昔康的含量,以0 h 药物含量为100%,计算各时间点相对百分含量,见表2。
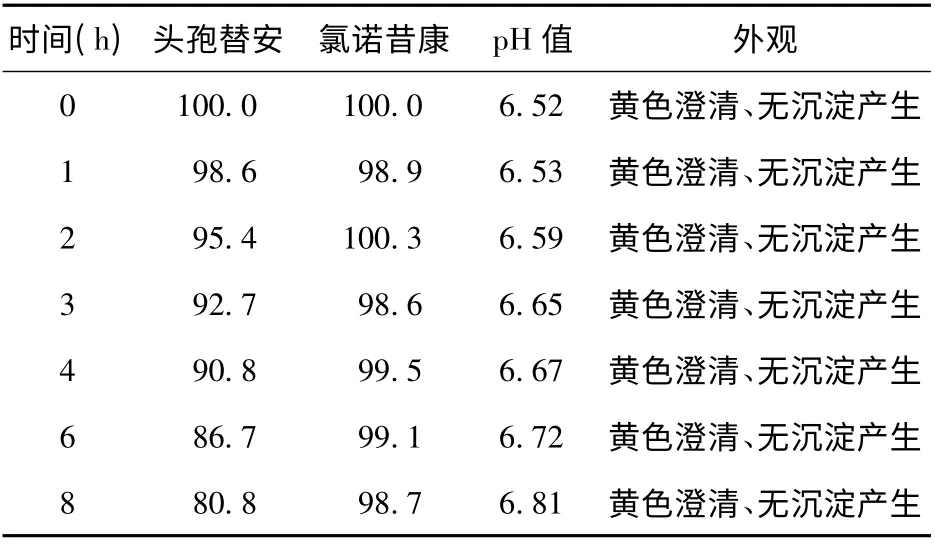
表2 注射用头孢替安与注射用氯诺昔康配伍后外观、pH 值及含量变化(%)
3 讨论
头孢替安的极性较强,具亲水性,在反相高效液相色谱法中,易被流动相洗脱;而氯诺昔康极性相对较弱,与固定相亲和力强,不易被洗脱,保留时间长,经反复测试流动性组成,无法在等度洗脱条件同时测定二者含量。为同时兼顾色谱选择性和分析时间等因素,最终确定“2.1”项梯度洗脱程序。在此条件下,头孢替安与氯诺昔康峰型较好,两色谱峰在较短时间获得很好的分离,理论塔板数高,符合含量测定要求。
注射用头孢替安与注射用氯诺昔康在0.9%氯化钠注射液中配伍后,在25 ℃条件下,混合液黄色澄明,未见气泡及肉眼可见的沉淀生成。经HPLC 法测定配伍液中两组分的含量,在8 h 内氯诺昔康含量无明显变化,头孢替安的含量呈下降趋势,8 h 含量为80.8%。配伍液pH 值随时间延长逐渐增大,溶液颜色随时间延长逐渐加深。综合试验结果,为保障临床用药安全,注射用头孢替安与注射用氯诺昔康在0.9%氯化钠注射液中可配伍使用,但应在4 h 内用完。
[1] 方宝霞,陈富超,李鹏,等.氯诺昔康静脉联合用药在术后镇痛中的应用及评价[J]. 中国医院用药评价与分析杂志,2011,11(8):684-686.
[2] 陈富超,李鹏,方宝霞,等.注射用氯诺昔康与氟哌利多注射液配伍稳定性研究[J].中国医药,2011,6(3):335-336.
[3] 伦新强. 注射用盐酸头孢替安与常用输液配伍稳定性考察[J].中国药业,2009,18(23):11.
[4] 刘芳艳,刘海燕,谢建忠.注射用盐酸头孢替安与氨甲环酸的配伍稳定性考察[J].中国医院药学杂志,2009,29(8):679-680.
[5] 方宝霞,陈富超,时晓亚,等.注射用氯诺昔康与盐酸氯胺酮注射液在0.9%氯化钠注射液中的稳定性研究[J]. 中国药师,2011,14(6):539-540.
[6] 林素梅.注射用盐酸头孢替安与甲硝唑注射液配伍稳定性考察[J].中国药业,2008,17(18):24-25.
[7] 张丽梅,邢建华,李俊.头孢替安在莫西沙星注射液中的配伍稳定性[J].中国药师,2008,11(12):1528-1529.
[8] 杨曼,丁洁,方宝霞,等.注射用氯诺昔康在不同输液容器中的稳定性考察[J]. 中国医院用药评价与分析,2010,10(12):1097-1099.
[9] 潘桂玲. 兰索拉唑与氯诺昔康在注射液中的配伍稳定性[J].中国医院药学杂志,2009,29(18):1589-1590.
