肥胖2型糖尿病的降糖新药及其临床应用
2012-05-26哈尔滨医科大学附属第二医院内分泌代谢病科李强
哈尔滨医科大学附属第二医院内分泌代谢病科 李强
2型糖尿病是一种进展性疾病,随着2型糖尿病的进展,血糖有逐渐升高的趋势,控制高血糖的治疗强度也应随之加强。但对于肥胖2型糖尿病患者,当口服药物联合治疗失效时,应用胰岛素不但会增加体重,而且伴有很高的低血糖风险。因此,对于这类患者的治疗,不仅应考虑血糖、胰岛功能等指标的改善,更应考虑使用不增加体重甚至减轻体重的药物,除传统的双胍类药物、α-糖苷酶抑制剂之外,近年来可使用肠促胰岛激素等。肠促胰岛激素包括胰高血糖素样肽1(GLP-1)和葡萄糖依赖性促胰岛素分泌多肽(GIP)。基于肠促胰素的治疗药物包括GLP-1受体激动剂和DPP-4抑制剂。以下对该类药物的机理及临床应用研究以及相关药物的研究进展做一综述。
GLP-1受体激动剂
GLP-1受体激动剂分为人GLP-1类似物(利拉鲁肽)和基于Exendin-4的治疗药物(艾塞那肽)。
1.利拉鲁肽
是人胰高血糖素样肽1(GLP-1)类似物,其分子结构的独特之处是在原GLP-1肽链骨架上共价添加了一个简单脂肪酸侧链和一个间隔区(C16-γGlu-Lys26,Arg34GLP-1(7-37)),可99%与白蛋白结合进而使血浆半衰期延长,其剂型中的七聚体结构则使吸收延迟。此外,利拉鲁肽的分子结构使其对二肽基肽酶(DPP-4)保持稳定的化学特性,不易被后者降解,这些特性可延迟利拉鲁肽的吸收并延长其在血浆中的半衰期,因此在人体仅需每日1次给药即可起到良好的临床效果。利拉鲁肽可以有效减少进食,降低体重,其作用机制可能是:①升高下丘脑弓状核的CART mRNA水平;②阻止体重减轻诱导的弓状核NPY和AgRP mRNA水平升高,因此可应用于肥胖2型糖尿病的治疗。
LEAD(Liraglutide Effect and Action in Diabetes)是一项4000多例2型糖尿病患者参与的研究,以利拉鲁肽作为基础药物,单独或联合一种或两种口服降糖药,研究其疗效及安全性。LEAD系列研究结果显示[1-7],利拉鲁肽无论单药或与二甲双胍、磺脲类(格列美脲)、格列酮类(罗格列酮)等药物联用都显示了优良的降糖疗效(表1),呈剂量依赖性降低患者体重,可达3.4kg(表2),并对B细胞功能具有明显改善作用。在LEAD-1研究中发现,与对照组相比,利拉鲁肽1.2和1.8mg治疗组胰岛素分泌指数(HOMA-β)明显改善(P<0.05)。另外,在LEAD-3和LEAD-4研究中应用相同剂量利拉鲁肽也使患者收缩压显著降低(LEAD-3:1.2mg、1.8mg和对照组分别降低2.1、3.6和0.7mmHg;LEAD-4:1.2mg、1.8mg和对照组分别降低6.7、5.6和1.1mmHg)。
胃肠道不适是利拉鲁肽治疗中最常见的不良反应,通常认为利拉鲁肽比较安全,但大鼠和小鼠实验显示可剂量依赖性和用药持续时间依赖性地诱发甲状腺C细胞肿瘤,但尚无导致人类发生甲状腺髓样癌等甲状腺C细胞肿瘤的证据。
2.艾塞那肽
艾塞那肽最初由毒晰属动物唾液中分离,是发现的第一个可由唾液腺分泌的内分泌物质。艾塞那肽有53%的氨基酸序列与哺乳动物GLP-1同源,与GLP-1受体具有高度亲和性,并具有相似的生物学作用。艾塞那肽的N端不被DPP-4分解,故血浆半衰期更长。
艾塞那肽的临床研究覆盖了2型糖尿病的不同治疗阶段:包括单个口服药失效、多个口服药失效、和胰岛素治疗相比。AMIGO研究及开放延伸试验在用二甲双胍和/或磺脲类药物治疗的2型糖尿病患者中加用艾塞那肽治疗超过3年,可以持久有效控制HbA1c,改善血脂及血压。3项AMIGO研究合并结果显示[8-10]:艾塞那肽5ug和10ug治疗30周较安慰剂可以显著降低餐后血糖(P<0.0001),并且10ug组降低幅度更大。初期12周时,患者的体重平均减轻约1.6kg。而当研究持续进行至3年,患者减重达到5.3kg。3年治疗期间,艾塞那肽组体重持续进行性降低,用二甲双胍(MET)+10 g艾塞那肽治疗的患者体重减轻幅度最大。
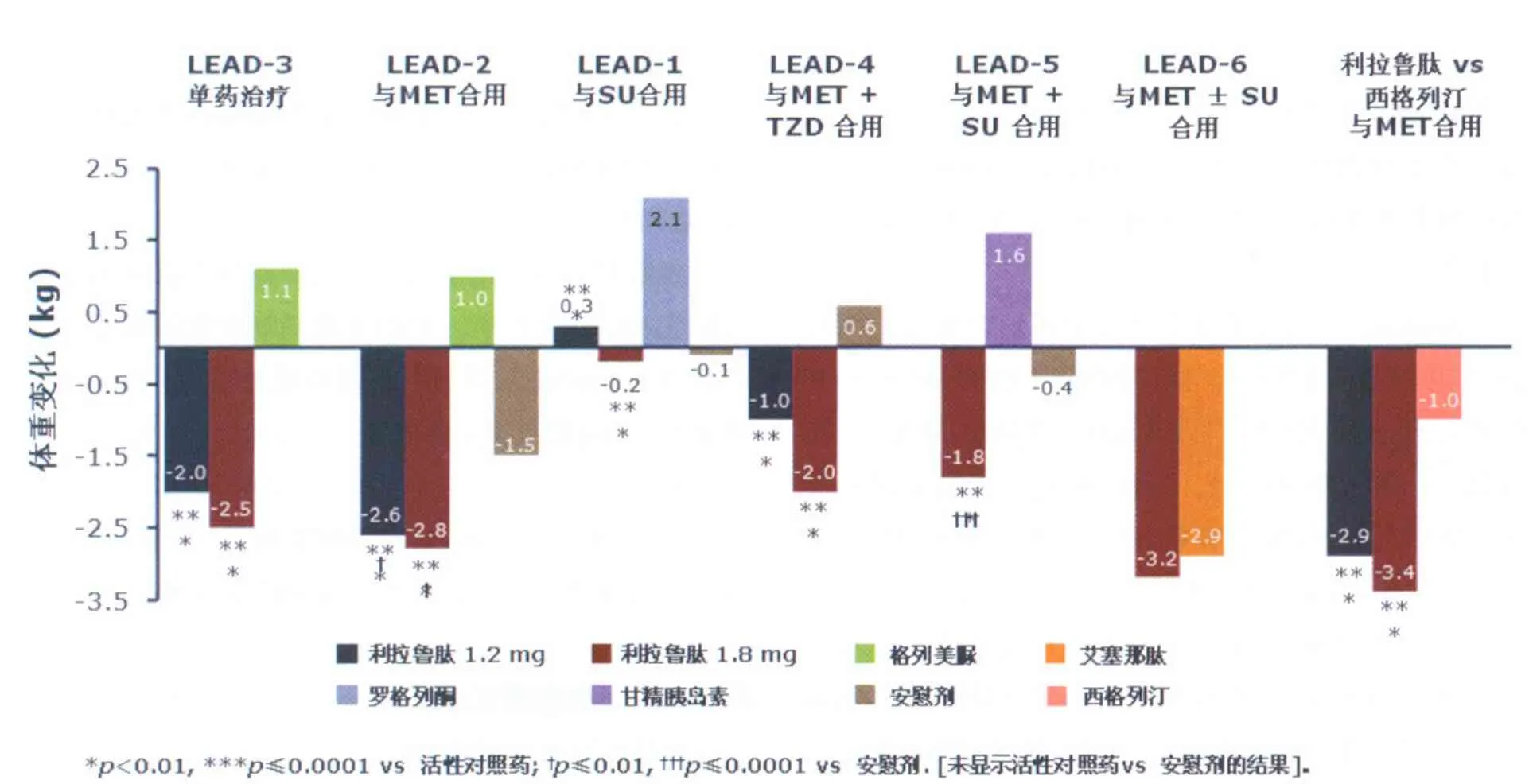
表1 LEAD系列研究利拉鲁肽组血糖变化

表2 LEAD系列研究利拉鲁肽组体重变化
在艾塞那肽开放标签延伸研究中,前30周分别接受安慰剂、艾塞那肽5ug、艾塞那肽10ug组30周后都接受艾塞那肽10ug治疗。3.5年时,艾塞那肽组较安慰剂组脂代谢与血压显著改善,TG降低12%,LDL降低6%,TC降低5%,HDL增加24%;同时SBP降低2%,DBP降低4%,均有统计学意义。艾塞那肽长期治疗可以获得显著的血糖和血压改善,提示艾塞那肽长期治疗糖外获益显著。3.5年时,基线ALT正常患者,艾塞那肽治疗对ALT几乎无影响,且患者体重减轻;基线ALT升高患者,ALT显著降低的同时体重也显著降低,且体重降幅大于ALT正常患者。总体人群156周体重变化与ALT变化略有相关性(r=0.31)。艾塞那肽在控制血糖的同时降低ALT,显示出显著的糖外获益。
在分别与长效和预混胰岛素(甘精胰岛素和双相门冬胰岛素)的比较研究中,艾塞那肽不仅具有相同的降糖疗效,同时使患者体重获得明显减轻,在一项与双相门冬胰岛素对比的研究中,治疗第52周时,艾塞那肽组较胰岛素组体重差距超过5kg。
艾塞那肽最常见的不良反应是恶心、呕吐,嘱患者少量、缓慢、清淡进餐,根据个体差异调整艾塞那肽剂量、调整注射时间、选择非工作日开始首次注射有助于减少恶心呕吐的发生。有文献报告使用艾塞那肽治疗可出现胰腺炎,应识别胰腺炎高危人群(过度饮酒、高甘油三酯血症、胆结石、胆囊疾病),并注意胰腺炎症状的出现。
3.其他药物
如CJC-1131、他司鲁泰(Taspoglutide)、阿必鲁泰(Albiglutide),均为对GLP-1进行结构修饰的GLP-1类似物。
DPP-4抑制剂
包括西格列汀(Sitagliptin)、维格列汀(Vildagliptin)、沙格列汀(Saxagliptin)、阿格列汀(Alogliptin)、利格列汀(Linagliptin)等。
1.西格列汀
首个上市的DPP-4抑制剂,它的研发始于对原有化合物库的筛选,在活性较好的先导物左侧用类肽结构β-氨基酰胺替换,然后在哌嗪环上骈入一个杂环形成双环,将哌嗪环转变为三氮唑并哌嗪环,并用三氟甲基取代后对左侧苯环进行修饰,最终发现2,4,5-三氟取代的化合物,其生物活性(IC50=16nmol/L),口服生物利用度87%,血浆半衰期8~14h,代谢稳定性也较高。
Aschner等观察了西格列汀单药治疗和安慰剂对2型糖尿病患者的疗效。随访24周研究结果显示,与安慰剂相比,西格列汀(每日100mg)显著降低HbA1c水平,降幅达0.79%(P<0.001)。基线HbA1c水平高者降幅较大,患者基线时HbA1c水平≥9%,降幅达到1.5%。西格列汀组患者的空腹血糖(FPG)也显著下降,与安慰剂组相比下降1.0mmol/L(P<0.001)。接受西格列汀治疗后,患者胰岛素原/胰岛素比值明显下降,HOMA-β水平显著提升,差异有统计学意义(P<0.05)。在另几项针对日本及亚洲2型糖尿病患者的研究中发现,西格列汀短期应用即有明显的降糖获益,HbA1c降幅均达1.0%左右。提示相对白种人来说,西格列汀在亚洲人群中的降糖效果可能会更好。
在与二甲双胍联合应用方面,Nauck等进行了以二甲双胍为基础治疗,对比西格列汀和磺脲类药物(格列吡嗪)疗效的随机双盲研究。该研究为期52周,纳入1172例2型糖尿病患者。研究结果显示,与二甲双胍(每日≥1500mg)合用时,西格列汀(每日100mg)降糖效果与格列吡嗪(每日可高达20mg,平均10mg)相当,HbA1c降幅均为0.7%。但是,西格列汀联合二甲双胍能显著减轻体重,而格列吡嗪与二甲双胍联用时体重增加(P<0.001)。与格列吡嗪相比,西格列汀组症状性低血糖事件发生风险降低93%,并且西格列汀组老年患者(≥65岁)低血糖事件风险的降低比中青年患者(≤65岁)更显著(97% vs 91%)。
西格列汀不良反应可能出现超敏反应、肝酶升高、上呼吸道感染、鼻咽炎等。
2.维格列汀
维格列汀是一类含有氰基吡咯烷结构的DPP-4抑制剂,氰基吡咯烷结构能占据DPP-4的S1口袋,且氰基能与Ser 630产生共价作用,具有较高的酶抑制活性。引入大体积的仲胺基团,如3羟基金刚烷胺,IC50=35nmol/L。口服100mg,每天2次,24h内DPP-4抑制率可达到90%。在动物实验中出现过皮肤坏死和肾损伤等副作用,但在临床研究中未出现过。
3.沙格列汀
沙格列汀是在维格列汀的结构基础上将环丙基骈入氰基吡咯烷结构中,增加了氰基吡咯烷的稳定性,IC50=3.37nmol/L,口服生物利用度为75%,血浆半衰期为2.1h,每日仅需口服1次。
4.其他
阿格列汀IC50=7nmol/L、利格列汀IC50=1nmol/L,Carmegliptin IC50=6.8nmol/L。临床较少应用。
新型糖尿病药物研究进展
1.高选择性SGLT-2抑制剂
钠-葡萄糖同向转运体(SGLT)是一种仅在肾小管和肠道基底外侧膜表达的膜蛋白,以主动方式逆浓度梯度转运葡萄糖,同时消耗能量,SGLT主要分布于肾小管上皮细胞管腔侧。小管液中葡萄糖通过SGLT进入细胞后,能被上皮细胞基底膜侧的葡萄糖转运蛋白(GLUT)转运至周围毛细血管网中,从而完成肾小管对葡萄糖的重吸收,对维持人体血糖稳定起着关键作用。SGLT主要分为SGLT-1和SGLT-2两种类型,其中SGLT-1主要表达于小肠刷状缘和肾近曲小管较远的S3节段中,少量表达于心脏和气管,SGLT-2则主要表达于肾近曲小管前S1节段中。SGLT-1负责转运葡萄糖和半乳糖,而SGLT-2则只负责转运葡萄糖。SGLT-2在葡萄糖的重吸收中起主要的作用,它负责转运肾重吸收葡萄糖的90%,而SGLT-1转运其余的10%。因此SGLT-2在葡萄糖的动态平衡中发挥重要的作用,选择性抑制SGLT-2的活性可特异性地抑制肾脏对葡萄糖的重吸收。其抑制剂如Sergliflozin的IC50=350nmol/L,在一项为期14d的双盲试验中发现,给药组受试者肾脏葡萄糖的重吸收受到持续性抑制,呈现剂量依赖性尿糖,与安慰剂组相比,给药组也出现了不同程度的体重减轻。其他类似药物还有Remogliflozin和Dapagliflozin。
2.G蛋白偶联受体119激动剂
G蛋白偶联受体119(GPR119)是A型视紫红质孤立G蛋白偶联受体(GPCR),被激动后与其偶联的G蛋白α亚基与β、γ亚基解离,并分别介导胞内不同的信号通路,如刺激腺苷酸环化酶,导致细胞内cAMP水平升高和PKA活化,引起一系列级联反应,可调节胰岛素分泌和促进肠降血糖素GLP-1的释放。AR-231453是第一个通过高通量筛选及一系列结构改造获得的可以口服的GPR119小分子激动剂,可以通过特异性激活GPR119引起cAMP水平的上升,从而诱导胰岛β瘤细胞及小鼠原代胰岛细胞葡萄糖依赖性地分泌胰岛素,控制血糖,改善葡萄糖耐受性。还可刺激肠内分泌细胞株GLUTag分泌GLP-1,并且能够以间接方式促进GIP的释放,通过肠肽激素调节血糖水平,减少摄食,控制体重。PSN-375963的EC50=8.4μmol/L,对其进行结构修饰获得PSN-632408的EC50=5.6μmol/L。
3.其他靶点药物研究和中药提取物
糖尿病的发病涉及到糖代谢的各个环节,发病学说纷纭,作用靶点众多,所以围绕着GK、PTP1B、GSK等靶点其治疗药物也不断涌现。基于葡萄糖激酶(GK)为靶点的小分子激活剂,分别为RO-28-0450、GKA1和GKA2。糖基化终末产物抑制剂、蛋白激酶C-β抑制剂、醛糖还原酶抑制剂、抗氧化剂等可以作用于不同环节。Starlix是一种氨基酸衍生物,能刺激胰腺快速释放胰岛素,能全面降低血糖水平特别是餐后血糖高峰。此外,从天然药物中也可以提取、分离出多种具有药理活性的化合物,如黄芩苷具有有效的醛糖还原酶(AR)抑制剂,苦骨根的提取物含异黄酮,桑白皮、桑叶及桑椹中分离出多羟基生物碱,从嫩桑枝以及蚕沙中提取了1-脱氧野尻霉素等。
[1]Marre M, Shaw J, Br ndle M, et al.Liraglutide, a once-daily human GLP-1 analogue, added to a sulphonylurea over 26 weeks produces greater improvements in glycaemic and weight control compared with adding rosiglitazone or placebo in subjects with Type 2 diabetes(LEAD-1 SU)[J].Diabet Med, 2009, 26(3): 268-278.
[2]Nauck M, Frid A, Hermansen K, et al.Efficacy and safety comparison of liraglutide, glimepiride, and placebo, all in combination with metformin in type 2 diabetes mellitus (LEAD-2 Met)[J].Diabetes Care, 2009, 32: 84-90.
[3]Garber A, Henry R, Ratner R, et al.Liraglutide versus glimepiride monotherapy for type 2 diabetes (LEAD-3 Mono): a randomised, 52-week, phase III, double-blind, parallel-treatment trial[J].Lancet, 2009,373(9662): 473-481.
[4]Zinman B, Gerich J, Buse JB, et al.Efficacy and safety of the human GLP-1 analog liraglutide in combination with metformin and TZD in patients with type 2 diabetes mellitus (LEAD-4 Met+TZD)[J].Diabetes Care, 2009, 32: 1224-1230.
[5]Russell-Jones D, Vaag A, Schmitz O, et al.Liraglutide vs insulin glargine and placebo in combination with metformin and sulfonylurea therapy in type 2 diabetes mellitus (LEAD-5 met+SU): a randomised controlled trial[J].Diabetologia, 2009, 52(10): 2046-2055.
[6]Buse JB, Rosenstock J, Sesti G, et al.Liraglutide once a day versus exenatide twice a day for type 2 diabetes: a 26-week randomised,parallel-group, multinational, open-label trial (LEAD-6)[J].Lancet,2009, 374(9683): 39-47.
[7]Pratley RE, Nauck M, Bailey T, et al.Liraglutide versus sitagliptin for patients with type 2 diabetes who did not have adequate glycaemic control with metformin: a 26-week, randomised, parallel-group, openlabel trial[J].Lancet, 2010, 375:1447-1456
[8]DeFronzo R, Ratner R, Han J, et al.Effects of exenatide (synthetic exendin-4) on glycemic control and weight over 30 weeks in metformin-treated patients with type 2 diabetes [abstract].Presented at: American Diabetes Association 64th Annual Scientific Sessions;June 4-8, 2004; Orlando, Fla.Abstract 6-LB.
[9]Buse JB, Henry RR, Han J, et al.Effects of exenatide (exendin-4) on glycemic control over 30 weeks in sulfonylurea-treated patients with type 2 diabetes.Diabetes Care.2004, 27: 2628-2635.
[10]Kendall DM, Riddle MC, Dongliang Z, et al.Effects of exenatide(exendin-4) on glycemic control and weight in patients with type 2 diabetes treated with metformin and a sulfonylurea.Presented at:American Diabetes Association 64th Annual Scientific Sessions; June 4-8,2004; Orlando, Fla.Abstract 10-LB.
