汽车发动机废热化学水解制氢系统结构设计与分析*
2012-05-15朱景建
朱 景 建
(湖州职业技术学院 机电工程分院, 浙江 湖州 313000)
课题的提出主要基于以下三个方面:其一,内燃机废气带走的热能占加入燃料总热值的45%左右,排气废热回收一直是行业研究的重点。尽管普遍采用的废气涡轮增压技术较为成熟,但还存在不尽人意的地方,且该技术的废热回收率已到了极限;其二,汽车发动机加氢燃烧是节能和改善燃烧品质的新途径,该技术在国外已经用于汽车发动机。其三,汽车发动机采用富氧燃烧技术,以改善排放品质的研究方兴未艾,但在膜过滤技术中的膜材料成本和寿命问题难以解决[1]。如果能在燃烧过程的中后期实现喷氧助燃,将会有更好的效果。
鉴于此,将热化学水解制氢技术与汽车发动机废热回收及排放控制技术进行整合,将是一个两全其美的方案,在发动机上实现三种技术整合的关键:一是热化学水解制氢设备及工艺技术的微型化;二是汽车发动机排气温度的适度提高;三是在各化学反应阶段合理利用排气热量。本课题针对这三个技术问题,结合当前汽车发动机技术现状,以及汽车发动机技术的发展趋势。进行了如下理论研究、技术方案设计和基本数据测量。
1 热化学水解制氢基本原理
在全球能源生产向“氢能经济”转型的发展趋势下,以可再生资源水为原料生产氢气代替日益枯竭的化石能源,是一项巨大而又十分有意义的工程。目前分解水制氢的方法很多,包括光催化分解水制氢、电解水制氢、热解水制氢等。其中,硫碘循环反应热解水制氢方案,最被各国所看好,在日本等国已走出实验室,进入实验性生产阶段。硫碘循环反应热解水制氢整个生产过程的热效率已达到53 %以上,水的分解率达到32 %以上[2]。
硫碘循环反应热解水制氢的基本原理是控制以下四个化学反应进行的温度、速率以及中间生成物的浓度,并对中间产物进行有效的分离,从而维持反应的循环进行。整个反应过程只有热能的消耗和水的分解,而无其他物质的消耗和产生[3]。
SO2(g)+2I(s)+2H2O(l)→H2SO4(aq)+2HI(aq)
(1)
ΔrHm= -106.80 kJ/mol (反应温度:20℃-100℃)
2HI(g) → I2(g)+ H2(g)
(2)
ΔrHm=12.80 kJ/mol (反应温度:300℃-500℃)
H2SO4(aq) → SO3(g)+H2O(g)
(3)
ΔrHm=123.14 kJ/mol (反应温度:500℃-800℃)
SO3(g) → SO2(g)+ 1/2O2(g)
(4)
ΔrHm=62.76 kJ/mol (反应温度:800℃-950℃)
整个反应过程的基本条件是持续的高温热能,制约反应速率的关键是两种酸的液相分离和硫酸分解所需的恒定高温条件。对于硫碘循环反应热解水制氢,氢气的生产成本主要是反应所需要的热能成本。
2 发动机废热用于热化学水解制氢的优点
发动机废热用于热化学水解制氢技术方案的优点体现在以下几个方面:
一、为发动机废热回收利用开辟了新途径,间接提高了发动机热效率。
二、扩展了热化学水解制氢技术的应用领域,避开了该技术的推广利用受高能耗制约的难题。
三、可将废热制取的氢气和氧气用于发动机燃烧做功,有效改善燃烧品质,大幅度降低CO和HC等有害物的排放[4]。
3 发动机废热用于热化学制氢技术方案设计
热解水制氢设备外形结构及内部结构如图1所示,反应工艺流程图2所示。
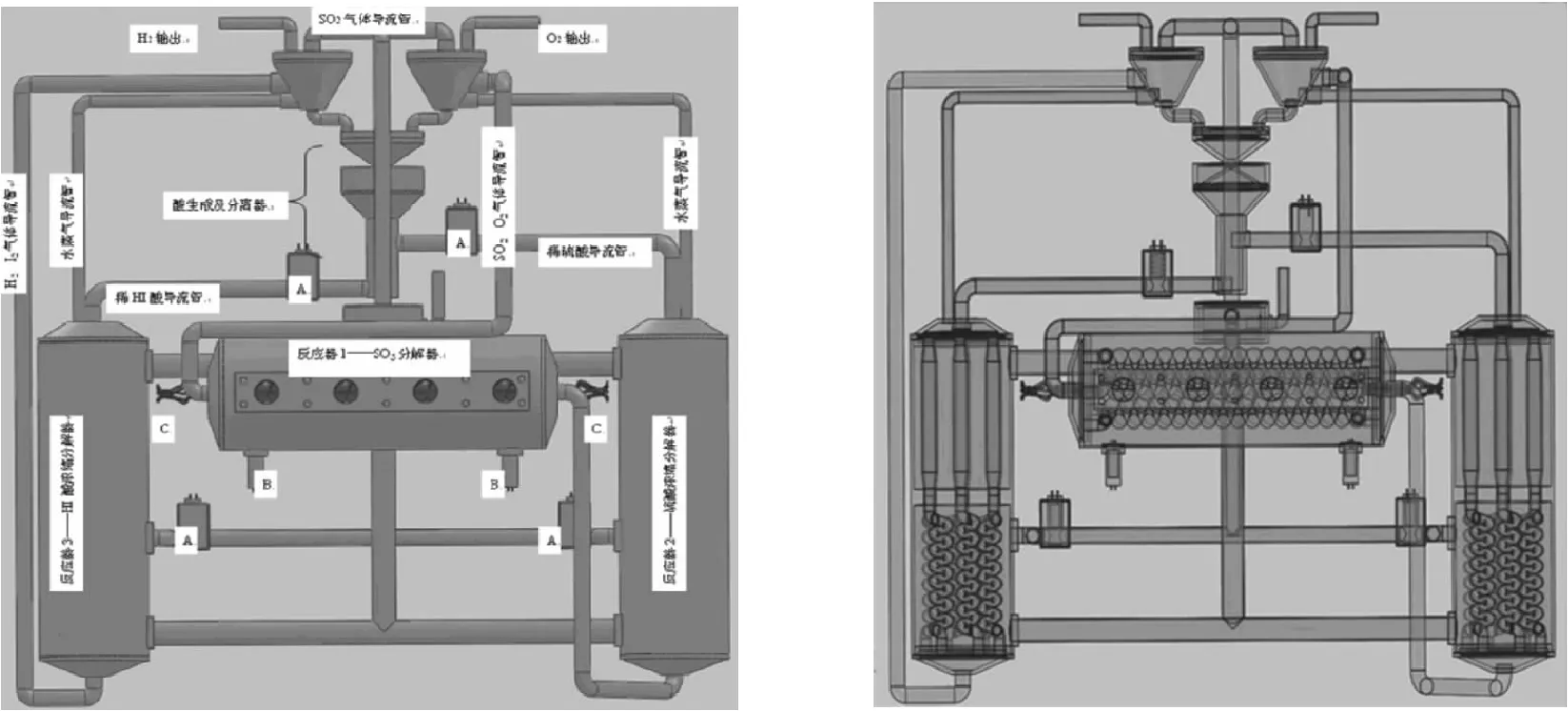
(a) 外形结构 (b)内部结构
图1硫碘循环反应热解水制氢系统结构图(A-温控开关, B-温度传感器, C-加热导线)
为了利用汽车发动机废气热量,对制氢设备与汽车发动机的连接处理如下:反应器1的法兰面安装在气缸盖排气出口位置上,四个圆孔对应发动机的各缸排气出口,SO3在其内部加热分解。反应器芯上缠绕有辅助加热电阻丝,可使反应器1内部温度始终维持在850 ℃-950 ℃之间;反应器2分为上、下两部分,上部加热浓缩稀硫酸,下部加热分解浓硫酸为H2O+SO3。反应器3分为上、下两部分,上部加热浓缩稀氢碘酸,下部加热分解浓氢碘酸为H2+I2。反应器4是一个组合容器,在其中完成了SO2的吸收、I2的溶解以及两种酸溶液的分离。
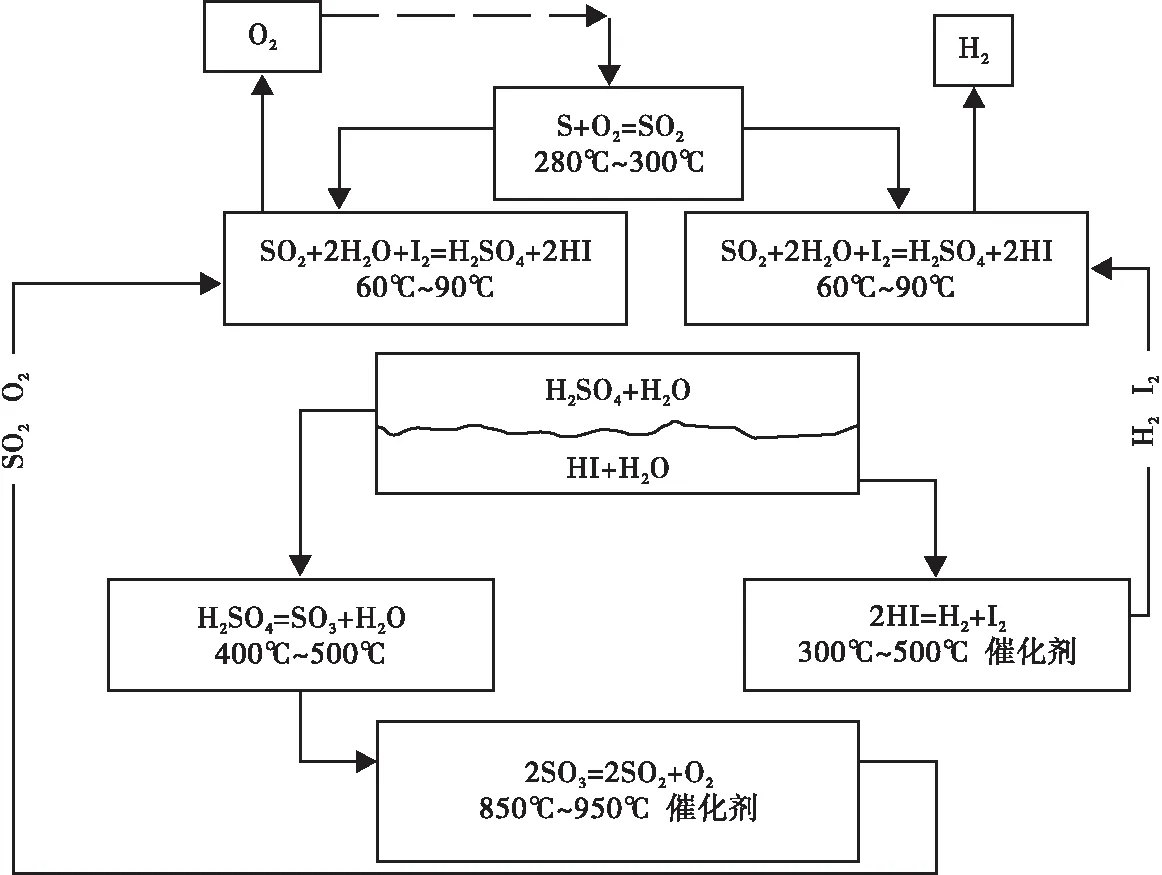
图2 硫碘循环反应热解水制氢工艺流程
发动机在额定工况下的排气温度大约是850 ℃(气缸盖出口处测量),在气缸盖的排气道上加装一个陶瓷绝热隔套,出口温度可提高40-70 ℃,在不采取保温措施的情况下,距离气缸盖500 mm处,排气温度降到了650 ℃左右。将发动机排气管换成模拟化学反应器的加热管道(具有双层绝热陶瓷外壳),测量以上(2)、(3)、(4)化学反应进行所在位置的温度,可以分别达到700-600 ℃、700-600 ℃、900-850 ℃。测量结果表明:发动机排气系统进行结构改造后,排气温度可以满足所选化学反应进行的温度条件。为使发动机排气维持较高的温度,在缸盖排气道上加装陶瓷绝热隔套,进一步降低排气热量耗散;采用双层陶瓷绝热外壳的化学反应装置代替传统的排气管。
4 热能条件及效益分析
4.1 热能条件分析
实验用一台额定功率100 kW的发动机工作一小时,额定工况油耗为8 L/h。发动机正常燃烧时,排气带走的热量占所燃汽油热值的40-45 %,取40 %计算。每小时排气带走热量为:8L×0.73 kg/L×44 000 kJ /kg×40 %=102.78×103 kJ。制取150 g氢气所需理论热量(根据化学反应式(2)、(3)、(4)算得)[5]:
QHI=150 g×12.8/2=0.960×103kJ
QH2SO4=150 g×123.14/2=9.235×103kJ
QSO3=150 g×62.76/2=4.707×103kJ
理论上化学反应总吸热量为:
Q=QHI+QH2SO4+QSO3=(0.960+9.235+4.707)×103 kJ=14.902×103kJ
由于循环水的分解率只有三分之一,实际生产所需总热量应为:
3Q=44.706×103kJ
理论化工热量利用率=44.706×103kJ /102.78×103kJ =43.5 %。
初步计算说明:发动机废气热量能够充分满足制氢生产的热能条件。一般的化工生产热效率通常小于50 %,本文设计的设备热效率为43.5 %,略低于日本该制氢工艺的最高热效率53 %。
4.2 实际效益分析
发动机排气废热制取氢气150 g,相当于0.67 L汽油热值。但保持SO3分解反应温度不低于900 ℃,所采用的辅助加热电阻增加了发动机油耗0.14 L/h。回收废热制取的氢气用于燃烧后,实际节油相当于:(0.67 -0.14)=0.53 L/h。回收排气废热制取了氢气,用于发动机加氢燃烧,直接降低油耗6.6 %。实际上,由于加氢燃烧,改善了燃烧品质,油耗降低值会远大于6.6 %。
5 结 论
本文通过热力学计算和对汽车发动机排气系统改造,设计了一个化学反应系统,采集排气的高温热能,用于硫碘循环反应热解水制氢。通过本文的设计,使制取的氢气和氧气反馈到发动机燃烧,其热效率达到43.5 %,直接降低发动机油耗6.6 %以上。
参考文献:
[1] 李胜琴,关 强.汽油发动机富氧燃烧特性研究[J].小型内燃机与摩托车,2007(6):30-33.
[2] 刘广义.热化学硫碘循环制氢中Bunsen反应与碘化氢分解的模拟与实验研究[D].浙江大学硕士学位论文,2006.
[3] 翟秀静.新能源技术----氢燃料[M].北京:化学工业出版社,2006:83-84.
[4] 刘福水,郝利君.氢燃料内燃机技术现状与发展展望[J].汽车工程,2006(7):621-624.
[5] 刘宝兴.工程热力学[M].北京:机械工业出版社,2006:32-33.
