硫酸依替米星临床安全性研究综述
2012-05-08陈永法曹文帅
陈永法 曹文帅
硫酸依替米星临床安全性研究综述
陈永法 曹文帅
目的了解硫酸依替米星在临床使用安全性及不良反应,促进合理用药。方法检索2000~2012年硫酸依替米星相关文献并整合分析。结果与结论依替米星主要不良反应为耳毒性、肾毒性、变态反应、肝损害以及恶心呕吐等胃肠道反应。不良反应发生率大多在1%以下且低于阿米卡星,肝损害发生率显著低于妥布霉素和头孢呋辛,耳毒性发生率略低于奈替米星,其他不良反应发生率与奈替米星大致相当。
硫酸依替米星;安全性;不良反应
氨基糖苷类抗生素上市至今已有70多年历史,随着临床的广泛运用,人们对氨基糖苷类抗生素安全性也具有了较深的了解。这类抗生素的不良反应主要包括耳毒性、肾毒性、神经肌肉阻滞作用、变态反应和其他不良反应[1]。依替米星作为第三代氨基糖苷类抗生素,与早期氨基糖苷类药物相比,以上不良反应发生率大大降低[2]。为研究硫酸依替米星临床安全性情况,本文检索2000~2012年硫酸依替米星相关文献并进行整合分析,探讨其安全性。以下就依替米星不良反应与其他同类抗生素进行对照分析。
1 耳毒性
氨基糖苷类药物成分会在耳内蓄积,使感觉毛细胞发生永久性改变,从而造成失聪。此外它还会造成前庭和耳蜗神经等内耳结构的损伤,内耳结构不仅与听力有关,还与平衡感有着密切的关系,因而氨基糖苷类药物常见的不良反应还有眩晕、恶心、呕吐、眼球震颤和平衡失调[3]。
1.1硫酸依替米星耳毒性临床表现依替米星 II期临床试验耳毒性不良反应发生率为 1.9%,III期临床试验耳毒性发生率为 0.73%[4],从临床实验结果看,依替米星耳毒性发生率较低,安全性较高。依替米星上市后,很多学者对依替米星耳毒性进行临床研究。选取例数大于300例的临床研究,总结其耳毒性研究结果,详见表1。
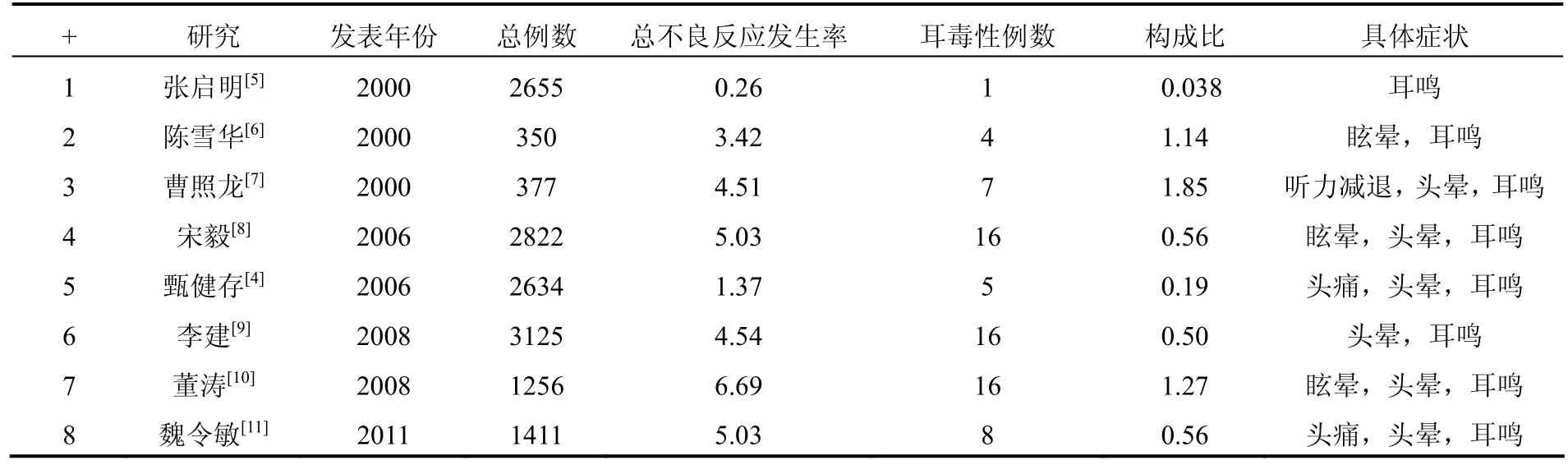
表1 不良反应-耳毒性表(n,%)
以上研究可以发现,依替米星耳毒性主要症状为头晕、眩晕、耳鸣,发生率大多在 1%以下,发生率较低。
1.2耳毒性不良反应发生率与同类产品比较依替米星与阿米卡星安全性对照研究结果显示,依替米星组耳毒性发生率为 1.54%(1/65),阿米卡星组为15.15%(10/66)[12],可以看出依替米星耳毒性显著低于阿米卡星。依替米星与奈替米星安全性对照研究结果显示,依替米星组耳毒性发生率为1.89%(2/106),奈替米星组为3.77%(4/106)[13],崔学军[14]曾对以上研究结果进行验证,依替米星组发生1例眩晕,发生率为1.25%(1/80);奈替米星组发生2例耳鸣,发生率为2.50%(2/80),由此可见在耳毒性方面依替米星略低于奈替米星,由于以上两种试验数据量较小,结果还需进一步验证。
2 肾毒性
氨基糖苷类药物经肾代谢,会在肾脏蓄积并损害肾小管上皮细胞,有明显的肾毒性。同时,在使用过程中会出现蛋白尿、管形尿甚至无尿症的肾毒性反应[3]。虽然氨基糖苷类药物的肾毒性可逆,即停药后肾功能会恢复,但是药物对肾脏的影响会减缓其经肾的代谢和排泄,从而提高体内药物的含量,加剧药物的肾毒性[15]。
2.1硫酸依替米星肾毒性临床表现依替米星 II期临床试验肾毒性发生率为2.8%,稍高于奈替米星(2.0%),III期临床试验肾毒性发生率下降到0.37%[4],随着临床试验例数的增多,肾毒性发生率有较大的下降。选取例数大于300例的临床研究,其依替米星肾毒性研究结果,见表2。

表2 不良反应-肾毒性表(n,%)
以上研究可以看出,依替米星肾毒性主要症状为BUN升高,Cr升高,UA升高,蛋白尿,尿素氮升高,尿中红细胞,管型尿等。大样本数据发生率多在1%以下,发生率较低。
2.2肾毒性不良反应发生率与同类产品比较依替米星与阿米卡星安全性对照研究结果显示,依替米星组未发现肾毒性反应,而阿米卡星组却发现 2例蛋白尿、管型尿等肾损害[17]。较多学者对依替米星与奈替米星进行安全性对照研究,其结果存在一定差异,但相差不大,例如在治疗下呼吸道感染研究中,依替米星组肾毒性发生率为1.22%(1/82),奈替米星组为 2.44%(2/82)[18];在治疗细菌性感染多中心临床试验中,依替米星组肾毒性发生率为1.89%(2/106),奈替米星组为0.94%(1/106)。由此可以看出,依替米星肾毒性与奈替米星大致相当,而低于阿米卡星。
3 神经肌肉阻滞作用
氨基糖苷类药物会与突触前膜表面的钙离子结合部位结合,阻止乙酰胆碱的释放。乙酰胆碱是在突触间传导神经冲动的递质,抑制这种物质的释放会阻碍神经冲动在神经和肌肉之间的传导。此类不良反应严重者会产生肌肉麻痹甚至呼吸暂停。依替米星上市后,较少有学者报道依替米星引起神经肌肉阻滞作用的副作用,这说明依替米星在此方面具有较高的安全性[19]。
4 变态反应
变态反应即通常的过敏反应,是各类药物都会出现的不良反应。氨基糖苷类药物多为微生物代谢产物提取物,变态反应发生率比合成药物更高,使用时会发生皮疹、血管神经性水肿、发热、剥脱性皮炎等症状,个别严重者会引起过敏性休克[19]。
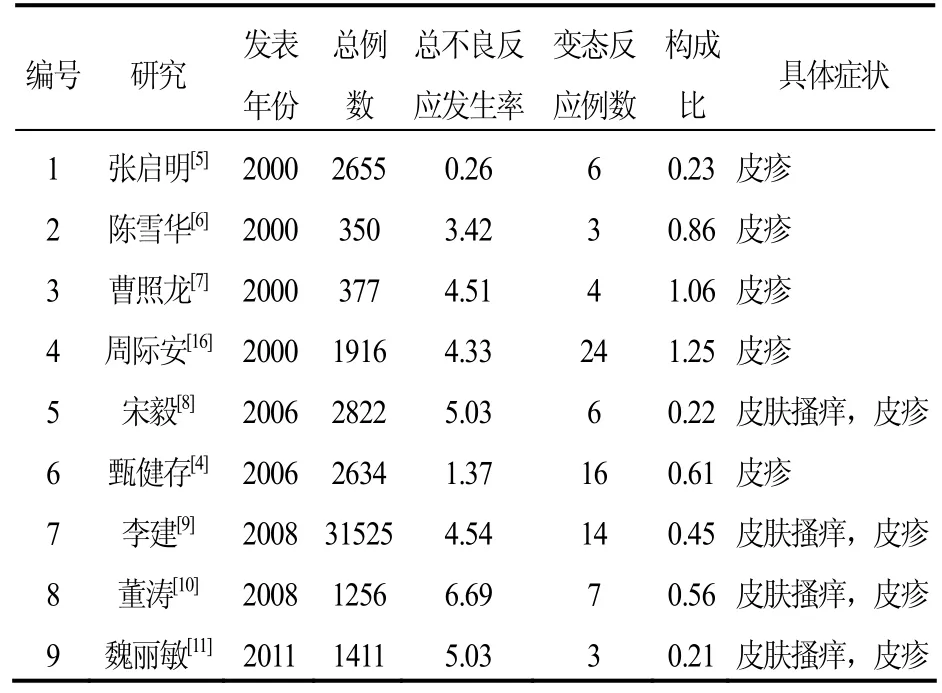
表3 不良反应-变态反应表(n,%)
4.1硫酸依替米星变态反应临床表现变态反应为氨基糖苷类药物较常见的不良反应,对硫酸依替米星,学者临床试验记录比较多的为皮疹。选取例数大于300例的临床研究(见表3),结果显示依替米星皮疹发生率大多在1%以下,发生率较低。
4.2变态反应发生率与同类产品比较较少有学者提及依替米星与阿米卡星关于变态反应的对比,而与奈替米星对比较多。李家泰[13]、唐春兰[18]、崔学军[14]三人研究结果均显示依替米星组皮疹发生率与奈替米星组相同,分别为0.94%、1.2%、1.25%。由此可以看出在变态反应方面依替米星与奈替米星大致相当。
5 其他
部分氨基糖苷类药物可能引起肝损害,使转氨酶升高,表现为食欲下降、恶心呕吐,少数还会出现黄疸,一旦停药很快恢复正常;也可能引起多发性周围神经炎,但比较少见[19]。
5.1硫酸依替米星肝损害临床表现在依替米星研究中,学者比较重视药物是否对肝功能产生影响,对肝功能指标进行监测,其中例数大于300例的临床研究结果(见表 4)显示,依替米星肝损害主要症状表现为ALT升高。
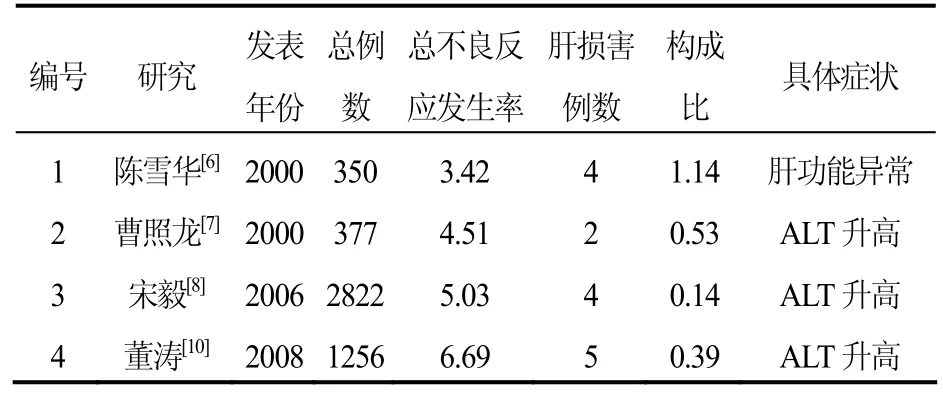
表4 不良反应-肝损害表(n,%)
5.2肝损害不良反应发生率与同类产品比较依替米星与妥布霉素的对照试验中,依替米星组ALT升高率为 1.22%(1/82),而妥布霉素组升高率为4.23%(3/71)[20],依替米星肝损害发生率明显低于妥布霉素。依替米星与头孢呋辛的对照试验中,依替米星组ALT升高率为1.47%(2/136),头孢呋辛组为7.46%(5/67),依替米星肝损害发生率也明显低于头孢呋辛[21]。依替米星与奈替米星临床对照研究显示,两者 ALT升高率大致相当,均为 3.12%(1/32)[12]。通过以上研究可以看出,依替米星肝损害发生率显著低于妥布霉素和头孢呋辛,与奈替米星大致相当。
5.3硫酸依替米星恶心呕吐临床表现也曾有学者在研究中报道恶心、呕吐等不良反应,但与同类产品对比较少,在此仅列出总例数大于 300的临床试验结果(见表5)显示,其发生率在0.23%~3.02%。
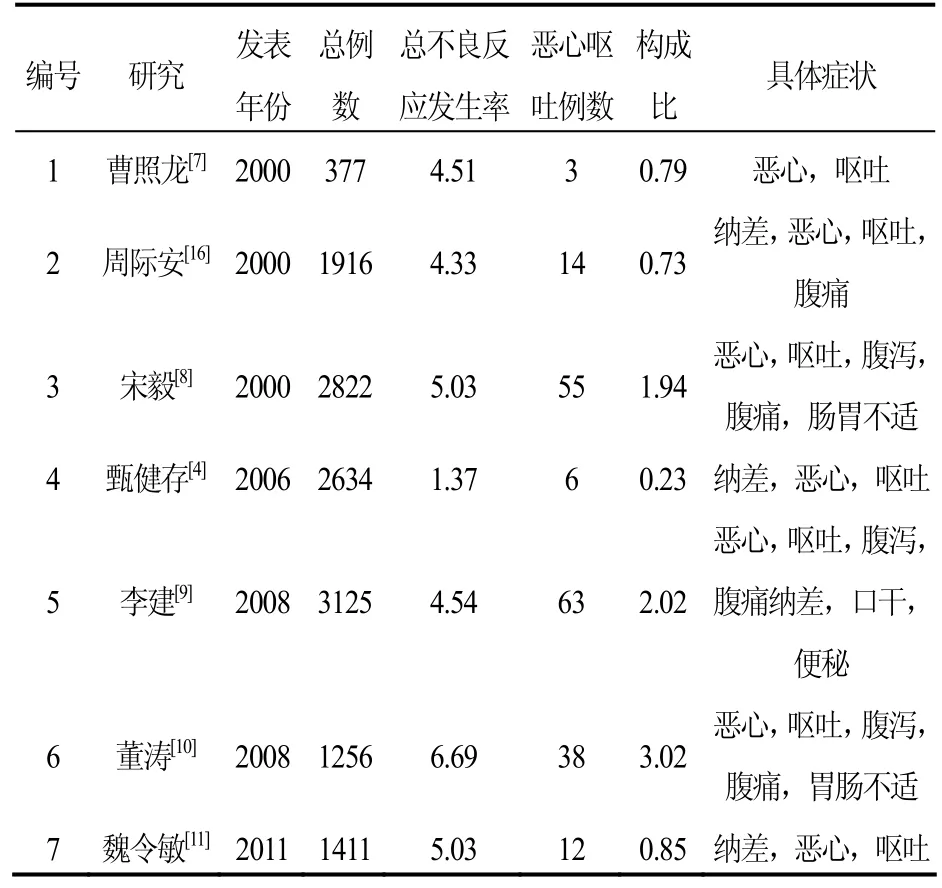
表5 不良反应-恶心呕吐表(n,%)
6 结论
通过以上分析表明,依替米星的主要不良反应为耳毒性(头晕、眩晕、耳鸣),肾毒性(BUN升高、Cr升高、UA升高、蛋白尿、尿素氮升高、尿中红细胞、管型尿),变态反应(皮肤搔痒,皮疹),肝损害(ALT升高)及恶心、呕吐等胃肠道反应,发生率大多在1%以下,发生率较低。其各方面不良反应发生率均低于阿米卡星,肝损害不良反应显著低于妥布霉素和头孢呋辛,耳毒性不良反应略低于奈替米星,其他不良反应发生率与奈替米星大致相当。
[1]胡华成,刘诗丽.氨基糖苷类抗生素不良反应[J].医师进修杂志,2005,28(11):3-4.
[2]诸玲玲,孟现民,张永信.氨基糖苷类药物的发展历程[J].上海医药,2011,32(7):322-236.
[3]赵曲川,王长远.硫酸依替米星的临床应用研究进展[J].山东医药,2009,49(49):118-119.
[4]甄健存,王育琴.依替米星上市后安全性初步调查[J].药物不良反应杂志,2006(01):59-61.
[5]张启明,丁少华,吴伟.硫酸依替米星用于骨科术后的疗效分析[J].中国抗生素杂,2000(S1):49-50.
[6]陈雪华,何礼贤,胡必杰.硫酸依替米星治疗350例细菌性感染的临床研究[J].中国抗生素杂志,2000(S1):6-10.
[7]曹照龙,陈尔璋.依替米星治疗细菌性感染377例临床评价[J].中国抗生素杂志,2000(S1):11-13.
[8]宋毅.2822例患者应用硫酸依替米星注射剂安全性分析[J].中国抗生素杂志,2006(01):31-32.
[9]李建,宋毅,徐廷.硫酸依替米星注射剂不良反应的临床观察[J].华西医学,2008,23(1):83-84.
[10]董涛.注射用硫酸依替米星的临床不良反应分析[J].中国医院用药评价与分析,2008,8(10):795-796.
[11]魏令敏.应用硫酸依替米星注射剂 1411例患者安全性探讨[J].中国实用医药,2011,6(12):148-149.
[12]张传军,鲁惠敏.依替米星与阿米卡星临床疗效及安全性比较[J].医药论坛杂志,2008(02):4-6.
[13]李家泰.依替米星与奈替米星随机对照治疗细菌性感染多中心临床试验[J].中国临床药理学杂志,2000(01):10-14.
[14]崔学军.对贵刊《依替米星与奈替米星治疗下呼吸道细菌感染》一文的验证[J].中国新药与临床杂志,2005(11):920-921.
[15]邓拮杰.依替米星治疗细菌性感染 53例临床分析[J].中华实用中西医杂志,2000,13(11):2359-2359.
[16]周际安.注射用硫酸依替米星 III期临床试验[J].中国抗生素杂志,2000,25:1-5.
[17]杨宇,赵丽娟,张晓莉,等.硫酸依替米星治疗风湿免疫性疾病合并各类感染的临床疗效[J].中国抗生素杂志,2000(S)1:25-27.
[18]唐春兰.依替米星与奈替米星治疗下呼吸道细菌感染临床疗效及安全性比较[J].中国新药与临床杂志,2004(02):83-87.
[19]邓筱华.硫酸依替米星的临床应用与安全性评价[J].中国临床药学杂志,2004,14(5):320-322.
[20]李航,李鹏.依替米星与妥布霉素治疗急性细菌性感染的疗效比较[J].中国药房,2000(03).
[21]涂明义,马燕妮.依替米星治疗脑出血继发肺部感染的临床观察[J].中国抗生素杂志,2000(S1):36-37.
中国药科大学国际医药商学院,江苏南京 211198
