水合肼直接还原硫代钼酸铵晶体制备超细二硫化钼
2012-04-24刘前明肖连生曾理龚柏凡
刘前明,肖连生,曾理,龚柏凡
(中南大学,湖南长沙410083)
0 前言
二硫化钼为银灰色的粉末,属于六方晶系。天然二硫化钼是一种抗磁性且具有半导体性质的化合物,其Mo-S棱面相当多,比表面积大,层内是很强的共价键,层间则是较弱的范德华力,键能很低,层与层之间容易剥离,显示出很低的摩擦因数。因硫对金属具有很强的粘附力,使二硫化钼能很好地附着在金属表面始终发挥润滑功能,特别是在较高温、高真空等条件下仍具有较低的摩擦因数[1]。因此二硫化钼有很广阔的应用前景,除了可以应用于摩擦润滑[2]领域外,还可以应用于储氢[3,4]、电极[5]、催化[6]等领域中。
制备超细二硫化钼的方法一般分为物理法和化学法。物理法是指天然矿物辉钼矿经浮选、化学浸取等方法提纯后借助机械研磨[7]、高能物理[8]等手段对二硫化钼进行粉碎、切割或喷涂从而制备出超细的二硫化钼,物理法一般不破坏二硫化钼的天然晶格,但设备要求高,方法不灵活,获得的产物种类少。化学法是指通过化学反应制备二硫化钼,并在制备过程中通过控制反应条件来达到降低粒度的目的,从而制备出超细的二硫化钼,一般包括还原法[9-10]、分解法[11]、氧化法[12]、电化学法[13]等,化学法灵活性强,产物纯度高,能制备出符合不同功能需求的二硫化钼。
在仲钨酸铵(APT)生产过程中,为了获得纯的钨产品,现大多数采用加硫化剂来实现钨与钼的分离,因而会产生硫代钼酸铵这种副产品,利用这些副产品来制取二硫化钼,具有重要的意义。而国内以硫代钼酸铵为原料直接制备二硫化钼的研究很少[14],本文以水合肼为还原剂直接还原硫代钼酸铵晶体,制备超细颗粒的二硫化钼,并研究了不同的实验条件对还原反应的影响。
1 实验
1.1 基本原理
硫代钼酸铵晶体与强还原剂水合肼发生还原反应得到产品二硫化钼,化学反应式如下:
(NH4)2MoS4+1/2N2H4—→MoS2↓+1/2N2↑
+(NH4)2S+H2S↑
1.2 实验试剂及仪器
实验采用的原料是某工厂在钨钼生产流程中得到的副产品硫代钼酸铵晶体,化学式为(NH4)2MoS4,属正交晶系,暗红色针状晶体,有刺鼻的氨味,其化学元素成分含量及物相分析结果如表1和图1。

表1 原料XRF 分析结果%

图1 原料(NH4)2MoS4的XRD分析结果
由表1可知,原料中Mo与S的摩尔比接近1∶4,结合图1的XRD物相分析结果得出原料为硫代钼酸铵晶体,并且(NH4)2MoS4的纯度很高。
其他试剂有:水合肼(80%,16.8 mol/L),纯水等。主要仪器有:三口瓶(250 mL、500 mL),SENCO搅拌浆,KDM型控温电热套(250 mL、500 mL),真空干燥箱等。
1.3 实验过程
取一定量的硫代钼酸铵晶体和水合肼溶液加入到三口瓶中,并加入适量的纯水,三口瓶的三个口一个接温度计控制温度,一个接搅拌浆,一个接冷凝管,控制电热套的温度并搅拌。反应过程中溶液从暗红色渐渐转变为黑色溶液,反应结束后,取出进行过滤,滤液计量体积并分析钼含量,滤渣体放于真空干燥箱中干燥至恒重,称重并送分析。
1.4 元素分析及数据处理
因为原料中(NH4)2MoS4的纯度很高,因此本实验分析的元素主要为Mo,采用硫氰酸按比色法分析滤液中钼的含量,根据下式计算硫代钼酸铵的还原率ω为:

2 条件实验结果与分析
2.1 反应温度
实验过程中不变的条件:水合肼与硫代钼酸铵的摩尔比为20∶1(水合肼5 mL,硫代钼酸铵晶体1.092 g),加纯水100 mL,反应时间为4 h,搅拌转速为320 r/min,考察不同的反应温度对还原效果的影响。实验的结果如图2所示,可知随着反应温度的增加,还原率逐渐升高,当温度升到95℃以上时,还原率增幅很小,再升高温度对反应的意义不大,因此选择反应温度为95℃。
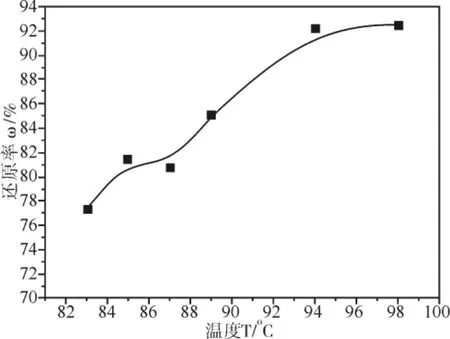
图2 不同的反应温度对还原的影响
2.2 反应时间对还原的影响
实验过程中不变的条件::水合肼与硫代钼酸铵的摩尔比为20∶1(水合肼5 mL,硫代钼酸铵晶体1.092 g),温度为95℃,加纯水100 mL,搅拌转速为320 r/min,考察不同的反应时间对还原效果的影响。实验结果如图3所示,可知2~3 h之间还原率增幅较大,当反应时间为3 h时其还原率达到最佳,而3 h之后增加反应时间,其还原率略微有些下降,可能的原因是反应时间的增加,反应的溶液体积减少的缘故,因此反应时间可以选择为3 h。
2.3 水合肼与硫代钼酸铵的摩尔比对还原的影响
实验过程中不变的条件:温度为95℃,时间为3 h,加纯水100 mL,搅拌转速为320 r/min。考察在不同的水合肼与硫代钼酸铵的摩尔比对还原反应的影响,其结果如图4所示,可知在摩尔小于5∶1时还原率很低,在小于10∶1时,发现滤液浑浊,难以过滤澄清,过滤几次后通过离心机分离才能取得澄清的滤液,当摩尔比达到10∶1时溶液过滤容易,还原率达到97%,再增大摩尔比对还原率的影响没有很大的改善,因此水合肼与硫代钼酸铵的摩尔比可选择为10∶1。
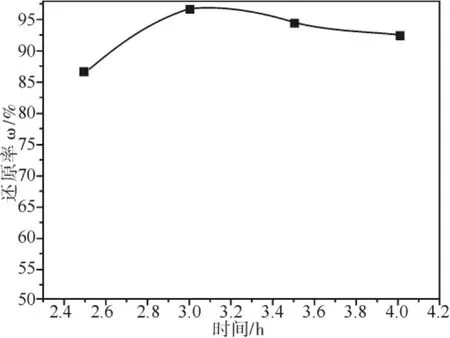
图3 不同的反应时间对还原的影响
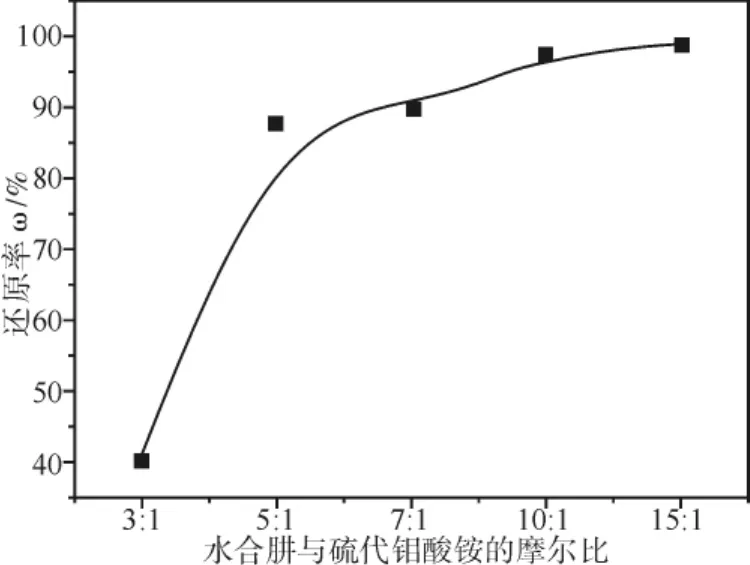
图4 不同的摩尔比对还原反应的影响
2.4 搅拌速度对还原的影响
实验过程中不变的条件:水合肼与硫代钼酸铵的摩尔比为10∶1(水合肼5 mL,硫代钼酸铵晶体2.641 g),温度为95℃,时间为3 h,加纯水100 mL,考察了搅拌转速对还原反应的影响。其结果如图5所示,由图5可知随着搅拌转速的增加,其还原率变化幅度较小,因此可以忽略不计。
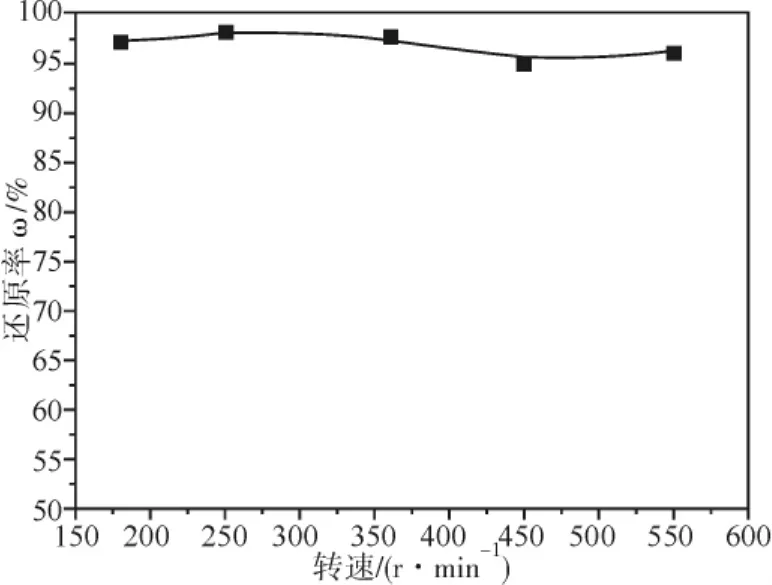
图5 搅拌转速对还原反应的影响
2.5 表征
依据前面的条件实验得到最佳的实验条件为:水合肼与硫代钼酸铵的摩尔比为10∶1,温度为95℃,反应时间为3 h,转速取250 r/min。图6为最佳实验条件下得到的产物的XRD图,由图5可知产物为非晶型的粉末,对比图1可知硫代钼酸铵晶体已经不存在。图7是产物MoS2的扫描电镜照片和EDS图,由图可知,最大的颗粒只有几微米,小的可以达到几纳米,而且产物触手滑腻。由EDS图可知产物中主要的元素为Mo和S,根据表3的结果得到其原子分数的比值接近1∶2,可以判断产物为MoS2。
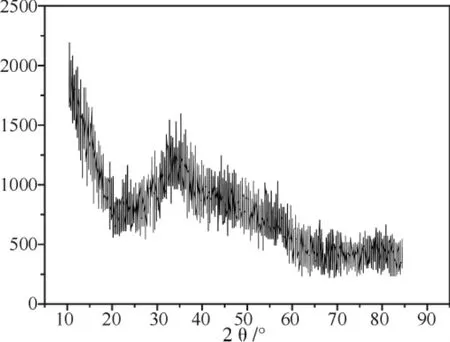
图6 产物的XRD图

图7 产物的SEM照片和EDS图
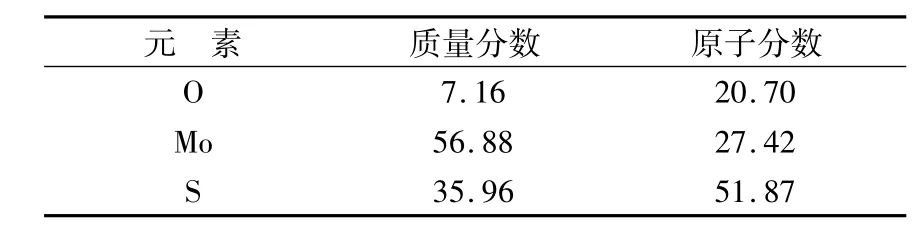
表3 EDS微区元素分析结果
3 结论
(1)探索了一条简单的制备细颗粒MoS2的方法,由实验可知,反应过程中水合肼与硫代钼酸铵的摩尔比、反应温度、反应时间均对还原反应的影响很大,而搅拌器的转速等对还原反应的影响微乎其微,在这一基础上最终优化了其反应条件为:控制水合肼与硫代钼酸铵的摩尔比为10∶1,反应温度为95℃,反应时间为3 h。
(2)所制备的二硫化钼产品触手滑腻,具备一定的润滑效果,而且颗粒细小,最大的颗粒只有几微米,小的可以达到几纳米。
(3)由SEM图可知,由于分散效果差,很多细颗粒团聚在一起,因此团聚依然是制备细颗粒MoS2的难点,可以尝试添加表面活性剂,达到分散的效果。
[1]松永正久.固体润滑手册[M].机械工业出版社,1986:87-98.
[2]Cizaire L.,Vacher B.,et al.,Mechanisms of ultra-low friction by hollow inorganic fullerene-like MoS2nanoparticles[J].Surface and Coatings Technology,2002,160:282-287.
[3]Chen J.,Kuriyama N.,et al.,Electrochemical hydrogen storage in MoS2nanotubes[J].J.Am.Chem.Soc.2001,123:11813-11814.
[4]Chen J.,Li S.L.and Tao Z.L.,Novel hydrogen storage properties of MoS2nanotubes[J].Journal of alloys and compounds,2003.356-357:413-417.
[5]WANG S.Q.,Li G.H.,et al.Hydrothermal synthesis of molybdenum disulfide for lithium ion battery applications[J].Chinese Journal of Chemical Engineering,2010,18(6):910-913.
[6]Del Valle M.,Cruz-Reyes J.,et al.,Hydrodesulfurization activity of MoS2catalysts modified by chemical exfoliation[J].Catalysis letters,1998.54:59-63.
[7]Kuriki Y.,Uchida K.,et al.,Ultra fine particles of molybdenum disulfide prepared by the mechanical method and their activity:Hydrogenation of 1-methylnaphthalene and coal liquefaction[J].Journal of the National Institute of Materials and Chemical Research,1999,7(3):143-155.
[8]Chhowalla M.and Amaratunga GAJ.Thin films of fullerene-like MoS2nanoparticles with ultra-low friction and wear[J].Nature,2000,407(6801):164-167.
[9]Zhan J.H.,Zhang Z.D.,et al.,Solvothermal synthesis of nanocrystalline MoS2from MoO3and elemental sulfur[J].J.Solid State Chem.,1998,(141):270-273.
[10]Pavel Afanasiev,et al.Surfactant-assisted synthesis of highly dispersed molybdenum sulfide[J].Chem.Mater.1999,11:3216-3219.
[11]Wang H.W.,Skeldon P.,Thompson G.E.,Thermogravimetric-differential thermal analysis of the solid-state decomposition of ammonium tetrathiomolybdate during heating in argon[J].J.Mater.Sci.,1998(33):3079-3083.
[12]Duphil D.,Bastide S.,et al.,Chemical synthesis of molybdenum disulfide nanoparticles in an organic solution[J],J.Mater.Chem.,2002,12:2430-2432.
[13]Ponomarev E.A.,Neumann-Spallart M.et al.,Electrochemical deposition of MoS2thin films by reduction of tetrathiomolybdate[J].Thin Solid Films,1996,280(1-2):86-89.
[14]马江虹,翟玉春.热分解法制备二硫化钼纳米粉末的研究[J].稀有金属与硬质合金,2004,32(3):1-4.
