地塞米松羧甲基魔芋胶小丸的大鼠体内释药探讨
2012-04-06侯世祥
张 瑜,侯世祥
(1.河南大学 药物研究所,河南 开封 475004;2.四川大学 华西药学院,四川 成都 610041)
地塞米松羧甲基魔芋胶小丸的大鼠体内释药探讨
张 瑜1,侯世祥2*
(1.河南大学 药物研究所,河南 开封 475004;2.四川大学 华西药学院,四川 成都 610041)
目的研究地塞米松羧甲基魔芋胶小丸体内释药情况,评价其结肠定位释药特性。方法以地塞米松羧甲基纤维素钠混悬液为对照,将地塞米松羧甲基魔芋胶小丸大鼠灌胃给药(以地塞米松量计,给药剂量为10mg/kg),采用HPLC法测定大鼠体内血药浓度经时变化和粪便排泄物中药物量经时变化,计算制剂在结肠内容物的相对靶向释药指数。结果与对照组相比,小丸组血药浓度存在1h时滞,Tmax由4h延至8h,Cmax由(6.46±0.92)mg/L明显降低为(1.33±0.36)mg/L,P<0.01;AUC0→24由(70.72±9.62)mg·L-1·h-1明显降低为(15.82±4.01)mg·L-1·h-1,P <0.01;粪便中排泄药物量由(29.20±5.77)μg明显提高为(198.2±38.07)μg,P<0.01;小丸组在大鼠结肠内容物的药物相对靶向释药指数为30.34。结论地塞米松羧甲基魔芋胶小丸具有结肠定位释药特性。
地塞米松;羧甲基魔芋胶小丸;结肠定位释药系统;体内释药
炎症性肠道疾病(inflammatory bowel disease,IBD)是一类常见的结肠局部疾病,包括溃疡性结肠炎和克罗恩氏病等,在西方国家发病率高。随着我国人民生活水平不断提高及人们饮食习惯的改变,其发病率呈逐年上升趋势。此病的发病部位主要位于胃及肠道下段的盲肠、结肠处,普通制剂口服给药在胃、肠道上段较多被吸收,使得患处药物浓度低,影响药效,同时进入体循环的药物易产生毒副作用。口服结肠定位给药系统可通过制剂学手段,减少药物胃、肠道上段的释放,使药物到达盲肠、结肠部位后,崩散释放。这种新型给药系统,是目前研究的热点[1-2]。前期体外释药研究发现,地塞米松羧甲基魔芋胶小丸具有结肠模拟酶-β-甘露聚糖酶降解释药的特性。考虑到体内、体外试验通常存在一定偏差,为进一步评价小丸是否具有结肠定位释药特性,我们采用滴制离子凝胶法制备地塞米松羧甲基魔芋胶小丸,大鼠灌胃给药后测定血浆和肠道排泄物中药物浓度的经时变化情况,并与对照组进行比较,评价其结肠定位释药特性。
1 实验材料
1.1 药品与试剂
地塞米松(天津天药药业股份有限公司,含量99.5%);地塞米松对照品(中国药品生物制品检定所);羧甲基魔芋胶(自制,取代度为0.479);甲醇(色谱纯);其他试剂均为分析纯。
1.2 仪器
SHIMAZU LC-10A(日本);Startorious 1721型电子天平(西德);YKH-II型液体快速混合器(江西医疗器械厂);SK-5200H超声清洗仪(上海科导超声仪器有限公司);TGL-16G台式高速离心机(上海安亭科学仪器厂)。
1.3 动物
Sprague Dawley大鼠,体质量220~250g,四川大学实验动物中心提供。
2 方法和结果
2.1 制剂的制备
2.1.1 地塞米松羧甲基魔芋胶小丸 配制20g/L的羧甲基魔芋胶水溶液,然后加入地塞米松(药物与羧甲基魔芋胶的质量比为1∶1),充分搅拌得均匀混悬液,用注射器将上述混悬液经16号针头滴加至10倍量慢速搅拌的凝胶液中,凝胶液为5g/L的FeCl3和2.5g/L的壳聚糖混合液(pH为3),凝胶化8h,过滤收集小丸,用蒸馏水冲洗丸粒2次,37℃条件下干燥,50℃热处理10h,得载药小丸。将上述小丸在30g/L的氯化钙溶液中浸泡10min后,取出吸干表面溶液,置于6g/L的海藻酸钠溶液中包衣10min,过滤,收集包衣小丸,用水冲洗除去丸粒表面未凝胶化的海藻酸钠,37℃烘干,即得(地塞米松质量百分数为40.07% ,粒径0.804mm)。
2.1.2 地塞米松羧甲基纤维素钠混悬液 称取地塞米松20mg,用5g/L的羧甲基纤维素钠溶液配成质量浓度为2g/L的混悬液。
2.2 地塞米松体内测定方法的建立
2.2.1 色谱条件 迪马C18硅烷基键合相不锈钢柱(250mm×4.6mm,5μm);预柱:干法自填(10μm);流动相:水-甲醇(45∶55);流速:1mL/min;柱温:30℃;检测波长:240nm;进样量:20μL。
2.2.2 生物样品的处理及测定方法 取大鼠粪便,加5倍量0.05mol/L的pH 6.8PBS均浆得混悬液,离心(6000r/min)2min得粪便上清液。精密吸取大鼠血浆和粪便上清液0.2mL,分别置离心管中,加入甲醇0.8mL,旋涡振荡5min,离心(12000r/min)10min,取上清液20μL进高效液相色谱仪,测定。
2.2.3 方法专属性 按“2.2.2”项下操作,得空白血浆、空白粪便及各生物样品色谱图,见图1。由色谱图可知血浆和粪便中内源性物质与地塞米松分离良好,不干扰测定,样品中地塞米松的保留时间为14min左右。
2.2.4 标准曲线的制备 精密量取空白血浆、粪便上清液0.2mL,分别加入不同量的地塞米松,配成含系列浓度药物的生物样品(血浆分别为0.105、0.210、0.525、2.100、4.200、8.400、21.000mg/L;粪便分别为0.105、0.210、0.525、2.100、4.200、8.400、16.800mg/L)。按“2.2.2”项下方法进行处理和测定,将地塞米松峰面积(A)对其浓度(C)线性回归,得相应生物样品中地塞米松的标准曲线:血浆A=3937.3×C -197.8,r = 0.9988;粪 便 A =4110.6×C-26.82,r=0.9997。各生物样品中,地塞米松峰面积与其浓度线性关系良好。
2.2.5 检测限测定 配制系列浓度的地塞米松血浆和粪便上清液样品,依次进样,以信号/噪音=3∶1计算,地塞米松在血浆中的检测限为75μg/L,在粪便上清液中的检测限为60μg/L。
2.2.6 回收率和精密度测定 精密量取与标准曲线制备时等量的血浆与粪便上清液,精密加入不同量地塞米松(血浆中加入量分别为0.0378、0.3360、3.7800μg,粪便上清液中加入量分别为0.0315、0.2100、1.5960μg),得到高、中、低3种浓度。按“2.2.2”项下操作,测定地塞米松量,与实际加入量比较计算回收率,分别于同一日测定5次,连续测定5d,计算日内精密度和日间精密度。数据显示,该方法准确度和重复性均良好,符合测定结果要求,结果见表1。
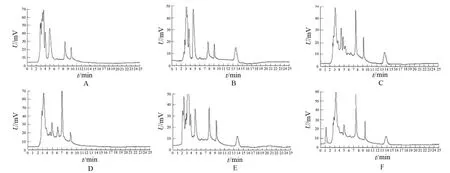
图1 血浆、粪便中地塞米松高效液相色谱图
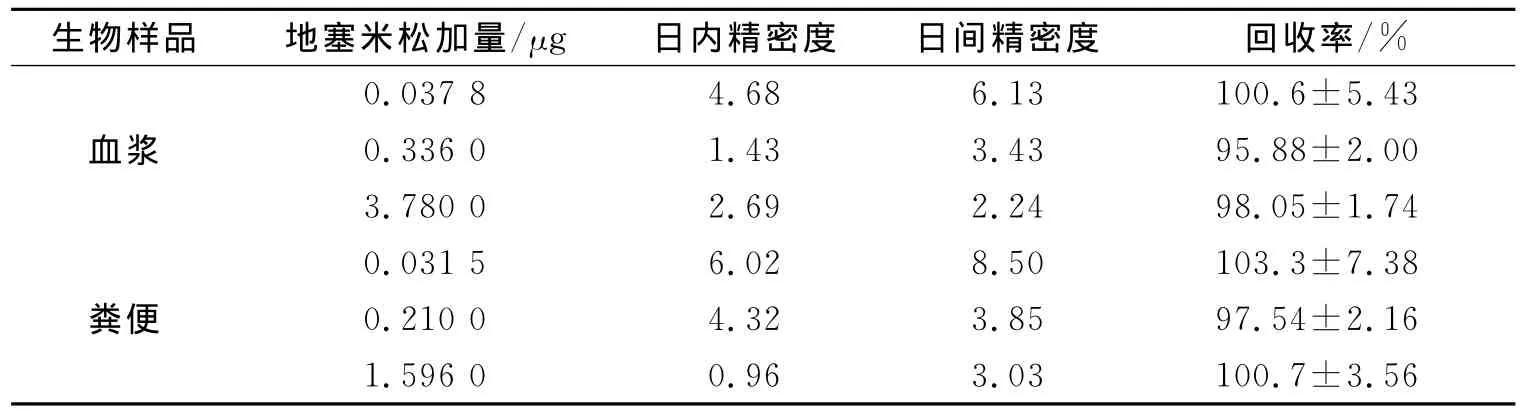
表1 各生物样品中地塞米松测定回收率和日内、日间精密度(n=5)
2.3 实验安排和数据处理
2.3.1 实验安排 取体质量在220~250g之间的Sprague Dawley大鼠10只,随机分成2组,每组5只,实验前禁食12h,其中一组给予地塞米松小丸(主药含量为40.31%),经口插入聚乙烯管,通过聚乙烯管给大鼠口服小丸适量(以地塞米松量计,给药剂量为10mg/kg大鼠体质量),再灌服5g/L羧甲基纤维素钠溶液1mL作为实验组;另一组大鼠灌胃地塞米松羧甲基纤维素钠混悬液适量(给药剂量为10mg/kg大鼠体质量)作为对照组。给药后,分别于0.5、1、2、4、6、8、12、24h时间点,将大鼠断尾并取血0.6mL置于含2mL肝素钠的离心管中,离心(6000r/min)10min,分离得到血浆,冷藏备用,同时分别于(0~2)、(2~4)、(4~6)、(6~8)、(8~12)、(12~24)h,收集粪便,冷藏备用。将上述血浆及粪便样品按“2.2.2”项下操作,测定地塞米松量。
2.3.2 血浆药物浓度经时曲线 地塞米松原药混悬液对照组与包衣小丸组给药后,血药浓度随时间的变化曲线,见图2,其中达峰时(Tmax)与峰浓度(Cmax)用实测值,AUC0→24按梯形法计算。
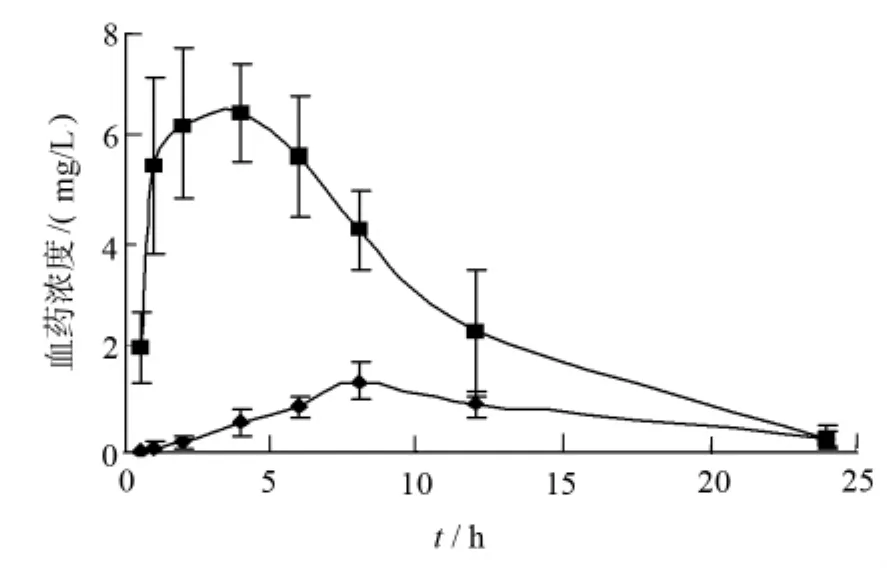
图2 不同制剂大鼠灌胃给药后血浆药-时曲线
由图2发现,与对照组相比,地塞米松小丸给药后,药物吸收进入血液循环的速度明显减慢,药时曲线存在约1h时滞,血药浓度Tmax由4h延至8h,C 由(6.46±0.92)mg/L明 显 降 低 为 (1.33±0.36)mg/L(P<0.01),同时吸收进入体循环的药物量减少,表现为 AUC小丸组明显低于 AUC原药组(P<0.01),约为对照组的1/5。实验说明,小丸给药后,在胃肠道上端药物释放少,吸收进入体循环的药物量与原药相比,明显减少。
2.3.3 粪便中排泄药物量 测给药后不同时间段,粪便中地塞米松的量,对取样时间段作图,得到粪便中药物量随时间变化的直方图,见图3。
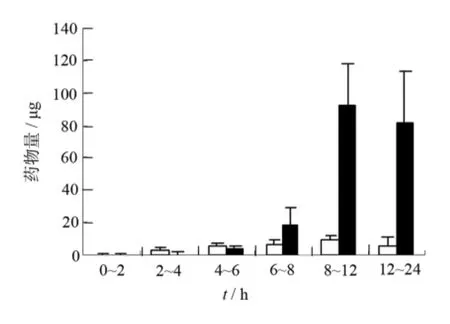
图3 不同制剂大鼠灌胃给药后粪便药量-时间直方图
由图3发现,对照组给药后,经粪便排泄的药物量少,说明在结肠内容物中存在的药物量少,这与药物通过胃、肠道上段吸收进入体循环较多有关。地塞米松小丸给药后,经粪便排泄药物量低于对照组,与对照组药物在胃、肠道可迅速转运分布,而小丸组在转运通过胃、肠道上段时药物释放少有关。(6~8)h后,小丸组粪便中药物量高于对照组,与小丸转运至盲肠、结肠部位,丸粒骨架在微生物酶作用下降解溶蚀而释放药物,同时药物在盲肠、结肠部位吸收进入体循环量少有关,尤其是(8~24)h时,粪便中药物量显著高于对照组(P<0.01)。总的来说,给药后(0~24)h范围内,粪便中排泄药物量对照组(29.20±5.77)μg 明 显 低 于 小 丸 组 (198.2±38.07)μg,P<0.01。说明小丸给药后,药物主要在盲肠、结肠部位释放。
2.4 结肠定位效果的评价
采用药物的相对靶向释药指数(DDI)评价包衣小丸的结肠定位效果[3]。药物的相对靶向指数(DDI)=(AUC1/AUC2)/(AUC3/AUC4)。 其中AUC1、AUC3、AUC2、AUC4分别表示大鼠灌胃地塞米松小丸后(0~24)h结肠内容物(粪便)中排出的药物量和血药浓度-经时曲线下面积;大鼠灌胃地塞米松混悬液后(0~24)h结肠内容物(粪便)中排出的药物量和血药浓度-经时曲线下面积。数据显示,与地塞米松混悬液相比,小丸在结肠内容物DDI值为30.34,结果见2。

表2 地塞米松小丸在结肠内容物的药物相对靶向指数
3 讨论
在口服结肠定位给药系统的体内药物释放研究主要有3种:①血药浓度经时变化规律[4];②胃肠道不同部位药物浓度经时变化规律[5];③γ-闪烁成像法监测经放射性标记后的制剂在体内的转运及存在状态[6]。我们通过测定小丸组与对照组灌胃给药后的血药浓度经时变化和经粪便排泄药物量随时间的变化情况,了解制剂在大鼠体内的药物释放和吸收进入体循环的情况,从而评价其释药特性。
大鼠灌胃地塞米松小丸和原药混悬液后,二者在胃、肠道中的药物释放和吸收情况表现为:①与原药混悬液相比,小丸组给药后,血药浓度经时曲线存在约1h时滞,Tmax延后,Cmax和血药浓度经时曲线下面积AUC0→24明显降低,说明混悬液给药后,药物在胃、肠道上段可被较快吸收进入血液循环。血药浓度随时间变化迅速,峰浓度高,吸收进入体循环的药物量多,而地塞米松小丸给药后,药物在胃、肠道上段释放少,到达盲肠、结肠部位后丸粒骨架被降解溶蚀而释放药物,但结肠部位不是药物主要吸收部位,因此,血药浓度随时间变化缓慢,峰浓度低,吸收进入体循环的药物量少。②地塞米松小丸给药后(0~24)h粪便中排泄药物量明显高于对照组,说明药物混悬液给药后,大多数药物在通过胃、肠道上段的过程中,被胃肠道黏膜吸收进入体循环,转运到达结肠部位的药物量较少,而小丸在胃、肠道上段释放药物少,转运至盲肠、结肠部位后,在降解酶作用下释放药物,药物吸收少,因此,结肠局部内容物中药物浓度高。③与原药混悬液对照组比,小丸在结肠内容物(粪便)DDI值为30.34。由以上结果可见,地塞米松小丸在大鼠体内具有结肠定位释放药物特性。
血药浓度经时曲线下面积可反映吸收进入体循环的药物量。地塞米松小丸的血药浓度经时曲线下面积仅为口服同剂量原药的1/5,说明小丸用药后,可明显降低进入体循环的药物量,而血液中外源性糖皮质激素的水平直接与肾上腺皮质抑制等一系列副作用有关[7]。因此,推测地塞米松羧甲基魔芋胶小丸用于治疗炎症性肠道疾病,可有效降低药物副作用,还需通过体内试验进一步证实。
4 结论
大鼠口服给药后,与原药混悬液相比,地塞米松小丸可降低胃、肠道上段药物的释放及吸收,表现为血药浓度经时曲线存在时滞,达峰时延后,峰浓度明显降低,血药浓度经时曲线下的面积 (即吸收进入体循环的药物量)明显减少。转运至盲肠、结肠部位,丸粒骨架降解溶蚀而大量释放药物,表现为粪便中排泄的药物量明显高于原药对照组。因此,地塞米松小丸在大鼠体内具有结肠定位释药特性。
[1]Friend D R.New oral delivery systems for treatment of inflammatory bowel disease[J].Adv Drug Delivery Rev,2005,57(2):247-265.
[2]金剑,李伟宁,李琦,等.口服结肠定位给药系统的研究进展[J].中国临床药学杂志,2011,20(3):184-187.
[3]Richard N F,Barbara H,Lonmie R,et al.Colonic delivery of dexamethasone from a prodrug accelerates healing of colitis in rats without adrenal suppression[J].Gastroenterology,1995,108(9):1688-1699.
[4]Krishnaiah Y S,Veer R P,Dinesh K B,et al.Pharmacokinetic evaluation of guar gum based colon-targeted drug delivery systems of mebendazole in healthy volunteers[J].J Controlled Release,2003,88(1):95-103.
[5]Tozak I H,Odoriba T,Okad A,et al.Chitosan capsules for colon-specific drug delivery:enhanced localization of 5-aminosalicylic acid in the large intestine accelerates healing of TNBS-induced colitis in rats[J].J Controlled Release,2002,82(1):51-61.
[6]Sinha V R,Mittal B R,Kumria R.In vivo evaluation of time and site of disintegration of polysaccharide tablet prepared for colon-specific drug delivery [J].Int J Pharm,2005,289(1):79-85.
[7]English J J,Chakraborty J,Marks V,et al.Prendnisolon levels in the plasma and urine:a study of two preparation in man[J].Br J Clin Pharmacol,1975,2(2):327-332.
[责任编辑 时 红]
Studies on in vivo release of dexamethasone from carboxymethyl konjac glucomannan pellets in rats
ZHANG Yu1,HOU Shi-xiang2*(1.Institute of Materia Medica,Henan University,Kaifeng,Henan 475004,China;2.West China School of Pharmacy,Sichuan University,Chengdu,Sichuan 610041,China)
ObjectiveTo studyin vivorelease of dexamethasone(Dex)from carboxymethyl konjac glucomannan(CMKGM)pellets and evaluate colon-specific drug delivery characteristics of the pellets.MethodsCompared with Dex containing carboxymethyl cellulose suspension,the concentration of Dex in plasma and dejecta after intragastric administrated to rats were measured periodically by HPLC,and used to calculate the relative targeting drug delivery index(DDI).ResultsCompared with the suspension,the Tmaxof the pellets was about 1h,the Tmaxof drug in plasma shifted from 4hto 8h,the Cmaxdecreased significantly from (6.46±0.92)mg/L to (1.33 ±0.36)mg/L (P<0.01),the AUC0→24decreased significantly from (70.72±9.62)mg·L-1·h-1to(15.82±4.01)mg·L-1·h-1(P <0.01);the amount of drug excreted in dejecting from 0hto 24hafter administration increased significantly from (29.20±5.77)μg to (198.2±38.07)μg(P <0.01).The DDI value of the pellets to deject was 30.34against the suspension.ConclusionDex-containing CMKGM pellets may have the location delivery properties.
Dexamethasone;Carboxymethyl konjac glucomannan pellets;Colon-specific drug delivery system;In vivorelease
R943
A
1672-7606(2012)02-0083-05
2012-03-30
张瑜(1972-),男,河南 开封 人,博士,副教授,从事药剂学的教学和科研工作。
*通讯作者:侯世祥(1943-),男,四川仁寿人,博士生导师,教授,从事药剂学教学和科研工作。
