啤酒泡沫蛋白质的二级结构特点及其质谱鉴定
2012-03-15李维虎郑飞云刘春凤李永仙
李维虎 ,郑飞云 ,刘春凤 ,李永仙 ,李 崎 *
(1.江南大学 工业生物技术教育部重点实验室,江苏 无锡 214122;2.江南大学 生物工程学院,江苏 无锡,214122)
啤酒泡沫性能包括起泡性、泡持性、挂杯性以及洁白细腻程度等[1],是啤酒有别于其它酒类的重要特征之一。其中蛋白质对起泡性和维持泡沫结构的稳定具有重要作用。啤酒泡沫蛋白质主要来源于大麦,具有较强的疏水性,疏水性越强,泡沫越稳定[2-5]。在啤酒酿造过程中,由于酶、高温等因素,蛋白质的性质和结构经历了大而复杂的变化,蛋白质热稳定性、溶解性和抗酶水解的能力都有很大程度的提高[6-9],进而影响啤酒及啤酒泡沫的稳定性。
蛋白质理化性质改变的本质是蛋白质空间结构发生了变化。采用圆二色谱技术对啤酒泡沫和麦芽中的蛋白质二级结构特点进行比较与研究,并利用单向SDS-聚丙烯酰胺凝胶电泳 (SDS-PAGE)与液质联用技术(LC-MS/MS)对泡沫蛋白质进行分离与鉴定。研究初步揭示了泡沫蛋白质的二级结构特点及蛋白质组成,丰富了泡沫蛋白质的理论研究,对揭示啤酒泡沫稳定性机制有一定推进意义。
1 材料与方法
1.1 主要试剂与仪器
1.1.1 主要试剂 protein marker:大连宝生物技术公司产品;trypsin:sigma公司产品; 丙烯酰胺,N,N′-甲叉双丙烯酰胺,SDS(十二烷基硫酸钠),Tris(三羟基甲烷氨基丙烷),甘氨酸,TEMED(N,N,N',N'-四甲基乙二胺),DTT(二硫苏糖醇),β-巯基乙醇,CAN(乙腈),碘乙酰胺:均为分析纯。
1.1.2 主要仪器 圆二色谱仪MOS-450/AF-CD:法国Bio-Logic公司产品;凝胶成像系统:美国UVP公司产品;LCQ Deca XPplus液质联用质谱仪:美国Thermo公司产品;垂直板电泳仪:DYY-8 C,北京六一仪器公司产品;高速冷冻离心机:德国eppendorf公司产品。
1.2 实验方法
1.2.1 啤酒泡沫蛋白样品制备 取600 mL啤酒缓缓倒入分液漏斗中充分起泡,静止10 s,分液除去液体部分,收集泡沫浓缩液;4℃下用质量分数60%硫酸铵沉淀,8 000 g离心15 min,弃去上清液,沉淀用60%硫酸铵溶液洗涤两次,用适量pH 7.5磷酸缓冲液溶解,透析过夜,用BaCl2检验透析效果,然后冷冻干燥。
1.2.2 荧光分光光度法测蛋白质疏水性 蛋白质样品用pH 7.0的10 mol/L磷酸缓冲液分别稀释一系列质量浓度:0.05、0.10、0.15、0.20、0.25、0.30 μg/μL,分别取 4 mL,一式两份,其中一份加入 20 μL浓度为8 mol/L的ANS溶液,另外一份不加ANS的蛋白质溶液作为空白。振荡混匀,然后测其荧光强度(FI)。荧光条件:激发波长390 nm,发射波长470 nm。以荧光强度对蛋白质浓度作图,初始段的斜率即为蛋白质分子的表面疏水性指数H。
1.2.3 圆二色谱法(CD)分析蛋白质二级结构 取制备好的蛋白质样品适量溶于超纯水,稀释到0.1 mg/mL进行测定。测定条件:0.1 cm石英比色杯,温度 25℃,光径 0.1 cm,带宽 1 nm,扫面范围 250~190 nm,速度 0.5 nm/s,用平均残基摩尔椭圆率[θ]表示CD光谱数据,单位deg·cm2/dmol,通过在线引擎采用SELCON3方法计算蛋白质二级结构(http://dichroweb.cryst.bbk.ac.uk/html/home.shtml)。
1.2.4 SDS-PAGE聚丙烯酰胺凝胶电泳 根据文献[10],分离胶质量浓度 15 g/dL(1 mm×80 mm×80 mm),浓缩胶质量浓度4 g/dL,蛋白质样品溶于上样缓冲液 (62.5 mmol/L Tris-HCl,pH 6.8, 质量分数2%SDS,20%甘油,5%β-巯基乙醇,0.01%溴酚蓝),沸水中水浴 5 min,上样量 15 μL,浓缩胶电压为80 V,分离胶电压调整为200 V,待溴酚蓝条带移动到距离分离胶下边缘1 cm左右时关闭电源,结束电泳,凝胶进行考马斯亮蓝G-250染色,脱色后拍照保存。
1.2.5 胶内酶切 据文献 [11]作适当修改,选取SDS-PAGE凝胶上所需分析的条带,切胶后进行胶内酶切。从胶上切下考马斯亮蓝染色的蛋白质条带,转移到小EP管中,加10 mmol DTT的50 mmol NH4HCO3溶液,56℃、45 min进行还原处理。加55 mmol碘乙酰胺的50 mmol NH4HCO3溶液室温避光30 min进行烷基化处理。加100 mL 50%ACN的50 mmol NH4HCO3溶液,室温振荡30 min,可重复操作,直到胶粒脱去考马斯亮蓝的蓝色。加入100 μL ACN,室温放置15 min后吸去ACN,抽真空离心干燥。 加入20 μL测序级胰蛋白酶 (10 ng/μL,sigma)4 ℃放置 45 min,吸取多余酶液,加入 10 μL、50 mmol NH4HCO3,37℃孵育酶解16 h。吸取小EP管中的酶解液放入干净EP管中;向原EP管加入30 μL 5%甲酸-50%ACN,漩涡振荡 30 min,提取液加入含酶解液的EP管中,重复提取一次。肽段提取液用speed vac(真空离心蒸发浓缩器)彻底抽干后,-20℃保存。
1.2.6 蛋白质质谱分析 酶切完成后用Ziptip C18将肽片段脱盐[12],抽干后用0.1%甲酸溶解,用于液质联用质谱分析。质谱数据用SEQUEST软件在NCBI数据库进行搜索和匹配。
2 结果与讨论
2.1 泡沫蛋白质的二级结构
蛋白质二级结构包括蛋白质多肽链的折叠和盘绕方式,主要有α-螺旋、β-折叠、β-转角以及无规则卷曲等单元组分。圆二色(Circular Dichroism,简写为CD)光谱法是分析蛋白质二级结构的研究工具,远紫外区是肽键的吸收范围,可以反映主链的构象,不同二级结构的蛋白质或多肽产生的CD光谱谱带位置、吸收强弱有差异,通过CD图谱可以计算蛋白质α-螺旋和β-折叠等组分的含量[13]。通常典型α-螺旋结构在208 nm和222 nm左右有2个负峰,在192 nm有1个正峰,β折叠在214 nm处有1个负峰,β转角在206 nm有1个正峰,无规则卷曲在200 nm附近有1个负峰,在210~230 nm有1个正峰。实验测定了啤酒泡沫和麦芽中蛋白质水溶液的二级结构,结果见图1。同时检测了两种蛋白质的表面疏水性指数,结果见图2。

图1 大麦芽和泡沫蛋白质的二级结构CD图谱Fig.1 CD spctra of barley malt proteins and foam proteins
圆二色(CD)图谱显示,泡沫蛋白质在190~250 nm远红外区有1个明显的负吸收峰,最大负吸收位置在202 nm附近,并未表现出α-螺旋特有的双负峰CD特征。为了对比泡沫蛋白质二级结构特点,对啤酒泡沫蛋白质来源——麦芽蛋白质二级结构进行CD光谱扫描。结果显示,麦芽蛋白质在208 nm和222 nm左右处有2个负峰,在192 nm附近有1个正峰,具有典型的α-螺旋双负峰结构特点。根据Levitt[14]对规则蛋白质结构的分类,麦芽蛋白质属于全α-型,其中208 nm处负峰是由于α-螺旋π-π*跃迁所致,222 nm附近负峰对应于n-π跃迁[15]。CD图谱显示,啤酒中的泡沫蛋白质已经失去酿造前麦芽蛋白质中α-螺旋的典型双负峰结构,反映了蛋白质发生了明显的去折叠,α-螺旋减少,无规则卷曲特征增加明显,从而190~220 nm之间平均残基摩尔椭圆率负值增加,208 nm峰位蓝移至202 nm左右,主要是由于无规则卷曲的增加和α-螺旋特征叠加的结果,222 nm附近的负峰被β-折叠产生的弱正峰补平,形成几乎没有起伏的斜坡。蛋白质这种明显的去折叠现象可能与啤酒酿造过程中剧烈条件对蛋白质空间构象的影响有密切关系。先前报道[9,16]指出,煮沸阶段是影响蛋白质去折叠的重要阶段,来自麦芽浸出物的还原性物质有利于LTP1发生去折叠,并且蛋白质的去折叠对LTP1表面活性的表达有重要作用[17]。
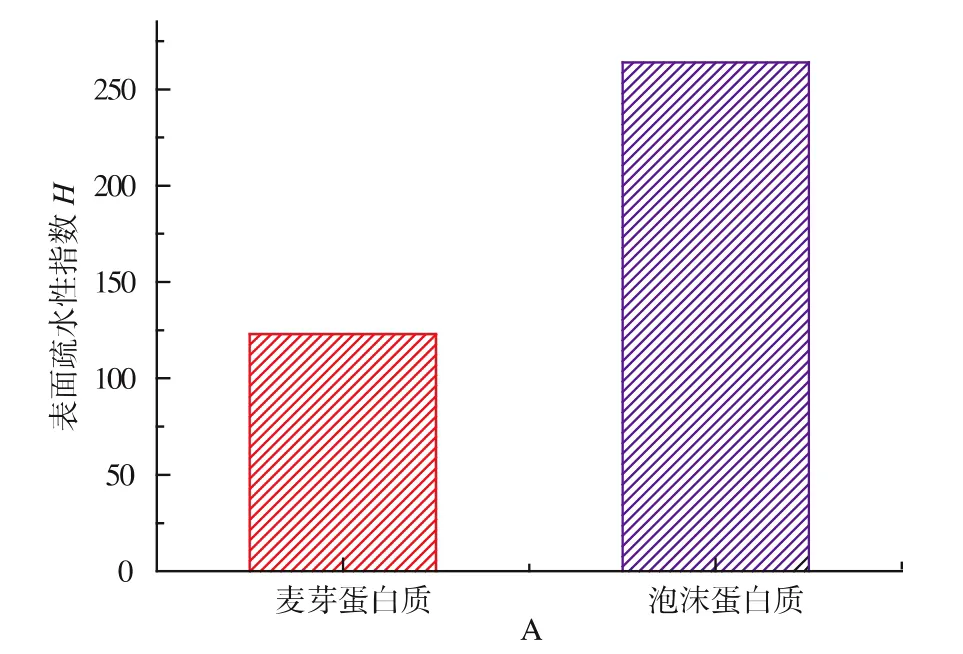
图2 大麦芽和泡沫蛋白质的表面疏水指数Fig.2 Surface hydrophobic index of barley malt proteins and foam proteins
使用SELCON3方法对圆二色谱的扫描数据进行计算后得到蛋白质二级结构各单元含量,见表1所示。与麦芽蛋白质相比,泡沫蛋白质的α-螺旋的相对含量低,有较多的β-折叠和无规则卷曲。蛋白质表面疏水性测定结果见图2。泡沫蛋白质的疏水性高于麦芽蛋白质,疏水蛋白质对啤酒泡沫稳定性有明显的积极的作用,β-折叠有较多的非极性残基,可以在蛋白质内部形成疏水核心[18],增加蛋白质的疏水性。疏水蛋白质由于表面活性可以富集在气泡的表面,在气-液界面形成粘滞薄膜,降低气泡的表面张力,从而有利于泡沫的稳定性。据文献[19]报道,赖氨酸残基位于α-螺旋的区域,其糖基化修饰会影响该区域的结构,因此糖基化可能也是引起泡沫蛋白α-螺旋含量较低的因素之一。泡沫蛋白的无规则卷曲含量较多,有较大的柔性,展开的多肽链上氨基酸残基的暴露不仅有利于蛋白质的疏水性,而且可能更有利于蛋白质的修饰(如赖氨酸残基糖基化修饰[20]),使得泡沫蛋白质具有很好的双亲性和表面活性,从而对啤酒泡沫性能发挥作用。
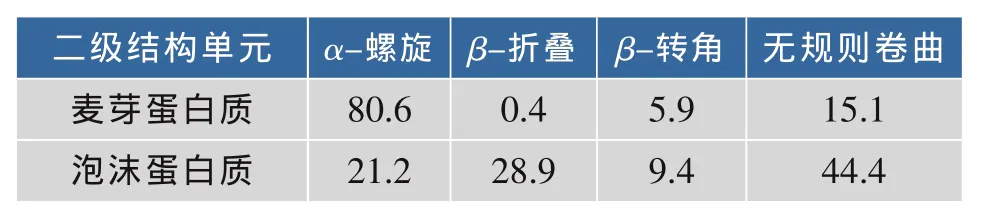
表1 麦芽蛋白质和啤酒泡沫蛋白质二级结构的含量Tab.1 Contents of second structures of malt proteins and foam proteins
2.2 泡沫蛋白质的提取和SDS-PAGE分离
对冷冻干燥后的啤酒泡沫蛋白进行SDSPAGE电泳,结果见图3。蛋白质相对分子质量主要分布在40 000左右和5 000~20 000之间,并未发现66 000蛋白质条带[16]。图3是凝胶分析软件Gel-Pro Analyzer根据光密度得到的胶内蛋白质条带分布,便于较准确切胶。根据蛋白质胶内条带结合光密度分析扫描图,共分为5份,分别收集每份胶条置于小EP管中进行胶内酶解。
2.3 啤酒泡沫蛋白质的质谱分析
用LCQ-Deca XP plus对胶内酶解的肽段进行质谱分析,共得到5套质谱数据,经过SEQUEST软件在NCBI数据库搜索和配对,共鉴定出11种来自大麦的可信度较高蛋白质,见表2。有5个电泳条带由3种或3种以上蛋白质组成,说明泡沫蛋白质组分的复杂。这些蛋白质包括较完整的蛋白质Z4和LTP1(脂转移蛋白),还有蛋白质Z4的不完整片段、BDAI-1(大麦α-淀粉酶抑制剂二聚体-1)以及hordein(大麦醇溶蛋白)片段;另外还鉴定出CMa、CMb、CMd(均属于α-淀粉酶/胰蛋白酶抑制剂家族)、CMe(属于胰蛋白酶抑制剂家族)、BMAI-1(大麦α-淀粉酶抑制剂单聚体-1)和WMAI-1(小麦-淀粉酶抑制剂单聚体-1)。

图3 泡沫蛋白质的SDS-PAGE图Fig.3 SDS-PAGE of foam proteins

图4 泡沫蛋白凝胶光密度分析剖面图Fig.4 Relative densitometric profile of foam protein gel
本次鉴定啤酒泡沫蛋白质发现40 000的条带为蛋白质 Z4,未发现 Z7,有实验证明[17,21],蛋白质Z4与泡沫稳定性的相关性远远大于Z7。同时,在低相对分子质量区域检测到蛋白质Z4不完整片段,郝俊光在检测泡沫蛋白质时也检测到Z4片段[22],Gianluca等[23]检测到Z4和LTP1的C-末端片段,因此尽管普遍认为泡沫蛋白质有较强的抗酶解能力,但是在一定的条件下可能会受到麦芽酶或酵母蛋白酶A的影响。LTP1来自大麦胚乳蛋白部分,具有很强的起泡性能。LTP包括LTP1和LTP2两种多肽,LTP2含量仅有LTP1的1/10,但实验未检测到LTP2存在。BDAI–1疏水性较强,能被糖基化和磷基化,对泡沫稳定性起积极作用[24],也可能参与浑浊形成[25]。只检测到30196.2的醇溶蛋白片段。先前报道[22,26-28]称啤酒中部分醇溶蛋白对泡沫稳定和啤酒浑浊有重要作用,最近研究发现[23,25],啤酒中醇溶蛋白很少,未检测到完整蛋白质,不存在较完整结构,因此它们对泡沫的贡献非常有限。CMa、CMb、CMd和CMe相对分子质量较低,含量很少,脯氨酸含量不高,属于酶抑制剂系列,可能增强啤酒蛋白质的抗酶水解能力。据文献 [29-31]报道BMAI-1和WMAI-1都是一种昆虫α-淀粉酶抑制剂,两者在泡沫中的作用目前未知,有待进一步研究。
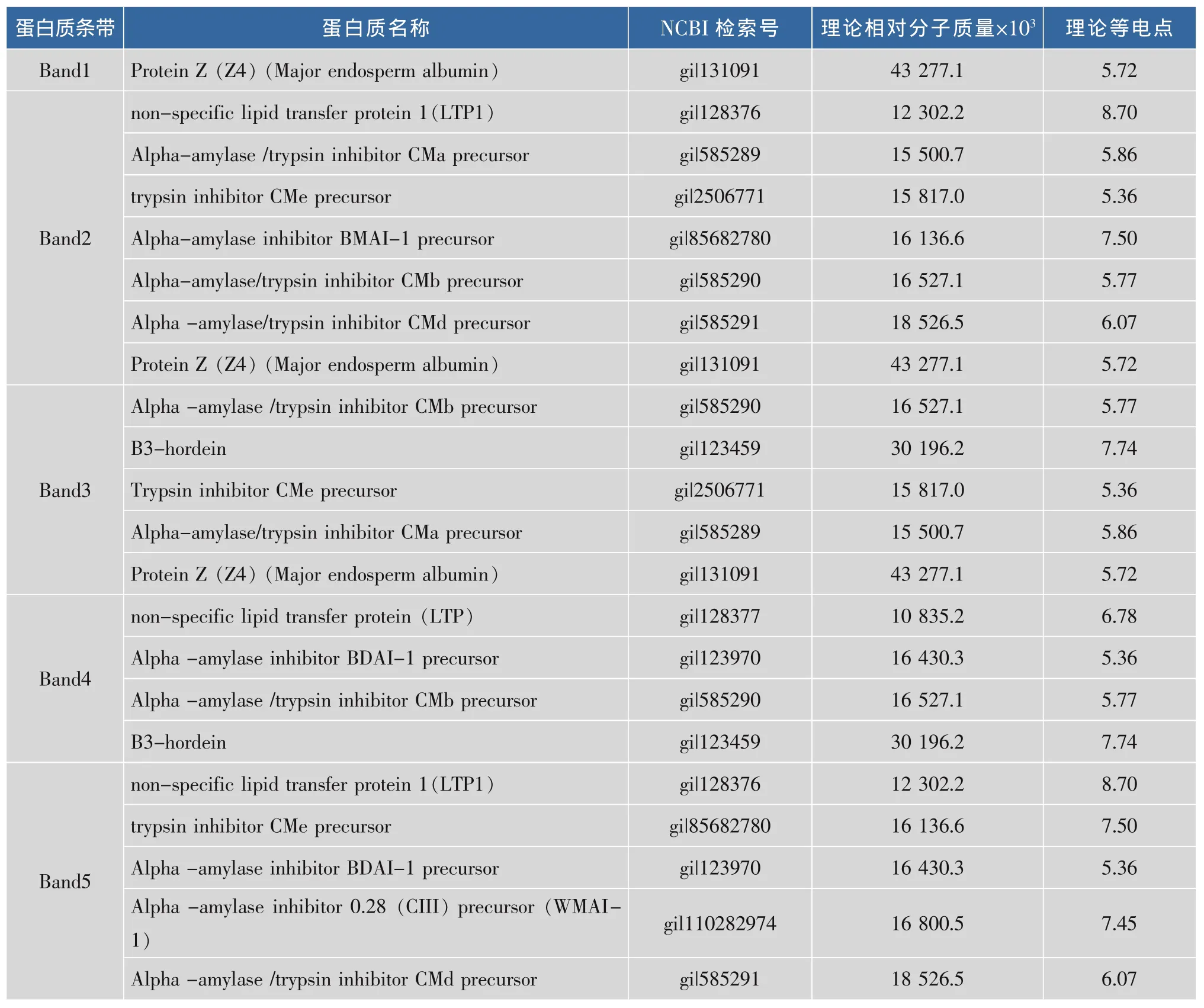
表2 蛋白质质谱鉴定结果汇总Tab.2 Summary of protein identification by mass spectrometry analysis followed by a database search
经过复杂的酿造过程,留在啤酒中的蛋白质种类仍然很多,但大部分已经不完整,且空间构象已经发生改变,变性和去折叠,导致多肽链伸展,这些蛋白质可能由于结构的改变从而产生了有利于提高啤酒泡沫性能的性质。蛋白质Z4维持泡沫稳定性,LTP1具有较强的起泡性,完整的蛋白质Z4和LTP1可能作为“核心”维持啤酒泡沫性能,而其他蛋白质组分作为参与者共同决定泡沫性能。酿造过程中蛋白质结构变化的复杂性以及泡沫蛋白质组成的多样性在一定程度上说明了啤酒泡沫机制的复杂性。
3 结语
圆二色(CD)谱结果显示,啤酒泡沫蛋白质在195 nm处有1个正峰,在202 nm附近有1个最大负峰,与酿造前的麦芽蛋白相比,其二级结构并未表现出α-螺旋特有的双负峰特征,β-折叠和无规则卷曲相对含量较高,并且泡沫蛋白质的疏水性高于麦芽蛋白质,因此这种结构有利于泡沫蛋白质的疏水性,从而有利于啤酒泡沫的稳定性。经质谱鉴定,啤酒泡沫蛋白中共有11种来自麦芽的可信度较高蛋白质, 包括蛋白 Z、LTP1、BDAI-1, 以及 CMa、CMb、CMd、CMe、BMAI-1、WMAI-1 等酶抑制剂和少量醇溶蛋白,其含量很少,可能参与啤酒泡沫稳定性和浑浊,其作用尚待探索。蛋白质在酿造前后结构发生很大变化,并且泡沫蛋白组成复杂,因此关于蛋白质在酿造过程结构、组成和性质的变化有待进一步分析与研究,为探索泡沫蛋白质的泡沫稳定性机制奠定一定的理论基础,以期对实际生产作出理论指导。
(
)
[1]Bamforth C W.The foaming properties of beer[J].Journal of the Institute of Brewing,1985,91:370-383.
[2]Slack P T,Bamforth C W.Fractionation of polypeptides from barley and beer by hydrophobic interaction chromatography:the influence of their hydrophobicity on foam stability[J].Journal of the Institute of Brewing,1983, 89:397-401.
[3]Asano K,Hashimoto N.Isolation and characterization of foaming proteins of beer[J].Journal of the American Society of Brewing Chemists, 1980, 38:129-137.
[4]Onishi A,Proudlove M O.Isolation of beer foam polypeptides by hydrophobic interaction chromatography and their partial characterisation[J].Journal of the Science of Food and Agriculture, 1994, 65(2):233-240.
[5]Bech L M,Vaag P,Heinemann B,et al.Throughout the brewing process barley lipid transfer protein (LTP1)is transformed into a more foam-promoting form[J].Proceedings of the European Brewery Convention Congress, 1995,25:561-568.
[6]Sandrine J,Jean-Paul D,Daniel M,et al.Evidence of the glycation and denaturation of LTP1 during the malting and brewing process[J].Journal of Agricultural and Food Chemistry, 2001, 49(10):4942-4949.
[7]Lindorff-Larsen K, Winther J R.Surprisingly high stability of barley lipid transfer protein, LTP1, towards denaturant, heat and proteases[J].FEBS Letters, 2001, 488(3):145-148.
[8]Perrocheau L, Rogniaux H, Boivin P, et al.Probing heat-stable water-soluble proteins from barley to malt and beer[J].Proteomics, 2005, 5(11):2849-2858.
[9]Perrocheau L,Bakan B,Boivin P,et al.Stability of barley and malt lipid transfer protein 1 (LTP1)toward heating and reducing agents:relationships with the brewing process[J].Journal of Agricultural and Food Chemistry, 2006, 54(8):3108-3113.
[10]郭尧君.蛋白质电泳实验技术[M].北京:科学出版社,2003.
[11]Mao S,Luo Y,Zhang T,et al.Proteome reference map and comparative proteomic analysis between a wild type Clostridium acetobutylicum DSM 1731 and its mutant with enhanced butanol tolerance and butanol yield [J].Journal of Proteome Research, 2010, 9(6):3046-3061.
[12]Bobálová J, Petry-Podgórska I, Marketa L, et al.Monitoring of malting process by characterization of glycation of barley protein Z[J].European Food Research and Technology, 2010, 230(4):665-673.
[13]Keiderling T A.Protein and peptide secondary structure and conformational determination with vibrational Circular dichroism[J].Current Opinion in Chemical Biology,2002,6:682-688.
[14]Levitt M, Chothia C.Structural patterns in globular proteins[J].Nature, 1976, 261(5561):552-558.
[15]Sreerama N, Woody R W.Computation and analysis of protein Circular Dichroism spectra[J].Methods Enzymol, 2004, 383:318-351.
[16]Kordialik-Bogacka E,Ambroziak W.Investigation of foam-active polypeptides during beer fermentation[J].Journal of the Science of Food and Agriculture, 2004, 84(14):1960-1968.
[17]Evans D E,Hejgarrd J.The impact of malt derived proteins on beer foam quality.Part I:the effect of germination and kilning on the level of protein Z4, protein Z7 and LTP1[J].Journal of the Institute of Brewing, 1999, 105(3):159-169.
[18]胡红雨,许根俊.蛋白质的结构转换[J].生物化学与生物物理进展,1999,26(001):9-12.HU Hong-yu,XU Gen-jun.Structural transformation of proteins[J].Progress in Biochemistry and Biophysics,1999,26(001):9-12.(in Chinese)
[19]Watanabe K,Sato Y,Kato Y.Chemical and conformational changes of ovalbumin due to the maillard reaction[J].Journal of Food Processing and Preservation, 1980, 3(4):263-274.
[20]Kato A,Mifuru R,Matsudomi N,et al.Functional casein-polysaccharide conjugates prepared by controlled dry heating[J].Bioscience, Biotechnology and Biochemistry, 1992, 56(4):567-571.
[21]Evans D E,Sheehan M C,Stewart D C.The impact of malt derived proteins on beer foam quality.PartⅡ:the influence of malt foam-positive proteins and non-starch polysaccharides on beer foam quality[J].Journal of Insitute of Brewing, 1999, 105:171-177.
[22]Hao J, Li Q, Dong J, et al.Identification of the major proteins in beer foam by mass spectrometry following sodium dodecyl sulfate polyacrylamide gel electrophoresis[J].Journal of the American Society Brewing Chemists, 2006, 64(3):166-174.
[23]Gianluca P,Francesco B,Stefania I, et al.Proteomic and peptidomic characterisation of beer:immunological and technological implications[J].Food Chemistry,2011,124:1718-1726.
[24]Limure T, Takoi K, Kaneko T, et al.Novel prediction method of beer foam stability using protein Z, barley dimeric α-amylase inhibitor-1 (BDAI-1) and yeast thioredoxin[J].Journal of Agricultural and Food Chemistry, 2008, 56:8664-8671.
[25]Limure T,Nankaku N,Hirota N,et al.Construction of a novel beer proteome map and its use in beer quality control[J].Food Chemistry, 2010, 118(3):566-574.
[26]Kaverva P,Sontag-Strohm T,Lehtonen P.Determination of prolamins in beers by ELISA and SDS–PAGE[J].Journal of the Institute of Brewing,2005, 111(1):61-64.
[27]Kauffman J A,Clare Mills E N,Brett G M,et al.Immunological characterisation of barley polypeptides in lager foam[J].Journal of the Science of Food and Agriculture, 1994, 66(3):345-355.
[28]Evans D E,Robinson L H,Sheehan M C,et al.Application of immunological methods to differentiate between foam-positive and haze-active proteins originating from malt[J].Journal of the American Society Brewing Chemists, 2003, 61(2):55-62.
[29]Barber D, Sanchez Monge R, Gomez L, et al.A barley flour inhibitor of insect α-amylase is a major allergen associated with baker's asthma disease[J].FEBS Letters, 1989, 248(1-2):119-122.
[30]Mena M,Sanchez-Monge R,Gomez L,et al.A major barley allergen associated with baker's asthma disease is a glycosylated monomeric inhibitor of insect α-amylase:cDNA cloning and chromosomal location of the gene[J].Plant Mol Biol, 1992, 20(3):451-458.
[31]Wang J R,Wei Y M,Yan Z H,et al.SNP and haplotype identification of the wheat monomeric α-amylase inhibitor genes[J].Genetica, 2008,134(3):277-285.
