取代基对1-甲基尿嘧啶与N-甲基乙酰胺氢键复合物中氢键强度的影响
2012-03-06刘冬佳王长生
刘冬佳 王长生
(辽宁师范大学化学化工学院,辽宁大连116029)
1 引言
氢键在生物分子体系中起着十分重要的作用,其强弱对蛋白质核酸结构和功能有重要影响,因此对其强度和本质进行研究具有重要意义.1-12Mohajeri和Nobandegani5使用不同方法研究了15个核酸碱基对中的N-H…N和N-H…O氢键强度. Kolew等9使用密度泛函理论方法对甲醇与系列分子形成的氢键复合物进行了研究.Dong等13提出了一种预测多重分子间氢键体系中单个氢键相对强度的方法,并应用于计算腺嘌呤-胸腺嘧啶和鸟嘌呤-胞嘧啶碱基对中单个氢键的强度.Vargas等14对N-甲基乙酰胺二聚体和甲酰胺二聚体中N-H…O=C型的氢键强度进行了研究,发现N-甲基乙酰胺二聚体中N-H…O=C型氢键平均键能为-36.0 kJ·mol-1,而甲酰胺二聚体中N-H…O=C型氢键平均键能为-29.7 kJ·mol-1.Kawahara与其合作者15,16使用MP2方法研究了取代作用对沃森-克里克型碱基对AX-U、CX-G中氢键强度的影响,研究表明取代基的取代位置不同对氢键强度的影响不同.Wang与其合作者17-22提出了一种快速预测分子间氢键能量的势能函数,并应用于氢键体系的计算,计算精度与包含了基组重叠误差(BSSE)校正的MP2方法相媲美.Dannenberg与其同事23-25使用B3LYP/D95**方法对甲酰胺链中氢键的协同效应进行了理论研究.Wu和Zhao26,27通过研究发现,蛋白质的α-螺旋结构和310-螺旋结构中存在氢键协同效应.Tan等28使用B3LYP/cc-pVTZ方法研究了顺式N-甲基甲酰胺低聚物中氢键的协同效应,指出引起氢键协同效应的重要因素之一是电荷转移.
研究氨基酸多肽和核酸碱基间的氢键作用对深刻理解生物体内蛋白质合成机制,进而设计合成新的生物分子材料有重要指导价值.Hunter等29使用密度泛函理论方法研究了氨基酸与碱基间的氢键作用对碱基尿嘧啶上N1位酸性的影响.Jeong等30发展了一组算法用于分析蛋白质-RNA复合物的结构.Cheng和Frankel31使用HF/6-31G(d)方法优化了28个氨基酸-碱基复合物模型体系的结构,发现21个稳定结构含有两个以上的氢键作用.新近发展的ProtNA-ASA数据库已经包含有214个蛋白质-DNA和28个蛋白质-RNA复合物的结构信息.32本文使用MP2方法对由1-甲基尿嘧啶与N-甲基乙酰胺所形成氢键复合物中的N-H…O=C型氢键强度进行研究,探讨了氢键受体分子中不同取代基对N-H…O=C氢键强度的影响和氢键的协同效应.
2 计算方法
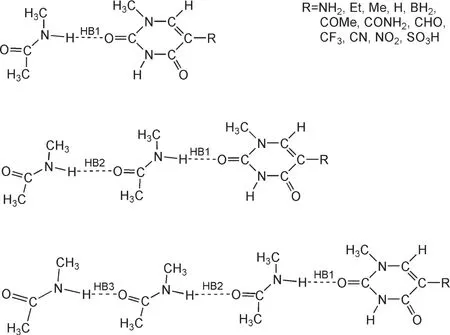
图1 氢键复合物的分子结构Fig.1 Structures of hydrogen-bonded complexes
图1为本文研究的氢键二聚体、三聚体、四聚体氢键复合物的分子结构.复合物中的N-H…O=C型氢键分别用HB1、HB2、HB3表示.本文使用B3LYP/6-31+G(d,p)方法对氢键复合物进行结构优化和频率计算,得到其稳定构型,进而使用包含BSSE校正的MP2/6-311++G(d,p)和MP2/6-311++ G(3df,2p)方法计算其结合能.为了深入理解这些复合物中的氢键作用,本文还使用B3LYP/6-31+G(d, p)方法进行了自然键轨道分析计算.全部计算均采用Gaussian 03程序包33完成.
3 结果与讨论
3.1 几何结构
本文共优化得到36个氢键复合物的稳定结构,图2给出了15个氢键复合物的稳定结构及主要结构参数.其他21个氢键复合物的稳定结构及主要结构参数列于图S1(见Supporting Information).以氢键三聚体为例,R=H时是由1-甲基尿嘧啶与两个N-甲基乙酰胺所形成的N-H…O=C氢键三聚体,其氢键HB1的键长r(H…O)HB1为0.2016 nm,氢键HB2的键长r(H…O)HB2为0.1950 nm.当取代基R是NH2、Et、Me等供电子基团时,氢键HB1和HB2的键长均比R=H时的短,且HB1的键长变化更大.例如:R= NH2,r(H…O)HB1为0.1987 nm,缩短了0.0029 nm; r(H…O)HB2为0.1947 nm,缩短了0.0003 nm.当取代基R是BH2、COMe、CONH2、CHO、CF3、CN、NO2、SO3H等吸电子基团时,与R=H时相比较,氢键HB1和HB2的键长均伸长.例如:R=NO2时,r(H…O)HB1为0.2076 nm,伸长了0.0060 nm;r(H…O)HB2为0.1965nm,伸长了0.0015 nm,取代基对与其相近的HB1的键长影响更大.取代基对二聚体和四聚体中氢键键长的影响同上所述.
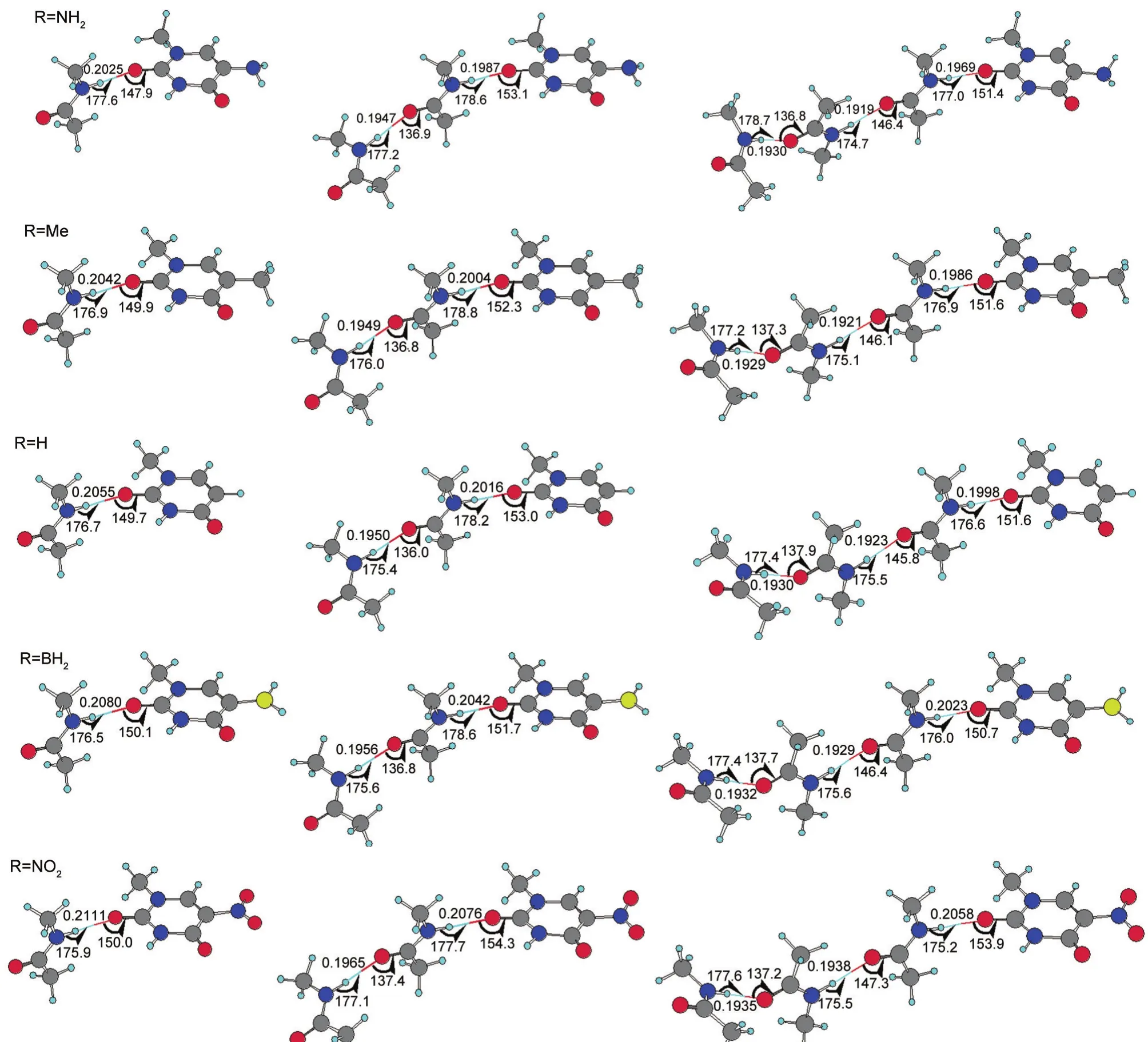
图2 15个氢键复合物体系的优化构型Fig.2 Optimal geometries of 15 hydrogen-bonded complexesbond length in nm,bond angle in degree
比较二聚体、三聚体、四聚体中的氢键HB1可发现,四聚体中的HB1氢键键长小于三聚体中的,三聚体中的HB1氢键键长小于二聚体中的.比较三聚体、四聚体中的HB2可发现,四聚体中的HB2氢键键长小于三聚体中的.由此可知,随着氢键链的伸长,处于相同位置的氢键键长变短.
3.2 氢键受体分子中的取代基对氢键强度的影响
表1列出了本文所研究的36个氢键复合物体系中的氢键键长和氢键能量.由表1可知,用不同取代基取代氢键复合物中氢键受体分子1-甲基尿嘧啶上的氢原子对氢键强度有不同影响.当取代基为供电子基团NH2、Et、Me时,氢键强度增强;当取代基为吸电子基团BH2、COMe、CONH2、CHO、CF3、CN、NO2、SO3H时,氢键强度减弱.以包含了BSSE校正的MP2/6-311++G(d,p)方法的计算结果为例,在二聚体中,R=H时,氢键HB1的强度为EHB1=-22.6 kJ·mol-1;当H被供电子基团NH2取代,EHB1=-24.5 kJ·mol-1,氢键能增强了1.9 kJ·mol-1;当H被吸电子基团SO3H取代,EHB1=-16.9 kJ·mol-1,氢键能减弱了5.7 kJ·mol-1.在三聚体中,R=H时,EHB1=-25.9 kJ· mol-1,EHB2=-34.0 kJ·mol-1;当H被供电子基团NH2取代,EHB1=-28.2 kJ·mol-1,氢键能增强了2.3 kJ· mol-1,EHB2=-34.4 kJ·mol-1,氢键能增强了0.4 kJ· mol-1;当H被吸电子基团SO3H取代,EHB1=-17.3 kJ· mol-1,氢键能减弱了8.6 kJ·mol-1,EHB2=-31.2 kJ· mol-1,氢键能减弱了2.8 kJ·mol-1.在四聚体中,R=H时,EHB1、EHB2和EHB3分为-26.4、-40.7、-36.6 kJ·mol-1;当H被供电子基团NH2取代,EHB1、EHB2和EHB3分别为-29.0、-41.3、-36.9 kJ·mol-1,氢键能分别增强了2.6、0.6、0.3 kJ·mol-1;当H被吸电子基团SO3H取代, EHB1、EHB2和EHB3分别为-17.6、-37.4、-36.2 kJ·mol-1,氢键能分别减弱了8.8、3.3、0.4 kJ·mol-1.由此可知,供电子基团使氢键复合物中氢键相互作用增强,吸电子基团使氢键相互作用减弱,并且取代基对与其相近的氢键强度影响更大.
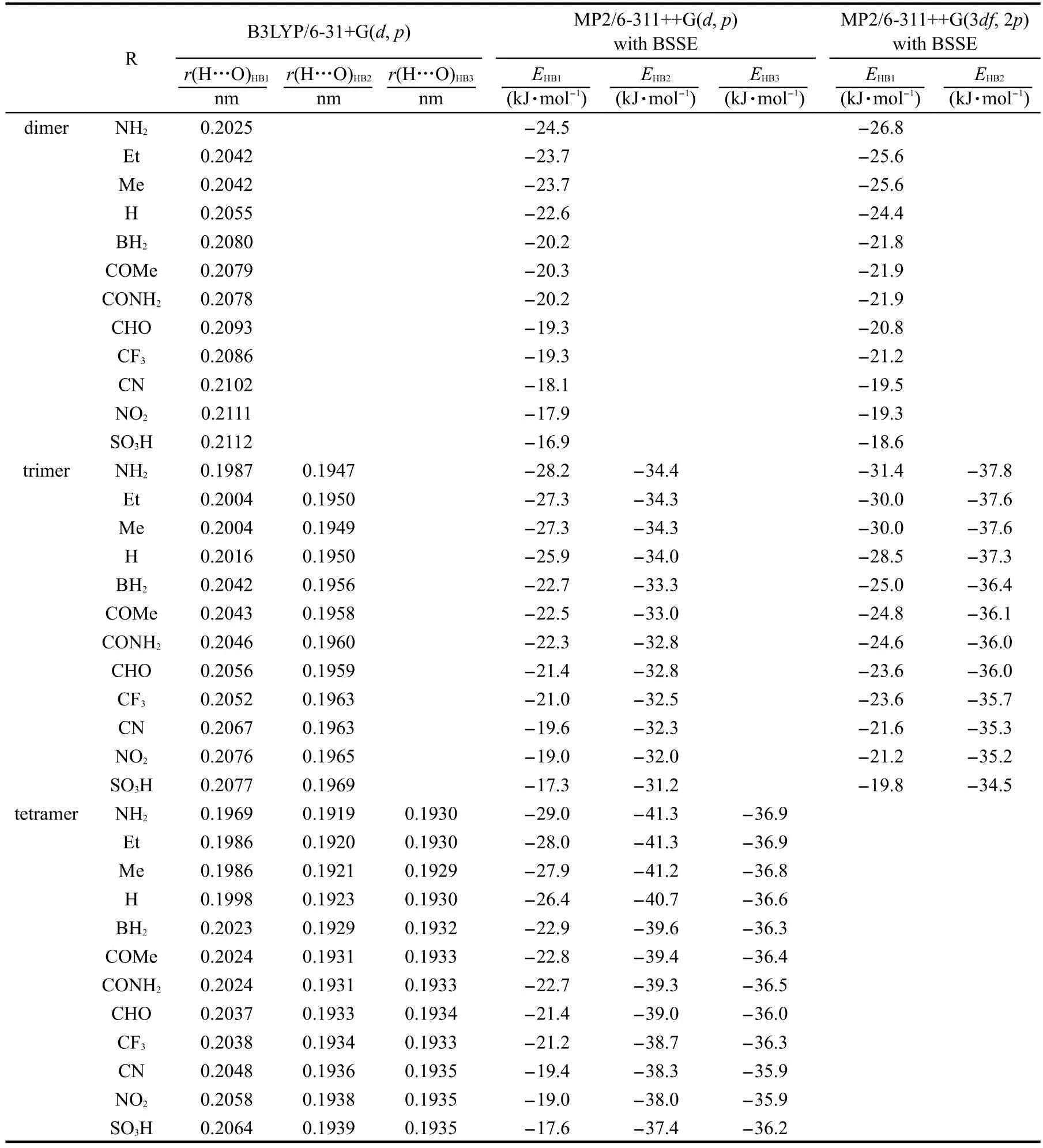
表1 36个氢键体系的氢键能量及键长Table 1 Hydrogen bond energies and hydrogen bond distances of thirty-six hydrogen-bonded complexes
比较二聚体、三聚体、四聚体中的EHB1可发现,四聚体中的EHB1强于三聚体中的EHB1,三聚体中的EHB1强于二聚体中的EHB1,即随着氢键链的伸长,氢键HB1强度增大.比较三聚体、四聚体中的EHB2可发现,四聚体中的EHB2强于三聚体中的EHB2,即随着氢键链的伸长,氢键HB2强度增大.由此可知,随着氢键链的伸长,处于相同位置的氢键强度增大,即在1-甲基尿嘧啶与N-甲基乙酰胺所形成的N-H…O=C氢键复合物中存在着氢键协同效应.
3.3 自然键轨道(NBO)分析
表2是使用B3LYP/6-31+G(d,p)方法计算得到的36个氢键复合物的自然键轨道(NBO)分析结果.其中,qH为参与形成氢键的氢原子的电荷,qO为参与形成氢键的氧原子的电荷,qt为参与形成氢键的质子供体和质子受体分子间的电荷转移量,Eij为质子受体分子中形成氢键的氧原子的孤对电子轨道n(O)对质子供体分子中形成氢键的N-H反键轨道σ*(N-H)的二阶相互作用稳定化能.下面以三聚体为例进行说明.
当R=H时三聚体复合物中氢键HB1的氢原子电荷为0.4592e,氧原子电荷为-0.6784e(表2中第3、4列);氢键HB2的氢原子电荷为0.4621e,氧原子电荷为-0.6947e(表2中第7、8列).以R=H为标准进行比较,当取代基为供电子基团NH2时,氢键HB1的qH为0.4614e,正电荷增加了0.0022e,qO为-0.6984e,负电荷增加了0.0200e;氢键HB2的qH为0.4625e,正电荷增加了0.0004e,qO为-0.6969e,负电荷增加了0.0022e.这是由于NH2是供电子基团,使1-甲基尿嘧啶中形成氢键的氧原子上的负电荷增加,接受质子的能力增加,因此氢键强度增强,即氢键受体分子中具有供电子诱导效应的取代基有利于氢键的形成.当取代基R为吸电子基团SO3H时,氢键HB1的qH为0.4543e,正电荷减少了0.0049e,qO为-0.6506e,负电荷减少了0.0278e;氢键HB2的qH为0.4612e,正电荷减少了0.0009e,qO为-0.6908e,负电荷减少了0.0039e.这是由于SO3H是吸电子基团,使1-甲基尿嘧啶中形成氢键的氧原子上的负电荷减少,接受质子的能力减弱,因此氢键强度减弱,即氢键受体分子中吸电子取代基不利于氢键的形成.对于其它氢键复合物体系,电荷变化的规律同上所述,即供电子基团使氢键中氢原子正电荷增加,氧原子负电荷增加,吸电子基团使氢键中氢原子正电荷减少,氧原子负电荷减少.
由表2中第5列可以看出,对于HB1氢键,R=H时三聚体复合物中质子供体和受体分子间电荷转移量为0.0194e;由表2中第9列可以看出,对于HB2氢键,R=H时三聚体复合物中质子供体和受体分子间电荷转移量为0.0282e.取代基为供电子基团NH2时,其氢键HB1和HB2的质子供体和质子受体分子间电荷转移量分别为0.0214e和0.0286e,比R=H时分别增加了0.0020e和0.0004e.取代基为吸电子基团SO3H时,氢键HB1和HB2的质子供体和受体分子间电荷转移量为0.0145e和0.0257e,比R=H时分别减少了0.0049e和0.0025e.这表明,氢键受体分子中供电子取代基使参与形成氢键的质子供体和受体分子间的电荷转移量增加,吸电子取代基使其减少.由表2还可知,取代基对氢键HB1的氢原子和氧原子的电荷以及对氢键HB1的质子供体和受体分子间的电荷转移量的影响要大于对氢键HB2的影响.
由表2中第6列和第10列可以看出,R=H时三聚体复合物中氢键HB1和HB2的二阶相互作用稳定化能分别为41.9和59.8 kJ·mol-1.与其相比较,当取代基为供电子基团Me时,Eij(HB1)为43.9 kJ·mol-1,增加了2.0 kJ·mol-1,Eij(HB2)为60.0 kJ·mol-1,增加了0.2 kJ·mol-1.当取代基为吸电子基团BH2时,Eij(HB1)为36.6 kJ·mol-1,减少了5.3 kJ·mol-1,Eij(HB2)为58.5 kJ·mol-1,减少了1.3 kJ·mol-1.由此可知,供电子取代基使二阶相互作用稳定化能增加,吸电子取代基使其减少,并且取代基对与其相近的氢键HB1的二阶相互作用稳定化能的影响更大.
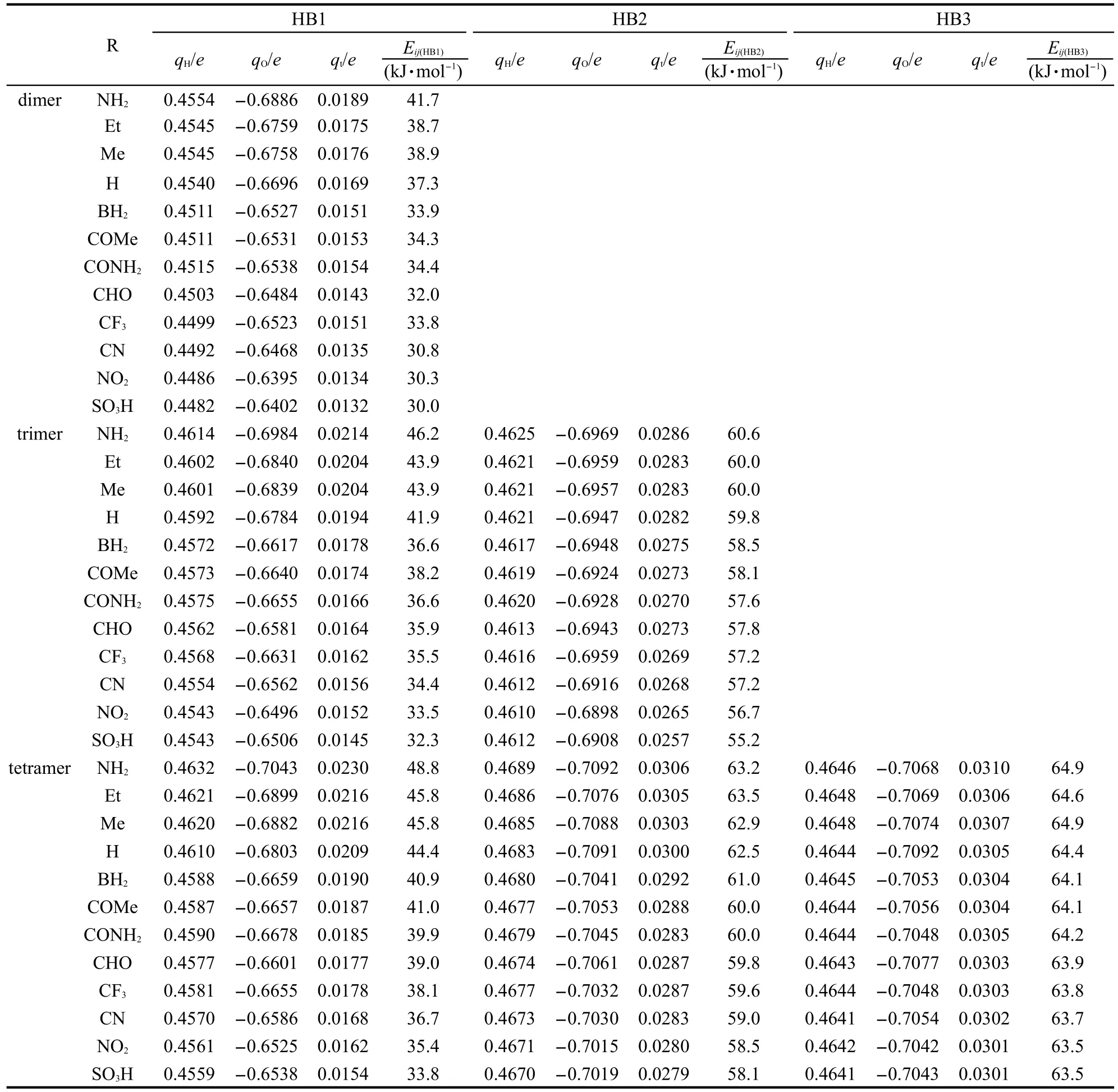
表2 氢键复合物的n→σ*二阶相互作用稳定化能及自然键轨道(NBO)分析Table 2 n→σ*second-order interaction energies and nature bond orbital(NBO)analysis for the hydrogen-bond complexes
对于其它氢键复合物,电荷和二阶稳定化能变化规律同上所述.
比较二聚体、三聚体、四聚体中HB1的qt、Eij(HB1)可发现,四聚体中HB1的qt、Eij(HB1)分别大于三聚体中HB1的qt、Eij(HB1),三聚体中HB1的qt、Eij(HB1)分别大于二聚体中HB1的qt、Eij(HB1),即随着氢键链的伸长, HB1的qt和Eij(HB1)均增大.比较三聚体、四聚体中HB2的qt、Eij(HB2)可发现,四聚体中HB2的qt、Eij(HB2)分别大于三聚体中HB2的qt、Eij(HB2),即随着氢键链的伸长,HB2的qt和Eij(HB2)均增大.由此可知,随着氢键链的伸长,处于相同位置的参与形成氢键的质子供体和质子受体分子间的电荷转移量增大,质子受体分子中形成氢键的氧原子的孤对电子轨道n(O)对质子供体分子中形成氢键的NH反键轨道σ*(N-H)的二阶相互作用稳定化能也增大.由此推测,1-甲基尿嘧啶与N-甲基乙酰胺所形成的N-H…O=C氢键复合物中存在的氢键协同效应与质子供体和质子受体分子间的电荷转移量以及二阶相互作用稳定化能密切相关.

图3 ΔE与Δqt、ΔEij的关系图Fig.3 Relationship between ΔE and Δqt,ΔEijΔE is the relative hydrogen bonding energy obtained by subtracting the hydrogen bonding energy of the R=H system. Δqtis the relative charge transfer and ΔEijis the relative second-order interaction energy obtained using the similiar way as ΔE.
图3中ΔE是各个氢键复合物中氢键能量相对于R=H时的变化值,Δqt是各个氢键复合物中氢键受体和供体分子间电荷转移量相对于R=H时的变化值,ΔEij是各个氢键复合物中氢键受体和供体分子间二阶相互作用稳定化能相对于R=H时的变化值.图3表明,ΔE与Δqt和ΔEij线性相关.由于分子间电荷转移量的大小以及二阶相互作用稳定化能的强弱反映了氢键供体和受体分子间的轨道作用(或共价成分)的强弱,因此ΔE与Δqt和ΔEij线性相关反映的是这样一种事实,即相对于R=H而言,供电子取代基使本文所研究体系的氢键强度增强的原因是供电子取代基增强了氢键供体和受体间的轨道作用,吸电子取代基使本文所研究体系的氢键强度变弱的原因是吸电子取代基削弱了氢键供体和受体间的轨道作用,换言之,轨道作用或共价成分在本文所研究体系的这些氢键作用中起重要作用.
4 结论
研究结果表明,可以通过改变氢键受体分子上取代基的供电性或吸电性来达到调控碱基与酰胺化合物所形成的N-H…O=C型氢键复合物中氢键强度的目的.氢键受体分子中的取代基为供电子基团时,氢键键长r(H…O)缩短,氢键强度增强;取代基为吸电子基团时,氢键键长r(H…O)伸长,氢键强度减弱.自然键轨道(NBO)分析表明,氢键受体分子中的供电子取代基使参与形成N-H…O=C氢键中氢原子的正电荷增加,氧原子的负电荷增加,质子受体和供体间的电荷转移量增加,使N-H…O=C氢键中氧原子的孤对电子轨道n(O)对N-H的反键轨道σ*(N-H)的二阶相互作用稳定化能增强;氢键受体分子中的吸电子取代基的作用则相反.1-甲基尿嘧啶与N-甲基乙酰胺所形成的NH…O=C氢键复合物中存在的氢键协同效应与质子供体和质子受体分子间的电荷转移量以及二阶相互作用稳定化能密切相关.
Supporting Information: The optimal geometries of hydrogen-bonded complexes at the B3LYP/6-31+G(d,p)level have been included.This information is available free of charge via the internet at http://www.whxb.pku.edu.cn.
(1) Desiraju,G.R.;Steiner,T.The Weak of Hydrogen Bond; Oxford University Press:New Nork,1999;pp 343-412.
(2) Jeffrey,G.A.An Introduction to Hydrogen Bonding;Oxford University Press:New York,1997;pp 184-212.
(3) Scheiner,S.Hydrogen Bonding:A Theoretical Perspective; Oxford University Press:New York,1997;pp 105-117.
(4) Chalaris,M.;Samios,J.J.Phys.Chem.B 1999,103,1161. doi:10.1021/jp982559f
(5) Mohajeri,A.;Nobandegani,F.F.J.Phys.Chem.A 2008,112, 281.doi:10.1021/jp075992a
(6) Sun,C.L.;Wang,C.S.Sci.China Ser.B-Chem.2009,39(6), 481.[孙长亮,王长生.中国科学B辑:化学,2009,39(6), 481.]
(7)Jiang,X.N.;Wang,C.S.ChemPhysChem 2009,10,3330. doi:10.1002/cphc.200900591
(8)Li,Y.;Jiang,X.N.;Wang,C.S.J.Comput.Chem.2011,32, 953.doi:10.1002/jcc.v32.5
(9)Kolew,S.K.;Petkow,P.S.;Rangelow,M.A.;Vayssilow,G.N. J.Phys.Chem.A 2011,115,14054.doi:10.1021/jp204313f
(10)Angelina,E.L.;Peruchena,N.M.J.Phys.Chem.A 2011,115, 4701.doi:10.1021/jp1105168
(11) Ji,C.G.;Zhang,Z.H.J.Phys.Chem.B 2011,115,12230.doi: 10.1021/jp205907h
(12) Izgorodina,E.I.;MacFarlane,D.R.J.Phys.Chem.B 2011, 115,14659.doi:10.1021/jp208150b
(13) Dong,H.;Hua,W.J.;Li,S.H.J.Phys.Chem.A 2007,111, 2941.
(14) Vargas,R.;Garza,J.;Friesner,R.A.;Stern,H.;Hay,B.P.; Dixon,D.A.J.Phys.Chem.A 2001,105,4963.doi:10.1021/ jp003888m
(15) Kawahara,S.;Kobori,A.;Sekine,M.;Taira,K.;Uchimaru,T. J.Phys.Chem.A 2001,105,10596.doi:10.1021/jp0124645
(16) Kawahara,S.;Uchimaru,T.;Taira,K.;Sekine,M.J.Phys. Chem.A 2001,105,3894.
(17) Sun,C.L.;Zhang,Y.;Jiang,X.N.;Wang,C.S.;Yang,Z.Z.Sci. China Ser.B-Chem.2008,38(9),762.[孙长亮,张 艳,姜笑楠,王长生,杨忠志.中国科学B辑:化学,2008,38(9),762.]
(18) Sun,C.L.;Jiang,X.N.;Wang,C.S.J.Comput.Chem.2009, 30,2567.doi:10.1002/jcc.v30:15
(19)Wang,C.S.;Zhang,Y.;Gao,K.;Yang,Z.Z.J.Chem.Phys. 2005,123,024307.doi:10.1063/1.1979471
(20) Zhang,Y.;Wang,C.S.J.Comput.Chem.2009,30,1251.doi: 10.1002/jcc.v30:8
(21) Sun,C.L.;Wang,C.S.J.Mol.Struct.-Theochem 2010,956,38. doi:10.1016/j.theochem.2010.06.020
(22) Jiang,X.N.;Sun,C.L.;Wang,C.S.J.Comput.Chem.2010, 31,1410.
(23) Chen,Y.F.;Dannenberg,J.J.J.Am.Chem.Soc.2006,128, 8100.doi:10.1021/ja060494l
(24) Nobko,N.;Dannenberg,J.J.J.Phys.Chem.A 2003,107,6688. doi:10.1021/jp0345497
(25) Nobko,N.;Dannenberg,J.J.J.Phys.Chem.A 2003,107, 10389.
(26)Zhao,Y.L.;Wu,Y.D.J.Am.Chem.Soc.2002,124,1570.doi: 10.1021/ja016230a
(27) Wu,Y.D.;Zhao,Y.L.J.Am.Chem.Soc.2001,123,5313.doi: 10.1021/ja003482n
(28)Tan,H.W.;Qu,W.W.;Chen,G.J.;Liu,R.Z.J.Phys.Chem.A 2005,109,6303.doi:10.1021/jp051444q
(29)Hunter,K.C.;Millen,A.L.;Wetmore,S.D.J.Phys.Chem.B 2007,111,1858.doi:10.1021/jp066902p
(30) Jeong,E.;Kim,H.;Lee,S.W.;Han,K.Mol.Cells 2003,16, 161.
(31) Cheng,A.C.;Frankel,A.D.J.Am.Chem.Soc.2004,126,434. doi:10.1021/ja037264g
(32) Tkachenko,M.Y.;Boryskina,O.P.;Shestopalova,A.V.; Tolstorukov,M.Y.Int.J.Quantum Chem.2010,110,230.doi: 10.1002/qua.v110:1
(33) Frish,M.J.;Trucks,G.W.;Schlegel,H.B.;et al.Gassian 03, Revision D.01;Gaussian Inc.:Pittsburgh,PA,2003.
