双层聚吡咯/普鲁士蓝复合膜的制备与性能研究
2012-02-19宋诗稳甄延忠
宋诗稳,, 甄延忠, 于 浩*, 张 军
(1.延安大学 能源与环境工程学院, 陕西 延安 716000; 2.延安大学 化学与化工学院, 陕西 延安 716000)
0 引言
多核金属铁氰化物(MHCF)是一类重要的微溶金属混合价态化合物,利用MHCF极强的电催化活性以提高测定方法的灵敏度和选择性引起了电化学工作者的兴趣[1-7].从同时含有目标金属离子、铁氰化钾及支持电解质阳离子的混合溶液中,利用电化学方法在线电沉积是制备MHCF修饰电极最常用的方法.但其生成速率较快易团聚, 故采用上述方法难以得到均匀致密的MHCF膜,这直接影响了电极的稳定性及电催活性.自从Diza[8]采用电化学方法制备出导电聚吡咯(Ppy)膜以来,Ppy修饰电极引起了人们的广泛关注[9-12],利用Ppy可以导电的特点,可通过化学衍生等手段引入活性基团,调控聚合物分子与MHCF间的相互作用,以提高MHCF在电极表面的分散性以及修饰电极的稳定性[13].
本文以Ppy/CCE为基础电极,采用循环伏安法制备了Ppy/PB复合膜,为进一步改善修饰电极的稳定性,采用聚合物涂层保护法,在复合膜表面沉积了第二层Ppy膜,制得了双层-Ppy/PB修饰的复合陶瓷碳电极,并研究了该修饰电极对H2O2的电催化活性.
1 实验部分
1.1 试剂和仪器
LK98BII型电化学工作站(天津市兰力科公司).采用三电极系统电化学池,以修饰电极为工作电极,铂丝电极为辅助电级,饱和甘汞电极(SCE)为参比电极.文中电位值均是相对于饱和甘汞电极的电位.甲基三甲氧基硅烷(MTMOS,杭州硅宝化工),吡咯(国药集团化学试剂公司),使用前在氮气保护下连续两次蒸馏提纯,置于冰箱中避光保存.其余试剂均为分析纯,水为二次蒸馏水.
1.2 电极的制备
1.2.1单层-Ppy/PB/CCE的制备
裸CCE的制备参考Lev等人工作[14].将处理好的CCE浸入1.5×10-2mol/L Py+0.10 mol/L KCl (pH=1.0)中,以50 mV/s的扫速,在-0.3~0.8V范围内循环8圈,清洗电极后于5.0×10-3mol/L FeCl3+5.0×10-3mol/L K3Fe(CN)6+0.10 mol/L KCl(pH=1.0)中,在0.8~-0.2V范围内,以50 mV/s的扫速循环4圈沉积PB,电极记为S-Ppy/PB/CCE.
1.2.2双层-Ppy/PB/CCE的制备
将S-Ppy/PB/CCE置于1.5×10-2mol/L Py+0.10 mol/L KCl(pH=1.0)中,以50 mV/s扫速于-0.3~0.8V范围内循环2圈,电极记为D-Ppy/PB/CCE.
1.3实验方法
动力学计时安培实验:以修饰电极为工作电极,控制工作电位为一定值,向连续搅拌的溶液中每隔一定时间加入一定量H2O2,记录i-t曲线.
2 结果与讨论
2.1 D-Ppy/PB/CCE的电化学沉积
采用循环伏安法在CCE表面沉积了Ppy膜.当电位超过0.8V后,氧化峰电流明显增大,这来源于Py单体在电极表面的氧化聚合,沉积后电极表面生成一层均匀致密的蓝色薄膜.图1(A)为Ppy/CCE表面沉积PB的CV曲线.图中0.3V处的氧化还原峰来源于Fe(CN)63-/Fe(CN)64-电对在电极表面的氧化还原,0.15 V处的氧化还原峰来源于PB电对的氧化还原.随着扫描圈数的增加,PB氧化还原峰逐渐增大,当循环圈数达到4圈时,0.15 V处氧化还原峰电流增加缓慢,故选择PB沉积圈数为4圈.为了提高修饰电极的稳定性,在S-Ppy/PB/ CCE表面沉积了第二层Ppy膜(如图1B所示).当第二层Ppy膜沉积圈数过多时,电极导电性降低且背景电流增大,故选择第二层Ppy膜的沉积圈数为2圈.
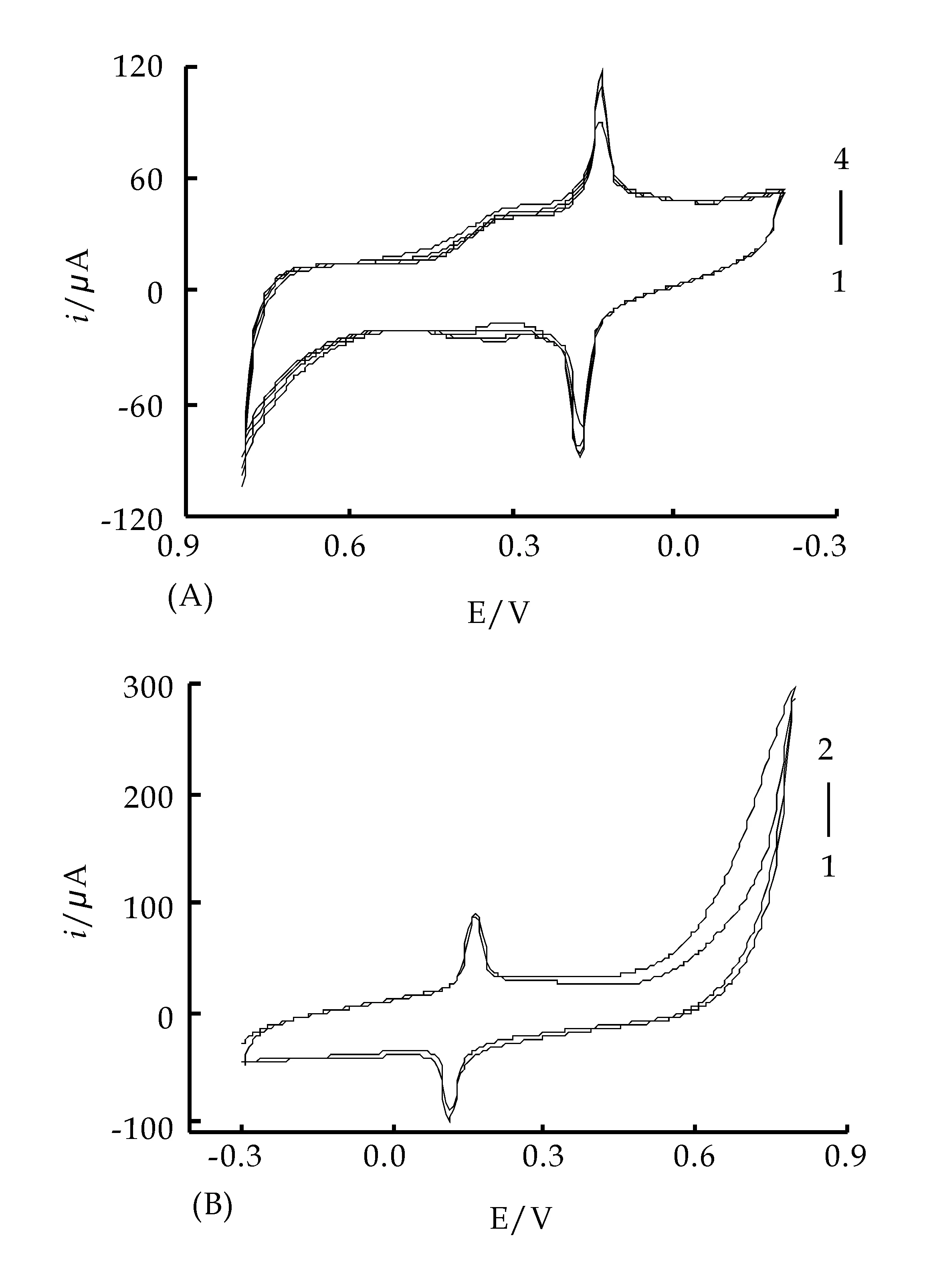
图1 D-Ppy/PB/CCE的沉积图
由图2可以看出,在0.10 mol/L KCl中,当扫率为5mV/s时,修饰电极在CV曲线上出现一对氧化还原峰(式量电位0.15 V),阴、阳极峰电流比值约为1,表明该电极反应为一准可逆过程.根据Laviron理论[15],在一定扫速范围内ΔEp(Ep-E0′)与lnv呈线性关系,求得电子转移系数(α)和电极反应速率常数(ks)分别为0.42与9.44 s-1.

图2 D-Ppy/PB/CCE的循环伏安图
2.2 计时安培实验
采用计时安培法测定了H2O2的扩散系数及异相催化反应的速率常数[16,17](如图3所示).由图可知,当t-1/2在0.5~1.0范围内时,i-t-1/2呈线性关系,以这些线性关系的斜率对H2O2浓度作图所得直线斜率为18.19,则扩散系数为2.25×10-6cm2/s.另外,由计时安培实验估测了电子递质与底物间催化反应的异相催化反应速率常数.icat/iL-t1/2曲线斜率与H2O2浓度平方根作图所得直线斜率为69.93(t1/2:1.4~2.0),则异相催化反应速率常数为1.56×103L/mol s.
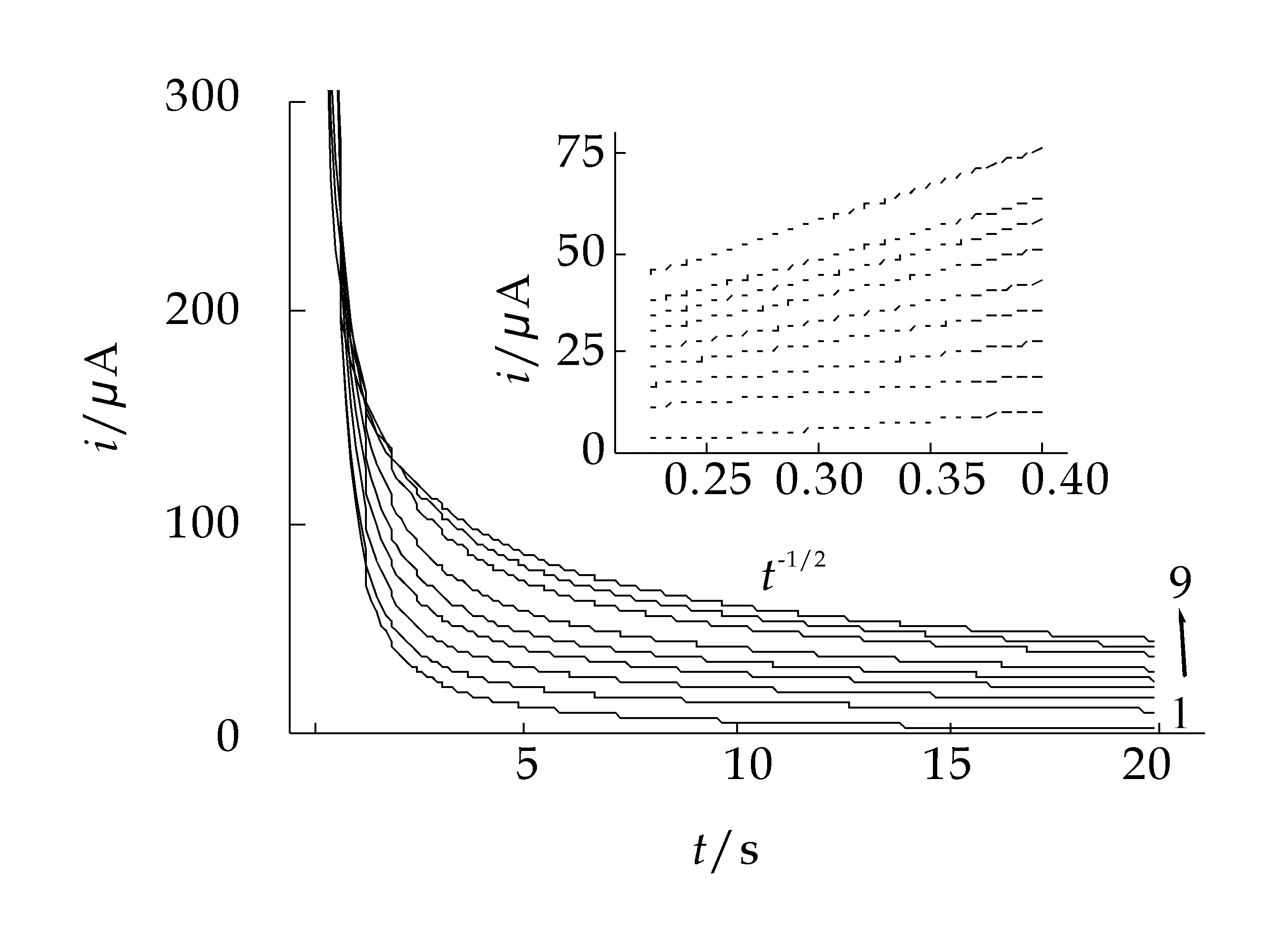
图3 D-Ppy/PB/CCE在H2O2中的计时安培曲线c(H2O2)1~9:0.00,1.96,2.91,3.85,4.76,5.66,6.54,7.41,8.26×10-3 mol/L,E:0.45~0.10 V
2.3 线性范围及检出限
在优化的实验条件下,动力学安培法电流响应与H2O2浓度在2.0×10-6~2.5×10-3mol/L(r=0.9977)范围内呈线性关系,检出限为6.5×10-7mol/L,灵敏度为3593.2μA/(mmol/L)cm2,响应时间小于5s(如图4B所示).采用动力学安培实验研究了第二层Ppy对修饰电极稳定性的影响,由图可知,在D-Ppy/PB/CCE上(如图4b所示),修饰电极检测H2O2的灵敏度略有降低,稳定性却得到了极大提高.

图4 修饰电极的安培响应工作电位:-0.05 V,底液:0.10 mol/L PBS H2O2加入量:2.0×10-5,5.0×10-5,1.0×10-4,2.0×10-4,5.0×10-4,1.0×10-3,2.0×10-3 mmol各3次
2.4 修饰电极的稳定性和重现性
在优化的实验条件下,对0.1mmol/L H2O2连续平行测定10次的相对标准偏差为6.4%.电极于室温下放置30 d后重新进行测试,其对H2O2的响应电流几乎不变,表明该修饰电极对H2O2的测定具有较好的稳定性和重现性.
3 结束语
采用循环伏安法制备了D-Ppy/PB/CCE修饰电极,研究了该电极的电催化性能.结果表明:第一层Ppy膜的存在可调控聚合物分子与PB间的作用,从而提高PB在电极表面的分散性.第二层Ppy膜的涂层保护作用极大地提高了修饰电极的化学及电化学稳定性.该修饰电极具有响应时间短、价格低廉和表面容易更新等特点,对H2O2的还原表现出良好的电催化活性,在生物电化学传感器制作方面具有潜在的应用价值.
[1] Arduini F.,Cassisi A.,Amine A.,et al. Electrocatalytic oxidation of thiocholine at chemically modified cobalt hexacyanoferrate screen-printed electrodes[J].Journal of Electroanalytical Chemistry,2009,626(1):66-74.
[2] Abbaspour A.,Khajehzadeh A.,Ghaffarinejad A..Electro -catalytic oxidation and determination of hydrazine on nickel hexacyanoferrate nanoparticles-modified carbon ceramic electrode[J].Journal of Electroanalytical Chemistry,2009, 631(1): 52-57.
[3] Sheng Q.L., Luo K., Zheng J.B., et al. Enzymatically induced formation of neodymium hexacyanoferrate nanoparticles on the glucose oxidase/chitosan modified glass carbon electrode for the detection of glucose[J].Biosensors and Bioelectronics,2008,24(3):429-434.
[4] Liu Y.,Chu Z.Y.,Zhang Y.N.,et al. Amperometric glucose biosensor with high sensitivity based on self-assembled Prussian blue modified electrode[J]. Electrochimica Acta,2009,54(28):7490-7494.
[5] 胡 荣,双雅琼,李 伟,等.普鲁士蓝/多壁碳纳米管修饰电极测定维生素C[J].分析试验室,2009,28(7):61-64.
[6] Yang M.H., Jiang J.H., Lu Y S., et al. Functional histidine/nickel hexacyanoferrate nanotube assembly for biosensor applications[J].Biomaterials,2007,28(23):3408-3417.
[7] 余淑娟,张云怀,肖 鹏,等.基于纳米铁氰化镍修饰二氧化钛纳米管阵列电极的非酶葡萄糖传感器[J].分析化学,2012,40(2):313-316.
[8] Diaz A.F.,Kanzawa K.K.,Gardini G.P.Conducting poly-N- alkylpyrrole polymer films[J].Journal of Electroanalytical Chemistry,1982,133(2):233-239.
[9] 鲁理平,王 飞,康天放,等. 过氧化聚吡咯修饰金电极研究全氟化合物对核糖核酸的损伤[J].分析化学,2011,39(3):392-396.
[10] 刘利兵,庞月红,钱 和,等. 毛细管电泳-多壁碳纳米管/聚吡咯/磷钼酸修饰电极电化学检测饮用水中的溴酸根[J].分析科学学报,2011,27(4):479-482.
[11] Tian Y., Wang J.X., Wang Z. Solid phase extraction and amperometric determination of nitrite with polypyrrole nanowire modified electrodes[J].Sensors and Actuators B: Chemical,2005,104(1):23-28.
[12] Daizaf A.F., Castllo J.I. A polymer electrode with variable conductivity: polypyrrole[J]. Journal of the Chemical Society,Chemical Communications,1980,14(9):397-398.
[13] Zou X.Q., Shen Y., Peng Z.Q. Preparation of a phosphor- polyoxomolybdate P2Mo18O626- doped polypyrrole modified electrode and its catalytic properties[J].Journal of Electroanalytical Chemistry,2004,566(1):63-71.
[14] Tsionsky M., Gun G., Glezer V., et al. Sol-gel-derived ceramic-carbon composite electrodes: introduction and scope of applications[J].Analytical Chemistry,1994,66(10):1747-1753.
[15] Laviron E. General expression of the linear potential sweep voltammogram in the case of diffusionless electrochemical systems[J].Journal of Electroanalytical Chemistry,1979,101(1):19-28.
[16] Bard A.J., Faulkner L.R. Electrochemical methods, fundamentals and applications[M].2nd Edition, New York: Wiley,2001:163.
[17] Pournaghi-azar M.H., Sabzi R. Electrochemical characterristics of a cobalt pentacyano-nitrosylferrate film on a modified glassy carbon electrode and its catalytic effect on the electrooxidation of hydrazine[J]. Journal of Electro- analytical Chemistry,2003,543(2):115-125.
