RP-HPLC法测定妇炎净胶囊中原儿茶酸的含量
2012-02-05杨仕林舒海燕王雨来湖北阳新县人民医院湖北阳新43500黄石市中心医院湖北黄石435000
杨仕林,舒海燕,王雨来(.湖北阳新县人民医院,湖北阳新 43500;.黄石市中心医院,湖北黄石435000)
RP-HPLC法测定妇炎净胶囊中原儿茶酸的含量
杨仕林1*,舒海燕1,王雨来2(1.湖北阳新县人民医院,湖北阳新 435200;2.黄石市中心医院,湖北黄石435000)
目的:建立测定妇炎净胶囊中原儿茶酸含量的方法。方法:采用高效液相色谱法。色谱柱为Hypersil C18(250mm×4.6 mm,5μm),流动相为甲醇-0.05%磷酸水溶液(20∶80),流速为1.0m L·min-1,检测波长为258 nm,柱温为40℃,进样量为20μL。结果:原儿茶酸的检测浓度在0.903~18.060μg·m L-1范围内与峰面积积分值呈良好的线性关系(r=0.999 8);平均加样回收率为98.7%,RSD=1.8%(n=9)。结论:该方法简便、准确、重复性好,可用于妇炎净胶囊的质量控制。
妇炎净胶囊;原儿茶酸;含量测定;反相高效液相色谱法
妇炎净胶囊是2010年版《中国药典》(一部)收录的中药制剂,以苦玄参、地胆草、当归、鸡血藤、两面针等中药为原料,经加水煎煮、浓缩、干燥,粉碎,装入胶囊制成。它具有清热祛湿、调经止带的功能,用于湿热蕴结所致的月经不调、痛经、附件炎、盆腔炎及子宫内膜炎的治疗。在其药品标准中仅对苦玄参苷ⅠA进行了含量测定[1],国内还有文献对该药中氯化两面针碱、绿原酸的含量测定进行了研究[2~5],但对鸡血藤中原儿茶酸的含量测定方法未见报道。因此,笔者采用反相高效液相色谱(RP-HPLC)法测定该药中原儿茶酸的含量,该法简便、快速、准确、重复性好,可用于妇炎净胶囊的质量控制。
1 仪器与试药
LC-10A型高效液相色谱(HPLC)仪(日本岛津公司);BS124S型天子天平(北京赛多利斯仪器系统有限公司)。
原儿茶酸对照品(中国食品药品检定研究院,批号:0809-200102);妇炎净胶囊(广西梧州制药(集团)股份有限公司,规格:0.4 g,批号:091004、100208、100432);甲醇(色谱纯,天津市标准科技有限公司)。
2 方法与结果
2.1 色谱条件与系统适用性试验
色谱柱:Hypersil C18(250mm×4.6mm,5μm);流动相:甲醇-0.05%磷酸水溶液(20∶80);流速:1.0m L·min-1;检测波长:258 nm;柱温:40℃;进样量:20μL。在该色谱条件下,原儿茶酸峰与相邻峰的分离度均>1.5,理论板数按原儿茶酸峰计算为5 700。色谱见图1。

图1 高效液相色谱图A.对照品;B.供试品;C.阴性对照;1.原儿茶酸Fig 1 HPLC chromatogram sA.substance control;B.test samples;C.negative control;1.protocatechuic acid
2.2 溶液的制备
2.2.1 对照品溶液 取原儿茶酸对照品适量,精密称定,置50 m L棕色量瓶中,用甲醇溶解并稀释至刻度,摇匀,制成原儿茶酸浓度为180.6μg·m L-1的对照品溶液。
2.2.2 供试品溶液 取本品内容物,混匀,研细。取约0.8 g,精密称定,加乙醇-醋酸(10∶1)50m L,置水浴上加热回流1 h,放冷,滤过,滤液蒸干,残渣加甲醇使溶解并定容至10m L,摇匀,用0.45μm微孔滤膜滤过,取续滤液作为供试品溶液。
2.2.3 阴性对照溶液 按本品处方配比及制备工艺制备除鸡血藤外的阴性样品,再按“2.2.2”项下方法制得阴性对照溶液。
2.3 线性关系考察
分别精密量取原儿茶酸对照品溶液0.5、2.0、4.0、5.0、6.0、8.0、10.0m L,置于100m L量瓶中,用甲醇稀释至刻度,摇匀,制得系列对照品溶液。精密吸取系列对照品溶液各20μL,注入液相色谱仪。以对照品浓度(X,μg·m L-1)为横坐标,峰面积积分值(A)为纵坐标,进行线性回归,得回归方程为A=4 823.1X-751.6(r=0.999 8,n=7)。结果表明,原儿茶酸检测浓度在0.903~18.060μg·m L-1范围内与峰面积积分值呈良好的线性关系。
2.4 精密度试验
精密量取原儿茶酸对照品溶液(9.03μg·m L-1)20μL,注入液相色谱仪,重复进样5次,测定峰面积。结果,RSD=0.5%(n=5),表明仪器精密度良好。
2.5 稳定性试验
精密量取同一供试品溶液适量,分别于1、2、4、6、8 h测定峰面积。结果,RSD=1.2%(n=5),表明供试品溶液在8 h内稳定性良好。
2.6 重复性试验
精密称取同一样品(批号:091004)适量,按“2.2.2”项下方法平行制备6份供试品溶液,依法测定峰面积。结果,RSD=1.8%(n=6),表明该方法重复性良好。
2.7 加样回收率试验
取已测知含量的妇炎净胶囊(批号:091004)20粒,倾取内容物,混匀,研细,取0.4 g,精密称定,分别精密加入原儿茶酸对照品溶液(9.03μg·m L-1)4.0、5.0、6.0m L,再加适量乙醇-醋酸(10∶1)溶液,按“2.2.2”项下方法制备供试品溶液,在上述色谱条件下测定样品含量,计算加样回收率,结果见表1。
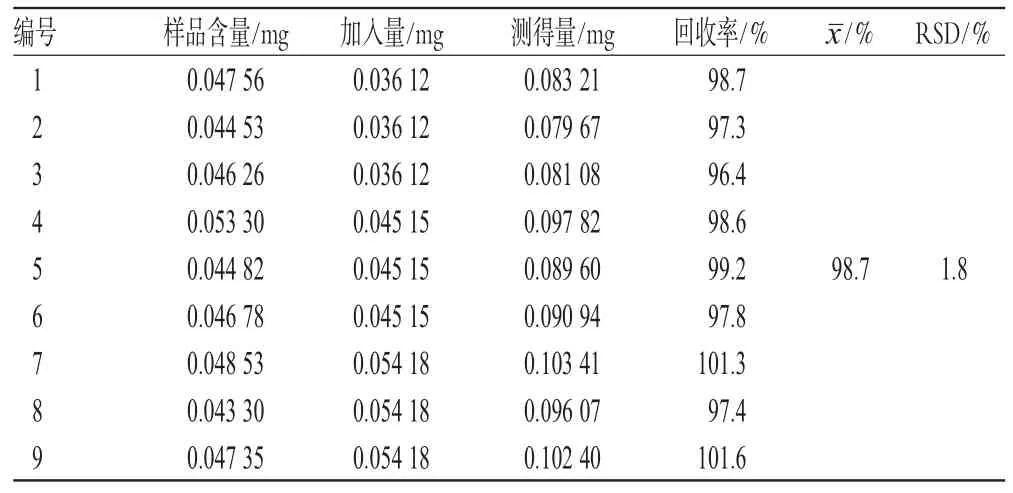
表1 加样回收率试验结果(n=9)Tab 1 Resultsof recovery tests(n=9)
2.8 样品含量测定
取3批样品(091004、100208、100432)各适量,分别按“2.2.2”项下方法制备供试品溶液,精密吸取20μL,注入液相色谱仪,记录峰面积;另取原儿茶酸对照品溶液(9.03μg·m L-1)适量,同法测定,按外标法以峰面积计算妇炎净胶囊中原儿茶酸的含量。结果,3批样品中原儿茶酸的平均含量分别为每粒0.046、0.053、0.059mg。
3 讨论
3.1 色谱条件的优化
将原儿茶酸的甲醇溶液在200~400 nm波长范围内进行紫外扫描,发现其在258 nm波长处有最大吸收,故选择258 nm作为检测波长。
原儿茶酸属于酚酸类物质,易解离,因而会导致色谱峰出现拖尾、变宽和不对称现象,在流动相中加入酸性抑制剂可以抑制此类化合物的电离,改善峰形。试验对比了甲醇-0.05%磷酸水溶液和甲醇-0.1%冰醋酸水溶液,发现前者的分离效果较佳、峰形对称、干扰较少,故选其作为流动相。
3.2 提取方法的考察
笔者考察了加热回流、超声2种样品提取方式,发现加热回流较超声法的提取率高出近10%,故选择加热回流提取法。再根据原儿茶酸易溶于水、甲醇、乙醇的性质,对提取溶剂的组成、用量等进行了考察。结果显示,以乙醇-醋酸(10∶1)为溶剂、用量50m L,提取效果最好。此外,还对加热回流的时间和次数进行了考察,结果发现加热回流提取1次、时间1 h即可基本提尽样品中的原儿茶酸。
[1] 国家药典委员会.中华人民共和国药典(一部)[S].2010年版.北京:中国医药科技出版社,2010:724.
[2] 唐秀玲,吕轶峰.HPLC法测定妇炎净胶囊中苦玄参苷ⅠA的含量[J].中国药师,2011,11(3):429.
[3] 刘鹏翰,陆来祥,潘声遣,等.HPLC法测定妇炎净片中氯化两面针碱的含量[J].食品与药品,2005,7(10):45.
[4] 陈军霞,卞 凌,李 炜,等.HPLC法测定妇炎净颗粒中绿原酸的含量[J].南京中医药大学学报,2009,25(6):459.
[5] 徐 玲,张继芬,吴芳洲,等.HPLC法测定双花颗粒中绿原酸的含量[J].中国药房,2011,22(23):2 156.
Determ ination of Protocatechuic Acid in Fuyanjing Capsules by RP-HPLC
YANG Shi-lin,SHU Hai-yan(Yangxin County People’s Hospital of Hubei Province,Hubei Yangxin 435200,China)
WANG Yu-lai(HuangshiMunicipal Central Hospital of Hubei Province,Hubei Huangshi435000,China)
OBJECTIVE:To establish the method for the determ ination of protocatechuic acid in Fuyanjing capsules.METHODS:HPLC method was adopted.The determ ination was performed on Hypersil C18(250 mm×4.6 mm,5μm)column w ith mobile phase consisted of methanol-0.05%phosphoric acid solution(20∶80)at the flow rate of 1.0 m L·m in-1.The detection wavelength was set at 258 nm and column temperature was 40℃.The injection volume was 20μL.RESULTS:The linear range of protocatechuic acid was 0.903~18.060μg·m L-1(r=0.999 8)w ith an average recovery of 98.7%(RSD=1.8%,n=9).CONCLUSION:Themethod is simple,accurate and reproducible,which can be used for the quality control of Fuyanjing capsules.
Fuyanjing capsules;Protocatechuic acid;Content determination;RP-HPLC
R283.65;R927.2
A
1001-0408(2012)23-2174-02
DOI 10.6039/j.issn.1001-0408.2012.23.24
*主管药师。研究方向:临床药学。电话:0714-7393081。E-mail:119139247@qq.com
2011-12-26
2012-04-19)
