冠心宁注射液中单糖、寡糖的定量测定研究
2012-01-29黄琴伟唐登峰李樱红
黄琴伟, 唐登峰, 李樱红, 李 正, 祝 明
(浙江省食品药品检验所,杭州浙江310004)
冠心宁注射液具有活血化瘀,通脉养心作用,用于冠心病心绞痛[1]。由于冠心宁注射液由丹参、川芎两味药组成,为中药注射液,所含成分复杂,故其成分分析对保障临床用药安全起着至关重要的作用。作者曾对丹参和川芎中的水溶性成分丹参素钠、原儿茶醛、阿魏酸、迷迭香酸和丹酚酸B等进行定量测定,所测得的量占总固体仅为2%~3%,表明冠心宁注射液中仍有大部分成分为未知成分。查阅冠心宁注射液的质量标准[1],制法项未添加果糖、葡萄糖、蔗糖等辅料。另根据文献报道[2-4],川芎药材中含有较多糖类成分,丹参药材中也含有少量的糖类,故对冠心宁注射液的糖类成分进行分析有助于完善其基础物质研究,完善冠心宁注射液的质量控制方法。本实验从临床用药安全角度出发进而提高和完善样品质量控制,对冠心宁注射液中糖类成分进行分析测定。
1 仪器与试药
1.1 仪器 Agilent1100型系列高效液相色谱仪:包括G1311A四元泵,G1322A脱气机,G1329A自动进样器,G1316A柱温箱,Alltech 2000蒸发光散射检测器。
1.2 试药 果糖对照品 (批号:100231-200303)、D-无水葡萄糖对照品 (批号:110833-200904)、蔗糖对照品 (批号:1507-200001)均由中国药品生物制品检定所提供,供含量测定用。乙腈为色谱纯,水为重蒸水。共收集了6个厂家共71批样品,样品信息见表1。
吸取上述对照品贮备液3.0 mL,置10 mL量瓶中,加蒸馏水定容至刻度,摇匀即得,作为线性溶液①。
2 方法与结果
2.1 色谱条件 以糖基为填充剂 (Prevail Carbohydrate ES柱4.6 mm×250 mm,5 μm);流动相为乙腈-水 (79∶21);体积流量1.0 mL/min;ELSD检测器;漂移管温度100℃;N2流量2.8 L/min。
2.2 对照品溶液的制备 分别称取果糖对照品、葡萄糖对照品、蔗糖对照品377.50 mg、282.05 mg及408.21 mg,置25 mL量瓶中,加水使溶解并稀释至刻度,摇匀即得,作为对照品贮备液。
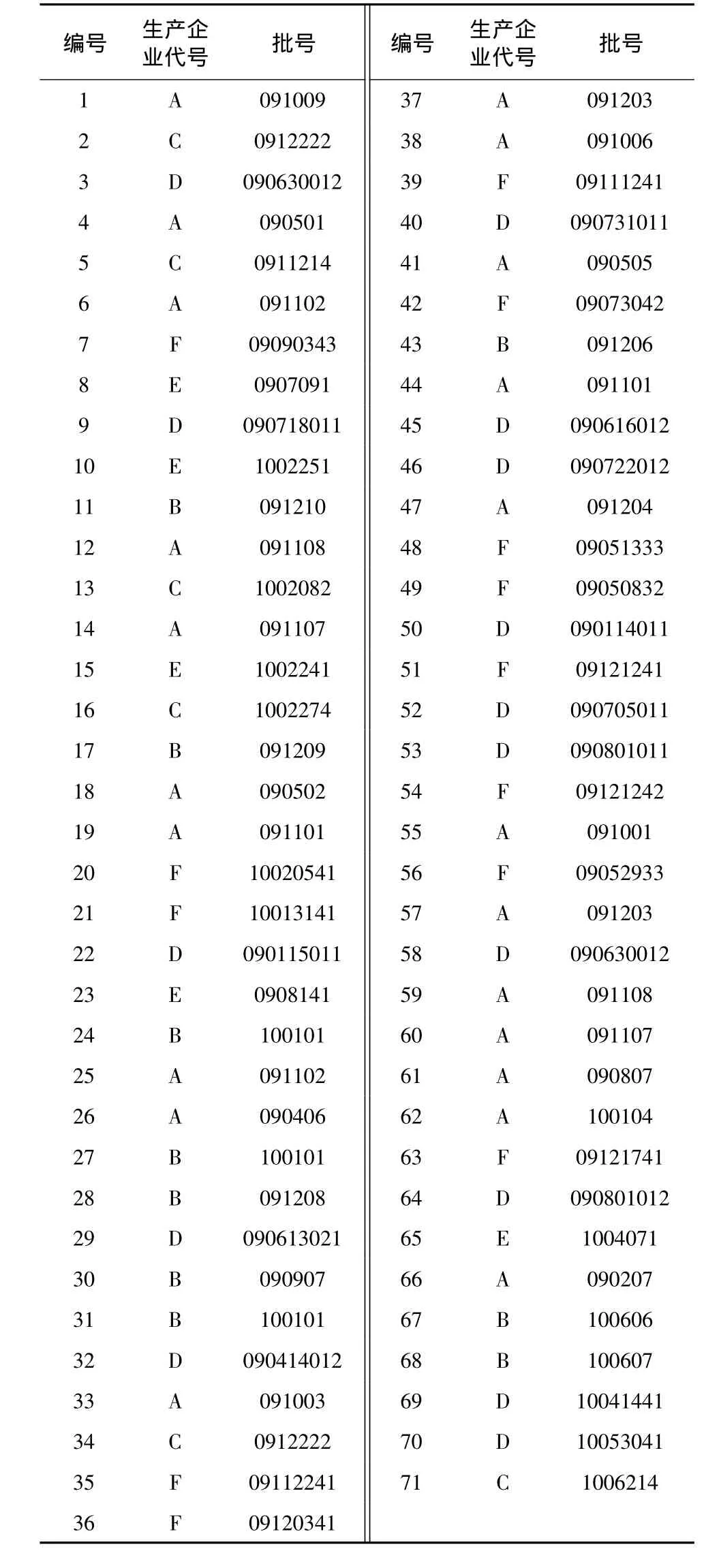
表1 71批冠心宁注射液信息Tab.1 Information of 71 batches of Guanxinning Injection
吸取上述线性溶液①2.0 mL,置5 mL量瓶中,加蒸馏水定容至刻度,摇匀即得,作为线性溶液②。
另分别称取果糖对照品、葡萄糖对照品、蔗糖对照品249.10 mg、175.75 mg及255.56 mg,置15 mL量瓶中,加蒸馏水使溶解并定容至刻度,摇匀即得,作为对照品溶液③。
吸取对照品溶液③3.0 mL,置10 mL量瓶中,加蒸馏水定容至刻度,摇匀,作为对照品溶液④。
2.3 供试品溶液的制备 取冠心宁注射液2.0 mL置10 mL量瓶,加水至刻度,摇匀,作为供试品溶液。色谱图见图1。
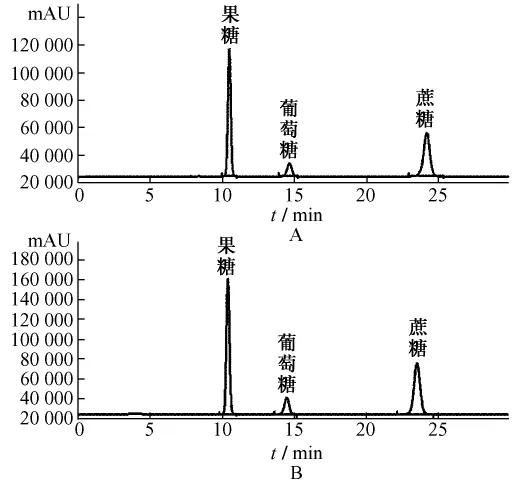
图1 冠心宁注射液单糖、寡糖测定对照品(A)和样品 (B)HPLC图Fig.1 HPLC chromatograms of reference substances(A)and Guanxinning Injection(B)
2.4 线性关系考察 精密吸取一定体积的上述各对照品溶液 (线性溶液①1、2、5、10、15、20、25、30 μL;线性溶液②1、2 μL)分别注入色谱仪,以进样量 (μg)的对数值 (lgW)为横坐标(X),以峰面积的对数值 (lgA)为纵坐标 (Y)进行线性回归,建立3种标准糖的线性回归方程,分别为:果糖 Y=1.707 1 X+8.707 8,r=0.999 6;葡萄糖 Y=1.762 9 X+7.323 2,r=0.999 7;蔗糖 Y=1.672 3 X+8.253 9,r=0.998 7。结果表明:果糖、葡萄糖、蔗糖分别在1.812 ~45.300 μg、1.354 ~ 101.538 μg、1.959 ~146.956 μg范围内呈良好的对数线性关系。
2.5 精密度考察 取同一份供试品溶液 (批号:091108),重复进样6次,记录峰面积,果糖、葡萄糖、蔗糖的RSD分别为0.2%、0.3%、0.2%,结果表明仪器精密度良好。
2.6 稳定性试验 取同一份供试品溶液 (批号:091108),分别在 0、4、8、12、16、21、26 h时注入色谱仪,记录果糖、葡萄糖、蔗糖峰面积,考察样品的稳定性,试验结果果糖、葡萄糖、蔗糖的RSD分别为0.1%、0.2%、0.2%,表明被测溶液在26 h内稳定。
2.7 重复性试验 按供试品溶液制备方法,取同一批样品 (批号091108)共6份,注入液相色谱仪,依法测定。结果表明,冠心宁注射液中果糖、葡萄糖、蔗糖及总糖质量浓度分别为32.584、24.225、35.140 mg/mL及91.949 mg/mL,其RSD分别为0.21%、0.37%、0.18%及0.23%。
2.8 准确度试验 取同一批样品 (批号091108)各1.0 mL,共9份,每3份为一个水平,分别精密加入对照品溶液③1.0、2.0、3.0 mL,按2.3项下制备供试品溶液并按上述色谱条件进行分析,计算回收率和RSD。结果表明,果糖、葡萄糖、蔗糖及总糖的平均回收率分别为105.9%、105.8%、105.3%及105.6%,RSD分别为3.5%、4.2%、3.5%及3.6%,回收率符合要求,结果见表2。
2.9 样品测定 按供试品溶液制备方法,取71批供试品溶液各5 μL,注入液相色谱仪,依法测定,结果见表3。
3 讨论
3.1 糖类物质是含多羟基的醛类或酮类化合物。糖类化合物包括单糖、单糖的聚合物及衍生物。以它们水解的情况分类,凡不能被水解成更小分子的糖为单糖,能水解成少数 (2~10个)单糖分子的为寡糖 (或低聚糖)。由于冠心宁注射液的制备工艺中有二次醇沉过程,药材中的多糖类成分均被醇沉,故仅对药材中的单糖寡糖进行分析。
3.2 查阅文献,目前各种单糖和寡糖的分析方法有薄层色谱法 (TLC)[5-7]、薄层色谱扫描法(TLCS)[7]、气相色谱法[8-9]、高效毛细管电泳法(HPCE)[10]、聚丙烯酰胺凝胶电泳法 (PAGE)[11]、和高效液相色谱法 (HPLC)[12-13]。本实验拟采用高效液相色谱法,由于糖类没有紫外吸收,故用高效液相色谱法测定糖类化合物多采用HPLC-RID、HPLC-ELSD和衍生化,为使方法简单、可行,本实验采用ELSD-HPLC法对糖类成分进行分析。
3.3 收集多个单糖、寡糖对照品,采用对照品对照法,通过保留时间比较,确证了色谱图中3个主要色谱峰,分别为果糖、葡萄糖、蔗糖。
3.4 通过对6个不同企业抽验的71批样品进行果糖、葡萄糖、蔗糖3种糖的测定,分析3种糖质量浓度可知,6个厂家的冠心宁注射液中均含有果糖、葡萄糖和蔗糖,但从数据可见F厂家的冠心宁注射液中蔗糖的质量浓度极低,为1.943~5.306 mg/mL,B厂家的冠心宁注射液中的葡萄糖质量浓度相对较低,为6.209~18.897 mg/mL。

表2 冠心宁注射液中单糖、寡糖准确度试验结果 (n=9)Tab.2 Results of recovery tests of Guanxinning Injection(n=9)
3.5 结合总固体物测定结果进行分析,3种糖总量占总固体比例为38.0%~90.9%,A厂家糖总量占总固体比例为42.0%~74.9%、B厂家糖总量占总固体比例为43.9%~58.8%、C厂家糖总量占总固体比例为38.0%~54.3%、D厂家糖总量占总固体比例为38.0%~90.9%、E厂家糖总量占总固体比例为48.5%~53.5%、F厂家糖总量占总固体比例为50.0%~77.0%。其中A厂家糖总量占总固体比例相对偏高,糖总量占总固体60%以上的占72.7%,C厂家和E厂家糖总量占总固体比例相对偏低。
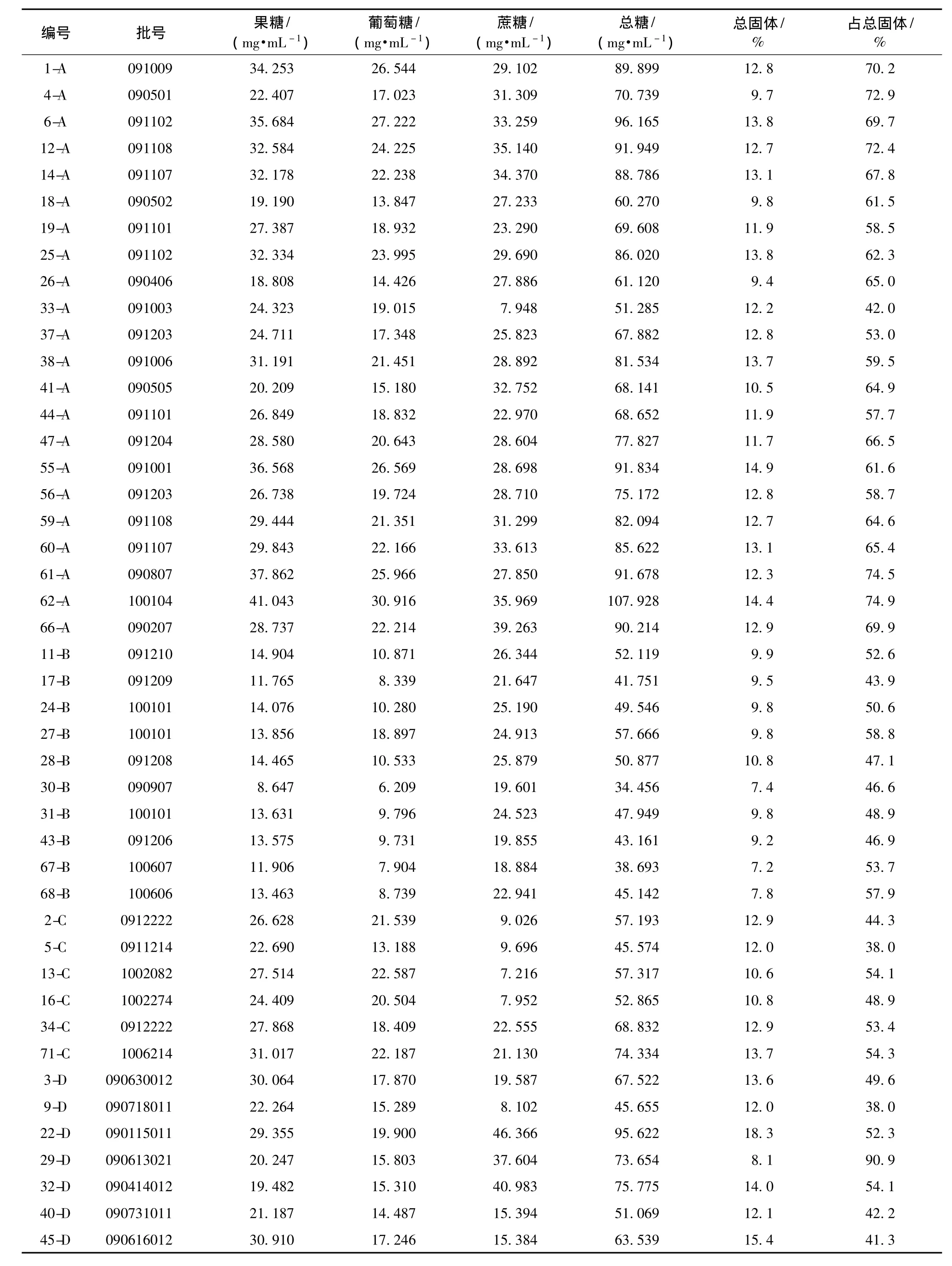
表3 冠心宁注射液中单糖、寡糖测定结果 (n=2)Tab.3 Result of content determination of samples(n=2)
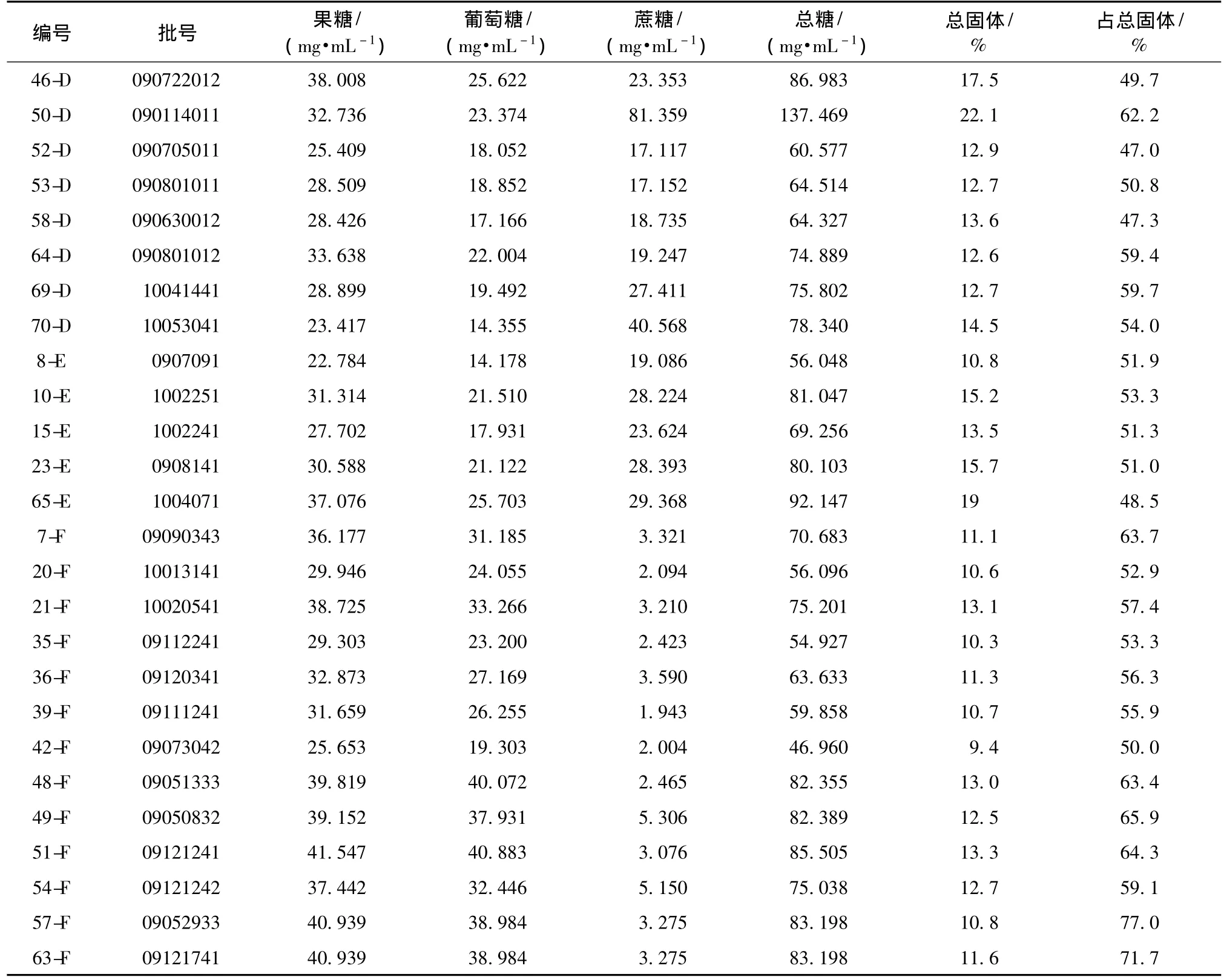
续表3
[1]卫生部药品标准中药成方制剂(第17册)[S].1998:174.
[2]李秋怡,干国平,刘焱文.川芎的化学成分及药理研究进展[J].时珍国医国药,2006,17(7):1298-1299.
[3]蒋爱军,朱 斌,王钢力,等.注射用丹参(冻干)中糖和糖醇类成分的定性定量分析[J].药物分析杂志,2011,31(7):1313-1316.
[4]孙晓春,颜 军,何 钢,等.川芎多糖的分离纯化及其单糖组成测定[J].四川农业大学学报,2011,29(1):56-60.
[5]张真庆,于广利,管华诗,等.几种糖醛酸及其寡糖的薄层层析分析[J].分析化学,2005,33(12):1750-1752.
[6]焦广玲,于广利,赵 峡.几种寡糖和单糖在不同展开体系中的薄层色谱行为[J].中国生化药物杂志,2007,28(6):372-374.
[7]沈德艳,郁建平,张训海,等.几种单糖、寡糖TLC条件的确立及草石蚕寡糖中水苏糖含量测定[J].食品工业科技,2009(9):306-308,310.
[8]周 欣,王庆彪,刘锡均,等.气相色谱法检测葡萄糖、麦芽糖、果糖和葡萄糖[J].海峡药学,2001(4):48-49.
[9]罗晓清,杨化新,杨洪淼,等.尖吻蝮蛇降纤酶寡糖链的甲基化分析[J].药物分析杂志,2010,30(3):357-360.
[10]贾国惠.糖类的高效毛细管电泳分析[J].中国医院药学杂志,2003,23(8):492-493.
[11]于广利,迟连利,李桂玲,等.PAGE在海洋酸性寡糖分析中的应用[J].中国海洋药物,2001,20(3):7-11.
[12]赵仁邦,刘孟军,葛 微,等.高效液相色谱法测定枣中的糖类物质[J].食品科学,2004,25(8):138-141.
[13]郑小迅,李 泽,杜嘉木,等.高效液相色谱法测定寡糖链结构[J].分析化学,2005(3):291-295.
