检测可溶性TREM-1的 ELISA法的建立及初步应用①
2012-01-23何绮霞蔡树云姚业兴徐军发张良清广东医学院附属医院麻醉科湛江524001
卢 燕 何绮霞 蔡树云 姚业兴 徐军发 张良清 (广东医学院附属医院麻醉科,湛江524001)
髓样细胞触发受体-1(Triggering receptor expressed on myeloid cells-1,TREM-1)是在髓样细胞上表达的免疫球蛋白家族成员[1],是一种在炎症反应的触发及放大过程中具有重要作用的蛋白,选择表达于髓样细胞(如单核/巨噬细胞、中性粒细胞)表面,可放大促炎性细胞因子的释放。TREM受体家族现已确认的成员有6个,其中TREM-1是该受体家族最具特征性的一员。TREM-1的基因位于人类6号染色体(6p 21.1)与 MHC区域相邻[2],其相对分子质量约为26×103,含234个氨基酸,氨基酸序列开始于一个疏水性的信号缩氨酸,胞外区由一个单独的免疫球蛋白V区结构域构成,约194个氨基酸,跨膜区包括一个带正电的赖氨酸残基,有29个氨基酸,胞质区仅由几个氨基酸组成。TREM-1结合糖基后分子量为30 kD,未结合糖基为26 kD,感染早期还可以可溶性形式sTREM-1释放进入体液,而且sTREM-1与感染严重程度有较好的相关性,提示sTREM-1是一种早期诊断感染的新指标,为了进一步研究TREM-1在急性肺部感染发生发展中的作用,本研究建立了一种检测 sTREM-1的 ELISA方法。
1 材料与方法
1.1材料 酶联微量反应板,来源于cloning公司。鼠抗人TREM-1单克隆抗体(mAb),购自Invitrogen公司;纯化的人TREM-1蛋白和兔抗人TREM-1多克隆抗体由本室自制。HRP标记羊抗兔IgG,购自北京博奥森生物技术有限公司,TMB底物及显色剂,沈阳惠民公司产品。BIOTEK Elx800型酶标仪等。
1.2方法
1.2.1酶标抗体工作浓度的选择 采用夹心ELISA法,用PBS将兔抗人TREM-1多抗稀释为100 μg/L,每孔 100 μl包被于酶标板,4℃过夜,加洗涤液洗板5次,加入封闭液37℃孵育2小时,再洗板5次,将羊抗兔酶标抗体进行一系列稀释(1∶2 000、1∶3 000、1∶4 000、1∶5 000、1∶6 000),37℃孵育 1 小时,洗板5次,加底物显色,选取A450值为1.0时的酶标抗体浓度为工作浓度。
1.2.2抗原抗体工作浓度的选择 采用棋盘方阵滴定法确定单抗最佳包被稀释度和多抗的最适工作浓度,具体方法如下:以pH9.6的碳酸盐缓冲液(包被液)将鼠抗人TREM-1单克隆抗体(1 mg/ml)分别稀释为 1∶2 000、1∶3 000、1∶4 000,分别在 ELISA板上进行包被,每一浓度包被9个孔,4℃过夜。次日洗涤后封闭液封闭2小时,再洗涤,在三个纵行各包被孔中加入强阳性抗原液(50 μg/ml TREM-1蛋白),另三纵行加入弱阳性抗原液(5 μg/ml TREM-1蛋白),剩余三纵行加入PBS作为阴性对照,37℃温育1小时。洗涤后加入兔抗人TREM-1多抗,稀释倍数分别为1∶1 000、1∶2 000、1∶3 000,分别加入每一抗原浓度9个孔,37℃温育1小时,洗涤,每孔加入本节1.2.1中确定的HRP标记羊抗兔IgG工作浓度,37℃温育1小时,洗涤,加底物显色,加酸终止反应后测A450值,选择强阳性抗原液的A值在1.0左右,阴性参考的A值小于0.1的条件作为最佳单抗包被和多抗最适工作浓度。
1.2.3封闭液和封闭时间的选择 用最佳的鼠抗人TREM-1单抗包被稀释度和包被条件包被酶标板,4℃包被过夜,洗涤后分成 3组。第1组:用10%FCS封闭;第2组:用1%BSA封闭;第3组:用5%BSA 封闭;200 μl/孔,37℃ 孵育 2小时。按照ELISA基本步骤检测阴、阳性样品,取OD值接近1.0且P/N值最大的一组为确定的最佳封闭液。
用单抗最佳的包被稀释度和包被条件包被酶标板,4℃包被过夜,洗涤后加入选定的封闭液,200 μl/孔,分成4组,第1组:37℃封闭4小时;第2组:37℃封闭2小时;第3组:4℃过夜;第4组:37℃封闭2小时后过夜。按照ELISA基本步骤检测阴、阳性样品OD值,取OD值接近1.0且P/N值最大的一组为确定最佳封闭时间。
1.2.4测定范围的选择 按以上优化的实验最佳条件,将重组人 TREM-1蛋白(200 mg/ml)做1∶500稀释后再进一步做二倍稀释,如 1∶1 000、1∶2 000、1∶4 000、1∶8 000,直到 1∶256 000 进行测定,以抗原浓度为横坐标,A450为纵坐标,绘制标准曲线,确定检测范围及最小检出浓度。
1.2.5重复性检测 (1)批内重复试验:在同一批内对50 μg/L纯化重组人TREM-1蛋白进行20次平行检测,测其A450,计算CV值。(2)批间重复试验:分5次检测50 μg/L纯化重组人TREM-1蛋白,每次设置4个重复孔,测其A450,计算CV值。
1.2.6TREM-1含量的检测 按实验1.2.3最佳优化条件,按夹心ELISA法基本步骤测定30例急性肺部感染患者和30例健康体检正常人的A450值,再根据实验1.2.5测定得到的标准曲线算出它们的各自值,采用±s表示,组间比较采用t检验,以P<0.05为差异有统计学意义,采用 SPSS16.0软件分析。
2 结果
2.1双抗体夹心ELISA检测方法最佳反应条件的确定
2.1.1酶标抗体最佳工作浓度的确定 选取A450值接近1.0时的酶标抗体浓度为工作浓度,从(表1)可以看到二抗比例为1∶5 000时吸光度值为0.991,最接近1.0,因此确定酶标抗体最佳工作浓度为1∶5 000。
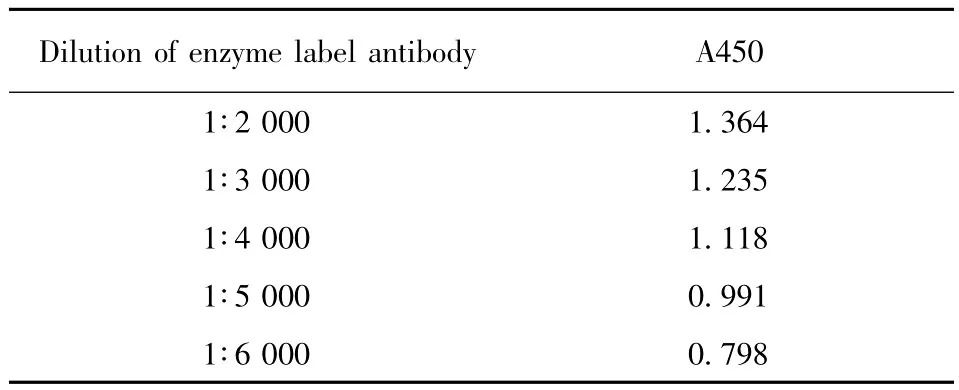
表1 不同浓度酶标二抗A450值Tab.1 The absorbance about different percentage of enzyme label antibody
2.1.2鼠抗人TREM-1包被单抗和兔抗人TREM-1多抗最适工作浓度的确定 根据棋盘法测定的结果(表2),取OD值接近于1.0,P/N值最大的工作浓度为最佳浓度,由表中可以看到包被单抗浓度为1∶3 000和多抗浓度为 1∶2 000时,其 A450值为0.993,接近1.0,阴性对照A450值低于0.1。因此,确定包被的鼠抗人TREM-1包被单抗工作浓度为1∶3 000,兔抗人 TREM-1多抗最适工作浓度为1∶2 000。

表2 棋盘法比色结果Tab.2 Result of checherboard method

图1 不同封闭液检测结果Fig.1 The result of different block buffer

图2 不同封闭时间检测结果Fig.2 The result of different block time
2.1.3封闭液及封闭时间的选择 从不同封闭液检测结果(图1)可见10%FCS的封闭效果OD值最接近1.0,P/N值最大,所以采用10%FCS作为本实验的封闭液。不同封闭时间结果(图2)显示37℃ 2小时和4℃过夜方法相比无明显区别,为节省实验时间采用37℃ 2小时。

图3 双抗体夹心ELISA法检测TREM-1工作曲线Fig.3 Standard curve of TREM-1 by sandwich ELISA
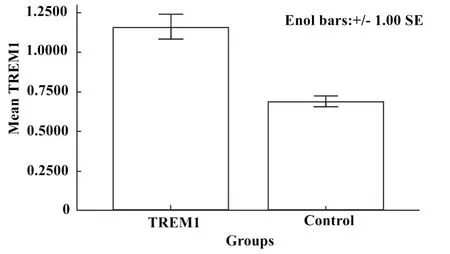
图4 急性肺部感染组与对照组TREM-1浓度柱状图Fig.4 The concentration of TREM-1 between patient with acute lung infection and the control group
2.2测定范围的确定 结果显示0.78~200 μg/L范围线性较好,以这段结果绘制标准曲线(图3),回归方程为y=0.006 4x+0.184 8,R2=0.993 3。当抗原稀释到1∶128 000时已经检测不出,因此此方法最低检出限为0.78 μg/L。
2.3重复性试验 批内重复性试验和批间重复性试验的变异系数分别为6.52%和9.46%,说明该方法重复性和稳定性都较好。
2.4TREM-1检测结果统计分析 根据TREM-1标准曲线直线回归方程代入各样本OD值,计算出它们各自浓度,采用SPSS16.0软件统计分析,采用±s表示;急性肺部感染组:(1.16±0.42)μg/L;对照组为:(0.69±0.18)μg/L,两者比较差异有统计学意义(P<0.001,图4)。
3 讨论
TREM-1是2000年Bouchon首先发现的一种新的免疫球蛋白超家族受体,选择性表达于血液中的中性粒细胞和单核细胞表面,能触发及扩大细菌感染后细胞因子的级联反应并进一步影响脓毒性休克的病理过程,因此被认为可能在炎性反应的触发及放大过程中具有重要作用[3]。TREM-1可溶性形式sTREM-1是TREM-1的mRNA剪接突变体编码的一种缺乏跨膜结构域的分泌亚型[4],研究发现肺部感染过程中sTREM-1可以释放入体液且与感染严重程度密切相关,可用于评价疗效和评估预后[5]。Tejera等[6]对226例社区获得性肺炎(Community acquired pneumonia,CAP)患者血清 sTREM-1水平检测发现,sTREM-1水平是CAP独立诊断和预测指标,与患者死亡率密切相关,而且其预测价值独立于此前已经确认的CAP预测指标,提示sTREM-1是急性肺炎患者特殊的预测标志物。我们前期研究制备了纯化的人TREM-1蛋白和兔抗人TREM-1多克隆抗体[7]。因此建立一个快速简便的检测方法可为TREM-1的基础和临床应用研究都具有积极的意义。
本实验以鼠抗人TREM-1单抗作为包被抗体,以兔抗人TREM-1多抗作为夹心抗体,建立了定量检测TREM-1的夹心ELISA方法,经过条件优化最终选择1∶3 000抗人TREM-1单抗包被,4℃包被过夜,10%FCS封闭2小时,1∶2 000的多抗为捕获多抗,1∶5 000的HRP标记二抗,各步骤采用洗涤液洗3分钟×5次,显色10分钟,A450测吸光度值,结果批内和批间CV值分别为6.52%和9.46%,说明实验的重复性和稳定性均可。线性分析结果本实验最低检测含量为0.78 μg/L,R2为0.993 3说明相关性尚好,截距为0.184 8,大于0,说明该方法仍存在一定的系统误差。实验中采用鼠抗人TREM-1单克隆抗体作为包被抗体,而二抗采用羊抗兔IgG多抗,理论上不产生交叉反应,但实验证实了单抗与多抗之间有少量交叉反应的结合,这可能是导致本实验阴性对照的吸光度值较高、重复性试验的CV值较高的原因。
我们利用建立的标准曲线对30例急性肺部感染患者和30例正常健康体检者血清sTREM-1含量进行检测,结果显示:急性肺部感染组sTREM-1含量为(1.16±0.42)μg/L;而对照组为(0.69±0.18)μg/L,证明了急性肺部感染患者血清中TREM-1表达增加,与对照组比较有统计学意义。该方法的建立为以后对TREM-1与急性肺部感染关系的研究奠定基础,特别是可望研制出商品化的ELISA试剂盒,使sTREM-1的检测在早期诊断急性肺部感染中得到广泛的应用。
1 Bouchon A,Dietrich J,Colonna M.Cutting edge:inflammatory responses can be triggered by TREM-1,a novel receptor expressed on neutrophils and monocytes[J].Immunol,2000;164(10):4991-4995.
2 Allcock R J,Barrow A D,Forbes S et al.The human TREM gene cluster at 6p21.1 encodes both activating and inhibitory single IgV domain receptors and includes NKp44[J].Eurr Immuno1,2003;33(2):567-577.
3 Nathan C,Ding A.TREM-1:a new regulator of innate immunity in sepsis syndrome[J].Nat Med,2001;7(5):530-532.
4 Mahdy A M,Lowes D A,Galley H F et al.Production of soluble triggering receptor expressed on myeloid cells by lipopolysaccharide-stimulated human neutrophils involves de novo protein synthesis[J].Clin Vaccine Immunol,2006;13(4):492-495.
5 Chastre J,Luyt C E,Trouillet J L et al.New diagnostic and prognostic markers of ventilator-associated pneumonia[J].Curr Opin Crit Care,2006;12(5):446-451.
6 Tejera A,Santolaria F,Diez M L et al.Prognosis of community acquired pneumonia(CAP):value of triggering receptor expressed on myeloid cells-1(TREM-1)and other mediators of the inflammatory response[J].Cytokine,2007;38(3):117-23.
7 卢 燕,郑淑华,刘 伟 et al.人髓样细胞触发受体-1原核表达载体的构建和表达及多克隆抗体的制备[J].中华实验外科杂志,2011;28(9):1438-1440.
