赖诺普利关键中间体的合成研究
2012-01-14谢媛媛李坚军
宁 衡 谢媛媛 李坚军
(浙江工业大学 绿色制药技术与装备教育部重点实验室,浙江 杭州 310014)
0 前言
赖诺普利(Lisinopril)是由默克公司研制的第三代血管紧张素酶抑制剂(ACEI),其化学名为N-[N-[(S)-1-羧基-3-苯丙基]-L-赖氨酰]-L-脯氨酸二水合物,其商品名为Prinivil,于1987年12月29日在美国获FDA批准上市。由于具有起效快、疗效长、毒副作用少等优点,在临床上得到了广泛应用[1],成为高血压治疗的首选药物之一。
目前,国内外有关赖诺普利的合成路线主要是以3-苯甲酰丙烯酸乙酯(1)为起始原料,与三氟乙酰赖氨酸(2)在氢氧化锂的作用下,发生不对称加成反应,再经Pd/C氢化还原、环合、缩合、水解等反应过程制备得到[2]。此工艺具有步骤短、产率中等、加成反应选择性较低(75:25)等特点,为目前工业生产上采用的主要方法。
N2-(1-乙氧羰基-3-苯丙基)-N6-三氟乙酰基-L-赖氨酸(LA2)是合成赖诺普利的关键中间体,其化合物中手性氨基的构建方法有:(1)3-苯甲酰丙烯酸乙酯法[2-4],即采用保护的L-赖氨酸与3-苯甲酰丙烯酸乙酯发生1,4-Michael加成,再经氢化还原合成;(2)α-卤代-4-苯基丁酸乙酯法[5],α-卤代-4-苯基丁酸乙酯与取代氨基酸通过缩合反应合成;(3)2-羰基-4-苯基丁酸酯法[6],由保护的氨基跟2-羰基生成烯胺再加氢还原合成。以上三种方法还存在有毒有害试剂氰基硼氢化钠等的使用、选择性差、原料价格昂贵等问题。因此,开发一条简便、低成本及环境友好的新工艺路合成赖诺普利关键中间体LA2有较大的应用价值,环境和社会效益显著。
1 合成路线
由于在Michael加成反应过程中,会产生一个新的手性中心,这将直接影响到产品的收率及后续的分离过程,因此如何实现选择性加成反应是研究的重点。本工艺路线以3-苯甲酰丙烯酸乙酯(1)为起始原料,与三氟乙酰赖氨酸(2)在三氟甲磺酸三正丁胺盐的作用下,发生不对称加成反应,后经氢化还原得到LA2,实验方案如Scheme 1。
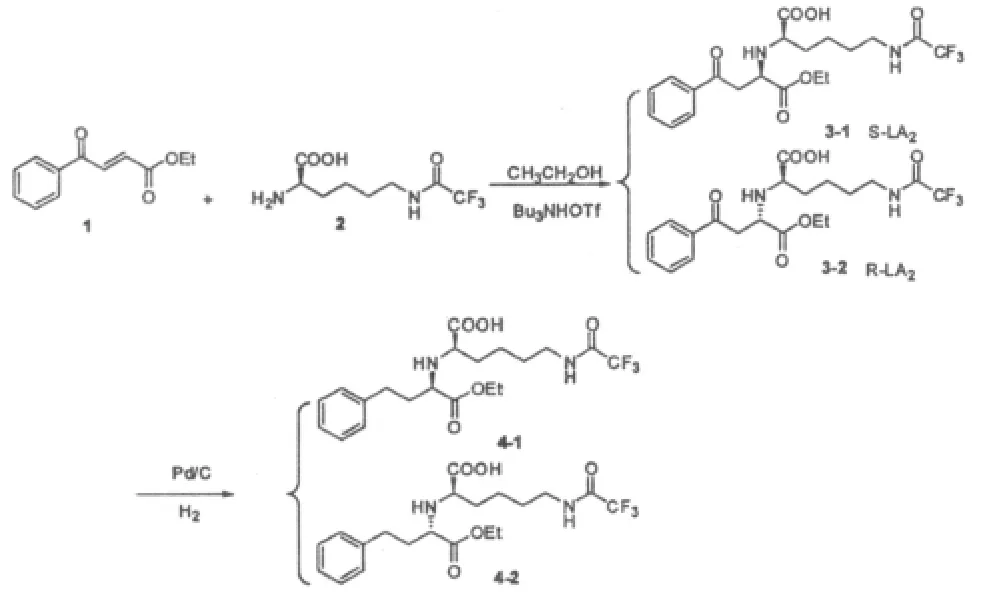
Scheme1 The synthesis of LA2in the presence of Bu3NHOTf
2 实验部分
2.1 仪器及试剂
实验仪器:DLSB-3006低温冷却液循环泵;DZF-6050真空干燥箱;Agilent 1100液相色谱仪。
实验试剂:3-苯甲酰丙烯酸乙酯(BZ),三氟乙酰赖氨酸(LA1)等试剂为化学纯或分析纯试剂,催化剂三氟甲磺酸三正丁胺盐自制。
2.2 LA2氢化物的合成
加成反应过程:在装有机械搅拌、温度计、恒压滴液漏斗的1000mL四口烧瓶中,加入三氟乙酰赖氨酸41.7g(0.172mol),3-苯甲酰丙烯酸乙酯38.6g(0.189mol),并加入400mL无水乙醇,将反应液冷却至-7℃,搅拌下加入三氟甲磺酸三正丁胺盐(5.77g,0.16mol),保温反应4h,TLC跟踪反应过程(CH2Cl2:CH3OH=10:1),反应结束后缓慢滴加5.0mL浓盐酸。减压浓缩回收乙醇,类白色固体以少量冷乙醇洗涤过滤,40℃真空干燥,得N2-(1-乙氧羰基-3-苯丙甲酰基)-N6-三氟乙酰基-L-赖氨酸55.9g,收率为67%,LA2加成物S-构型与R-构型达到84:16,含量为92%。
氢化反应过程:将上述的加成物55.9g与13.5g钯碳(含量为8%)混合加入到含400mL乙醇的高压氢化釜,控制温度在40℃,反应压力为0.2MPa,搅拌反应12h后结束反应,过滤回收钯碳。滤液加200mL水并使用适量的30%氢氧化钠溶液调节pH至4.5左右,保持真空条件浓缩回收乙醇。加100mL水洗后抽滤得到白色固体,50℃真空干燥,得N2-(1-乙氧羰基-3-苯丙基)-N6-三氟乙酰基-L-赖氨酸47.9g,收率58%,含量99%。
HPLC条件:流动相为0.25%磷酸二氢钾溶液与乙腈(体积比6:4),色谱柱:VP-ODS 5μm 150×6.0mm柱温:30℃流速:1.0mL/min检测波长:210nm进样量:20μL。
3 结果与讨论
加氢工艺已经较为成熟,进行较多尝试,没有明显的提高。故本文具体考察投料比,反应温度,催化剂对LA2加成物比例的影响。
3.1 催化剂对反应选择性的影响
在投料比确定的情况下,两种原料的摩尔比(LA1/BZ=1.00:1.00)时,考察不同催化剂对Michael加成反应收率及选择性的影响,反应结果如Table 1所示。
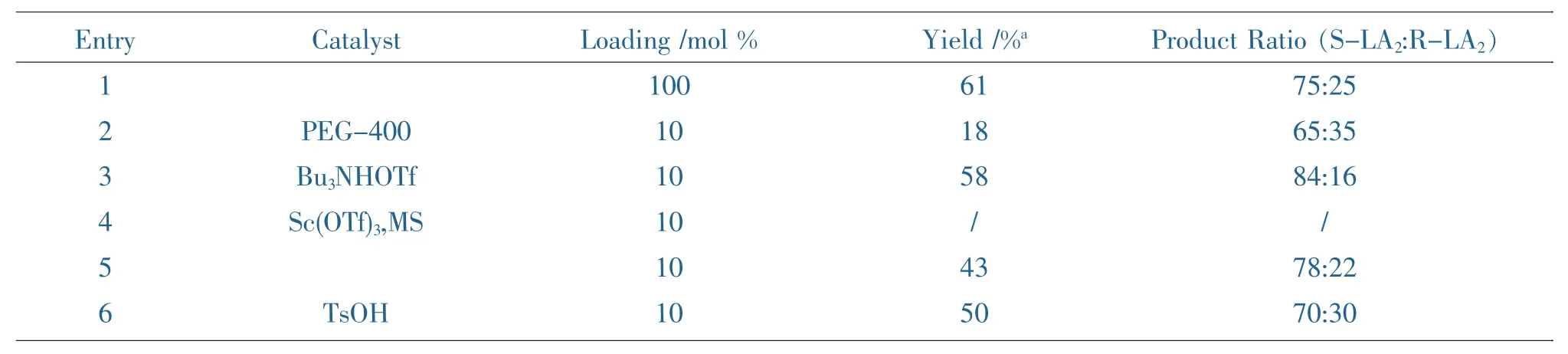
Table 1 The effect of catalyst on the selective of the addition compounds of LA2
理论上,发生Michael加成只需要少量的催化剂引导即可。使用氢氧化锂催化反应时,虽然收率更高一些,但氢氧化锂使用量大,选择性一般;当以三氟甲磺酸三正丁胺盐为催化剂时,由于该催化剂能有效与苯酯上羰基配位得到活化,在保持产品LA2中等收率的情况下,选择性相对较高。而以三氟甲磺酸钪为催化剂时将会造成加成后氢化过程Pd/C失活,最终确定以三氟甲磺酸三正丁胺盐来催化反应。
3.2 物料比对反应选择性的影响
物料比将对反应的有较大的影响,考察不同的物料比对反应结果的影响,如Table 2所示。
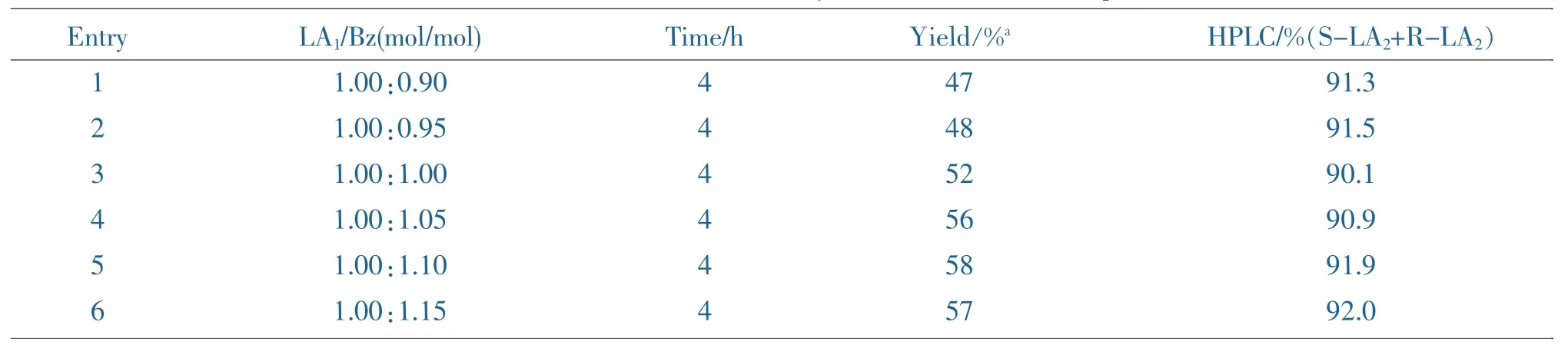
Table 2 The effect of ratio of LA1/Bz on the yield of the addition compounds of LA2
实验发现,3-苯甲酰丙烯酸乙酯随反应进行有部分水解,因此当投料比LA1/BZ大于1时,反应不完全,收率低;当两者比例为1.00:1.10时,收率和纯度较好,再提高3-苯甲酰丙烯酸乙酯的比例,对反应影响不大。综合化学平衡和原料的成本,3-苯甲酰丙烯酸乙酯过量10%是较优的选择,如表2所示,两种原料的摩尔比为1.00:1.10时,产品的纯度和收率较佳。
3.3 温度及反应时间对反应的影响
因为迈克尔加成是一个竞争性反应,温度对反应影响较为明显。考察温度和反应时间对加成物中的影响。

Table 3 The effect of Temperature and Time on the yield of the addition compounds of LA2
从热力学角度考虑,温度高对反应有利,反应速度快,但是温度高会破坏产物的结构,造成乙酯基团的水解;从动力学角度考虑,低温对选择性的提高有利,选择性好收率高,但反应时间要相应延长,故综合考虑在-7℃时反应4h为较优的条件。
4 结论
本文探索了一条制备赖诺普利中间体的新工艺,以3-苯甲酰丙烯酸乙酯(BZ)和三氟乙酰赖氨酸(LA1)为原料,在催化剂作用下,发生迈克尔反应,再经氢化还原合成N2-(1-乙氧羰基-3-苯丙基)-N6-三氟乙酰基-L-赖氨酸(LA2),收率为38.8%,加成过程中立体选择性可达到84:16。其中加成反应过程较佳的工艺条件为LA1:BZ的摩尔比为1.00:1.10,三氟甲磺酸三正丁胺作催化剂,反应温度-7℃,反应时间4h。该工艺加成反应的选择性高,且操作简便,原料利用率好,成本低,具有潜在应用前景。
[1]杨逸卫.赖诺普利的临床应用进展[J].世界临床药物,2003,(10):629-633.
[2]Kumar R,Sharma R,Bairwa K,et al.Modern development in ACE inhibitors[J].Der Pharmacia Lettre,2010,2(3):388-419.
[3]Yu L T,Huang J L,Chang C Y,et al.Formal Synthesisofthe ACE InhibitorBenazepril·HClvia an Asymmetric Aza-Michael Reaction[J].Molecules 2006,(11):641-648.
[4]Himeji Y U,Matsumoto A,Manabe H.Process for the preparation of 1-alkoxycarbonyl-3-phenylpropyl derivatives:US,6118010[P].2000-12-12.
[5]Blacklock T J,Shuman R F,Butcher J W,et al.Synthesis of semisynthetic dipeptides using N-carboxyanhydrides and chiral induction on Raney Nickel.A method practical for large scale[J].J.Org.Chem.1988,53:836-844.
[6]马大为,邓平.赖诺普利类化合物的前体及其合成方法:CN,1539826[P].2004-10-27.
[7]Keller E,Feringa B L.Ytterbium triflate catalyzed Michael additions of β-ketoesters in water[J].Tetrahedron Lett,1996,37:1879-1882.
