杭州湾北岸近岸海域N、P降解系数的围隔实验研究
2012-01-12程金平朱惠琴赵文昌
席 磊, 程金平, 程 芳,2, 朱惠琴,3, 邵 悦,2, 王 茜, 赵文昌
(1. 上海交通大学 环境科学与工程学院, 上海 200240; 2. 上海师范大学 生命与环境科学学院, 上海200234; 3. 国家海洋局 东海分局, 上海 200137)
杭州湾北岸近岸海域N、P降解系数的围隔实验研究
席 磊1, 程金平1, 程 芳1,2, 朱惠琴1,3, 邵 悦1,2, 王 茜1, 赵文昌1
(1. 上海交通大学 环境科学与工程学院, 上海 200240; 2. 上海师范大学 生命与环境科学学院, 上海200234; 3. 国家海洋局 东海分局, 上海 200137)
通过制作生态系围隔实验装置, 采用模拟围隔实验的方法, 测定N、P营养盐的降解系数。基于夏秋两季杭州湾北岸近岸海域的现场水样采集, 测出杭州湾北岸近岸海域无机氮的生物降解系数在0.121~0.269 d-1范围内, 均值为0.225 d-1, 测得活性磷酸盐的降解系数在0.031~0.179 d-1, 均值为0.08 d-1。考虑到实验室静态模拟环境与真实海区状况的差异, 采用保守估计法和 Bosko公式进行处理, 最终计算得出的0.21 d-1和0.05 d-1可分别作为杭州湾北岸海域无机氮和活性磷酸盐的实际降解系数。
杭州湾; 降解系数; 围隔生态系实验; 模拟
杭州湾北岸是上海经济发展战略的重点地区。随着经济的迅猛发展和近岸资源的利用, 近岸水域环境正遭受严重污染, 尤其是上海化学工业园区和上海石化总厂的落成与投入使用, 更加速了该海域环境质量的恶化。据多年的研究成果可知, 无机氮和活性磷酸盐是影响杭州湾北岸海域环境质量的主要污染物[1]。因此, 要想有效控制污染, 实现近岸海域水质的改善, 较为科学的方法就是建立描述N、P等营养元素降解规律的水质模型, 估算其水环境容量,进而实行杭州湾北岸海域营养盐的总量控制规划。其中, 最为前提和根本的就是确定该海域的营养盐降解系数, 探索其水体自净能力。
水体自净能力是描述排入水体的污染物浓度在水体的流动过程中自然降低的现象, 其净化机制主要可分为物理净化、化学净化和生物净化等 3种类型[2]。海水中N、P的降解与沉积主要依赖于海洋生物的氧化分解作用[3]。目前, 国内外关于海水中N、P等营养元素降解系数研究的报道较少, 且多数基于现实条件的考虑偏向于采用实验室模拟的方法。季民等[4]通过实验室模拟的方法测定了不同环境条件下排海污水有机物生化降解动力学系数, 并建立了系数估算方程式; Gbariel M[5]、Gunnar E[6]等用实验分析的方法研究了沉积物对N、P的吸附与解析规律; 郭栋鹏[3]针对南通市尾水海洋处置工程系统设计和研究的需要, 定量化地研究了 COD、TN和 TP的动力学过程, 并得出不同条件下TN和TP均符合一级反应动力学模型; 王晓丽[7]、赵永志[8]等的研究也表明水中 TN、TP的降解符合一级动力学规律。营养盐降解系数的估算有多种方法[9], 如经验公式估算、现场实测、室内模拟实验测定等。而陆贤崑[10]等借用海洋生态系围隔实验[11]的方法研究汞在围隔生态系内的排除过程, 最值得借鉴。王修林等[12]据此方法对胶州湾溶解有机态营养盐的微生物降解速率常数进行测定, 并测得0℃时DON和DOP的微生物降解速率常数分别为 0.01d–1和 0.035d–1。
本研究在现有条件的基础上, 借用海上围隔生态系实验具有的时间连续性和能够较好保持目标海域实际情况的优点[13], 采用实验室模拟围隔生态系实验的方法, 测定杭州湾北岸海域无机氮和活性磷酸盐的生物降解系数, 期望能为近岸海域水环境容量的估算和污染物总量控制的研究提供参考。
1 实验设计
1.1 研究区域
针对杭州湾北岸近岸海域, 分别于2010年11月(秋季)和 2011年 5月(夏季), 选取 4个采样点(分别位于金山石化、金山嘴、漕泾镇和上海化学工业区的附近海域)进行现场海水采集, 均采集表层海水,避光保存, 带回实验室进行模拟围隔实验研究。具体采样位置见图1所示。
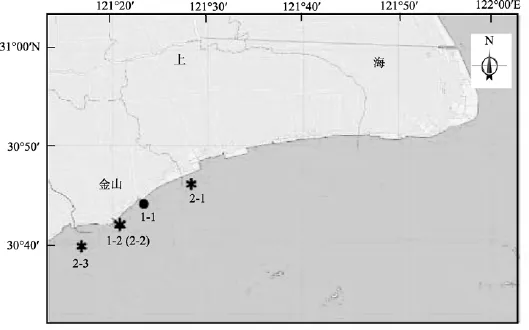
图1 围隔采样点Fig. 1 Enclosure sampling points
该海域N、P污染较为严重, 均超过二类水质标准, 水质交换能力较强, 金山断面潮流平均流速达1.51m/s[14], 海水温度最低为6℃, 最高达到29℃, 年均表层水温16.8℃, 表层盐度6~25。
1.2 实验原理及方法
营养盐在自然水体中易于被微生物降解, 围隔实验装置可模拟现场海水的生态结构与演变系数,间接测定海水中N、P浓度随时间的变化率, 即为其降解系数。本实验采用实验室模拟海上围隔生态系实验的方法来测定海水中N、P的降解系数。
N、P的降解过程基本符合一级反应动力学模式,降解系数方程为:

式中,C0为初始浓度, mg/L;C为t时刻浓度,mg/L;t为反应时间, d;kc为降解系数常数, d-1。
将其线性化, 转化为线性方程为(3), 利用最小二乘法作线性回归即可求得kc的值。
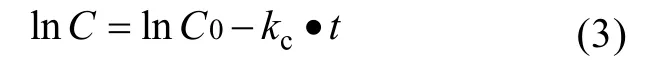
微生物对环境条件的变化是较为敏感的, 温度、水中溶解氧和 pH等的不同都可能导致降解系数的变化, 因此, 实验采用模拟围隔的方法, 尽可能严格控制温度、水中溶解氧和pH等条件, 使得模拟环境与实际海洋环境尽可能的吻合。
1.3 围隔实验装置

图2 围隔实验装置结构图Fig. 2 Enclosure experiment device
围隔实验装置(图2), 由钢骨架支撑的透明聚乙烯材料塑料袋(直径为0.6 m, 深度为0.8 m)及外部为钢质支架与帆布袋构成的循环水槽。实验在封闭的可控实验室内进行, 期间利用循环水保持整个帆布袋内水温的基本一致(实验温度由空调调控)。实验开始时, 将采集到的现场海水加入到一个大型容器内(滤掉浮游动物), 再分别分配各个围隔袋内, 以确保该组围隔袋的初始状态基本一致。实验共设 6个围隔袋, 分为空白组和对照组, 空白组编号分别为M1、M2和 M3, 未添加营养盐; 对照组编号分别为M4、M5和M6, 均加入一定量的硝酸钾和磷酸二氢钾, 使得对照组中 N、P的浓度为空白组浓度的 10倍左右。
2 模拟围隔实验
2.1 水样采集
实验开始时, 从各围隔袋中采集的水样用 GF/F膜(0.45 μm玻璃纤维滤膜, 使用前450℃灼烧5 h)过滤后贮存于250mL聚乙烯瓶中, 并添加0.5%的氯仿冰箱保存。活性磷酸盐水样, 每隔12 h采集1次, 共采集 8次, 采集时间依次为, 0、12、24、36、48、72、96、120 h; 无机氮水样, 每隔3 h采集1次, 共采集8次, 采样时间依次为0、3、6、9、12、24、36、48 h, 水样依次标记为M1、M2、M3、M4、M5、M6、M7和 M8。为防止实验过程中悬浮物质沉淀, 可不断进行搅拌, 保持水中微小颗粒的悬浮状态, 并起到大气富氧的作用。
2.2 水样测定方法
对采集水样, 按《海洋监测规范》(GBl7378-2007)中规定的方法测定 NO3-N、NO2-N、NH4-N、PO4-P的含量, 测定方法分别为锌-镉还原法、萘乙二胺分光光度法、次溴酸盐氧化法及磷钼蓝分光光度法。
2.3 数据处理
2.3.1 活性磷酸盐降解系数
将实验测得的活性磷酸盐浓度值转化为对数值,作为纵坐标, 以采样时间(0、0.5、1.0、1.5、2.0、3.0、4.0和5.0 d)为横坐标, 作线性回归分析, 见图3。
2.3.2 无机氮降解系数
将实验测得的无机氮(氨氮、亚硝态氮和硝态氮)浓度值转化为对数值, 作为纵坐标, 以采样时间(0、0.125、0.25、0.375、0.5、1.0、1.5和 2.0 d)为横坐标,作线性回归分析, 见图4。
2.4 结果
由上文给出的围隔实验结果, 可以看出, M1-M6号围隔袋中活性磷酸盐的降解系数值分别为0.105、0.031、0.069、0.179、0.059和 0.039 d–1, 均值为 0.08 d–1; M1-M6号围隔袋中无机氮降解系数值分别为0.234、0.233、0.226、0.121、0.265 和 0.269 d–1, 均值为0.225 d–1, 虽然各围隔袋中无机氮含量不同, 但48 h内的降解系数很是接近。
2.5 分析与讨论
(1)温度校正
一定温度范围内, N、P的降解系数kc与温度的关系可据Arrhenius 经验公式[15]表示为:

式中,kc为温度T时N、P的降解系数, d–1;k18为温度18℃时N、P的降解系数, d–1;θ为温度校正因子, 无量纲经验常数。基于杭州湾北岸近岸海域水温一般在6~29℃范围内, 可取θ为1.047。
(2)其他因素校正
kc值表示海水生物降解作用对N、P等营养元素的净化能力, 除了初始浓度和温度对kc值有影响外,海洋微生物的种类和数量、海面气体交换速度、近岸地质条件以及水动力因素等对kc值都有一定影响[4]。应用实验室的静态模拟结果估算真实海区的海水生物降解能力时, 一方面宜采用较保守数值, 即选择较低值。另一方面, 可根据近岸水体的水动力因素, 借用 Bosko得出的实验室测定值kT与实际水体降解系数kR之间的关系式对其进行修正[16]。Bosko公式为:
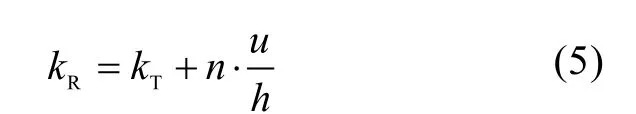
式中,kR表示实际水体的kc值;kT表示实验测得的kc值;u表示水体的流速(m/s);h表示平均水深(m);n表示与水流速度相关的系数, 一般取值为0.1。
依据实地监测数据和文献资料, 海水采集区域的平均水深约为10 m, 水体流速可取1.0 m/s[17]。基于保守考虑, 分别选择0.2 d–1和0.04 d–1作为本实验无机氮和活性磷酸盐的测定值, 因此依据公式 5计算得出, 杭州湾北岸海域无机氮和活性磷酸盐的实际降解系数分别为 0.21 d–1和 0.05 d–1。
(3)相关研究比较
目前, 关于N、P降解系数的研究报道并不多见。刘浩等[18]在研究辽东湾海域TP环境容量时, 取降解系数为0.01 d–1进行的模拟结果更接近实测值, 并且将无机氮视为保守物质; 朱虹[19]对无机氮和活性磷酸盐的降解转化系数进行实验室模拟研究时仅得出,活性磷酸盐的降解转化系数在 0.005 d–1~0.243 d–1范围内, 均值为0.062 d–1。在乐清湾环境容量模型[20]计算中, 考虑到乐清湾悬浮物浓度较高, 浮游植物对营养盐的吸收相对较慢, 取活性磷酸盐的降解系数为0.0075 d–1, 无机氮的降解系数为 0.005 d–1; 由于 N在海水中的存在形式多种多样, 而且三种主要无机氮(NO3-N、NO2-N、NH4-N)之间存在着硝化与反硝化的作用[21-22], 既可以相互转化又彼此制约,因此难以确定其降解系数, 多数将无机氮作为保守物质看待[20]。
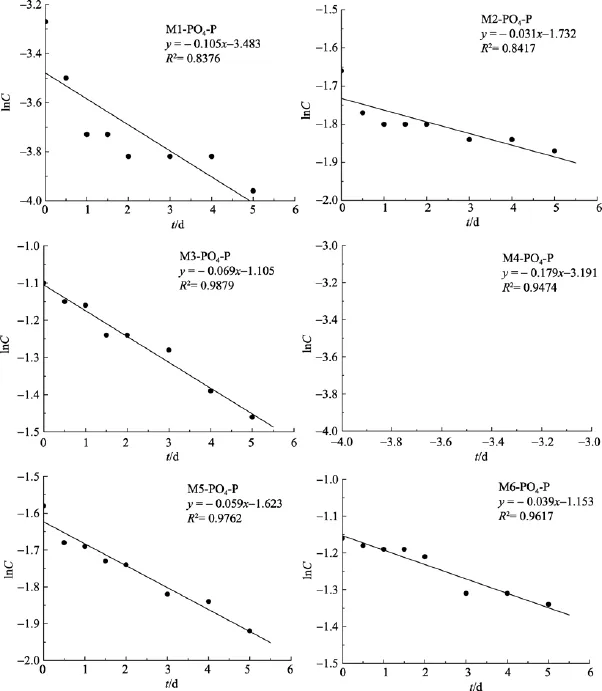
图3 活性磷酸盐降解曲线Fig. 3 Degradation curve of PO4-P
本文研究得出的N、P降解系数分别为0.21 d–1和 0.05 d–1, 虽然比前人的研究结果较为偏高, 但是考虑到杭州湾北岸海域环境开阔, 海洋水动力作用较强, 水体交换能力较好, 因而更为符合实际情况。另外该海域污染物排海量较大, 导致N、P等营养元素的初始浓度较高, 也是造成该海域营养盐降解系数较高的原因。
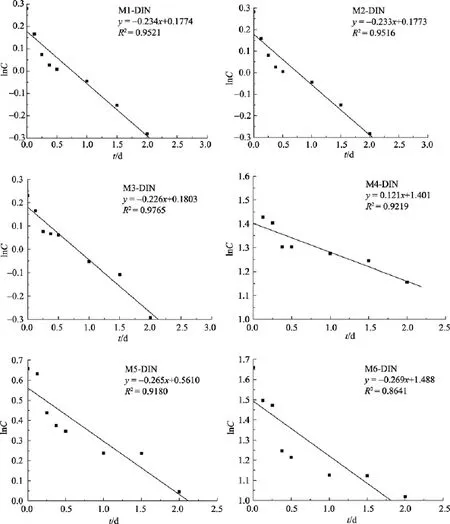
图4 无机氮降解曲线Fig. 4 Degradation curve of DIN
3 结论与展望
(1) 本文结合实验室模拟与海上围隔生态系实验的优点, 采用模拟围隔实验的方法测得无机氮的生物降解系数在 0.121~0.269 d–1范围内, 均值为0.225 d–1; 测得活性磷酸盐的降解系数在 0.0.031~0.179 d–1, 均值为 0.08 d–1, 与富国及刘浩等实验室测定值 0.01 d–1和 0.1d–1范围很接近。
(2) 两次实验温度均控制在 18℃左右, 可选取k18作为基准参照值, 依据 Arrhenius 经验公式对温度进行校正。
(3) 为消除实验室静态模拟结果与真实海区数值的差异, 本文采用保守估计法和 Bosko公式计算得出杭州湾北岸海域无机氮和活性磷酸盐的实际降解系数分别为 0.21 d–1和 0.05 d–1。
(4) 在人口膨胀压力、资源耗竭压力和环境污染压力直接冲击社会经济发展和人类生存的今天, 保护海洋环境, 充分发挥水体自净能力, 降低环境污染显得尤为重要, 本文尝试采用实验室模拟围隔生态系实验的方法对杭州湾北岸海域N、P的降解系数进行研究, 方法较为可行, 还有待于进一步的探讨和应用实践, 期望能为上海城市污水外排的规划决策提供参考。
[1]徐明德, 刘强. 杭州湾金山嘴海域水环境质量分析[J].科技情报开发与经济, 2006, 16(23):188-189.
[2]侯宇光, 杨龄真, 黄川友. 水环境保护[M]. 成都:成都科技大学出版社, 1990:29-30.
[3]郭栋鹏. 黄海南部海域排海尾水中污染物降解规律研究[D]. 太原:太原理工大学, 2006.
[4]季民, 孙志伟, 王泽良, 等. 污水排海有机物的生化降解动力学系数测定及水质模拟[J]. 中国给水排水,1999, 15(11):62-65.
[5]Gabriel M.Carbon and phosphorus cycling in anoxic sedments of the Saanich Inlet, British Columbia[J].Marine Geology(S0025-3227(00)00157-2), 2001, 74:307-321.
[6]Gunnar E, Carman R. Distribution and diagenesis of organic and inorganic phosphorus in sediments of the Baltic proper[J]. Elsevier Science, 2001, 45:1053-1061.
[7]王晓丽. 桑沟湾养殖水域颗粒态有机物迁移转化过程的研究[D]. 青岛:中国海洋大学, 2004.
[8]赵永志, 潘丽华, 古伟宏. 江水中有机氮降解规律的动力学研究[J]. 高师理科学刊, 1999, 19(3):55-57,85.
[9]蔚秀春. 河流中污染物综合降解系数的影响因素浅析[J]. 内蒙古水利, 2007, 110(2):116-117.
[10]陆贤崑. 海洋围隔生态系实验在海洋污染控制中的应用[J]. 环境科学, 1987, 8(4):78-83.
[11]Strickland J D H, Terhune L D B. The study of in situ marine photosynthesis using a large plastic bag. Limnol.Oceangr, 1961, 6:93-96.
[12]王修林, 李克强, 石晓勇, 著. 胶州湾主要化学污染物海洋环境容量[M]. 北京:科学出版社, 2006:170-173.
[13]Li Guanguo.Different Types of Ecosystem Experiments[A]//Lalli C M. Enclosed Experimental Marine Ecosystem:A Review and Recommendations. London:Springer-Verlag, 1990:7-19.
[14]谢世禄. 杭州湾北岸(上海段)岸滩保护和开发研究(续一)[J]. 围涂工程, 2000, 2:19-23.
[15]姚重华. 废水处理计量学导论[M]. 北京:化学工业出版社, 2002:122-125.
[16]傅国伟. 河流水质数学模型及其模拟计算[M]. 北京:中国环境科学出版社, 1987.
[17]茅志昌, 郭建强, 赵常青. 杭州湾北岸金汇潮滩冲淤分析[J]. 海洋湖沼通报, 2006, (4):9-16.
[18]刘浩, 尹宝树. 辽东湾氮、磷和 COD环境容量的数值计算[J]. 海洋通报, 2006, 25(2):46-54.
[19]朱虹. 杭州湾主要污染物降解转化模拟实验及其在环境容量计算研究中的应用[D]. 上海:上海海洋大学, 2010.
[20]黄秀清. 乐清湾海洋环境容量及污染物总量控制研究[M]. 北京:海洋出版社, 2011:259-262.
[21]Olson R J. 15N Tracer studies of the primary nitrite maximum[J]. Journal of Marine Research, 1981, 39(2):203-226.
[22]Olson R J. Differential photo-inhibition of marine nitrifying bacteria:a possible mechanism for the formation of the primary nitrite maximum[J]. Journal of Marine Research, 1981, 39(2):227-238.
Ecosystem enclosure experiments on degradation coefficient of N and P in the North Off-shore of Hangzhou Bay
XI Lei1, CHENG Jin-ping1, CHENG Fang1,2, ZHU Hui-qin1,3, SHAO Yue1,2,WANG Qian1, ZHAO Wen-chang1
(1. School of Environmental Science and Engineering, Shanghai Jiaotong University, Shanghai 200240, China; 2.College of Life and Environmental Sciences, Shanghai Normal University, Shanghai 200234, China; 3. East China Sea Branch of the State Oceanic Administration, Shanghai 200137, China)
Sep.,15,2011
Hangzhou Bay; degradation coefficient; ecosystem enclosure experiment; simulation
In this paper, the degradation coefficient of N and P was determined using simulation experiment method through setting up a ecosystem enclosure experiment device. Based on the field water samples obtained from the north Hangzhou bay in summer and autumn, the range of biodegradation coefficient of inorganic nitrogen was confirmed from 0.121 d–1to 0.269 d–1, mean 0.225 d–1, and for the activated phosphate, it was from 0.031 d–1to 0.179 d–1, mean 0.08 d–1. Considering the differences between laboratory simulation environment and real marine situation, the final actual degradation coefficient of inorganic nitrogen and activated phosphate, was calculated to be 0.21 d–1and 0.05 d–1respectively using conservative estimate method and Bosko formula.
P734.2 文献标识码:A 文章编号:1000-3096(2012)09-0032-07
2011-09-15;
2012-01-18
海洋公益性行业科研专项经费项目(200805065)
席磊(1986-), 男, 安徽蒙城人, 硕士研究生, 主要从事海洋化学和海洋生态方面的研究, E-mail:xiaoyao797@126.com; 程金平,通信作者, E-mail:jpcheng@sjtu.edu.cn
康亦兼)
