天然海水中微生物膜对碳钢腐蚀行为的影响
2012-01-12苏璐璐段继周侯保荣
赵 伟, 苏璐璐, 段继周 姜 江, 侯保荣
(1. 中国科学院 海洋研究所, 山东 青岛 266071; 2. 中国科学院 研究生院, 北京 100049; 3. 山东大学 材料学院, 山东 济南 250061)
天然海水中微生物膜对碳钢腐蚀行为的影响
赵 伟1,2, 苏璐璐1,3, 段继周1, 姜 江3, 侯保荣1
(1. 中国科学院 海洋研究所, 山东 青岛 266071; 2. 中国科学院 研究生院, 北京 100049; 3. 山东大学 材料学院, 山东 济南 250061)
通过对比碳钢在天然海水和灭菌海水中的腐蚀行为, 研究海洋微生物对碳钢材料的腐蚀行为的影响。结果表明, 海洋微生物可在碳钢表面形成微生物膜, 其对碳钢腐蚀速率的影响及作用机理与微生物的种类密切相关。在腐蚀初期, 海洋微生物膜对碳钢的腐蚀起到了抑制作用, 主要由多种好氧微生物协同作用的结果; 在腐蚀后期, 随着海洋微生物膜增厚导致厌氧腐蚀的出现从而加速腐蚀, 主要是硫酸盐还原菌等厌氧微生物的作用。
海水腐蚀; 电化学阻抗谱; 碳钢; 微生物膜
在海洋环境中, 微生物往往会附着于钢铁材料表面, 形成微生物膜。在微生物膜中微生物的种类、pH值、溶解氧、有机物和无机物的种类等相对于海洋本体环境发生了明显的改变。微生物膜内微生物的活性控制着腐蚀速率和类型, 这种由微生物膜内微生物的存在及其生命活动而引起的腐蚀称为微生物腐蚀[1-2]。微生物与金属间的相互作用主要包括微生物加速腐蚀及微生物抑制腐蚀两种[2-4]。
碳钢、低合金钢在海洋环境中广泛应用并且占据主导地位, 包括船体主结构、海上平台和沿海设施等,关于低碳钢海洋腐蚀的研究已有 60年的历史[5-6]。Melchers提出的海洋钢结构的腐蚀机理模型能解释典型的海洋碳钢腐蚀行为[7]。但是, 在这些实验中微生物的因素往往被忽略。目前国内外对海洋微生物腐蚀的作用及腐蚀机理已有一定的研究[8-12]。一些海洋微生物对腐蚀有显著影响并且被广泛关注, 如硫酸盐还原菌 (SRB) 和铁氧化细菌等[10,12-13]。但研究主要集中在单种微生物的腐蚀方面, 这很难说明多种细菌协同作用的结果, 并且关于海洋微生物对碳钢腐蚀的影响方面的研究还很少[14]。
本文采用了失重实验、电化学测试、微生物测试、扫描电镜和表面能谱等方法, 通过对比研究碳钢在天然和灭菌海水中的腐蚀行为, 以探究天然海水中微生物膜对碳钢腐蚀的影响。
1 材料与试验方法
1.1 实验材料和介质
实验材料为碳钢 Q235, 其成分如下:0.16C,0.53Mn, 0.30Si, <0.045P, <0.055S, 其余为 Fe。将材料加工成尺寸为 50 mm × 25 mm × 3 mm, 20 mm ×10 mm × 1 mm 和 10 mm × 10 mm × 1 mm 三种规格,按国标GB5776-86进行表面处理后保存在真空干燥器中。
实验分为天然海水和灭菌海水两种介质。模拟天然海水环境的实验装置为 800 mm × 500 mm ×600 mm的开放水缸。灭菌海水介质是采用天然海水在121 ℃的高温蒸汽灭菌锅中灭菌20 min。灭菌海水的实验装置为400 mm × 150 mm × 400 mm的封闭水缸, 采用空气泵始终通入经0.22 μm滤膜过滤后的空气。每天更换天然和灭菌海水一次。所有实验都是在室温下进行。天然海水取自青岛第一海水浴场, 净化海水的盐度 33.4~35.5, 溶解氧 5~7 mg/L, pH 7.8~8.1。经测定后, 灭菌海水的盐度、溶解氧浓度和 pH与天然海水差别不大, 可认为对实验结果影响不大。
1.2 失重实验和腐蚀表面分析
失重实验试样尺寸为50 mm × 25 mm × 3 mm。表面分析所用试样尺寸为20 mm × 10 mm × 1 mm。用SiC砂纸将工作面打磨至1200#, 用超声波在丙酮中清洗后, 自然干燥。
每组失重实验试样都选三组平行试样分别竖直悬挂于不同的海水介质中。灭菌海水中的试样实验前需采用紫外灯灭菌30 min。实验结束后, 试样按国标GB/T16545-1996去除腐蚀产物, 计算平均腐蚀速率。
将表面分析试样竖直悬挂于天然海水中。实验结束后, 将试样取出并用灭菌海水冲洗三次。对试样用 5 %戊二醛的溶液 (溶剂为灭菌海水) 浸泡 2 h,然后进行逐级脱水处理, 即用50 %、70 %、100 %乙醇 (溶剂为灭菌海水)分别浸泡15 min。自然干燥后,采用 JSM-6700F型扫描电子显微镜(SEM)和能谱仪(EDS)观察和分析腐蚀产物形貌和成分。
1.3 电化学实验
电化学实验所用试样尺寸为10 mm × 10 mm ×1 mm, 与铜导线焊接, 环氧树脂密封, 做成仅保留10 mm × 10 mm工作面的电极。实验之前, 电极均用SiC砂纸打磨至 1200#, 用去离子水清洗后用超声波在丙酮中清洗, 保存在真空干燥器中。灭菌海水中的电极实验前需采用紫外灯灭菌30 min。
采用 DDS 16/32动态信号测试系统 V 1.0 (Infotronix®北京世纪兴元科技发展有限责任公司) 记录电极随浸泡时间的开路电位变化, 每半个小时 1次。参比电极采用饱和甘汞电极 (SCE)。
电化学阻抗测试采用Parstat 2273电化学工作站(EG&G Princeton公司)。实验采用标准三电极体系,以SCE作为参比电极, 15 mm × 15 mm铂片电极作为对电极。电化学阻抗谱扫描频率范围为 100 kHz~10 mHz, 电压振幅为10 mV。用ZSimpWin Version 3.21电化学分析软件对实验结果进行分析。
1.4 微生物分析
取在天然海水中浸泡17 d的试样, 将锈层刮取下来, 接种到硫氧化细菌(SOB)培养基[15]和广泛培养基(LB)中。在37 ℃恒温摇床中培养两周之后, 逐级稀释涂布在固体培养基平板上培养。
当试样在天然海水中浸泡100 d之后, 取锈层接种于SRB培养基[13]中。在30 ℃恒温摇床中厌氧培养。SRB培养基需通入无菌N220 min, 同时加入少量经紫外线灭菌30 min的Fe粉。
三种培养基均用海水配制, 使用前需在 121 ℃的高温蒸汽灭菌锅中灭菌 30 min。所有细菌培养实验均在洁净工作台中进行。
2 结果与讨论
2.1 灭菌和天然海水中Q235钢失重实验
图1是Q235钢在灭菌和天然海水中不同浸泡时间的腐蚀速率对比。从图中可知, 灭菌海水中 Q235钢腐蚀速率开始逐渐变大, 后期又迅速变小, 天然海水中的腐蚀速率开始趋于稳定, 但腐蚀后期逐渐变大。在腐蚀初期灭菌海水中的腐蚀速率一直高于天然海水; 在 60 d时两者相差最大, 灭菌海水中的腐蚀速率是天然海水中的1.4倍。但在腐蚀后期 (浸泡120 d后) 天然海水中的腐蚀速率明显高于灭菌海水。因此, 可以初步判断, 在天然海水中碳钢表面形成了海洋微生物膜, 在腐蚀开始阶段微生物膜对碳钢腐蚀起到了抑制作用, 但随时间增加, 到腐蚀后期微生物膜又加速其腐蚀。

图1 Q235钢在灭菌和天然海水中不同浸泡时间的腐蚀速率对比Fig. 1 Corrosion rate of Q235 steel in sterile and natural seawater with different exposure time
2.2 灭菌和天然海水中 Q235钢的开路电位变化特征(Eoc)
在灭菌和天然海水中的Q235钢的Eoc随浸泡时间的变化, 如图2所示。Q235钢在天然和灭菌海水中Eoc从起始迅速变化, 呈现出指数减小(-0.5~0.7 V), 到1 d后缓慢变化。在1~7 d, 灭菌海水中的Eoc低于天然海水中的并且保持在-0.70 V左右, 随后,Eoc正移保持在大约-0.67 V直到结束。天然海水中的Eoc开始浮动比较大, 之后与灭菌海水中Eoc基本相同。随后又负移, 稳定在-0.72 V左右直至结束。该结果与Malard等研究的结果是相似的[12]。对比说明微生物膜的存在影响Q235开路电位的变化, 从而影响了腐蚀速率。

图2 Q235钢在灭菌和天然海水中开路电位随浸泡时间的变化Fig. 2 Open circuit potential-time curve of Q235 steel in sterile and natural seawater
2.3 灭菌和天然海水中 Q235钢的电化学阻抗谱特征
图3是Q235钢在灭菌海水中不同浸泡时间的电化学阻抗谱图。从图中可知, 圆弧直径开始比较小,在实验 7 d后一个快速增大过程, 然后又逐渐减小,到60 d之后又逐渐增大。同时, 可以发现在高频区和低频区各呈现一容抗弧, 体系存在2个时间常数。实验数据与拟合数据之间的平均方差 χ2值均小于10-3, 结合体系的自身特点, 选用图4(a)为碳钢在灭菌海水中的等效电路较为合理。其中Rs表示溶液电阻,Qcp表示腐蚀产物膜电容,Rcp表示腐蚀产物膜电阻,Qdl表示界面双电层电容,Rct表示电荷传递电阻。Q因子为常相位角元件, 是用来描述等效电容 C的参数发生偏离时的等效元件。电荷传递电阻Rct可以用来表征金属的腐蚀速率,Rct值越小表面金属腐蚀速率越大[13]。万逸等[16]在研究无菌海水培养基介质中碳钢腐蚀行为时也采用了类似的等效电路模型。经过数据拟合求得在灭菌海水中的电化学参数随时间的变化情况如表1所示。从表中可知,Rct值开始很小。这可能是因为灭菌海水中氧气与新鲜碳钢界面直接接触, 促进氧去极化腐蚀, 腐蚀速率很大。在实验7 d时Rct值迅速增大, 这说明在没有微生物的影响下, 碳钢表面形成了比较致密的氧化层膜, 阻碍氧气与试样表面接触, 暂时起到保护基体的作用。但是在实验14 d后Rct值逐渐减小, 这说明当浸泡时间进一步延长, 氧化层被破坏, 不能阻碍氧气的扩散,而且试样表面没有生物膜的形成, 使得氧气很容易扩散到碳钢表面上, 腐蚀速率逐渐变大。在实验60 d后Rct值又迅速上升, 这是因为在碳钢表面形成一层比较致密的腐蚀产物膜, 起到阻碍氧气扩散的作用,抑制了氧去极化作用, 使得腐蚀速率逐渐下降。关于碳钢在灭菌海水中的腐蚀行为与武素茹等[17]研究结果是类似的。

图3 Q235钢在灭菌海水中浸泡不同时间的交流阻抗谱图Fig. 3 Nyquist plots of Q235 steel in sterile seawater with different exposure time
从 Q235钢在天然海水中不同浸泡时间的电化学阻抗谱图(图5)中可以看出, 圆弧直径的变化规律与灭菌海水体系相比明显不同。在实验1~30 d内,圆弧直径随时间减小。然后在实验30~60 d内缓慢增大, 最后在75~135 d内又逐渐减小。与灭菌海水相比较, 天然海水体系应该增加一个时间常数, 新增的时间常数应该来自于海洋微生物膜。同时, 阻抗谱特征以及拟合数据与实验数据之间的平均方差 χ2值均小于 10–3, 表明实验数据与拟合数据吻合得很好。在海水介质的碳钢腐蚀研究中采用三个时间常数的等效电路模型已经被报道[16,18], 这与本研究结果是类似的。因此, 选用了图4(b)作为碳钢在天然海水中的模拟电路模型。其中Rs表示溶液电阻,Qcp表示腐蚀产物膜电容,Rcp表示腐蚀产物膜电阻,Qbf表示微生物膜电容,Rbf表示微生物膜电阻,Qdl表示界面双电层电容,Rct表示电荷传递电阻。经过数据拟合求得在天然海水中的电化学参数随时间的变化情况如表2所示。从表中可知, 开始Rct值明显比在灭菌海水中的大,腐蚀速率较小。这可能是因为有微生物在碳钢表面形成了微生物膜所导致氧气不易扩散到金属表面。Melchers等[11]研究表明当 Q235钢放入天然海水中,短时间内就会有细菌附着在上面形成微生物膜, 会对初期的腐蚀产生影响。随后Rct值逐渐减小, 说明腐蚀速率逐渐增大。这个阶段微生物膜还很薄, 氧气很容易扩散到基体表面。这个阶段的腐蚀速率是由氧气在海水中的扩散速度决定, 腐蚀速率与时间基本呈线性增大的关系[7]。随着浸泡时间的延长,Rct值逐渐增加, 腐蚀速率逐渐减小。这是因为腐蚀速率是由氧气在生物膜和腐蚀产物膜中的扩散速度决定, 微生物膜和腐蚀产物膜逐渐增厚, 到达基体表面氧气浓度就逐渐降低。当浸泡时间超过75 d之后,Rct值又开始减小, 这是因为随着微生物膜的增厚, 基体腐蚀出现近似厌氧环境,使得厌氧腐蚀出现从而加速腐蚀, 这与厌氧细菌有密切的关系。Melchers等[7]在总结多年研究的基础上提出了碳钢在天然海水中的腐蚀速率模型。这与本研究结果是相似的。

图4 Q235钢在灭菌海水(a)和天然海水(b)中的等效电路模型Fig. 4 Equivalent circuits of the impedance diagrams of Q235 steel in sterile (a) and natural (b) seawater

图5 Q235钢在天然海水中浸泡不同时间的交流阻抗谱图Fig. 5 Nyquist plots of Q235 steel in natural seawater with different exposure time
根据Rct值随时间的变化来比较碳钢在2种海水体系中的腐蚀行为, 如图6所示。在腐蚀初期, 灭菌海水的Rct值明显小于天然海水, 这说明在腐蚀初期灭菌海水中的碳钢腐蚀速率大于天然海水, 这是由于微生物膜抑制氧气向金属表面扩散, 从而减小腐蚀速率。有研究[3]将微生物膜抑制碳钢腐蚀归因于生物膜中活细菌对金属表面氧气的消耗。也有研究表明细菌的某些代谢产物能起到抑制腐蚀的作用[19]。当在浸泡75 d出现厌氧腐蚀后, 天然海水的Rct值又大于灭菌海水, 这也说明在腐蚀后期在天然海水中的碳钢腐蚀速率逐渐增大并且大于灭菌海水。这是因为厌氧微生物的出现大大加重了碳钢的腐蚀。关于厌氧腐蚀能加速腐蚀主要归因于SRB等厌氧细菌的生长造成的[20]。关于厌氧腐蚀机理较多, 如阴极去极化机理, 即 SRB将氢气从铁表面移除引起铁腐蚀的加速等[20-21]。这些结果与失重试验结果是相一致的。
2.4 微生物培养结果和分析
Q235钢在天然海水中浸泡17 d后, 发现试样表面生成一层薄薄的橘红色的锈层, 取锈层接种于SOB培养基中。从培养结果可以看出, 与空白试样相比, 加铁锈的培养基颜色变蓝 (中性指示剂), 这说明培养基成酸性。这与文献报道的结果是类似的[15], 说明铁锈中含有 SOB。这可能表明海洋环境中有SOB参与低碳钢腐蚀过程[10]。
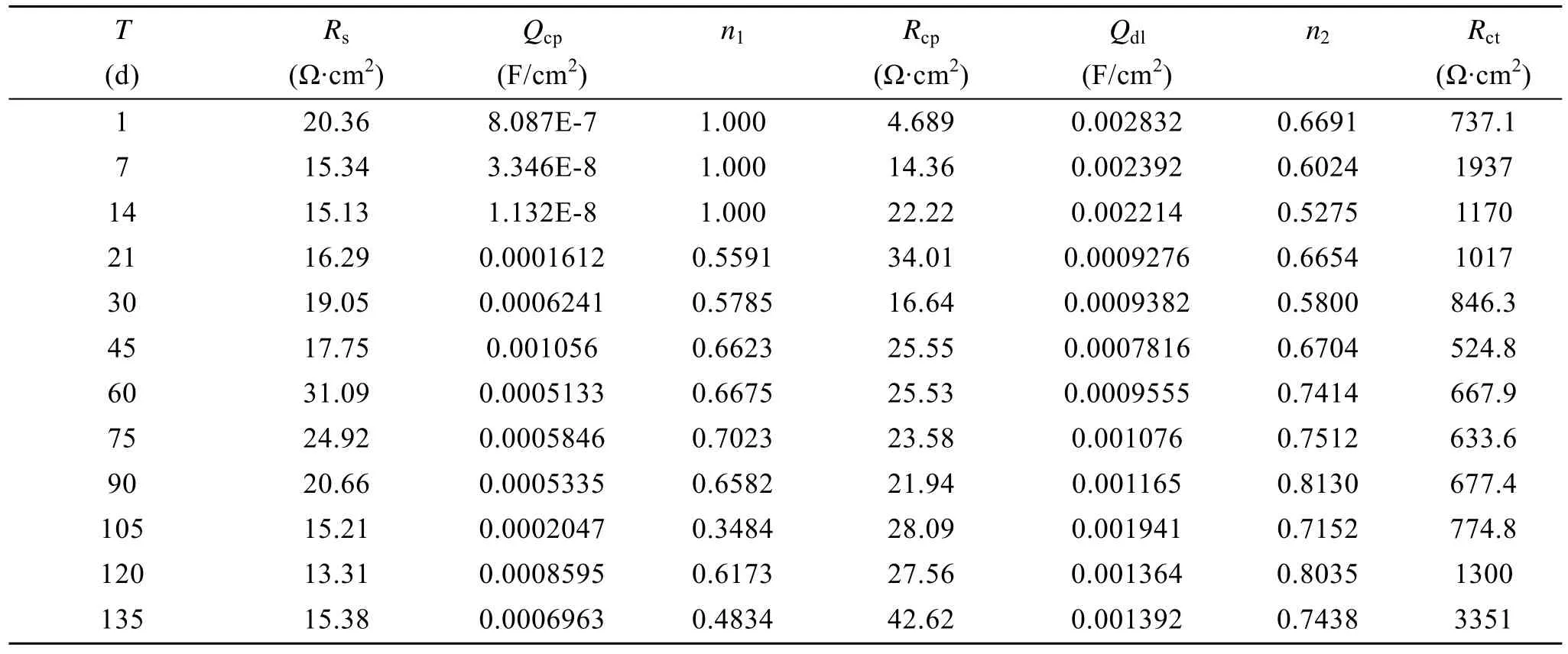
表1 Q235钢在灭菌海水中的电化学阻抗模型的参数分析Tab. 1 Electrochemical parameters of Q235 steel in sterile seawater

表2 Q235钢在天然海水中的电化学阻抗模型的参数分析Tab. 2 Electrochemical parameters of Q235 steel in natural seawater
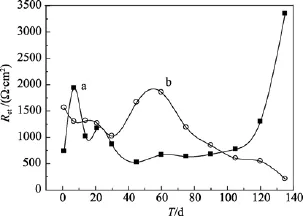
图6 Q235钢在灭菌(a)和天然海水(b)中电荷转移电阻随浸泡时间的变化曲线Fig. 6 Variation curve of Rct with time of Q235 steel in sterile (a) and natural (b) seawater
将锈层接种于LB中, 结果加铁锈的培养基变浑浊, 说明有细菌生长。将其稀释1 000倍后接种在固体培养基平板上观察菌落的形貌 (图7), 有三种明显不同的菌落出现:1. 桔红色, 2. 白色, 3. 黄色, 这可能是3种优势菌。这说明在腐蚀前期, 有SOB等多种好氧微生物参与碳钢腐蚀过程。
Q235钢在天然海水中浸泡100 d后, 通过表面肉眼观察锈层由初期疏松的橘红色逐渐变化分成两层, 分别是致密的黑色内锈层和棕黄色的外锈层。将内锈层接种于 SRB培养基。结果可以发现, 瓶中铁粉已经完全变黑, 打开密封盖后出现强烈的臭鸡蛋气味, 证明有 SRB参与腐蚀。这与前人研究的结果是一致的[13,22]。
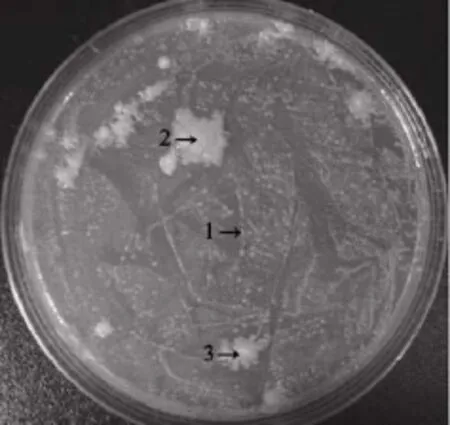
图7 接种铁锈在LB固体培养基上菌落的形貌Fig. 7 Morphology of colonies on LB solid medium with rust layer
2.5 在天然海水中浸泡不同时间的 Q235钢表面观察与分析
分别对浸泡不同时间的 Q235钢表面进行了SEM 分析, 分析结果见图8。同时, 选取不同区域EDS分析, 如表3所示。当浸泡7 d之后 (图8a), 基体表面出现两种形状的铁锈 (长棒状和球状)。从中可以发现相比较与b处, 其中a点处O含量较低, P含量比较高, 这说明此处细菌代谢旺盛, 产生磷酸盐相关的代谢产物, 这可能是好养细菌作用的结果。a点处有更高的 Fe, 这表明可能好氧细菌对铁氧化合物的形成有抑制作用。这可以用来解释开始阶段天然海水中的腐蚀速率比灭菌海水中的小。Jeffrey等[8]研究表明海水钢铁腐蚀产物的最初形式为Fe2O3·H2O和γ-FeOOH, Fe元素处于三价, 氧气很容易扩散到基体表面。这与电化学阻抗的分析结果是一致的。浸泡17 d后 (图8b), 出现海绵状的球状体,它有更加精细的结构, 但基本成分没有变化。从EDS分析表明c处C元素的增多也说明基体上附着了更多的生物有机体, 在初期阶段营养物质充足, 且较薄的微生物膜不能阻碍营养物质和氧气的扩散, 在碳钢表面微生物群落增多。这与LB广泛富集培养结果是一致的。同时, 出现S元素, 这可能是腐蚀前期SOB产生的。从图8c可以看出, 浸泡45 d后锈层和微生物膜比较致密。EDS分析显示d处C含量降至5%, 也说明微生物膜进一步增厚, 氧气和营养物质越来越难扩散, 好氧微生物群逐渐减少。同时, 细菌种类逐渐发生了变化, 并出现Mg元素, 这可能是另外一种细菌代谢的结果。微生物膜增厚为厌氧细菌的出现创造了条件。当浸泡 100 d后 (图8(d)和图8(e)), 基体有了致密的内锈层和棕黄色的外锈层。这与前人研究结果是一致的[13,23]。内锈层的EDS分析结果表明e处S含量较高, O含量较低, 说明在SRB等厌氧菌作用下, 铁氧化合物逐渐向铁硫化合物转变。Neal等[24]指出, 在 SRB代谢过程中, 产生有机酸、H2S等物质, H2S与铁氧化物反应逐步生成铁硫化物。而f处正好相反, 说明锈层主要还是铁氧化合物, 这表明内锈层的厌氧菌不是均匀出现的。这与Jeffrey等[8]研究结果是相似的。

图8 Q235钢在天然海水中浸泡不同时间下的SEM形貌图Fig. 8 Surface morphology of Q235 steel immersed in natural seawater with different exposure time
3 结论
(1)从失重实验和交流阻抗谱测试结果显示:在腐蚀初始, 在灭菌海水中的Q235钢腐蚀速率是大于天然海水, 这是由于微生物膜抑制了氧气向金属表面扩散, 从而减小腐蚀速率。但在腐蚀后期天然海水中的Q235钢腐蚀速率逐渐增大并且大于灭菌海水。这可能是因为厌氧微生物的出现大大加重了碳钢的腐蚀。微生物膜的存在抑制了初期的好氧腐蚀, 同时,加速了后期的厌氧腐蚀。
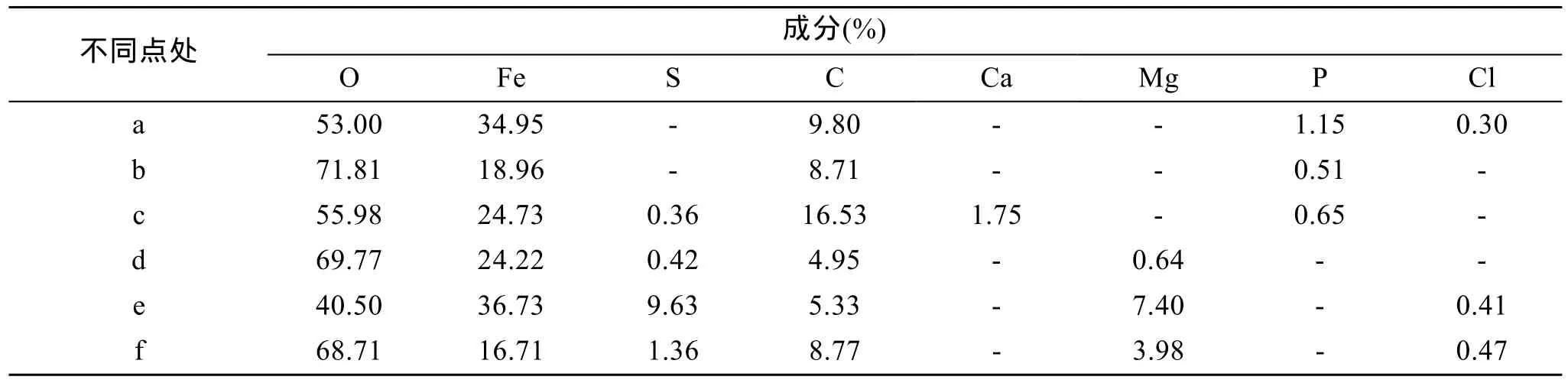
表3 Q235钢在天然海水中不同点处(图8)的EDS对比分析Tab. 3 EDS results of Q235 steel in natural seawater at different spots (Fig. 8)
(2)从微生物分析结果和 SEM、EDS分析表明:微生物膜对 Q235钢腐蚀速率及其机理与微生物的种类是密切相关的。在腐蚀的前期, 主要是由多种好氧微生物协同作用的结果; 在出现厌氧腐蚀之后,主要是SRB等厌氧微生物的作用。
[1]Beech I B, Gaylarde C C. Recent advances in the study of biocorrosion - An overview[J]. Revista De Microbiologia, 1999, 30(3):177-190.
[2]李相波, 王伟, 王佳, 等. 海水中微生物膜的生长对金属腐蚀过程的影响[J]. 腐蚀科学与防护技术,2002(04):218-222.
[3]Chongdar S, Gunasekaran G, Kumar P. Corrosion inhibition of mild steel by aerobic biofilm[J].Electrochimica Acta, 2005, 50(24):4655-4665.
[4]Little B, Ray R. A perspective on corrosion inhibition by biofilms[J]. Corrosion, 2002, 58(5):424-428.
[5]Hudson, J C. Corrosion of bare iron or steel in sea water[J]. Journal of the Iron and Steel Institute, 1950,166(2):123-136.
[6]Little B, Wagner P, Mansfeld F. Microbiologically influenced corrosion of metals and alloys[J].International Materials Reviews, 1991, 36(6):253-272.
[7]Melchers R E. Mathematical modelling of the diffusion controlled phase in marine immersion corrosion of mild steel[J]. Corrosion Science, 2003, 45(5):923-940.
[8]Jeffrey R, Melchers R E. Bacteriological influence in the development of iron sulphide species in marine immersion environments[J]. Corrosion Science, 2003,45(4):693-714.
[9]Boudaud N, Coton M, Coton E, et al. Biodiversity analysis by polyphasic study of marine bacteria associated with biocorrosion phenomena[J]. Journal of Applied Microbiology, 2010, 109(1):166-179.
[10]Beech I B, Campbell S A. Accelerated low water corrosion of carbon steel in the presence of a biofilm harbouring sulphate-reducing and sulphur-oxidising bacteria recovered from a marine sediment[J].Electrochimica Acta, 2008, 54(1):14-21.
[11]Melchers R E. Transient early and longer term influence of bacteria on marine corrosion of steel[J].Corrosion Engineering Science and Technology, 2010,45(4):257-261.
[12]Malard E, Kervadec D, Gil O, et al. Interactions between steels and sulphide-producing bacteria-Corrosion of carbon steels and low-alloy steels in natural seawater[J]. Electrochimica Acta, 2008, 54(1):8-13.
[13]Duan Jizhou, Wu Suru, Zhang Xiaodong, et al.Corrosion of carbon steel influenced by anaerobic biofilm in natural seawater[J]. Electrochimica Acta,2008, 54(1):22-28.
[14]吴进怡, 柴柯, 肖伟龙, 等. 25钢在海水中的微生物单因素腐蚀[J]. 金属学报, 2010(06):755-760.
[15]何环, 夏金兰, 彭安安, 等. 嗜酸硫氧化细菌作用下元素硫化学形态的研究进展[J]. 中国有色金属学报,2008(06):1143-1151.
[16]Wan Yi, Zhang Dun, Liu Huaiqun, et al. Influence of sulphate-reducing bacteria on environmental paramet-ers and marine corrosion behavior of Q235 steel in aerobic conditions[J]. Electrochimica Acta, 2010, 55(5):1528-1534.
[17]武素茹, 段继周, 赵晓栋, 等. 碳钢在富集硫酸盐还原菌海水中的腐蚀行为研究[J]. 腐蚀科学与防护技术, 2007(04):247-250.
[18]Perez E J, Cabrera R, Gonzalez I, et al. Influence ofDesulfovibriosp. biofilm on SAE 1018 carbon steel corrosion in synthetic marine medium[J]. Corrosion Science, 2007, 49(9):3580-3597.
[19]Ismail K M, Gehrig T, Jayaraman A, et al. Corrosion control of mild steel by aerobic bacteria under continuous flow conditions[J]. Corrosion, 2002, 58(5):417-423.
[20]Videla H A. An overview of mechanisms by which sulphate-reducing bacteria influence corrosion of steel in marine environments[J]. Biofouling, 2000, 15(1-3):37-47.
[21]Mansfeld F. The interaction of bacteria and metal surfaces[J]. Electrochimica Acta, 2007, 52(27):7670-7680.
[22]Muyzer G, Stams A M. The ecology and biotechnology of sulphate-reducing bacteria[J]. Nature Reviews Microbiology, 2008, 6(6):441-454.
[23]Zou Y, Wang J, Zheng Y Y. Electrochemical techniques for determining corrosion rate of rusted steel in seawater[J]. Corrosion Science, 2011, 53(1):208-216.
[24]Neal A L, Techkarnjanaruk S, Dohnalkova A, et al. Iron sulfides and sulfur species produced at hematite surfaces in the presence of sulfate-reducing bacteria[J].Geochimica Et Cosmochimica Acta, 2001, 65(2):223-235.
Effect of biofilms on corrosion of carbon steel in seawater
ZHAO Wei1,2, SU Lu-lu1,3, DUAN Ji-zhou1, JIANG Jiang3, HOU Bao-rong1
(1. Institute of Oceanology, Chinese Academy of Sciences, Qingdao 266071, China; 2. Graduate School of the Chinese Academy of Sciences, Beijing 100049, China; 3. Faculty of Materials, Shandong University, Jinan 250061,China)
Mar., 21, 2011
marine corrosion; electrochemical impedance spectroscopy; carbon steel; biofilms
Steel infrastructure immersed in natural seawater is exposed to important corrosion phenomena. Marine microorganisms have a significant influence on marine steel corrosion. In this work, the effect of biofilms on the corrosion behaviors of Q235 steel was studied by comparing the corrosion behaviors of the carbon steel immersed in natural and sterile seawater. The corrosion behaviors were observed by using gravimetric, microbiological, electrochemical measurements and corrosion product analyses. In the early phase, biofilms can decrease the corrosion rate. This is because the rate oxygen diffusion from the medium onto the steel surface was limited by the formation and growth of biofilms. It is correlated with synergistic action of a variety of aerobic microorganisms. In the later phase, it is marked by an increased rate of corrosion. It is related to the rapid growth of anaerobic microorganisms,such as sulphate reducing bacteria.
TG172.5; TG172.7 文献标识码:A 文章编号:1000-3096(2012)09-0024-08
2011-03-21 ;
2011-04-21
中国科学院知识创新工程重要方向资助项目(KZCX2-EW-205) ; 国家自然科学基金项目(40676048, 40976046)
赵伟(1987-), 男, 四川南充人, 硕士研究生, 主要从事海洋腐蚀与防护研究; 段继周, 通信作者, 电话:0532-82898851, E-mail:duanjz@qdio.ac.cn
康亦兼)
