混合萃取剂双氧水络合萃取分离钨钼的初步研究
2011-12-31张贵清关文娟肖连生
欧 惠,张贵清,关文娟,肖连生
(1.中南大学 冶金科学与工程学院,湖南 长沙 410083;2.中南大学 稀有金属与材料制备湖南省重点实验室,湖南 长沙 410083)
钨钼性质极其相似,钨钼分离一直以来是钨湿法冶金的难点和研究热点。长期以来,国内外学者围绕钨钼分离进行了大量的研究工作,并利用钨钼及其化合物在性质上微小差异提出了多种钨钼分离方法[1]。目前工业中广泛采用的钨钼分离方法有MoS3沉淀、季铵盐萃取、离子交换和选择性沉淀等方法[2-4],该类方法是向钨钼混合溶液中加入硫化剂,如(NH4)2S、Na2S和H2S等,使溶液中的钼酸根离子转化为硫代钼酸根离子,然后利用硫代钼酸根与钨的含氧酸根性质差异实现钨钼分离。硫化法适用于处理钼含量较低的钨原料(Mo/WO3<2%),但当钨原料中钼含量较高时,硫化剂用量大,分离成本高,另外,硫化剂有毒,存在操作环境差和潜在的安全问题。
另一类研究较多具有工业应用前景的钨钼分离方法是双氧水络合萃取法,该类方法采用的络合剂为双氧水,具有操作环境好、污染少和试剂价格较低的优势,尤其适合于处理高钼含量的钨原料。该方法是利用在酸性条件下钨、钼过氧络合物与中性或碱性萃取剂亲和力的显著差别,萃取剂优先萃取钼而实现钨钼分离[5-7]。Zelikman等人[5]在20世纪70年代首先对此方法进行了研究,采用的萃取剂包括TBP、季铵盐等。随后Ozensoy等人[6]在此基础上采用D2EHPA+TBP+TBPO混合萃取剂进行钨钼萃取分离,其特点是H2O2用量较少。上述研究成功实现了在钨酸盐溶液中深度除钼,但萃取钼的同时钨的共萃率较高(WO3萃取率达6%~7%)。20世纪80年代李伟宣等人[7]选用TRPO-MIBK-煤油体系在双氧水络合条件下萃取分离钨钼,钨钼的分离系数βMo/WO3高达100以上,钨共萃损失较小,但是MIBK水溶性较大,有机相流失较大。双氧水络合萃取法分离钨钼至今未得到工业化应用。
近年来中南大学配制了一种水溶性较小的混合萃取剂,对高钼钨酸盐进行了双氧水络合萃取分离钨钼的研究,取得了较好的钨钼分离效果,目前该技术已经完成了工业试验,试验结果显示出该技术具有很好的工业应用前景。本文是该萃取体系处理工业实际料液的初步试验研究结果。
1 试验
1.1 原料及试剂
钼含量高的钨酸铵溶液为高钼低品位白钨矿苏打高压浸出液经季铵盐碱性条件下萃钨后获得的反萃液[8],其中WO3110~160g/L,Mo/WO3约10%~15%,P/WO3,Si/WO3均小于0.01%,Na小于0.01g/L。该反萃液再经过双极膜电渗析制得含钼的偏钨酸铵溶液(pH值约3.0)[9],本试验以含钼的偏钨酸铵溶液作为原料配制络合料液进行萃取试验。
萃取剂为一种混合萃取剂CMIX,CMIX由两种工业级有机试剂A和B组成,A和B均为工业级产品,其在水中的溶解度均小于0.05%。稀释剂为磺化煤油。试验中有机相的组成为:45%CMIX+55%磺化煤油。
其他试剂均为分析纯化学试剂。
1.2 试验操作
萃取料液配制:向含钼偏钨酸铵溶液加入定量的H2O2,混合均匀,然后用硫酸或氨水调节pH值至指定值,备用。双氧水加入量按nH2O2/n(WO3+Mo)计算,其中nH2O2表示双氧水的摩尔数,n(WO3+Mo)为钨、钼的摩尔数之和。
萃取与反萃取:有机相与水相在锥形瓶中于水浴恒温振荡器上在设定温度下进行混合。混合相在分液漏斗中进行澄清分相。取样测定水相和有机相中的钨钼浓度。
1.3 分析方法
水相中钨采用硫氰酸盐比色法分析,钼采用硫氰酸铵比色法分析。有机相中的钼和钨浓度根据萃取前后水相的浓度和体积变化按差减法计算。
2 试验结果与讨论
2.1 萃取平衡时间的确定
试验考查了不同振荡平衡时间对钼和钨萃取的影响。试验条件:双氧水用量nH2O2/n(WO3+Mo)=1.4;相比O/A=2/1;温度为15℃;料液pH值为1.60,WO3109.79g/L,Mo 13.44g/L。试验结果如图1所示。
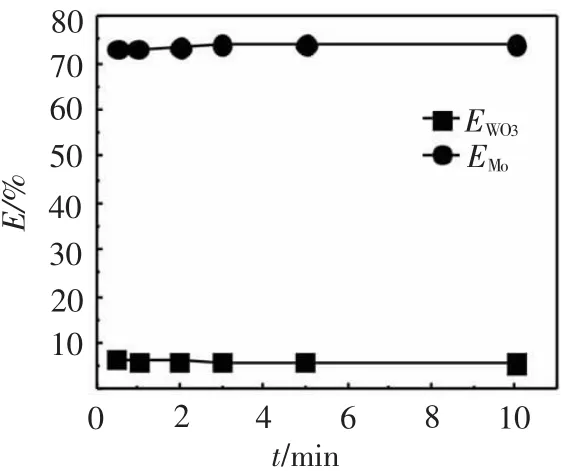
图1 振荡平衡时间对钼钨萃取率的影响
图1为振荡平衡时间对钼萃取率EMo、钨萃取率EWO3的影响。由图1可知,钼、钨萃取过程平衡时间短,萃取在3min以内即可达到平衡。为此,在以后的萃取操作中取振荡平衡时间为5min。
2.2 双氧水用量对萃取过程的影响
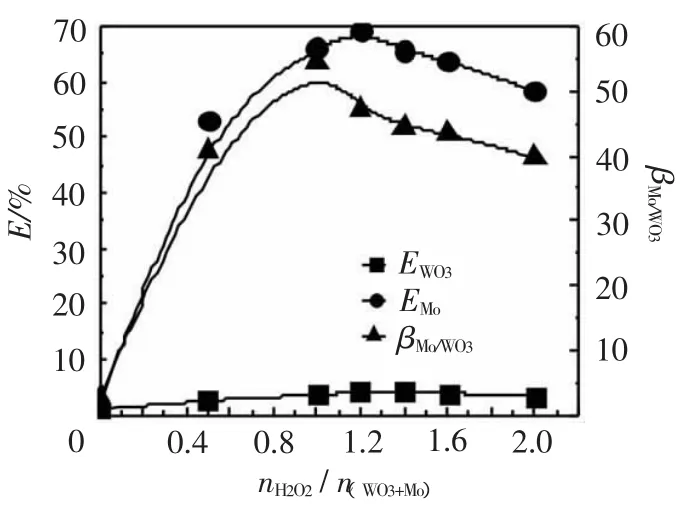
图2 双氧水用量对钼钨萃取分离的影响
图2为双氧水用量对钨钼萃取分离的影响。试验条件:相比O/A=2/1;温度为15℃;料液pH值为1.60,WO3109.03g/L,Mo 13.93g/L;振荡时间5min。
图2显示,随着nH2O2/n(WO3+Mo)的增加,Mo萃取率EMo,WO3萃取率EWO3和钼钨分离系数βMo/WO3均先增加后降低,EMo,EWO3和βMo/WO3分别在nH2O2/n(WO3+Mo)=1.2,1.2~1.4,1.0左右达到峰值。试验还发现,料液的稳定性与双氧水用量直接相关,即双氧水用量越大,料液越稳定,当nH2O2/n(WO3+Mo)<1.0时,料液不稳定,存放24h以上即会析出钨酸沉淀。综合考虑料液的稳定性,EMo,βMo/WO3和经济因素,选择nH2O2/n(WO3+Mo)=1.4。此时,βMo/WO3大于50。
2.3 水相平衡pH值对萃取过程的影响
试验发现,与料液相比,萃余液的pH值升高,说明H+参与了萃取反应。为此考查了水相平衡pH值对萃取过程的影响,试验结果如图3所示。试验条件:双氧水用量nH2O2/n(WO3+Mo)=1.4;相比O/A=2/1;温度为15℃;料液WO399.88g/L,Mo 12.58g/L;振荡时间5min。
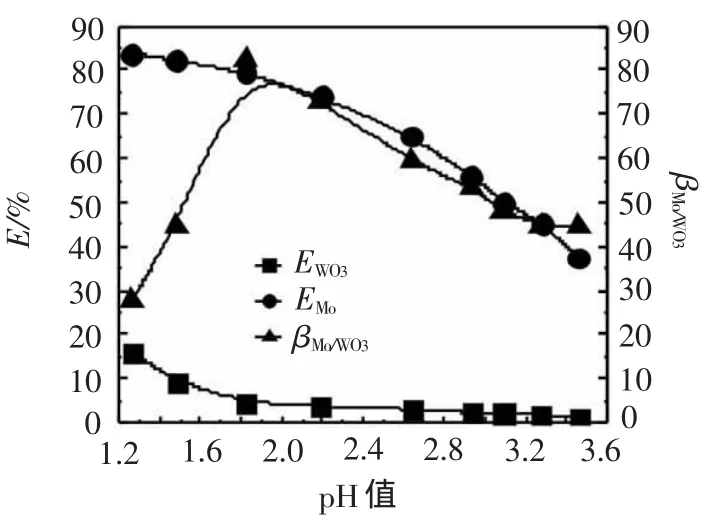
图3 水相平衡pH值对钼钨萃取分离的影响
图3显示,EMo,EWO3均随水相平衡pH值升高而降低,但下降的幅度不同。在试验考察的范围内(pH1.2~3.5),EMo随水相平衡pH值的升高平稳下降,而EWO3随水相平衡pH值的升高先急剧下降,而后缓慢下降。βMo/WO3则呈现先上升后下降的趋势,在水相平衡pH为1.8左右出现峰值,峰值时分离系数达70以上。综合考虑萃钼效果和钨钼分离效果,选择水相平衡pH值为1.8~2.2为宜。
2.4 温度对萃取过程的影响
图4为温度对钨钼萃取分离的影响规律。实验条件:双氧水用量nH2O2/n(WO3+Mo)=1.4;相比O/A=2/1;料液pH值为1.60,WO3109.28g/L,Mo13.93g/L;振荡时间5min。
由图4可知,EMo随着温度升高呈线性下降,EWO3在一定温度范围随温度的升高基本不变,而βMo/WO3随温度升高下降较快。因此选择较低的温度有利于钼的萃取和钨钼分离,然而过低的温度一方面导致分相性能下降,另一方面也消耗能量,综合考虑选择温度在15~20℃为宜。
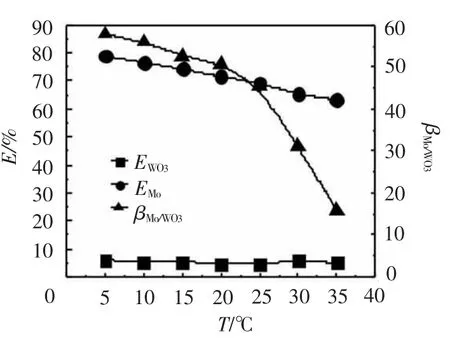
图4 温度对钼钨萃取分离的影响
2.5 萃取等温线
采用相比变化法绘制了钼的萃取等温线,结果如图5所示。试验条件:nH2O2/n(WO3+Mo)=1.4;温度15℃;料液pH值为1.60,WO3102.16g/L,Mo12.97g/L;振荡时间5min。试验中采用硫酸或氨水调节水相pH值,维持相同的水相平衡pH值,试验中控制水相平衡pH值为1.68。图5显示,萃取剂浓度为45%时,有机相对钼的饱和萃取容量为9.2g/L。
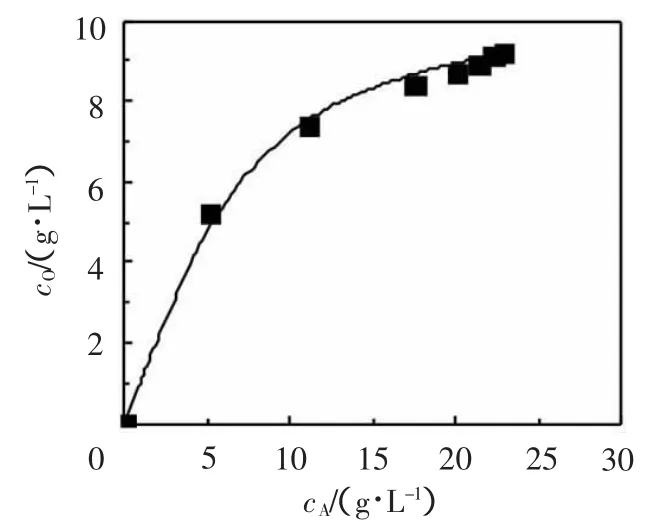
图5 钼的萃取等温线
2.6 反萃取
负载有机相中Mo 7.74g/L,WO30.96g/L,反萃剂为0.25mol/L NaOH水溶液,在温度15℃,相比1/1的条件下混合振荡15min,钼与钨的反萃率分别达到99.30%和93.54%。由此可见,NaOH溶液能有效反萃负载有机相中的钼和钨。
3 结论
(1)混合萃取剂双氧水络合萃取法能从钼含量高的钨酸盐溶液中有效分离钨钼,该萃取体系具有萃钼能力强、平衡时间短、钨钼分离效果好和反萃容易的特点。
(2)双氧水用量、水相平衡pH值和温度是影响钼萃取和钨钼萃取分离效果的关键因素。
[1]刘旭恒,孙 放,赵中伟.钨钼分离的研究进展[J].稀有金属与硬质合金,2007,35(4):42-45.
[2]龚柏凡,张启修.基于硫代钼酸盐分离钨钼的研究小结[J].中国钨业,1995,10(4):10-14.
[3]肖连生,张启修,龚柏凡.从钨酸盐溶液中除钼:中国,CN98122929.8[P].1998-12-05.
[4]孙培梅,霍广生.钨钼分离方法的研究进展[J].中国钼业,2003,27(2):35-38.
[5]Zelikman A N,Voldman G M,Rumyantsev V K.Process for separation of tungsten andmolybdenum by extraction:United States,US3969478[P].1976-07-13.
[6]Ozensoy E,Burkin A R.Separation of tungsten andmolybdenum by solvent extraction:United States,US4275039[P].1981-06-23.
[7]李伟宣,张礼权.液液萃取法分离钨钼的研究[J].稀有金属与硬质合金,1989,17(2):21-24.
[8]张贵清,关文娟,张启修,等.从钨矿苏打浸出液中直接萃取钨的连续运转试验[J].中国钨业,2009,24(5):49-52.
[9]张贵清,尚广浩,刘洪吉.双极膜电渗析制取偏钨酸铵溶液的研究[C]//第三届膜分离技术在冶金工业中应用研讨会论文集.山东:《膜科学与技术》编辑部,2009:145.
