尊重客观事实 走出认识误区——也谈氧化还原反应与四种基本类型反应的关系
2011-12-28马佩强
马佩强 孟 静
(1 淄博市教学研究室 山东 淄博 255030; 2 淄博第六中学 山东 淄博 255300)
化学反应根据不同的分类标准,可以有多种分类方式。 如根据化学反应中元素的化合价是否发生变化,可将其分为氧化还原反应和非氧化还原反应; 根据反应物、生成物种类和数量不同,则可分为化合反应、分解反应、置换反应和复分解反应等四种基本类型的反应……其中氧化还原反应与四种基本类型反应的关系是高中学习阶段经常讨论的问题,把握好它们之间的关系对于深入理解氧化还原反应的实质有着很重要的意义。 但笔者在听课研究中发现:有不少教师或学生在处理这个问题时,出现了个别误区,对二者关系的认识出现了偏差,因此撰文与广大同仁进行探讨,以免让谬误越传越远。
一、对氧化还原反应与四种基本类型反应关系认识上的主要误区
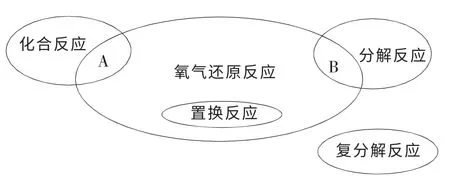
1.误区一:无单质参加的化合反应一定不是氧化还原反应; 无单质生成的分解反应一定不是氧化还原反应。 我们在认识氧化还原反应与化合反应、分解反应之间关系的时候,得出的结论是:有单质参加的化合反应一定是氧化还原反应;有单质生成的分解反应也一定是氧化还原反应。 这两个结论都是有充足的理论依据的,因为单质的化合价为零价,而在化合反应中,该元素转移到化合物中,其化合价必然不为零价;在分解反应中,元素由化合物中的非零价变为产物单质中的零价,这两种变化过程中都毋庸置疑地伴随了元素化合价的变化,因此二者皆属于氧化还原反应。 可笔者在听课过程中发现:有的教师为了引导学生“更加全面”地认识氧化还原反应与化合、分解反应之间的关系,又将上述结论引申为: 无单质参加的化合反应则一定不是氧化还原反应;无单质生成的分解反应也一定不是氧化还原反应。 这样拓展得到的这两个结论同样可靠吗? 笔者在一次听课后曾就这一问题在授课班级的学生中展开过随机调查,有70%以上的学生认为观点可信;有近30%的学生表示对这两个结论不信服,但苦于找不出可以反驳它们的实例。 事实上,这两个结论的确存在不严密之处,显得过于绝对和武断。 笔者分别试举两例加以说明:无单质参加的化合反应:①过氧化氢与二氧化硫化合:H2O2+SO2=H2SO4;②一氧化氮和二氧化氮的混合气体通入冰水中:NO+NO2+H2O(冰水)=2HNO2。在以上两个反应中,虽无单质的参与,但都有元素的化合价发生了变化,当属氧化还原反应。 无单质生成的分解反应:①硝酸铵在一定温度下的分解反应:NH4NO3=N2O+2H2O;②亚硫酸钠受热分解:4Na2SO3=Na2S+3Na2SO4。 同样可分析这两个反应也属于氧化还原反应。 这样的反应虽不多见,但以上的例子足以说明“无单质参加的化合反应一定不是氧化还原反应”、“无单质生成的分解反应一定不是氧化还原反应”这两个结论的谬误。 有的教师还把这种错误结论带到了下面的集合图示关系中,认为:化合反应、分解反应分别与氧化还原反应的交集A 和B 中所涉及的反应均分别为有单质参加的化合反应和有单质生成的分解反应,而把无单质参加或生成的化合、分解反应自然地排除在外,这样也就造成了学生对此问题认识上的偏差。2.误区二:有单质参加或生成的反应一定属于氧化还原反应。 这种错误主要出现在学生层面,即把正确结论中的化合、分解等字眼给抠掉了,认为它们是无关紧要、可有可无的,但是却忽略了同素异形体之间相互转化的这类反应。 如C(石墨)=C(金刚石)、3O2=2O3等反应中,虽然有单质参加和生成,但反应前后元素的化合价却始终为零,没有发生变化,自然不能归入氧化还原反应之列。 因此这一说法也是经不住推敲的。
二、这些认识误区带给我们的启示
1.在日常的教学中,我们必须以严谨求实的科学态度,从本质或源头出发认真对待每一个问题,不能采取想当然的态度,草率地作出结论,以免造成谬误。 如四种基本类型的反应中,哪些属于氧化还原反应,哪些不属于氧化还原反应,关键要从氧化还原反应概念本身去分析,看是不是真正有元素化合价发生变化,而不是仅凭“有无单质参加或生成”这些表面现象而作出判断。
2. 对于已知结论的迁移和拓展则要做到慎之又慎,采取科学严密的思维方法,仔细推理、小心求证,防止拓展结果的局限性和片面性。 从逻辑角度看,如果“有单质参加的化合反应一定是氧化还原反应”属于已经被证实的真命题,则其否命题“无单质参加的化合反应一定不是氧化还原反应”则可能是真命题也可能是假命题[1],需要求证后得知,不能仅凭感觉而作出主观臆断。
3.在教学和研究中,不可一味地追求规律的总结,而忽略一些不常见的化学事实[2],同时也要严格把握一些规律的限制条件,防止无限度地扩大规律的应用范围而造成错误。 如有单质参加或生成是化合反应或分解反应属于氧化还原反应的充分条件,而非所有化学反应属于氧化还原反应的充分条件,误区二的出现就是因为将原命题的应用范围无限扩大而造成的。
[1] 刘绍学.普通高中课程标准实验教科书·数学选修1-1.第2 版[M].北京:人民教育出版社,2007:5-7
[2] 刘前树,李广洲.中学化学教学中的潜在约定[J].中学化学教学参考,2010,(1-2):3-5
