改性羧甲基纤维素对铀吸附机理的试验研究
2011-12-21周书葵曾光明刘迎九杨金辉蒋海燕湖南大学环境科学与工程学院湖南长沙4008南华大学城市建设学院湖南衡阳400
周书葵,曾光明,刘迎九,杨金辉,蒋海燕 (.湖南大学环境科学与工程学院,湖南 长沙 4008;.南华大学城市建设学院,湖南 衡阳 400)
改性羧甲基纤维素对铀吸附机理的试验研究
周书葵1,2*,曾光明1,刘迎九2,杨金辉2,蒋海燕2(1.湖南大学环境科学与工程学院,湖南 长沙 410082;2.南华大学城市建设学院,湖南 衡阳 421001)
对羧甲基纤维素(CMC)进行改性,并将其用于吸附废水中的铀.研究结果表明:在温度为70℃~80℃、单体质量浓度为30%~35%、羧甲基纤维素:丙烯酸(质量比)为10:2.5、反应时间为3.5~4h条件下,CMC改性效果最好;在改性CMC质量浓度为0.10g/L,温度为25℃, pH值为5.0,反应时间60min的条件下,对废水中铀去除率达到了97.1%;改性CMC对溶液中U(VI)的吸附过程符合Freundlich方程,其吸附动力学数据符合准一级方程(R2=0.9618),表明改性 CMC的吸附主要是表面吸附;热力学研究表明,改性 CMC对铀的吸附吉布斯自由能(ΔG0)<0,而焓变(ΔH0)>0,吸附过程是自发的吸热反应、以物理吸附为主的过程.
改性CMC;吸附机理;铀
当前,包括我国在内世界上有18个国家从事铀矿冶生产.据估计我国核电对天然铀的需求量到2020年将达到3180~6540t[1].铀在生产环节及应用中将生产大量的含铀废水,若直接排放会造成水和土壤污染,将对环境和人类造成严重危害,因此,对含铀废水的处理刻不容缓.含铀废水通常可采用混凝过滤、蒸发浓缩、离子交换、膜分离、生物法、吸附等方法处理[2].混凝过滤法工艺简单,成本低,但出水铀浓度较高,需作进一步处理;蒸发浓缩法方法简单、有效,去除率高,但成本较高;离子交换法效果好,出水铀的浓度低,但处理费用高,易带来二次污染;膜分离法去除率高,但处理费用高,工业应用困难;生物法去除率高,但工业应用困难;吸附法是一种有效的方法,铀去除率高,与混凝沉淀结合,使用效果更佳,是一种极具发展前景的处理方法[3].
羧甲基纤维素常被应用于重金属废水的处理,但直接用来处理含铀废水,往往不能达到满意的效果.研究发现,CMC在与丙烯酸(AA)接枝聚合后,形成含有大量羧基、羟甲基等基团的胶体,这些基团能够增加废水处理中的负电荷数量和阳离子交换量;同时胶体三维网状结构对离子具有保蓄作用[4],且具有很大的内外表面积,这些性质决定了CMC具有较高的离子交换容量和很强的吸附能力.
本研究以 CMC为研究对象,首先通过实验方法对CMC改性条件进行了研究,在此基础上,主要从吸附热力学、反应动力学等方面分析了改性CMC对铀的吸附规律与机理,为改性CMC在含铀废水处理中的应用提供基础理论支撑.
1 材料与方法
1.1 试验材料
1.1.1 废水来源及试剂 废水为自行模拟含铀废水(模拟中国南部某铀矿酸法地浸废水),铀质量浓度为3.27mg/L,pH为2.73.
试验用水为超纯水,试验药剂有:羧甲基纤维素 CMC(市售),丙烯酸(AA)C3H4O2(化学纯),过硫酸铵(NH4)2S2O8(分析纯),N,N′-亚甲基双丙烯酰胺(MBAM)(分析纯),氢氧化钠NaOH(分析纯),环氧乙烷C2H4O(化学纯),U3O8(基准纯,国家标准物资中心).
铀的测定采用 GB6768-86[5]水中微量铀分析方法.
1.1.2 主要试验仪器 电子天平(AUY220,日本岛津);高速台式离心机(TGL-20B,上海安亭);精密pH计(pHS-3C型,上海雷磁仪器厂);恒温摇床(SI4-2,美国 SHELLAB);水浴箱(GD100-S18,英国GRANT);电热恒温干燥器(101-2A型,天津泰斯特仪器公司);马弗炉(SX-2.5-12,天津市泰斯特仪器有限公司);超纯水器(POWER-1000,韩国);分光光度计(2000,尤尼柯公司).
1.2 试验方法
1.2.1 改性 CMC的制备[6]将预先称量好的CMC10g放入锥形瓶中,加入超纯水100mL搅拌至溶液均匀,并向瓶内持续吹入一定量的氮气(起保护作用),通过小漏斗加入 100mg催化剂过硫酸铵((NH4)2S2O8),再加入 50mL 引发剂MBAM溶液至300mL锥形瓶中,再加10mg的丙烯酸(C3H4O2),搅拌均匀,水浴锅升温到 80℃,进行接枝共聚合成天然高分子改性反应,恒温 3.5~4h,当溶液出现黏稠爬杆现象,停止反应,将其产物转移到托盘中.蒸馏水反复冲洗上述产物,然后在 140℃的烘箱中烘干,即得羧甲基纤维素-丙烯酸接枝共聚物,即为改性 CMC.将所得到的改性CMC进行酶解和碱洗,计算接枝率.接枝率是评价接枝反应的一个重要指标,接枝率越高,则接枝上去的丙烯酸的量就越多,表明改性效果越好.
称取利用上述方法所得到的接枝共聚物,加入一定量(质量为接枝共聚物的 0.3~0.5%)的纤维素酶(用磷酸缓冲溶液调节 pH值为 4.5),在35℃环境下酶解4h.然后放入温度为60℃、浓度为0.1mol/L的NaOH水溶液中洗涤三遍,再用超纯水洗至中性,悬挂于100℃的烘箱中2~3h,再在干燥器中冷却到室温,并准确称重,计算接枝前后的重量增加率即为接枝率[7].
接枝率G根据以下公式计算:
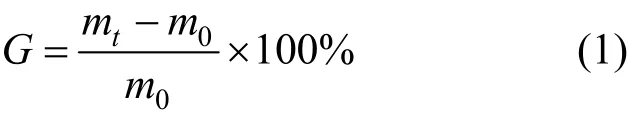
式中: G为接枝率; mt为接枝后共聚物的质量, g; m0为接枝前共聚物的质量,g.
接枝率G为65%以上时,即为符合要求.为了提高CMC的反应接枝率,分别就反应温度、单体质量浓度、CMC与AA的质量比、反应时间对接枝率的影响作了试验研究,试验表明:在温度为70~80℃、单体质量浓度为30%~35%、羧甲基纤维素:丙烯酸(质量比)为 10:2.5、反应时间为3.5~4h条件下,CMC改性效果较好,接枝率可达68%以上.
1.2.2 改性 CMC对铀的吸附性能试验 吸附容量测定:准确称取 10mg改性 CMC,分别加入3.27mg/L模拟含铀溶液100mL于250mL锥形瓶中,25℃下置于振荡器中,以150r/min振荡1h,然后于聚丙烯离心管中,离心过滤,测定溶液中铀平衡浓度.改性CMC吸附铀的平衡吸附量(qe)根据式(2)计算:

式中: c0、ce分别为溶液中铀的初始浓度和吸附平衡浓度, mg/L; v为溶液体积, mL; m为改性CMC的质量, g.
改性 CMC对铀的吸附等温线测定:分别取10mg改性CMC置于250mL锥形瓶中,加入一系列不同浓度的含铀溶液100mL,调节溶液pH值为5,分别放入20℃、25℃和30℃恒温摇床中振荡 1h,吸附平衡后立即离心过滤,测定溶液中铀的平衡浓度.
改性CMC对铀的吸附动力学:分别取10mg改性CMC置于250mL锥形瓶中,加入3.27mg/L的含铀溶液100mL,调节溶液pH为5,将锥形瓶放入恒温摇床中 25℃下振荡,时间分别为10,20,30,60,150和210min,吸附平衡后立即离心过滤,测定溶液中铀的平衡浓度.
溶液pH对改性CMC吸附铀的影响:考虑到因铀金属离子在pH过大的情况下会发生沉淀作用的情况,故取含铀质量浓度为3.27mg/L的模拟废水溶液700mL,平均转入到7个250mL锥形瓶中,调节 pH值分别为 2.00,2.73,3.50,4.00,5.00, 6.00和7.50,并分别加入10mg改性CMC,在25℃下振荡反应1h后离心过滤,测定溶液中铀的平衡浓度.
2 结果与讨论
2.1 改性CMC对铀的吸附等温线
本试验用 Langmuir等温吸附方程和Freundlich等温吸附方程拟合改性CMC对废水中铀的吸附过程,结果见图1和图2.
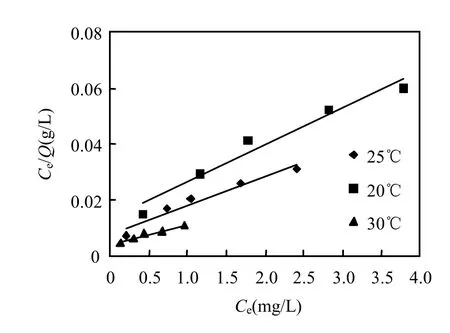
图1 Langmuir 等温吸附曲线Fig.1 Langmuir isothermal adsorption curve
Langmuir等温吸附方程:

Freundlich等温吸附方程:
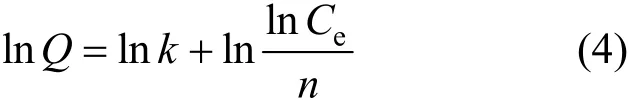

图2 Freundlich 等温吸附曲线Fig.2 Freundlich isothermal adsorption curve

式中: qt为t时刻的吸附量,mg/g;qe为平衡态时的吸附量,mg/g; k1为准一级吸附速率常数,min-1.
2.2.2 复合二级反应动力学方程[9-10]铀在吸附过程中,一方面铀离子向反应界面扩散,与改性CMC表面发生络合反应;另一方面铀离子可进一步向改性CMC内部扩散,发生交换反应.溶液中被吸附的金属铀离子可用如下复合二级反应动力学方程来描述:
图1、图2表明Langmuir 等温吸附方程和Freundlich 等温吸附方程均可描述改性CMC对铀的等温吸附行为,R2分别为 0.9638、0.9485、0.9696和0.9834、0.9772、0.9759,但Freundlich等温吸附方程中的 R2大于 Langmuir 等温吸附方程中的R2,说明改性CMC对铀的吸附是以表面为主要吸附位,并不是均匀的单层吸附.
2.2 改性CMC对铀的吸附动力学
通过准一级、复合二级和Elovich动力学方程对改性 CMC吸附铀的动力学数据进行拟合,研究改性CMC吸附铀的机理.
2.2.1 准一级吸附模型 采用Lageigren方程计算吸附速率[8]:

式中: [M]0和[M]s分别表示金属离子在溶液相和界面相中的浓度;kd为二级反应速度常数,则有:

2.2.3 Elovich动力学方程 Elovich[11-12]动力学方程描述了吸附速率随吸附剂表面吸附量的增加而成指数下降,其简化数学表达式为:

式中:Eα为初始吸附速率常数, mg/(g·min); βE为脱附速率常数,g/mg.
试验结果见图3、图4、图5和图6.

图3 25℃下,反应时间对铀吸附效果的影响Fig.3 Effect of contact time on adsorption of U at 25℃

图4 改性CMC吸附铀的准一级吸附动力学拟合曲线Fig.4 The pseudo-first-order reaction dynamic fitting curve of modified CMC
由图3可看出,在实验前30min内,随着反应时间的增加,吸附量显著上升,在 30min时改性CMC吸附量已达到28.62mg/g,此阶段的反应极快,主要原因是铀离子和改性 CMC表面官能团之间的吸附;反应时间超过60min后,吸附量变化不大,100min时吸附反应基本达到平衡.
图4、图5和图6表明,在相同初始浓度下,准一级方程拟合相关系数R2高于相对应的复合二级方程与Elovich方程,为0.9618,这说明改性CMC对铀的吸附动力学过程中,铀离子主要是被改性CMC表面吸附,与改性CMC表面的官能团之间发生络合反应,形成络合物.

图5 改性CMC吸附铀的复合二级反应动力学拟合曲线Fig.5 The composite-second-order reaction dynamic fitting curve of modified CMC

图6 改性CMC吸附铀的Elovich动力学拟合曲线Fig.6 The Elovich dynamic fitting curve of modified CMC
2.3 溶液pH对改性CMC吸附铀的影响
由图7可见,在铀初始质量浓度、改性CMC投加量、反应时间、温度等因素不变的情况下,在 pH值较低的情况下,随着 pH值的升高,改性CMC对铀的去除率呈上升趋势,即当pH值小于3.50时,去除率增加的速度较快,表明吸附效率有较陡势的提高; pH值在4~5之间去除率有较小幅度平缓升高的趋势;在 pH5.0时,溶液中铀的去除率达到最大值为 97.1%;此后随着 pH值的增大,改性CMC对铀的去除率开始缓慢下降.说明在酸性条件有利于改性CMC对铀的吸附,这与铀的性质有关.在酸性条件下铀以 UO22+形式存在,大量H+的存在减小了CMC聚合物胶体碳链之间的排斥作用,使 CMC聚合物胶体变得紧密,从而降低了对UO22+的保蓄作用,加强了铀与改性CMC表面的官能团之间的络合反应;在碱性条件下,铀以UO2OH+形式存在,更多的羧基和羟基负电荷被H+占据,使CMC聚合物对金属铀吸附能力降低.

图7 pH值对吸附效果的影响Fig.7 Effect of pH on uranium adsorption
2.4 吸附热力学计算
吸附过程的热力学参数 Δ G0通过式(9)计算,Δ H0和ΔS0通过式(10)计算[13]:
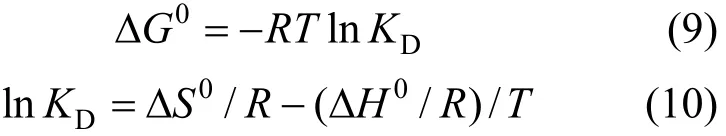
式中:Δ S0,Δ H0分别为吸附熵变, J/(mol·K)和吸附焓变, J/mol; R 为通用气体常数8.314J/(mol·K); 为热力学温度,K.
热力学参数可以通过不同温度下的热力学平衡常数KD进行计算. KD可以通过式(11)进行计算而得[14-15]:

ΔS0和 Δ H0可由lnKD对1/T作出的斜率和截距求得,铀在改性CMC上吸附的lnKD与1/T的拟合曲线如图8所示.线性方程的相关系数R2分别为0.9697、0.993、0.999.

图8 改性CMC吸附铀的lnKD与1/T的相关关系曲线Fig.8 The curve of relation between lnKD and 1/T of modified CMC

表1 改性CMC对铀吸附热力学参数Table 1 Thermodynamic parameters of modified CMC
热力学参数见表 1,吸附吉布斯自由能 ΔG0的值为负数,表明吸附反应是自发的过程.温度越高, ΔG0的值越小,升温有利于吸附反应; 焓变ΔH0为正值,改性CMC对铀的吸附过程是吸热过程,吸附是以物理吸附为主,铀离子主要与改性CMC表面上的羧基、羟甲基等官能团发生了离子交换反应.
3 结论
3.1 在温度为 70~80℃、单体质量浓度为30%~35%、羧甲基纤维素:丙烯酸(质量比)为10:2.5、反应时间为3.5~4h条件下,CMC改性效果最好,接枝率可达68%以上.
3.2 在改性 CMC质量浓度为 0.10g/L,温度为25℃,pH值为5.0,反应时间60min的条件下,对废水中铀去除率达到了97.1%.
3.3 Freundlich等温吸附方程较好地描述了改性CMC对铀的等温吸附行为,表明改性CMC对铀的吸附主要是以表面为主要吸附位,并向改性CMC内部扩散,发生交换反应,不是均匀的单层吸附.
3.4 动力学研究表明,准一级方程能较好地描述改性 CMC对铀的吸附动力学行为,R2为0.9618.铀离子主要与改性CMC表面官能团之间发生络合反应,形成络合物,而被改性CMC吸附.
3.5 热力学研究表明,改性CMC对铀的吸附吉布斯自由能(ΔG0)<0,而焓变(ΔH0)>0,改性 CMC对铀的吸附是自发的吸热反应过程.
[1] 李小燕,张 叶.放射性废水处理技术研究进展 [J]. 铀矿冶, 2010,29(3):153-155.
[2] 唐志坚,张 平,左社强.低浓度含铀废水处理技术的研究进展[J]. 工业用水与废水, 2003,34(4):9-12.
[3] 陈朝猛,曾光明,汤 池.羟基磷灰石吸附处理含铀废水的研究[J]. 金属矿山, 2009,295(5):135-137.
[4] Fang F, Satulovsky J, Szleifer I.Kinetics of protein adsorption and desorption on surfaceswith grafted polymers [J]. Biophysical Journal, 2005,89(3):1516-1533.
[5] GB6768-86 水中微理铀分析方法 [S].
[6] 刘作新,曲 威,苗永刚,等. CMC聚合物对重金属离子的吸附性能 [J]. 中国科学院研究生院学报, 2009,26(5):627-632.
[7] 马 静,赵妍嫣.羧甲基纤维素钠与丙烯酰胺的接枝共聚及其缓释性质研究 [J]. 农产品加工(学刊), 2006,10(10):157-158.
[8] Vieira R S, Beppu M M. Dynamic and static adsorption and desorption of Hg(II) ions on chitosan membranes and spheres [J]. Water research, 2006,40:1726–1734.
[9] 熊正为,王清良,郭成林.蒙脱石吸附铀机理实验研究 [J]. 湖南师范大学自然科学学报, 2007,30(3):75-79.
[10] 李明玉,陈伟玲,任 刚,等.改性聚合硫酸铁去除微污染水中Pb2+的影响因素 [J]. 中国环境科学, 2010,30(1):42-45.
[11] El Samrani A G, Lartiges B S, Villiéras F. Chemical coagulation of combined sewer overflow: Heavy metal removal and treatment optimization [J]. Water Research, 2008,42(4/5):951-960.
[12] Tutem E, Apak R, Unal C F. Adsorptive removal of chlorophenols from water by bituminous shale [J]. Water Res., 1998,32: 2315-2324.
[13] Smith J M, Van Ness H C. Introduction to chemical engineering thermodynamics [M]. 4th ed., Singapore: McGraw-Hill, 1997.
[14] Ho Y S. Removal of copper ions from aqueous solution by tree ferm [J]. Water Research, 2003,37(10):2323-2330.
[15] Ho Y S, Huang C T, Huang H W. Equilibrium sorption isotherm for metal ions on tree ferm [J]. Process Biochemistry, 2002, 37(12):1421-1430.
Equilibrium, kinetic and thermodynamic study of the adsorption of uranium (VI) onto modified CMC.
ZHOU Shu-kui1,2*, ZENG Guang-ming1, LIU Ying-jiu2, YANG Jin-hui2,JIANG Hai-yan2(1.College of Environmental Science and Engineering, Hunan University, Changsha 410082, China;2.School of Urban Construction, University of South China, Hengyang, 421001, China). China Environmental Science, 2011,31(9):1466~1471
The acrylic acid(AA)-modified carboxymethyl cellulose(CMC) resin was prepared and was explored to adsorb uranium(VI) ions from aqueous solution in a batch system. The experimental results showed that on the condition of reaction temperature 70~80 ℃, CMC 30%~35% (w/w), CMC to AA (w/w) of 10:2.5 and reaction time 3.5~4h, the modification effect was the best. High removal efficient of U(VI) was obtained 97.1% at temperature of 25℃ , pH value of 5.0, dosage of modified CMC resin 0.1 g/L and contact time of 60 min. It was found that the adsorption process was best described by Freundlich model and pseudo-first-order kinetic model (R2=0.9618), indicating that the adsorption was mainly on the surface of the resin. Thermodynamics parameters of negative value of ΔG0and positive value of ΔH0revealed the spontaneity and endothermic nature of the adsorption. The adsorption was primarily due to physical adsorption.
modified carboxymethyl cellulose (CMC);adsorption mechanism;uranium
X703.5
A
1000-6923(2011)09-1466-06
2011-02-18
国家自然科学基金资助项目(50608028,51174117);湖南省科技厅项目(06JT1002,2010FJ4121)
* 责任作者, 副教授, zhoushukui@usc.edu.cn
致谢:本实验得到了南华大学湖南省高校重点实验室—污染控制与资源化技术实验室及实验人员的大力支持,在此表示感谢.
周书葵(1965-),男,湖南浏阳人,副教授,湖南大学环境科学与工程学院博士研究生,主要从事水处理工程与技术、放射性废物监测与治理.发表论文30余篇.
