强极性化合物DMC及其杂质的HILIC分离方法研究
2011-12-20韩冰冰王翠翠李新军邹新琢
韩冰冰, 王翠翠, 李新军, 邹新琢
(华东师范大学 化学系,上海 200062)
强极性化合物DMC及其杂质的HILIC分离方法研究
韩冰冰, 王翠翠, 李新军, 邹新琢
(华东师范大学 化学系,上海 200062)
建立以亲水作用色谱法对强极性化合物甲基丙烯酰氧乙基三甲基氯化铵(DMC)及其杂质进行分离分析的方法.使用Sepax HP-Cyano和X-Bridge HILIC两种不同的亲水作用色谱柱,以乙腈和水为流动相进行梯度洗脱,高效快速地实现了DMC及其所含杂质的分离分析.通过这两种色谱柱,共可以分离出甲基丙烯酸二甲氨基乙酯(DM)、甲基丙烯酸(MAA)、三甲基羟乙基氯化铵(CC)和对羟基苯甲醚(MQ)4种杂质.该方法具有较好的实用价值,能有效地应用于强极性化合物的分离和分析中.
亲水作用色谱; 甲基丙烯酰氧乙基三甲基氯化铵; 强极性化合物; 分离
0 引 言
甲基丙烯酰氧乙基三甲基氯化铵(Methacryloyloxyethyl Trimethyl Ammonium Chlo-ride,DMC)是一种具有碳碳双键和季铵基的双官能团化合物.它可以作为单体通过均聚或与其它乙烯基单体共聚反应来合成各种阳离子型功能聚合物,被广泛应用于污水处理、造纸和石油开采等领域[1].
DMC的合成方法如图1所示,一般是以甲基丙烯酸甲酯(MMA)为原料,通过和N,N-二甲基氨基乙醇(DMAE)的酯交换反应得到甲基丙烯酸二甲氨基乙酯(DM),进一步经季铵化反应得到DMC.为防止聚合等副反应的发生,通常会在反应中加入少量的如对羟基苯甲醚(MQ)等阻聚剂.两步反应为连续过程,因此最终产物中往往会含有少量上述物质及在反应过程中产生的一些如甲基丙烯酸(MAA)、三甲基羟乙基氯化铵(CC)等其他杂质.这些杂质对DMC在下步的聚合反应中影响很大,因此DMC及其杂质的分离分析方法对于DMC的合成、生产及质量监控等有重要意义.

图1 DMC的合成Fig.1 Synthesis of DMC
液相色谱分析对易聚合的DMC来说是优选的分析方法.但由于DMC及其所含的杂质大都是强极性物质,而且性质极其相似.以C18为代表的反相液相色谱(Reversed Phase Liquid Chromatography,RPLC)分析是当前分离分析中应用最为广泛和常规的色谱模式.RPLC能对弱极性和中等极性化合物进行高效分离分析,但对于如DMC这样存在多种强极性物质的分析对象却难以得到满意的结果[2].因为强极性化合物分子中的极性基团易与流动相形成偶极矩作用,而与非极性的固定相则缺乏这种作用,导致样品难以或不被固定相保留,通常在死时间流出而无法达到彼此间的有效分离[3].
强极性有机小分子在天然产物、合成药物和各种有机中间体中广泛存在.由于其强极性部分在分子中所占的比例高,因此彼此间相似度高,分离难度很大.用亲水作用色谱法(Hydrophilic Interaction Liquid Chromatography,HILIC)来分离强极性化合物是近年来色谱研究的热点领域之一.HILIC是一种以极性固定相(如硅胶或修饰氨基、氰基和羟基等极性基团的硅胶柱等),极性有机溶剂或含水极性有机溶剂为流动相的色谱模式[4].与传统正相液相色谱(Normal Phase Liquid Chromatography,NPLC)相似,化合物的保留时间随化合物极性的增强而增加,但其所用的溶剂又与RPLC相似,采用与水互溶的极性有机溶剂(通常为乙腈),这样就可以解决正相色谱中水溶性物质不溶于流动相的问题.HILIC作为一种非常适合于强极性化合物定性定量分析的液相色谱新技术,自1990年被Alpert[5]提出以来,就广受重视,并在天然产物的分离分析、药物分析和蛋白质组学等领域得到广泛的应用[6-8].
本文尝试采用HILIC方法,通过比较不同的色谱柱,选择合适的流动相及其它相关色谱条件,辅以高分辨质谱联用(HILIC-HRMS)等方法,展开对强极性化合物DMC及其杂质的分离方法研究,提出了它的一种新的分离分析方法,也希望对类似的强极性有机小分子的分离提供参考.
1 实验部分
1.1 仪器与试剂
色谱仪 Waters高效液相色谱仪,包括Waters 2487 DualλAbsorbance Detector、Waters Binary HPLC Pump、Waters Breeze工作站.
色谱柱 美国Sepax公司赛分Sepax HP-Cyano(4.6 mm×250 mm,5μm)色谱柱;美国 Waters公司X-Bridge HILIC(4.6 mm×150 mm,3.5μm)色谱柱.
质谱仪 Agilent 1100 LC-MSD液质联用仪.选用 Waters公司ACQUITY UPLC(BEH HILIC)(2.1 mm×50 mm,1.7μm)超高效液相色谱柱,并与质谱联用.
试剂 水为超纯水(艾科浦超纯水系统),乙腈为色谱纯,二丁胺、磷酸、乙酸铵和乙酸均为市售分析纯试剂,流动相使用前用0.45μm滤膜过滤,并经超声脱气.MQ、MAA、DM和CC均为市售分析纯试剂,DMC样品(80%水溶液,某公司提供).
1.2 色谱条件
1.2.1 使用Sepax HP-Cyano(4.6 mm×250 mm,5μm)色谱柱 参考了文献[9]的色谱分析条件,流动相A为超纯水(0.01 mol/L二丁胺,用磷酸调节pH至3),流动相B为乙腈,流速为1 mL/min,柱温为室温,进样量为20.0μL,检测波长为224 nm,梯度洗脱条件为如表1所示.

表1 Sepax HP-Cyano柱的梯度洗脱条件Tab.1 Gradient condition with Sepax HP-Cyano column
1.2.2 使用 X-Bridge HILIC(4.6 mm×150 mm,3.5μm)色谱柱 流动相 A为乙腈(取300 mL加入0.12 mL乙酸),流动相 B为乙腈(0.005 mol/L乙酸铵,取300 mL加入0.12 mL乙酸),流速为0.8 mL/min,柱温为室温,进样量为20.0μL,检测波长为224 nm,梯度洗脱条件如表2所示.

表2 X-Bridge柱的梯度洗脱条件Tab.2 Gradient condition with X-Bridge column
1.2.3 质谱联用的色谱条件 使用 ACQUITY UPLC(BEH HILIC)(2.1 mm×50 mm,1.7μm)超高效液相色谱柱,流动相A为乙腈,流动相B为含10 mmol/L乙酸铵的乙腈,流速为0.4 mL/min,柱温为室温,进样量为5.0μL,检测波长为224 nm,梯度洗脱条件如表3所示.

表3 ACQUITY UPLC(BEH HILIC)柱的梯度洗脱条件Tab.3 Gradient condition with ACQUITY UPLC(BEH HILIC)column
1.3 溶液的制备
用微量移液器准确移取DMC样品1 mL于100 mL容量瓶中,加入流动相A定量稀释至刻度后摇匀,经超声脱气处理后待用.液体样品均用此法配置.
取MQ等各对照品适量,精密称定,加入流动相A溶解并定量稀释成1 mg/mL的溶液,经超声脱气处理后待用.其他固体样品均用此法配置.
2 结果与讨论
首先,我们尝试采用美国Sepax公司的赛分HP-Cyano(4.6 mm×250 mm,5μm)柱作为HILIC色谱柱.由于该柱的硅胶填料上键合了强极性的氰基柱,理论上它可以加强极性化合物与固定相的作用,提高极性化合物的保留时间,增强极性化合物的分离效果.
考虑到DMC及其大多数杂质只有低波长的紫外吸收,选择224 nm作为检测波长,在相应的色谱条件下对MDC样品进行检测,分离得到5个主要的色谱峰(见图2).用标准样品的叠加法或根据与各标准样品的色谱图的比较,确定了其中4个峰的归属:2.72 min处为甲基丙烯酸二甲氨基乙酯(DM)峰;3.39 min处为DMC主峰;5.31 min处为甲基丙烯酸(MAA)峰;7.95 min处为阻聚剂对羟基苯甲醚(MQ)峰.
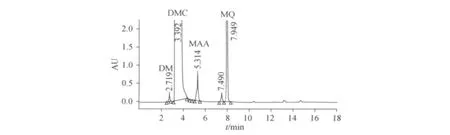
图2 80%DMC样品溶液的Sepax HP-Cyano柱检测图(检测波长224 nm)Fig.2 Chromatogram of the 80%DMC sample solution with UV detection
采用Sepax HP-Cyano柱的HILIC分析方法,在80%DMC样品中,除了DMC之外,还成功地分离检测到3个微量的强极性杂质:甲基丙烯酸二甲氨基乙酯(DM)、甲基丙烯酸(MAA)和对羟基苯甲醚(MQ).7.49 min峰与上述在反应中可能产生的各杂质样品无一重叠,无法归属.为了考察其它类型亲水色谱柱的分离分析效果,本文又尝试了另一种新型的亲水色谱柱X-Bridge.
X-Bridge HILIC柱是Waters公司近年来推出的新产品,由于其在硅胶骨架上引进了部分亚乙基桥,即有机-无机杂化硅胶,亚乙基桥的存在使硅氧键不易被水解,从而使该色谱柱对高pH值的碱性物质具有极好的耐受性和机械强度,提高了分析条件的稳定性及柱子的使用寿命.X-Bridge HILIC柱可以为强极性化合物提供合适的保留,如强极性碱或含胺的极性有机物等,同时又和多种检测器,尤其是质谱(MS)有良好的兼容性.和RPLC-MS相比,HILIC-MS的灵敏度较高,对含大量组分的复杂样品的分析能力可与RPLC-MS互补,适用于分析那些在RPLC柱上无法保留的强极性代谢物组分.
采用X-Bridge HILIC(4.6 mm×150 mm,3.5μm)柱,选择224 nm作为检测波长.按实验部分所述的色谱条件对MDC样品进行检测,分离得到了5个主要的色谱峰(见图3).用标准样品的叠加法或根据与各标准样品的色谱图的比较,我们分别确定了4个峰的归属:1.36 min处为甲基丙烯酸二甲氨基乙酯(DM)峰;2.51 min处为DMC主峰;4.09 min处为三甲基羟乙基氯化铵(CC)峰;8.17 min处为对羟基苯甲醚(MQ)峰.

图3 80%DMC样品溶液的X-Bridge HILIC柱检测图(检测波长224 nm)Fig.3 Chromatogram of the 80%DMC sample solution with UV detection
在此基础上,选用 Waters公司与X-Bridge HILIC柱同类型的 ACQUITY UPLC(BEH HILIC)(2.1 mm×50 mm,1.7μm)超高效液相色谱柱,并与高分辨质谱仪联用,对DMC样品进行HILIC-HRMS的分离与分析,得到的色谱图如图4所示.

图4 80%DMC样品溶液的ACQUITY UPLC柱检测图(检测波长224 nm)Fig.4 Chromatogram of the 80%DMC sample solution with UV detection
由图4可知,分别在1.16,2.61,3.22,3.63和4.50 min处分离出5个峰,各分出的峰进行联机高分辨质谱检测.1.16 min的质谱图如图5所示,因为甲基丙烯酸二甲氨基乙酯(DM)的分子量计算值为157.110 3,其 [DM+H]+分子量计算值为158.118 1,推测该化合物为DM;2.61 min的质谱图如图6所示,因[DMC-Cl]+分子量计算值为172.133 8,推测该物为DMC;3.22 min和3.63 min的质谱图如图7所示,因[CC-Cl]+分子量计算值为104.107 5,推测该物为CC;4.50 min的质谱图如图8所示,因[MQ+H]+分子量计算值为125.060 3,推测该物为 MQ.

图5 t=1.16 min峰的质谱图Fig.5 Mass spectrum of 1.16 min

图6 t=2.61 min峰的质谱图Fig.6 Mass spectrum of 2.61 min

图7 t=3.22 min和t=3.63 min的质谱图Fig.7 Mass spectrum of 3.22 min and 3.63 min

图8 t=4.50 min峰的质谱图Fig.8 Mass spectrum of 4.50 min
HILIC-HRMS的分析结果和用X-Bridge柱的HILIC的分析结果大体相符.也得到了较好的分离效果,高分辨质谱检测确认了DM、DMC、CC及MQ4种成分.
3 结 论
DMC及其杂质均为强极性化合物,用常规的反相液相色谱法分离分析,较难取得好的分离分析效果.而采用亲水色谱柱Sepax HP-Cyano柱和X-Bridge HILIC柱对DMC及强极性其杂质进行HILIC分析,都取得了较好的分离分析效果.除了DMC之外,都各自可分离检测到3个微量的强极性杂质.同为亲水色谱柱,Sepax HP-Cyano柱和X-Bridge HILIC柱由于柱子填充物结构的不同,其分离效果也略有不同.Sepax HP-Cyano柱可有效地同时分离出甲基丙烯酸二甲氨基乙酯(DM)、甲基丙烯酸(MAA)和对羟基苯甲醚(MQ)3种微量的强极性杂质;而X-Bridge HILIC柱则可分离出甲基丙烯酸二甲氨基乙酯(DM)、三甲基羟乙基氯化铵(CC)和对羟基苯甲醚(MQ)3种微量的强极性杂质.两种不同的色谱柱的交替使用,可以对DMC及其可能所含的4种杂质进行有效的分离分析.该方法具有较好的实用价值,也为强极性有机小分子化合物的亲水作用色谱分离方法提供参考.
致谢:沃特世科技(上海)有限公司白旭先生协助进行色质联用分析.
[1] 朱明,赵仕林.甲基丙烯酰氧乙基三甲基氯化铵的合成 [J].四川师范大学学报:自然科学版,2002,25(4):397-399.
ZHU M,ZHAO S L.Synthesis of methacryloyloxyethyl trimethyl ammonium chloride[J].Journal of Sichuan Normal University:Natural Science,2002,25(4):397-399.
[2] 郭志谋,张秀莉,徐青,等.亲水作用色谱固定相及其在中药分离中的应用[J].色谱,2009,27(5):675-681.
GUO Z M,ZHANG X L,XU Q,et al.Stationary phases for hydrophilic interaction liquid chromatography and their applications in separation of traditional Chinese medicines[J].Chinese Journal of Chromatography,2009,27(5):675-681.
[3] 王媛,顾惠新,路鑫,等.以亲水作用色谱为核心的液相色谱联用技术及其应用研究[J].色谱,2008,26(6):649-657.
WANG Y,GU H X,LU X,et al.Development of hydrophilic interaction chromatographic hyphenated techniques and their applications[J].Chinese Journal of Chromatography,2008,26(6):649-657.
[4] KEGAMI T,TOMOMATSU K,TAKUBO H,et al.Separation efficiencies in hydrophilic interaction chromatography[J].Journal of Chromatography A,2008,1184(1-2):474-503.
[5] ALPERT A J.Hydrophilic-interaction chromatography for the separation of peptides,nucleic acids and other polar compounds[J].Journal of chromatography,1990,499:177-96.
[6] JANDERA P.Stationary phases for hydrophilic interaction chromatography,their characterization and implementation into multidimensional chromatography concepts[J].Journal of Separation Science,2008,31(9):1421-1437.
[7] JINNO K,QUIMING N S,DENOLA N L,et al.Modeling of retention of adrenoreceptor agonists and antagonists on polar stationary phases in hydrophilic interaction chromatography:a review[J].Analytical and Bioanalytical Chemistry,2009,393(1):137-153.
[8] NGUYEN H P,SCHUG K A.The advantages of ESI-MS detection in conjunction with HILIC mode separations:fundamentals and applications[J].Journal of Separation Science,2008,31(9):1465-1480.
[9] HUNKELER D,NI H,HERNANDEZ-BARAJAS J,et al.HPLC analysis of mixtures of acrylamide and cationic quaternary ammonium monomers[J].International Journal of Polymer Analysis and Characterization,1996,2(4):409-423.
Research on separation method of highly polar compound DMC and impurities in it by HILIC
HAN Bing-bing, WANG Cui-cui, LI Xin-jun, ZOU Xin-zhuo
(Department of Chemistry,East China Normal University,Shanghai 200062,China)
HILIC method was established to separate and analyze highly polar compound methacryloyloxyethyl trimethyl ammonium chloride(DMC)and its impurities.Using two different chromatographic columns:HP-Cyano column and X-Bridge HILIC column,highly polar compound DMC and its impurities were all well separated by gradient elution using acetonitrile and water as mobile phase.With the two different chromatographic columns,four impurities in DMC were separated,such as dimethylaminoethyl methacrylate(DM),methacrylic acid(MAA),choline chloride(CC)and Hydroquinone monomethyl ether(MQ).This method has higher practical value,which can be used effectively in separated highly polar compounds.
hydrophilic interaction liquid chromatography(HILIC); methacryloyloxyethyl trimethyl ammonium chloride(DMC); highly polar compounds; separation
O657.7+2
A
10.3969/j.issn.1000-5641.2011.06.016
1000-5641(2011)06-0132-07
2010-12
韩冰冰,女,硕士研究生,研究方向为精细有机合成.
邹新琢,男,教授,博士生导师,研究方向为精细有机合成.E-mail:xzzou@chem.ecnu.edu.cn.
