响应面法优化大黄附子药对中蒽醌类成分的提取工艺
2011-12-19叶良红朱红云李芸霞
叶良红,朱红云, 李芸霞
大黄附子相互配伍应用首见于《金匮要略》大黄附子汤,是体现中医用药特色—中药配伍的代表药对之一。大黄苦寒攻下泄热,附子辛热散寒,寒热并用,相反相成,首创温下先河。主寒实内结证。寒实内结者,非温不能散其寒,非下不能去其积。而方中大黄性苦寒,不宜用之,但得附子之辛热,则大黄苦寒之性被制,而泻下之用犹存,共奏温下之功。附子、大黄是温下的经典药对,治寒实证用大黄就是去性取用[1]。本实验采用响应曲面法对大黄附子药对中游离蒽醌和结合蒽醌的提取工艺进行优化,以便对该药进行进一步研究。
1 仪器与材料
Varian-210高效液相色谱仪(瓦里安公司);K Q5200E型超声机 (昆山市超声仪器有限公司),频率为40khz;大黄素对照品(中国药品生物制品检定所,批号:110756-200110);大黄酸对照品(中国药品生物制品检定所,批号:110757-200206);大黄素甲醚对照品(中国药品生物制品检定所,批号:110758-200912);大黄酚对照品(中国药品生物制品检定所,批号:A0046);芦荟大黄素对照品(中国药品生物制品检定所,批号:110795-200806)。HPLC所用溶剂均为色谱纯,所用水为乐百氏纯净水,论文中涉及的其他试剂均为分析纯。大黄,附子购自同仁堂大药房,拣选清洗,粉碎,过四号筛。
2 方法
2.1 色谱条件
色谱柱为Hypersil ODS C18柱 (250mm×4.6mm,5µm);流动相为乙醇:1%冰醋酸水溶液(70:30,v/v); 流速为1.0mL.min-1;柱温为35 ℃;进样量为20μL;测定波长为254nm。
2.2 标准溶液的制备
精密称取大黄酸、大黄素、芦荟大黄素、大黄酚、大黄素甲醚对照品适量,分别置于五个25mL容量瓶中,用色谱甲醇稀释至刻度,得对照品储备液。取各储备液适量配成一系列不同质量浓度的混合对照品工作液。进样测定,以浓度C为横坐标,峰面积A为纵坐标,进行线性回归,得到芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚的标准曲线方程、相关系数r2和线性范围(见表1)。
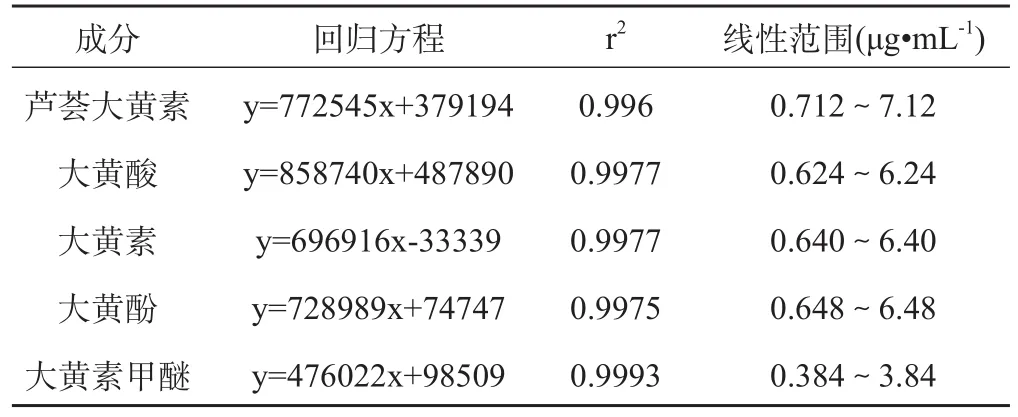
表1 5种蒽醌类成分的回归方程
2.3 精密度试验
日内精密吸取混合对照品溶液20μL,按HPLC条件,重复进样6次,结果各峰保留时间的RSD均2%,峰面积的RSD均1.4%。
2.4 重复性试验
按“2.2”项下方法平行制备配伍样品溶液5份,按“2.1”项色谱条件测定含量进行分析,结果表明5个指标成分保留时间RSD均1.3%,峰面积的RSD均1.6%。
2.5 稳定性试验
取统一混合标准品溶液,室温下放置,分别于0、2、4、8、12、24h内进样分析,结果表明5个指标色谱峰保留时间的RSD均1.1%,峰面积均1.5%,说明供试品溶液在24 h内基本稳定。
2.6 加样回收试验
取已知含量的大黄药材粉末0.5 g,附子药材1 g,加入适量大黄蒽醌类对照品,计算得平均加样回收率均在99.7%~100. 2%范围,RSD均在0.99%~1.95%范围。
2.7 含量测定
2.7.1 游离蒽醌的测定 根据参考文献[2~6]取2mL的供试品溶液,加10mL蒸馏水混匀,再加入10mL乙酸乙酯萃取,分取乙酸乙酯层,水层再用乙酸乙酯萃取2次,每次10mL,合并乙酸乙酯,挥干后残渣加甲醇溶解在25mL容量瓶中,按“2.1”项色谱条件测定含量。
2.7.2 结合蒽醌的测定 取“2.7.1”项剩余水层加2.5 mol•L-1的硫酸溶液20mL和10mL乙酸乙酯溶液水浴2h,放至室温,乙酸乙酯萃取3次,每次10mL,合并乙酸乙酯,挥干,残渣用甲醇定容在10mL容量瓶中,按“2.1”项色谱条件测定含量。
2.8 单因素试验
2.8.1 乙醇浓度对提取率的影响 根据参考文献[7]取一定量的大黄附子粉末各1g左右,分别按液料比10加入60%、70%、80%、90%、95%乙醇,50℃超声提取3次,每次25min,合并提取液,定容在50mL容量瓶中,用“2.7”项下含量测定方法分别测得游离蒽醌和结合蒽醌的含量。结果显示游离蒽醌和结合蒽醌的提取率随着乙醇浓度的增加先上升再下降,且都在70%时为最高。结果见图1、2。
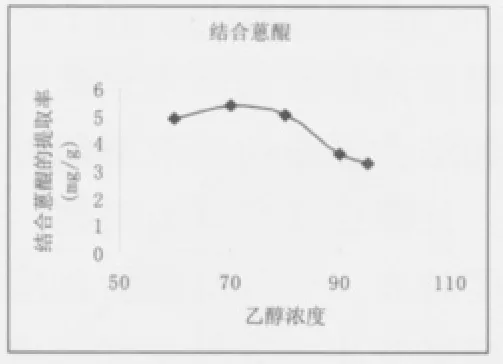
图1 乙醇浓度对结合蒽醌提取率的影响
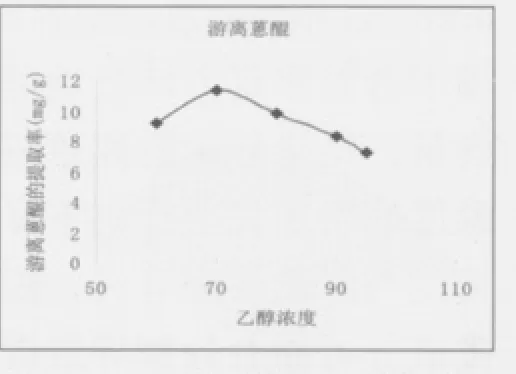
图2 乙醇浓度对游离蒽醌提取率的影响
2.8.2 料液比对提取率的影响 取一定量的大黄附子粉末各1g左右,分别按液料比5、8、10、12、15加入70%乙醇,50℃超声3次,每次25min,合并提取液,定容在50mL容量瓶中,用“2.7”项下含量测定方法分别测得游离蒽醌和结合蒽醌的含量。结果显示游离蒽醌和结合蒽醌的提取率随着乙醇用量的增加先上升再下降,在10mL左右时提取率最高。结果见图3、4。
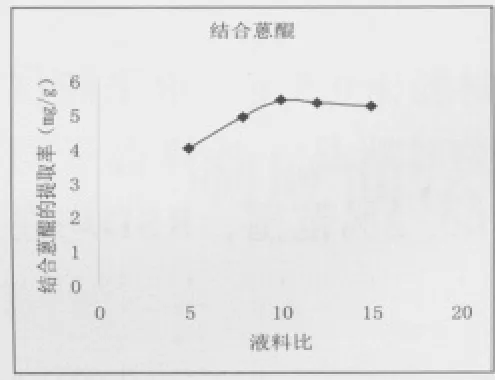
图3 液料比对结合蒽醌提取率的影响

图4 液料比对游离蒽醌提取率的影响
2.8.3 超声次数对提取率的影响 取一定量的大黄附子粉末各1g左右,分别按液料比10加入70%乙醇,50 ℃超声1、2、3、4、5次,每次25min,合并提取液,定容在50mL容量瓶中,用“2.7”项下含量测定方法分别测得游离蒽醌和结合蒽醌的含量。结果显示游离蒽醌和结合蒽醌的提取率随着超声次数的增加先上升,超声3次时基本达到最高,再增加超声次数,结合蒽醌的提取率无多大变化,游离蒽醌的提取率下降。结果见图5、6。
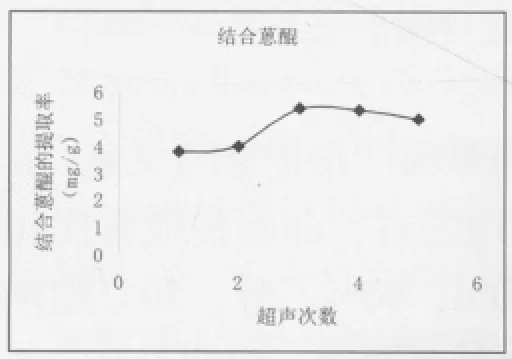
图5 超声次数对结合蒽醌的提取率的影响

图6 超声次数对游离蒽醌提取率的影响
2.8.4 超声温度对提取率的影响 取一定量的大黄附子粉末各1g左右,分别按液料比10加入70%乙醇,40℃、50℃、60℃、70℃、80℃超声3次,每次25min,合并提取液,定容在50mL容量瓶中,用“2.7”项下含量测定方法分别测得游离蒽醌和结合蒽醌的含量。结果显示游离蒽醌和结合蒽醌的提取率随着温度的增加先上升再下降,且都在50℃时为最高。可能与湿热效应有关,温度越高,一些敏感的蒽醌类成分可能会分解导致提取率变小。故温度宜选择50℃。结果见图7、8。
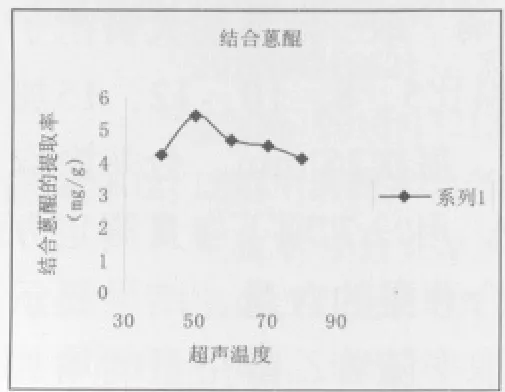
图7 超声温度对结合蒽醌提取率的影响
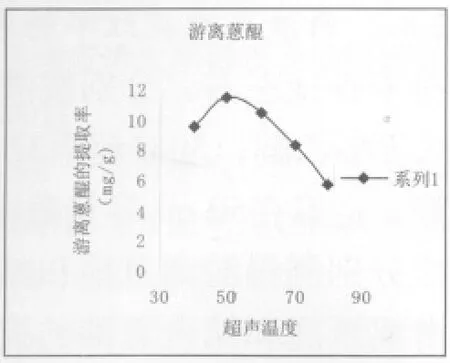
图8 超声温度对游离蒽醌提取率的影响
2.8.5 超声时间对提取率的影响 取一定量的大黄附子粉末各1g左右,分别分别按液料比10加入70%乙醇,50℃超声3次,每次15、20、25、30、35min,合并提取液,定容在50mL容量瓶中,用“2.7”项下含量测定方法分别测得游离蒽醌和结合蒽醌的含量。结果显示游离蒽醌和结合蒽醌的提取率随着超声时间的增加先上升,在超声25min左右提取率最高。结果见图9、10。

图9 超声时间对结合蒽醌提取率的影响

图10 超声时间对游离蒽醌提取绿的影响
所考察的因素中,对大黄游离和结合蒽醌的提取率的影响结果分析,选择超声次数,超声时间和液料比做响应面实验,而温度规定在50℃,乙醇浓度为70%。
2.9 响应面设计实验
2.9.1 实验因素与水平设计 根据响应面分析软件,以液料比、超声次数、超声时间为主要考查因素,分别用X1、X2、X3来表示,并以1、0、-1分别表示自变量的高低水平。分别以游离蒽醌、结合蒽醌的提取率为响应值。设计的实验因素和水平取值见表2。
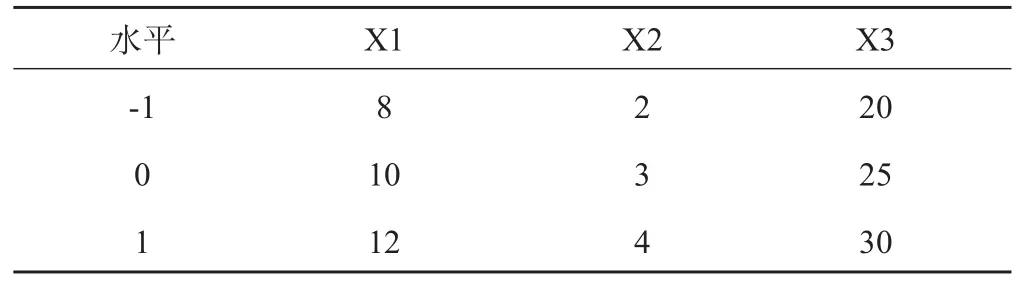
表2 因素与水平
2.9.2 响应面分析实验结果 分别以游离蒽醌和结合蒽醌的提取率为响应值,根据表3的结果,对其进行多元二次回归分析如表4和表5。从回归分析中可以看出一次项、二次项及交互项都有显著影响。各实验因子对响应值的影响呈显著的线性关系。实验因子对响应值的影响如下式:


表3 响应面曲线设计表及实验结果

表4 响应曲面模型分析及方差分析(游离蒽醌)

表5 响应曲面模型分析及方差分析(结合蒽醌)

A^2 0.2626 1 0.2626 2434.9972 < 0.0001 B^2 0.0912 1 0.0912 846.4437 < 0.0001 C^2 0.0793 1 0.0793 735.3806 < 0.0001 Residual 0.0008 7 0.0001 Lack of Fit 0.0005 3 0.0002 2.26190.2234 不显著
由表4和表5所示,超声时间、超声次数、液料比及其二次项对两种成分的提取率影响极显著。交互项也达到了显著水平。两个模型的决定系数R2值均为0.999,经拟合检验,p<0.0001差异极显著,说明该方程能够正确的反映提取量与超声时间、超声次数、液料比之间的关系。失拟检验p值分别为0.1531和0.2234,均大于0.05,说明本实验可代替试验真实点对实验结果进行分析。
通过响应面分析得到实验结果图11~图16,得到超声提取大黄附子药对中游离蒽醌的最佳条件为液料比10.31,提取次数3.53次,提取时间26.76min,在此条件下游离蒽醌的最佳提取量为11.629mg.g-1;结合蒽醌的最佳提取条件为液料比10.34,超声次数3.42次,超声时间24.25min,在此条件下的结合蒽醌的提取量为5.455mg.g-1。
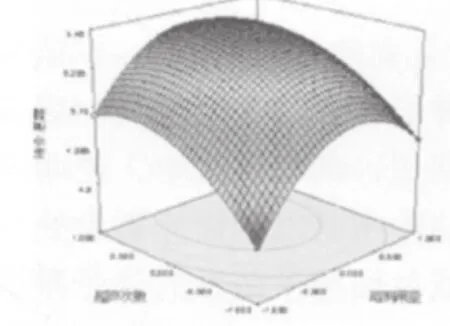
图11 溶剂用量和超声次数对结合蒽醌提取率的响应曲面图
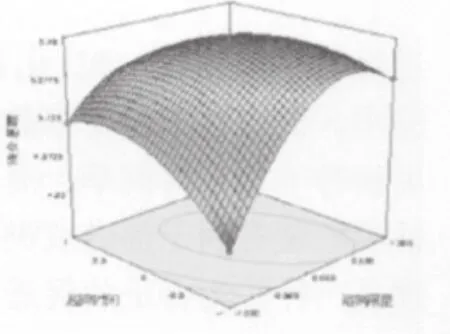
图12 溶剂用量和超声时间对结合蒽醌提取率的响应曲面图
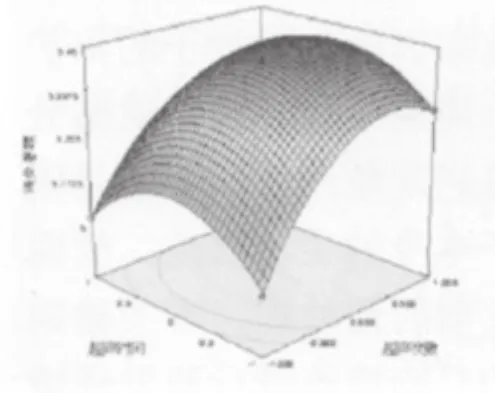
图13 超声时间和超声次数对结合蒽醌提取率的响应曲面图

图14 超声次数和液料比对游离 蒽醌提取率的响应曲图
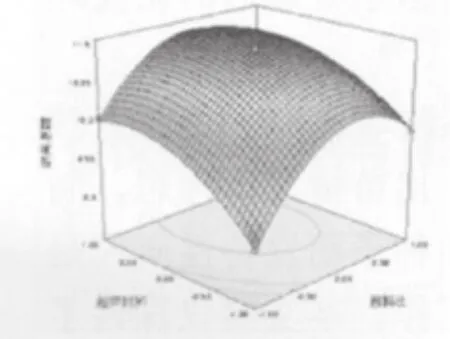
图15 超声时间和液料比对游离蒽醌提取率的响应曲面图

图16 超声时间和超声次数对游离蒽醌提取率的响应曲面图
为了验证响应面法的可靠性,采用最佳提取工艺条件进行5次平行超声提取验证试验,试验值与理论值相差0.87%和0.24%。因此通过响应曲面法优化得到的超声提取工艺条件参数是准确可靠,具有实用价值的。
3 讨论
在单因素实验的基础上,利用试验设计软件Design Expert设计了三因素三水平的中心组合设计,并对大黄附子的提取工艺进行了优化,建立了二次多项式的回归模型,拟合度良好。对模型进行分析,得到了最适提取工艺参数。游离蒽醌的最佳条件为液料比10.31,提取次数3.53次,提取时间26.76min。结合蒽醌的最佳提取条件为液料比10.34,超声次数3.42次,超声时间24.25min。验证实验表明所有优选出来的条件稳定性好,重复性高。本实验优选出来的实验条件对大黄附子药对中蒽醌类成分的进一步研究有指导意义。
[1]袁国卿,利顺欣.论仲景去性取用之立方方法[J].国医论坛,2004,19(4):2.
[2]吴振强,吴达荣,张鸿练.方药配伍对大黄附子汤的大黄酸提取率变化的影响[J].实用医技杂志,2005,12(12):3429.
[3]张海晖,裘爱泳,刘军海,等.超声技术提取大黄蒽醌类成分[J].中成药,2005,27(9):1075.
[4]韩燕全,洪燕,夏伦祝.高效液相色谱法同时测定黄琼抗栓胶囊中5种大黄成分的含量[J].中国中医药信息杂志,2010,17(6):47.
[5]杨跃龙.高效液相色谱法测定栀子金花丸中大黄素和大黄酚的含量[J].中国现代药物应用,2007,1(11):20.
[6]金林生,熊志立,李晓红,等.反相高效液相色谱法研究大黄附子配伍后化学成分含量的变化[J].中南药学,2009,7(4):252.
[7]何苗,陈钧.响应面法优化大黄游离蒽醌水解工艺[J].时珍国医国药,2009,20(4):988.
