一种新型 3-氧-戊基桥连双核 (C1-桥连二茂钛)的合成及其催化甲基丙烯酸甲酯聚合的研究*
2011-12-17仝水田莫海蓝肖孝辉
艾 文, 仝水田, 莫海蓝, 肖孝辉
(浙江师范大学化学与生命科学学院,浙江金华 321004)
茂金属催化剂中,2个茂环通过桥基连接形成桥连茂金属催化剂 (ansa-metallocene).桥基可以是各种碳链,也可以是含有硅、锗等杂原子的基团.桥基的引入使得 2个茂环不能以金属——茂环键为轴旋转,增加了分子的刚性[1],改变茂环取代基和桥连基团的结构,可以调节茂金属催化剂的催化活性和立体选择性.如:1988年,Ewen等[2]以Me2C为桥基的具有 Cs对称性的刚性桥连茂锆催化剂[Me2(Cp)(Flu)ZrCl2]/甲基铝氧烷(MAO)催化体系实现了丙烯的高活性间规立构聚合.双核茂金属化合物分子内具有 2个金属原子,不但具有单核茂金属催化剂的高活性和结构可控性等优点,同时,还由于金属之间的催化协同作用[3],在催化聚合反应中常表现出活性中心多样化、催化活性寿命长和聚合物分子量分布宽等特征[4].如:Alt等[5]合成了一系列硅烷链桥连双核二茂锆、二茚锆、二芴锆,发现在催化乙烯聚合时,随着亚甲基链的延长,催化活性逐渐增加,所得聚乙烯的分子量分布较宽,有的甚至呈现双峰分布.文献 [6]合成了桥中含联苯结构的双核二茚锆,在MAO作助催化剂催化乙烯聚合时表现出高活性,甚至在高温下也能保持较高的活性.文献[7]采用烯烃复分解反应,将含有烯丙基的单核茂金属化合物偶联成了含有硅桥连双核茂金属化合物.但近年来双核桥连茂金属化合物的研究仍主要集中在含硅桥连的双核茂金属化合物上,而有关双核 C1桥连茂金属催化剂的合成及其催化性能的研究报道极少.本文将报道一种新型3-氧-戊基桥连双核 (C1-桥连二茂钛)的合成方法及其催化甲基丙烯酸甲酯聚合的催化性能.
1 实验部分
1.1 原料
四氢呋喃、石油醚、甲苯和正己烷等溶剂用金属钠脱水,二苯甲酮作指示剂,加热回流至蓝紫色,随用随蒸;二氯甲烷用 CaH2干燥数天,随用随蒸;氯仿用无水 CaCl2干燥数天,随用随蒸;环戊二烯通过其二聚体在铁粉作用下裂解蒸馏所得,收集 40~42℃馏分;TiCl4(THF)2根据文献[8]合成;甲基铝氧烷 (MAO)是市售的含量为10%的甲苯溶液.其他原料均为化学纯试剂.
甲基丙烯酸甲酯 (MMA)的精制:用 5%NaOH溶液洗涤数次,直至无色,再用去离子水洗至中性,无水 Na2SO4干燥,然后在氮气保护及氯化钙存在下减压蒸馏.
1.2 测试方法
1H NMR,13C NMR通过核磁共振仪 (Bruker Avance 400)测定,以四甲基硅烷 (T MS)为内标,CDCl3为溶剂.聚甲基丙烯酸甲酯 (PMMA)的黏均分子量采用黏度法测定:以氯仿为溶剂,PMMA 0.02~0.03 g配制成 25 mL溶液,在 30℃下用乌式黏度计测定 P MMA溶液的特性黏度,再根据Mark-Hawink方程[9]计算出 P MMA的黏均分子量.PMMA的分子量分布采用凝胶渗透色谱(GPC)仪 (Waters-150-C-ALC)测定:紫外检测器,40℃,THF为流动相,标准 PMMA为标样,Q因子法校正.PMMA的立构规整度通过红外光谱 (Nexus 670)法确定:吸收率 D=lg(1/τ),τ为透射比 ,在红外谱图上直接读出相应吸收峰的透射比τ/%,计算 D1063cm-1/D1393cm-1和 D749cm-1/D757cm-1值,对照 PMMA立构规整度工作曲线[4],读出相应的 PMMA间同含量和全同含量.
1.3 催化剂的合成
1.3.1 亚环己基桥连二茂钛的合成
亚环己基桥连二茂钛 (Ⅲ)的合成[10]路线如图 1所示.
1.3.1.1 配体 (Ⅰ)的合成
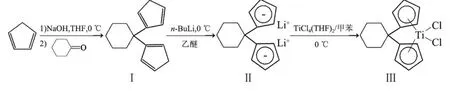
图 1 亚环己基桥连二茂钛 ([(CH2)5C](C5H4)2TiCl2,Ⅲ)的合成
在冰浴下,向反应瓶中依次加入颗粒状的NaOH(8 g,200 mmol),四氢呋喃 30 mL,新裂解的环戊二烯 (6.5mL,78mmol),自然升温至室温,搅拌 4 h后,加入环己酮 (4 mL,39 mmol),搅拌过夜,再加入 20 mL冰水淬灭反应,浓缩,乙醚萃取(3×20 mL),有机相水洗 (3×25 mL),无水硫酸钠干燥,过滤,浓缩,得到黑色油状物,柱色谱分离(洗脱剂:石油醚)得到配体 1,1-二环戊二烯基环己烷 (Ⅰ),黄绿色油状物,2.93 g,产率 35.4%.
1,1-二环戊二烯基环己烷 (Ⅰ)的1H NMR(CDCl3,δ/ppm):1.42~1.45(m,2H,CH2),1.49~1.54(m,4H,2CH2),1.92~1.94(m,4H,2CH2),2.77~2.79(m,2H,CH2),2.96~2.98(m,2H,CH2),6.00~6.06(m,2H,2CH),6.19~6.25(m,2H,2CH),6.34~6.46(m,2H,2CH).
1.3.1.2 配合物 (Ⅲ)的合成
在冰浴下,将正丁基锂溶液 (2.8 mL,2.5 mol/L)加入到配体Ⅰ(0.57 g,2.68 mmol)的乙醚(30 mL)溶液中,有白色固体生成,自然升温至室温,搅拌 3 h,离心后弃去上层清液,固体用乙醚(2×20 mL)洗涤,真空干燥,得到白色粉末状锂盐 (Ⅱ)0.53 g,产率 88.2%.
0℃,氮气保护下,将锂盐Ⅱ(0.53 g,2.36 mmol)分批加入到 TiCl4(THF)2(0.96 g,2.69 mmol)的甲苯 (30 mL)溶液中,溶液由黄色变成黑色,自然升温至室温,搅拌过夜,浓缩溶液,固体用CH2Cl2(3×20 mL)提取,合并提取液,浓缩至少量溶液,加入 20 mL正己烷,有棕褐色固体析出,过滤,固体用正己烷 (3×10 mL)洗涤,真空干燥,得到亚环己基桥连二茂钛 (Ⅲ)0.56 g,产率72.1%.
亚环己基桥连二茂钛 (Ⅲ)的1H NMR(CDCl3,δ/ppm):1.66(m,2H,CH2),1.77~1.78(m,4H,2CH2),2.26~2.27(m,4H,2CH2),5.65~5.66(m,4H,4CH),6.98~6.99(m,4H,4CH);13C NMR(CDCl3,δ/ppm):21.6,25.8,32.4,42.4,111.1,115.0,131.4.
1.3.2 3-氧 -戊基桥连双核 (C1-桥连二茂钛 )的合成
新型 3-氧-戊基桥连双核 (C1-桥连二茂钛)(Ⅷ)的合成路线如图 2所示.
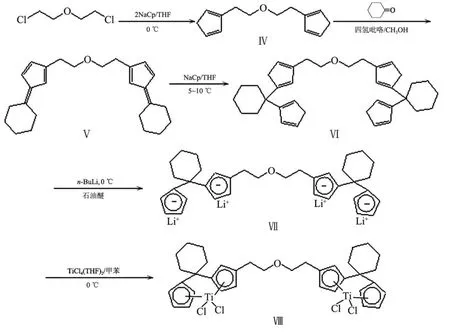
图 2 3-氧-戊基桥连双核 (C1-桥连二茂钛)({{[(CH2)5C](C5H3)(C5H4)TiCl2}CH2CH2}2O,Ⅷ)的合成
1.3.2.1 双富烯 (Ⅴ)的合成
在冰浴下,将 2,2′-二氯乙醚 (3.8 mL,31.97 mmol)滴加到环戊二烯基钠 (CpNa)的四氢呋喃溶液 (1.99 mol/L,32 mL)中,有白色沉淀产生,0.5 h内加完,自然升温至室温,继续搅拌 4 h,再加入 20 mL冰水,白色沉淀溶解,减压蒸馏浓缩,乙醚萃取 (3×20 mL),有机相水洗 (3×25 mL),无水硫酸钠干燥,过滤,浓缩,得黄色油状化合物2,2′-二 (环戊二烯基 )乙醚 (Ⅳ)6.02 g,产率89.8%.2,2′-二 (环戊二烯基 )乙醚 (Ⅳ)未经进一步纯化,直接用于下步反应.
向反应瓶中依次加入 2,2′-二 (环戊二烯基)乙醚 (Ⅳ)(6.02 g,29.73 mmol),环己酮 (6.2 mL,59.46 mmol),无水甲醇 20 mL,四氢吡咯(7.4 mL,89.19 mmol),室温下反应,薄层色谱法(石油醚作展开剂)跟踪,反应完后加入 20 mL冰水,浓缩除去大部分甲醇,乙醚萃取 (3×20 mL),有机相水洗 (3×25 mL),无水硫酸钠干燥,浓缩得橙黄色油状物,柱色谱分离 (洗脱剂:石油醚)得到双富烯 2,2′-二 (3-亚 环己基 -1,4-环 戊 二 烯基)乙醚 (Ⅴ)8.91 g,产率 82.8%.
2,2′-二 (3-亚环己基 -1,4-环戊二烯基 )乙醚(Ⅴ)的1H NMR(CDCl3,δ/ppm):1.65~1.66(m,4H,2CH2),1.70~1.72(m,8H,4CH2),2.57~2.60(m,8H,4CH2),2.70~2.73(t,J=7.2 Hz,4H,2CH2),3.64~3.68(t,J=7.2 Hz,4H,2CH2),6.26~6.27(dd,J1=2.0 Hz,J2=1.2 Hz,2H,2CH),6.40~6.42(dd,J1=5.2 Hz,J2=1.2 Hz,2H,2CH),6.52~6.54(dd,J1=5.2 Hz,J2=2.0 Hz,2H,2CH).13C NMR(CDCl3,δ/ppm):26.6,28.6,28.7,30.8,33.5,33.6,70.4,115.9,120.7,132.6,139.2,143.2,155.8.
1.3.2.2 配体 (Ⅵ)的合成
在冰浴下,向反应瓶中依次加入颗粒状的NaOH(8 g,200 mmol),四氢呋喃 30 mL,新裂解的环戊二烯 (16 mL,200 mmol),自然升温至室温,搅拌 4 h后分批加入双富烯Ⅴ(3.62 g,10.00 mmol),5~10℃下反应,薄层色谱法 (石油醚作展开剂)跟踪,反应完后加入 20 mL冰水,浓缩,乙醚萃取 (3×20 mL),有机相水洗 (3×25 mL),无水硫酸钠干燥,过滤,浓缩,得到黑色油状物,柱色谱分离 (洗脱剂:石油醚)得到配体 2,2′-二{3-[1-(1,4-环戊二烯基)环己基 ]-1,4-环戊二烯基}乙醚 (Ⅵ),黄绿色油状物,1.36 g,产率58.4%.
2,2′-二 {3-[1-(1,4-环戊二烯基 )环己基 ]-1,4-环戊二烯基 }乙醚 (Ⅵ)的1H NMR(CDCl3,δ/ppm):1.41~1.42(m,4H,2CH2),1.48~1.50(m,8H,4CH2),1.91~1.93(m,8H,4CH2),2.55~2.60(m,4H,2CH2),2.68~2.90(m,4H,2CH2),2.93~2.95(m,4H,2CH2),3.53~3.63(m,4H,2CH2),5.79~6.46(m,10H,10CH).
1.3.2.3 配合物 (Ⅷ)的合成
在冰浴下,将正丁基锂溶液 (5.5 mL,2.5 mol/L)加入到配体Ⅵ(1.36 g,2.75 mmol)的石油醚 (30 mL)溶液中,有白色固体生成,自然升温至室温,搅拌过夜,离心后弃去上层清液,用石油醚(2×20 mL)洗涤,固体真空干燥,得到白色的粉末状固体四锂盐 (Ⅶ)0.83 g,产率 58.4%.
0℃,氮气保护下,将四锂盐Ⅶ(0.83 g,1.60 mmol)逐渐加入 TiCl4(THF)2(1.26 g,3.77 mmol)的甲苯 (30 mL)溶液中,溶液由黄色变成黑色,自然升温至室温,搅拌过夜,浓缩溶液,固体用CH2Cl2(3×20 mL)提取,合并提取液,浓缩至少量溶液,加入 20 mL正己烷,有棕褐色固体析出,过滤,固体用正己烷洗涤 (3×10 mL),真空干燥,得到配合物 3-氧-戊基桥连双核 (C1-桥连二茂钛)( Ⅷ)0.45 g,产率 38.2%.
3-氧-戊基桥连双核 (C1-桥连二茂钛)(Ⅷ)的1H NMR(CDCl3,δ/ppm):1.65(m,4H,2CH2),1.75~1.85(m,8H,4CH2),2.18~2.26(m,8H,4CH2),2.92~2.96(m,4H,2CH2),3.68~3.69(m,4H,2CH2),5.19~5.22(m,2H,2CH),5.44~5.46(m,2H,2CH),5.59~5.61(m,2H,2CH),5.68(m,2H,2CH),6.57~6.61(m,2H,2CH),6.92(m,2H,2CH),7.07(m,2H,2CH).13C NMR(CDCl3,δ/ppm):21.6,25.6,25.8,32.3,32.4,42.3,31.2,69.6,110.4,110.6,110.9,112.6,113.5,113.9,129.8,130.1,131.0,141.2.
1.4 甲基丙烯酸甲酯的聚合
聚合反应瓶经过真空干燥后,通入氮气,依次加入 2.35 mL(8×10-3mmol/L)催化剂的二氯甲烷溶液,0.24 mL MAO的甲苯溶液,真空浓缩,去除溶剂,然后加入甲基丙烯酸甲酯,在设定的温度下反应到设定的时间后,用 10%的盐酸乙醇溶液淬灭反应,过滤,聚合物用乙醇和水洗涤,所得聚合物在 60℃下真空干燥至恒重,称量.
2 结果与讨论
2.1 3-氧 -戊基桥连双核 (C1-桥连二茂钛 )的合成
根据图 2合成路线,采用 Stone等[11]合成富烯的方法,用四氢吡咯作碱,通过 2,2′-二 (环戊二烯基)乙醚与环己酮的缩合反应合成得到双富烯 ——2,2′-二 (3-亚环己基 -1,4-环戊二烯基 )乙醚 (Ⅴ),该双富烯不稳定,暴露在空气中易被氧化,需要保存在低温和惰性气氛中.双富烯Ⅴ可以与环戊二烯负离子发生亲核加成反应,得到配体2,2′-二 {3-[1-(1,4-环戊二烯基 )环己基 ]-1,4-环戊二烯基}乙醚 (Ⅵ).化合物Ⅵ极易发生环加成反应而聚合,形成不溶于四氢呋喃、乙醚等的无色聚合物,因此,化合物Ⅵ的分离纯化需要在低温下进行,并且不宜久存.化合物Ⅵ与正丁基锂作用得到白色粉末状固体四锂盐 (Ⅶ),其对空气极其敏感,暴露在空气中会自燃,因此,四锂盐Ⅶ未经纯化表征即直接与 TiCl4(THF)2反应生成 3-氧-戊基桥连双核 (C1-桥连二茂钛)(Ⅷ).3-氧-戊基桥连双核 (C1-桥连二茂钛)(Ⅷ)同样对空气非常敏感,需在惰性气氛中纯化和保存.
2.2 催化剂结构对其催化活性及 PMMA分子量分布的影响
以MAO作助催化剂,分别以 3-氧-戊基桥连双核 (C1-桥连二茂钛)(Ⅷ)和亚环己基桥连二茂钛 (Ⅲ)为主催化剂,催化甲基丙烯酸甲酯(MMA)的本体聚合,结果见表 1.

表 1 催化剂结构对甲基丙烯酸甲酯聚合的影响
从表 1可以看出:与类似结构的单核茂金属催化剂——亚环己基桥连二茂钛 (Ⅲ)相比,双核茂金属催化剂——3-氧-戊基桥连双核 (C1-桥连二茂钛)(Ⅷ)作主催化剂时,MMA的转化率略高一些.这可能是 3-氧-戊基桥连双核 (C1-桥连二茂钛)分子中存在 2个金属中心,2个金属中心间存在协同效应,增加了催化剂的催化活性.此外,双核催化剂催化聚合反应所得的聚合物黏均分子量更大,分子量分布 (MWD)更宽,可能是双核催化剂分子中存在 2个金属中心,金属中心间微化学环境的改变有利于多活性中心的形成.
2.3 催化剂结构对 PMMA立构规整度的影响
聚甲基丙烯酸甲酯 (P MMA)有全同、间同和无规 3种立体异构,其红外光谱包括 4组谱带 (见图 3):在 2 951 cm-1处有一强吸收峰,是甲基、亚甲基 C—H伸缩振动吸收;1 722 cm-1处有一强吸1 365 cm-1,由于 C—H的弯曲振动显示 4个吸收峰;“规整性谱带”,1 063 cm-1处的吸收峰仅在间同聚甲基丙烯酸甲酯的红外光谱中出现.

图 3 聚甲基丙烯酸甲酯 (PMMA)的红外光谱
甲基丙烯酸甲酯 (MMA)的聚合一般以自由基聚合为主,但自由基聚合所得的 PMMA立构规整性差,通常是无规聚合物.郎五可等[4]合成了对称乙醚桥连双核钛催化剂和对称亚甲基联苯桥连双核钛催化剂,并用于催化甲基丙烯酸甲酯的聚合,分别得到了间规含量为 68%和 76%的聚合物.表 2表明:单核茂金属催化剂——亚环己基桥连二茂钛 (Ⅲ)和双核茂金属催化剂——3-氧-戊基桥连双核 (C1-桥连二茂钛)(Ⅷ)催化 MMA聚合所得聚合物PMMA的立构规整性都优于文献报道,可能是因为亚环己基的引入,一方面阻止了茂环的旋转,固定了化合物的对称性;另一方面使2个茂环形成夹心结构,影响金属中心的活性,增加茂环的二面角,从而增强了金属中心的亲电性,增大了反应空间[3].

表 2 聚甲基丙烯酸甲酯 (PMMA)的红外间同含量
2.4 聚合条件对催化剂性能的影响
以 3-氧-戊基桥连双核 (C1-桥连二茂钛 )(Ⅷ)为主催化剂,MAO作助催化剂,详细考察了聚合反应条件对催化剂Ⅷ性能的影响.
2.4.1 MMA单体与催化剂摩尔比的影响
从图 4可以看出,随着 n(MMA)/n(Cat)值的增大,MMA的转化率及 PMMA的黏均分子量都逐步增加,当 n(MMA)/n(Cat)=1 500时,两者同时出现最大值.这可能是 n(MMA)/n(Cat)的值较小时,催化剂的浓度过高,催化剂活性中心失活的几率增加,从而导致其催化活性下降,所得聚合物的分子量也随之减小.

图 4 MMA单体与催化剂的摩尔比对甲基丙烯酸甲酯聚合的影响
2.4.2 聚合反应温度的影响
聚合反应温度的升高,可以增加催化剂的催化活性,但同时也会加快催化剂活性中心的失活[2]和链转移反应速率.从图 5可以看出:聚合反应温度为 60℃时,MMA的转化率达到最大;而聚合反应温度为 40℃时,PMMA的黏均分子量达到最大.
2.4.3 甲基铝氧烷与催化剂摩尔比的影响
茂金属催化剂催化烯烃聚合时,通常需要大大过量的甲基铝氧烷 (MAO)或三异丁基铝作助催化剂,这是形成茂金属阳离子活性中心的必要条件,并且过量的助催化剂还能除去反应体系中微量的杂质,避免催化剂中毒.但过量的MAO也会与催化剂所形成的阳离子活性中心进一步络合,生成非活性的 Ti—CH2—Al络合物,从而降低催化剂的催化活性[4].此外,过量的MAO也会成为链转移剂,导致聚合物分子量的下降.从图 6可以看出,当n(MAO)/n(Cat)=60时,MMA的转化率和 PMMA的黏均分子量都达到最大值,然后随着其比值的增大两指标均呈逐渐下降的趋势.
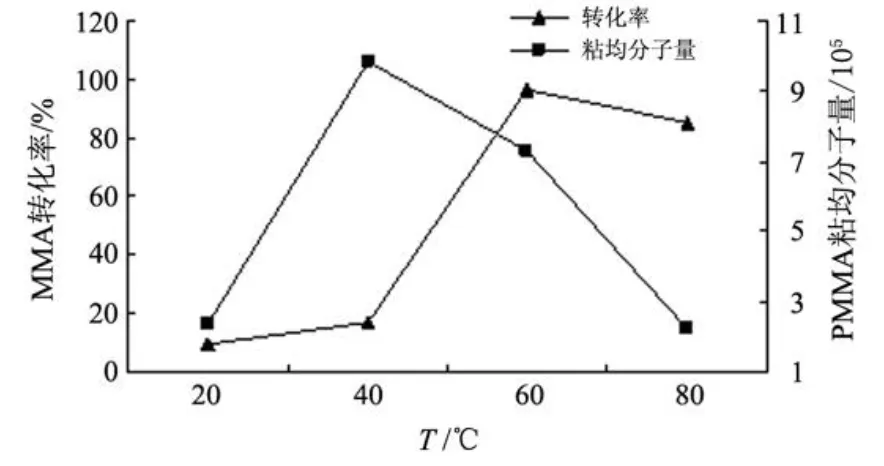
图 5 温度对甲基丙烯酸甲酯聚合的影响
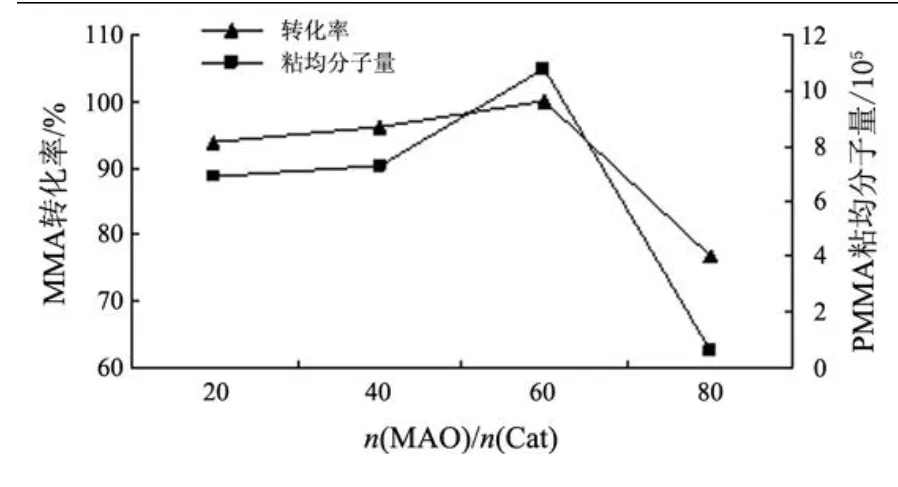
图 6 甲基铝氧烷与催化剂的摩尔比对甲基丙烯酸甲酯聚合的影响
2.4.4 聚合反应时间的影响
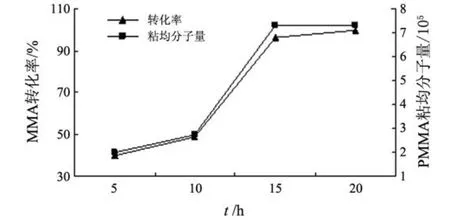
图 7 时间对甲基丙烯酸甲酯聚合的影响
从图 7可以看到,随着聚合反应时间的延长,MMA的转化率和 PMMA的黏均分子量都逐渐增大,说明该催化剂的活性中心相对比较稳定,寿命较长.
3 结 论
本文合成了一种新型3-氧-戊基桥连双核
(C1-桥连二茂钛)催化剂.在该催化剂分子中,通过亚环己基的桥联作用,固定了与金属钛配位的2个环戊二烯环的空间排列,使得其不能围绕金属中心自由旋转,从而提高了催化甲基丙烯酸甲酯(MMA)聚合的立体选择性,所得聚甲基丙烯酸甲酯 (PMMA)中间规含量超过 78%;通过 3-氧-戊基的桥联作用,将 2个金属中心连接起来,在一个催化剂分子中同时引入 2个金属核,在金属核间微化学环境的差异及金属中心间的相互作用下,在催化MMA聚合过程中可能形成一个以上的活性中心,使所得 PMMA的分子量分布达到 4.66~4.84,略宽于类似的单核茂金属催化剂.此外,以MAO作助催化剂时,用该新型双核茂金属催化剂催化MMA本体聚合时还体现出了较高的热稳定性和优异的催化活性.
[1]程正载,伍林,吕早生.桥联茂金属化合物催化烯烃聚合[J].工业催化,2007,14(7):1-7.
[2]Ewen J A,Jones R L,Razavi A,et al.Syndiospecific propylene polymerizations with group 4 metallocenes[J].J Am Chem Soc,1988,110(18):6255-6256.
[3]Jungling S,Mulbaupt R.Cooperative effects in binuclear zirconocenes:their synthesis and use as catalystin propene polymerization[J].J Organomet Chem,1993,460(2):191-195.
[4]郎五可,孙俊全,林峰,等.新型同双核钛茂金属催化MMA本体聚合[J].浙江大学学报:理学版,2007,34(1):50-55.
[5]Alt H G,ErnstR,Bohmer IK.Dinuclear ansa-zirconocene complexes containing a sandwich and a half-sandwich moiety as catalysts for the polymerization of ethlylene[J].J Organomet Chem,2002,658(1/2):259-265.
[6]Ban H T,Uozumi T,Soga K.Polymerization of olefins with a novel dinuclear ansa-zirconocene catalyst having a biphenyl bridge[J].J Polym Sci,PartA:Polym Chem,1998,36(13):2269-2274.
[7]Sierra J C,HüerländerD,HillM,et al.For mation of dinuclear titanium and zirconium complexes by olefin metathesis:catalytic preparation of organometallic catalyst systems[J].Chemistry-A European Journal,2003,9(15):3618-3622.
[8]ManzerL.Tetrahydrofuran complexes of selected early transition metals[J].Inorg Synth,1982,21(part 4):135-138.
[9]中国科学院大连化学物理研究所聚烯烃组.聚丙烯、聚乙烯黏均分子量的测定[M].北京:科学出版社,1979:69.
[10]WangBaiquan,Mu Bin,Deng Xiaobin,et al.Synthesis and structure of cycloalkylidene-bridged cyclopentadienylmetallocene catalysts:effects of the bridges of ansa-metallocene complexes on the catalytic activity for ethylene polymerization[J].Chem Eur J,2005,11(2):669-679.
[11]Stone K J,Little R D.An exceptionally simple and efficientmethod for the preparation of a wide variety of fulvenes[J].J Org Chem,1984,49(11):1849-1853.
[12]郑昌仁.高聚物分子量及分布[M].北京:化学工业出版社,1986:402.
