异构酒花浸膏中异α-酸氢化工艺优化*
2011-11-30贠建民董延虎蒲陆梅薛华丽连文绮
贠建民,董延虎,蒲陆梅,薛华丽,连文绮
1(甘肃农业大学食品科学与工程学院,甘肃兰州,730070);2(甘肃农业大学理学院,甘肃兰州,730070)
异构酒花浸膏中异α-酸氢化工艺优化*
贠建民1,董延虎1,蒲陆梅2,薛华丽2,连文绮1
1(甘肃农业大学食品科学与工程学院,甘肃兰州,730070);2(甘肃农业大学理学院,甘肃兰州,730070)
采用单因素筛选试验考察了氢化温度、pH值、氢气压力、氢化时间、催化剂用量、浸膏中异α-酸浓度对异α-酸氢化的影响。再利用Plackett-Burman设计研究了各因素对异α-酸氢化的影响。结果表明,底物异α-酸浓度、氢气压力和pH对异α-酸酒花浸膏氢化效果影响显著;在此基础上,采用L9(34)正交设计法对影响异α-酸酒花浸膏氢化的3个主要因素异α-酸浓度、氢气压力、pH进行了参数优化试验。结果表明,影响异α-酸酒花浸膏氢化的主次因素顺序为异α-酸浓度>氢气压力>pH值,异α-酸氢化的最佳工艺参数为:异α-酸的浓度55mg/mL,氢气压力0.2 MPa,pH值10,催化剂Pb/C用量3%,氢化时间4h。浸膏中四氢异α-酸的浓度达到58.89%,异α-酸氢化转化率达到89.73%。
氢化工艺,四氢异α-酸,异构酒花浸膏
啤酒花被誉为“啤酒之灵魂”,是啤酒酿造中必不可缺少的原料之一[1]。α-酸作为啤酒花中具有苦味和抑菌作用的主要物质,在光、热、碱的作用下极易改变其结构,如侧链氧化、侧链断裂、六碳环改变为五碳环等。在加热或弱碱中异构化生成黄色油状的异α-酸其衍生物[2],使其苦味和抑菌作用增强。而异α-酸对光亦不稳定,尤其是在光波长350~500 nm内的紫外线的催化作用下,使其底部侧链容易裂解,并很快与啤酒中的含硫化合物生成所谓的“日光臭”物质(3-甲基-2-丁烯-1-硫醇),会引起啤酒产生不快的异味[1-2],严重影响啤酒质量[3]。近年来随着啤酒品种的开发,一些传统的酒花制品严重地影响了啤酒的质量,如白瓶啤酒的“日光臭“问题,高浓度啤酒稀释后的泡沫问题。但随着酒花制品的开发,这些问题也必将得到很好的解决,新品四氢异构酒花浸膏的出现对啤酒质量的提高起到了明显改善的作用。而白色瓶装啤酒由于瓶体透明、色泽清亮、酒液金黄,给人以清新、爽快的感觉,深受人们的青睐[4]。因而越来越多的啤酒生产企业也开始关注四氢异构酒花浸膏制品。四氢啤酒花浸膏(简称Tetrahop)是在异构酒花浸膏的基础上进一步加氢制成的还原酒花浸膏,具有良好的光稳定性、纯正的苦味及口感,能明显改善啤酒泡沫的挂杯性能和泡沫稳定性[5]。
美国和德国发展还原酒花浸膏技术较早,20世纪70、80年代就开始氢化工艺的研究和还原浸膏产品的开发。Henry等在制备还原酒花浸膏的专利中提到,氢化的 pH 值为9,反应温度是80~100℃[6]。Patrick等通过氢化异α-酸的金属盐制备四氢异α-酸专利中,进一步采用了纯化技术和Pd/C催化剂优化工艺[7]。现已开发的哈斯、米勒等还原酒花浸膏倍受国内外啤酒生产厂家的喜爱,由于国外同类产品大多以专利形式对产权进行了保护,这在一定程度上限制了氢化浸膏产品在世界范围,尤其是在发展中国家的生产和使用。国内王少君等对四氢异α-酸的合成进行了初步研究,用氢氧化钾调pH值,催化剂为Pd/C[8]。罗介人等对酒花中α-酸进行了初步加氢试验,氢化压力0.5 MPa,氢化时间6h[9]。新疆大学化学系刘奎钫等及其研究室研发的"由酒花浸膏为原料制备四氢异a-酸的方法",获得国家专利,改变了过去中国“白瓶啤酒”生产技术一直依赖进口的现状。2007年甘肃玉门拓璞科技开发有限公司的刘启民等,在发明的专利“一种生产四氢异构化α-酸的方法”基础上,开发的“拓璞”牌浸膏,将酒花保质期从短短的几个月延长到8~10年,该产品已超越了啤酒花的定义,上升到一种“品牌”的高度。
综上所述,国内虽然对酒花异α-酸氢化工艺有所研究,也已有几家酒花浸膏加工企业生产还原酒花浸膏产品,但与国外进口产品相比,工艺稳定性还较低,高浓度氢化浸膏的溶解性能还较差。为此,本试验从工艺优化角度出发,较系统地研究氢化温度、pH值、氢气压力、氢化时间、催化剂用量、异α-酸浓度对酒花浸膏中异α-酸氢化效果的影响,旨在探索出以异构酒花浸膏为中间原料制备四氢异构浸膏制品过程中异α-酸氢化工艺的最佳参数,为酒花加工企业开发生产四氢异α-酸浸膏产品提供理论依据。
1 材料与方法
1.1 主要材料与试剂
青岛大花异构酒花浸膏:用甘肃玉门拓璞科技开发有限公司的压缩酒花经提取异构化自制制备方法:先采用超临界CO2萃取制成酒花浸膏,经酸碱沉淀初步分离得α-酸结晶物[2]再经常压煮沸法异构化工艺制得异构酒花浸膏[3](含异 α-酸42.42%)。
无水乙醇(AR),NaOH(AR),均为天津化学试剂厂家生产;5%Pd/C催化剂,陕西开达化工有限责任公司;H2(≥99.9%)市售。
1.2 主要仪器与设备
UV-2550型紫外光分光光度计,日本岛津;FF-2釜式反应装置,天津大学北方化工新技术开发公司;RE-52AA旋转蒸发器,上海亚荣生化仪器厂;PHS-3C型电子pH计,上海日岛科学仪器公司;SHZ-D(Ⅲ)循环水式真空泵,巩义市予华仪器有限责任公司;AL104型电子天平,梅特勒-托利多仪器公司;HHS型电热恒温水浴锅,上海博迅实业公司医疗设备厂。
1.3 试验方法
1.3.1 异α-酸氢化工艺
根据每组试验要求的溶液中α-酸的浓度,用电子天平称取相应质量(5~40g)的异构α-酸浸膏,放入250 mL烧杯中,加入Pb/C催化剂,倒入100 mL无水乙醇,置40℃水浴下加热,同时用1 mol/L NaOH溶液调pH,不断搅拌使浸膏充分溶解,然后转入1L的高压反应釜密封好,通入(0.1~0.7 MPa)的N2,在50~80℃维持2~10 h完成反应。氢化结束后,先滤除催化剂,再置旋转蒸发仪中用循环水式真空泵抽真空蒸出溶剂乙醇得到的膏状物即为四氢异α-酸浸膏。于40℃的烘箱中将浸膏干燥后,最后用1.3.10的方法,检测样品中四氢异α-酸的含量,并计算氢化转化率。
1.3.2 氢化温度
氢化温度依次选择为 50、60、70、80℃,H2压力0.1 MPa、异 α-酸浓度20 mg/mL、pH 值9、氢化时间6 h、Pb/C催化剂7%进行试验,以四氢异α-酸的含量为指标确定最佳的氢化温度。
1.3.3 pH值
依次设定溶液的 pH 值为8、9、10、11,氢气压力0.1 MPa、异 α-酸的浓度20 mg/mL、氢化温度80℃、氢化时间6 h、Pb/C催化剂7%进行试验,以四氢异α-酸的含量为指标确定最佳的pH值。
1.3.4 氢气压力
依次设定高压反应釜的压力为0.1、0.3、0.5、0.7 MPa,异 α-酸的浓度 20 mg/mL、pH9、氢化温度80℃、氢化时间6h、Pb/C催化剂7%进行试验,以四氢异α-酸的含量为指标确定最佳的氢气压力。
1.3.5 氢化时间
依次设定氢化时间为 2、4、6、8,10h,氢气压力0.1 MPa、异 α-酸的浓度 20 mg/mL、pH 值 9、氢化温度80℃、Pb/C催化剂7%进行试验,以四氢异α-酸的含量为指标确定最佳的氢化时间。
1.3.6 催化剂的量
依次设定 Pb/C 催化剂的含量为3、5、7、9,11%,氢气压力0.1 MPa、异α-酸的浓度20 mg/mL、pH 9、氢化温度80℃、氢化时间6h进行试验,以四氢异α-酸的含量为指标确定最佳的Pb/C催化剂的量。
1.3.7 异α-酸浓度
依次设定异 α-酸的浓度为 22.1、44.2、88.4、132.6,176.8mg/mL,H2压力 0.1 MPa、pH 9、氢化温度80℃、氢化时间6h进行试验,以四氢异α-酸的含量为指标确定最佳的异α-酸的浓度。
1.3.8 Plackett-Burman试验
在单因素实验的基础上,对以上影响氢化的5个因素进一步采用Plackett-Burman法进行各因素显著性的考察,通过标准化效应图(Pareto图)选出对氢化具有显著性影响的因素,从而达到进一步细化筛选因素的目的。
1.3.9 正交试验
在单因素实验和Plackett-Burman试验的基础上,对影响氢化率的主要因素再进行4因素3水平的正交组合试验。同样以四氢异α-酸的含量为指标优化氢化过程最佳的工艺参数。
1.3.10 四氢异 α-酸的测定[11-12]
准确称取0.4 g样品于100 mL容量瓶中,加入约50 mL甲醇,混匀并溶解,然后用甲醇定容,混匀后标记“溶液A”。吸取溶液A 2.0 mL至100 mL容量瓶中,加入约75 mL甲醇,加入1 mL 1.5 mol/L NaOH溶液,然后用甲醇定容至刻度,摇匀后标记“溶液B”。于50 mL容量瓶中加0.5 mL 1.5 mol/L NaOH溶液,用甲醇定容至刻度,摇匀后标记“空白”。然后在253 nm下测定“溶液B”的吸光度值,代入公式计算四氢异α-酸的百分含量和氢化转化率。
溶液B中的样品浓度(cs)计算:cs(g/mL)=样品质量(g)/溶液A体积(mL)×吸取溶液A体积(mL)/溶液B体积(mL);
异构酒花酸浓度计算:cacid/(g·mL-1)=A/ε;
酒花制品中酒花酸含量(W/W)=cacid/cs;
氢化转化率/%=新生成的四氢异α-酸含量/原浸膏中的异α-酸含量×100
2 结果与分析
2.1 氢化温度对酒花浸膏中四氢异α-酸含量的影响
图1所示结果为氢化温度对四氢异α-酸含量的影响。随着温度逐渐增加,四氢异α-酸的含量也在增加,在80℃时达到最大值,浸膏中四氢异α-酸的含量为50.56%。由于常压状态下无水乙醇沸点为78.2℃致使反应体系的沸点不易高于80℃,过高温度将使反应体系中乙醇气化,溶液浓度发生改变对反应设备造成伤害。所以试验中氢化温度就选为定值80℃。
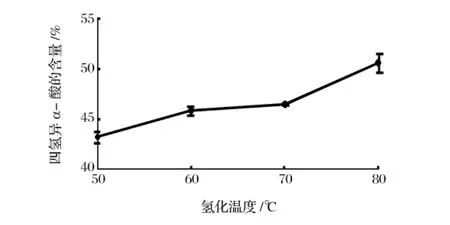
图1 氢化温度对四氢异α-酸含量的影响
2.2 pH值对酒花浸膏中四氢异α-酸含量的影响
图2所示结果为不同pH值对四氢异α-酸含量的影响。随着pH值逐渐增加,四氢异α-酸的含量先升高后下降,在pH 10时达到峰值,浸膏中四氢异α-酸的含量达到53.62%;pH 10以上氢化转化率迅速下降,到pH 11时四氢异α-酸的含量仅为46.2%。说明氢化过程pH值不易太低也不易太高,弱碱性为宜。
2.3 氢气压力对酒花浸膏中四氢异α-酸含量的影响
图3所示结果为不同氢气压力对四氢异α-酸含量的影响。随着氢气压力从0.1 MPa增加到0.3 MPa,四氢异α-酸的含量略微增加,并且在氢气压力为0.3 MPa时达到峰值,浸膏中四氢异α-酸的含量为51.31%,氢气压力0.3 MPa以上氢化转化率迅速下降,说明氢化过程氢气压力不易太高。
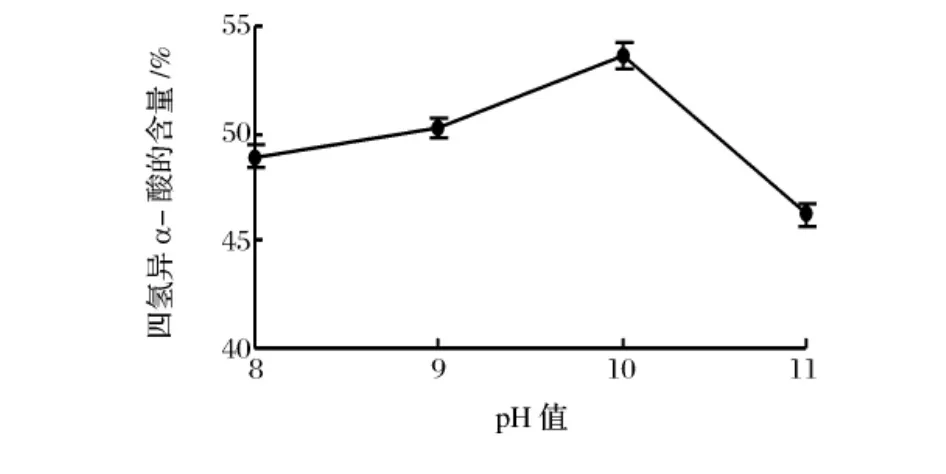
图2 pH对四氢异α-酸含量的影响

图3 氢气压力对四氢异α-酸含量的影响
2.4 氢化时间对酒花浸膏中四氢异α-酸含量的影响
图4所示结果为不同的氢化时间对四氢异α-酸含量的影响。从图4中可以看出随着加热时间的延长四氢异α-酸的含量逐渐增加,并且在4h时达到峰值,酒花浸膏中异α-酸氢化转化率为51.19%,4h后氢化转化率缓慢下降,到10h时四氢异α-酸的含量为47.81%。可见不同的氢化时间对四氢异α-酸含量的影响差别不大。
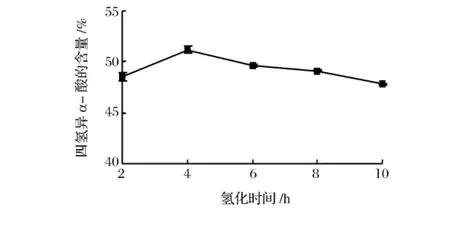
图4 氢化时间对四氢异a-酸含量的影响
2.5 催化剂的量对酒花浸膏中四氢异α-酸含量的影响
图5所示结果为不同催化剂的量对四氢异α-酸含量的影响。随着催化剂量的增加四氢异α-酸的含量先逐渐增加再缓慢下降,并且在催化剂的量5%时达到峰值,酒花浸膏中异 α-酸氢化转化率为51.33%,到催化剂的量增加到11%时四氢异α-酸的含量为48.33%。可见不同的催化剂添加量对四氢异α-酸含量的影响差别不大。

图5 催化剂的量对四氢异α-酸含量的影响
2.6 异α-酸浓度对酒花浸膏中四氢异α-酸含量的影响
图6所示结果为浸膏中不同异α-酸浓度对四氢异α-酸含量的影响。随着异α-酸浓度逐渐增大氢化转化率先增加,浓度在44.2 mg/mL时达到最大值,氢化浸膏中四氢异α-酸含量为50.32%。然后迅速下降,浓度为176.8mg/mL时四氢异α-酸含量仅为46.51%。试验中发现浓度太大反应体系过于黏稠,并且溶解状态不好,易造成反应不充分,氢化转化率反而较低。
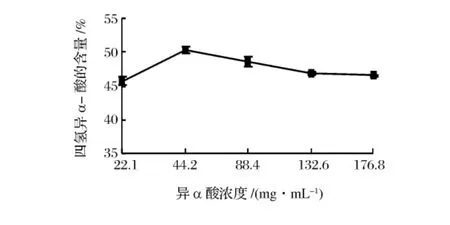
图6 原料浓度对四氢异α-酸含量的影响
2.7 筛选试验设计-Plackett-Burman法
在单因素试验的基础上,对影响氢化的氢气压力、异α-酸浓度、pH值、氢化时间、催化剂用量等5个因素进行筛选。每个变量分别设定高(+)和低(-)2个水平,Plackett-Burman试验设计的因素和水平见表1,Plackett-Burman试验设计及其结果见表2。
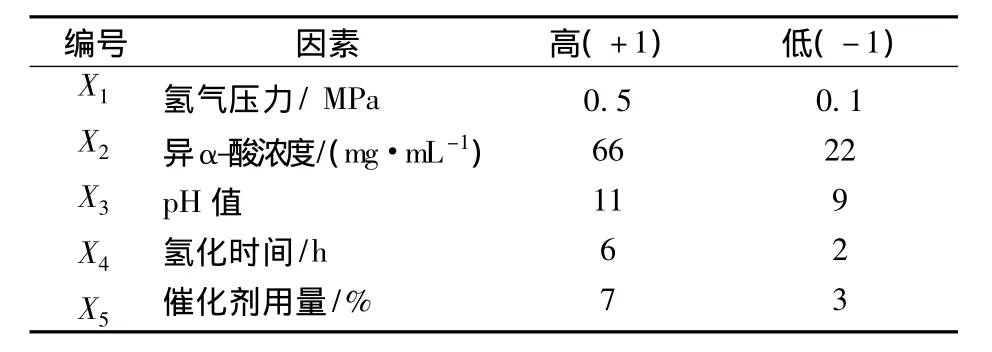
表1 Plackett-Burman试验因素水平及编码值

表2 Plackett-Burman试验设计及其结果(n=5)
采用Minitab15对表2中的试验数据进行回归分析,所得的结果见表3。
由表3可知,对四氢异α-酸含量有显著性影响(置信度大于95%,P<0.05)的因素有氢气压力、异α-酸浓度、pH值,且影响均为正效应,影响程度为:异α-酸浓度>氢气压力>pH值。其余2个因素对四氢异α-酸含量的影响不显著均为负效应,在后续试验中取低水平的点进行后续试验。
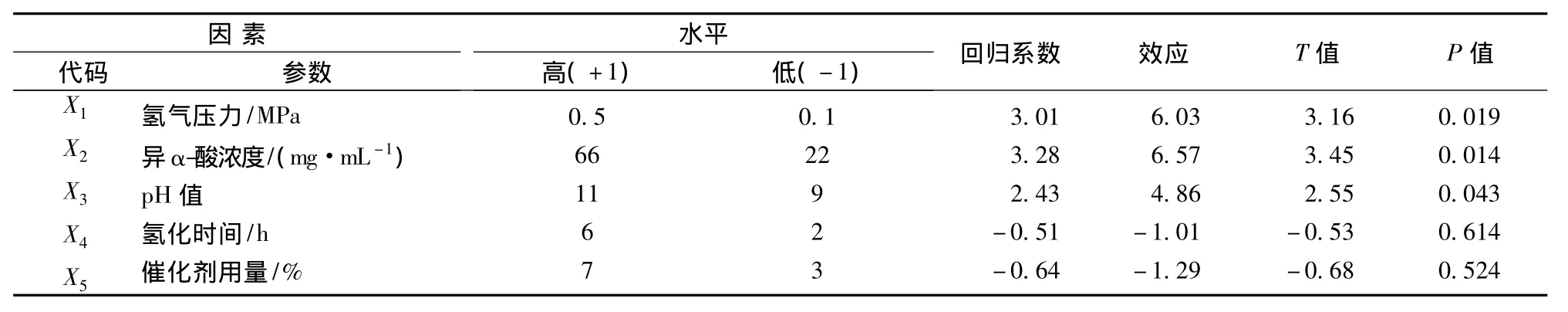
表3 Plackett-Burman试验设计结果分析
2.8 正交试验设计结果
经以上单因素和Plackett-Burman筛选试验后对四氢异α-酸含量影响显著的因素进一步做正交试验,其中对四氢异α-酸含量影响不显著的因素氢化时间,为了使反应更充分选用4h,考虑到Pb/C催化剂价格昂贵,催化剂用量选择3%。选定异α-酸浓度、氢气压力、pH值3个因素设计4因素3水平的L9(34)正交试验(表4),筛选最佳的氢化工艺参数。正交试验结果见表5。

表4 因素水平表
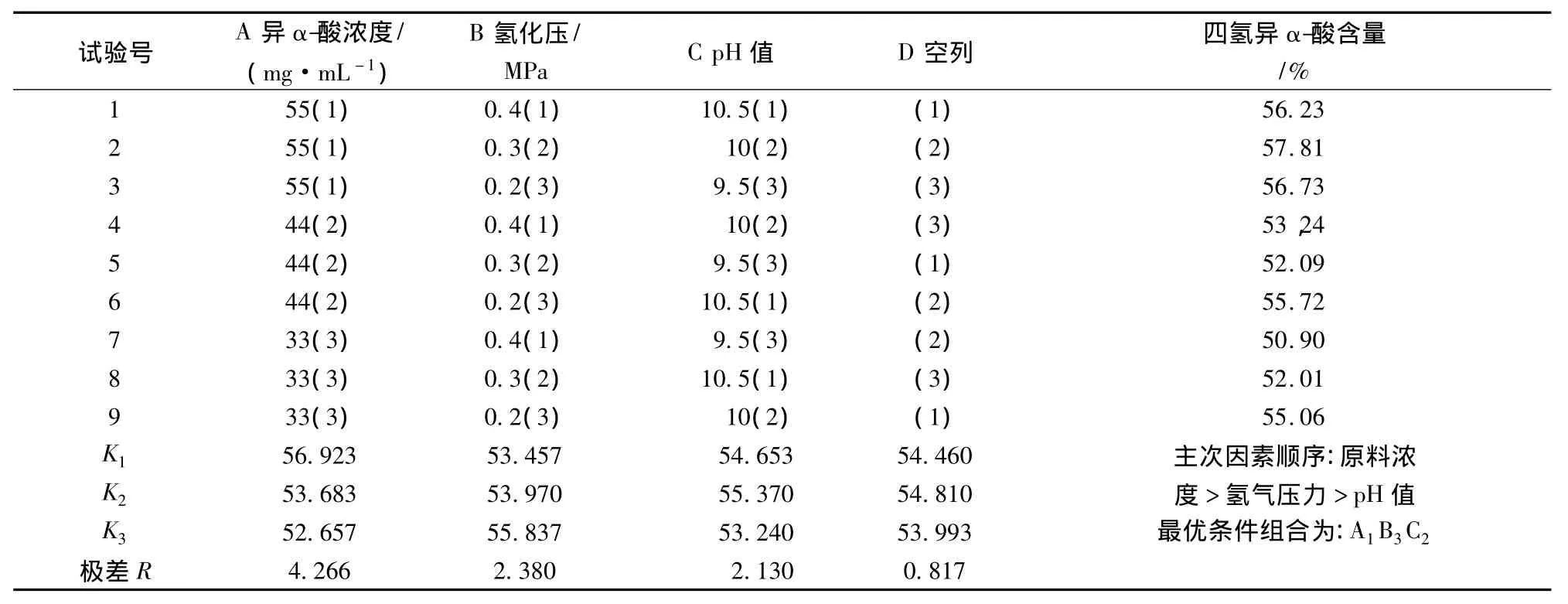
表5 正交试验结果
应用SPSS16.0统计软件对表5进行方差分析, 结果见表6。

表6 方差分析结果
由表5可知,试验2组合的四氢异α-酸含量最高为57.81%。各处理组合极差之间的关系为RA>RB>RC>RD。即:主次因素顺序:异α-酸的浓度>氢气压力>pH值。并得出α-酸的氢化最优条件组合为A1B3C2。即氢化的最优条件组合为异α-酸的浓度55 mg/mL,氢气压力 0.2 MPa,pH 10。
由表6方差分析可以看出,影响异α-酸氢化的因素 FA>F0.01(2,9)=8.02,A 因素为极显著;FB>FC>F0.05(2,9)=4.26,B、C 因素为显著;而空列 D 的 FD<F0.05(2,9),空列D为不显著,即误差不显著。并且有FA>FB>FC,与Plackett-Burman试验得出的影响程度和筛选出的最佳工艺条件一致。
3 结论
(1)基于Plackett-Burman筛选试验表明,在供试的5个因素(pH值、氢气压力、氢化时间、催化剂用量、异α-酸浓度)中,对异构浸膏中异α-酸氢化转化率及产品中四氢异α-酸含量有显著性影响的有3个因素:氢化压力、底物浸膏的异α-酸浓度和pH值,且影响均为正效应,影响程度为:异α-酸浓度>氢气压力>pH值。其余2个因素(氢化时间、催化剂用量)对四氢异α-酸含量的影响不显著,且均为负效应,在试验中只要达到一定取值,取低水平的点即可满足氢化要求,催化剂Pb/C用量3%,氢化时间4h。
(2)正交设计试验表明,影响异α-酸氢化效果的因素顺序为:异α-酸的浓度>氢气压力>pH;综合得出,在氢化温度80℃,催化剂Pb/C用量3%,氢化时间4h条件下,异构浸膏中异α-酸氢化的最佳工艺参数为:异 α-酸的浓度 55 mg/mL,H2压力 0.2MPa,pH10。氢化浸膏产品中四氢异 α-酸含量可达到58.89%,异α-酸氢化转化率达到89.73%。
[1] 贺西安,张小云.酒花制品[J].广州食品工业科技,2008,15(5):64 -68.
[2] 陆豫,王远兴,周江萍.酒花浸膏中的a-酸和β-酸的提取和提纯[J].南昌大学学报:理科版,2001,25(2):157-160.
[3] 董延虎,贠建民,蒲陆梅,等.利用酒花浸膏制备异 α-酸酒花浸膏的异构化工艺的研究[J].食品与发酵工业,2009,35(11):426 -428.
[4] 董小雷,于同立.白瓶啤酒生产的问题与解决措施[J].食品工业,2004(4):11-12.
[5] 刘辉,高建方,陈霞.啤酒风味稳定的研究-无色瓶装冰啤酒的工艺探讨[J].广州食品工业科技,2008,14(4):26-28.
[6] 任永新,王秀玲,崔进梅.浅谈酒花新制品四氢异构酒花浸膏[J].山西食品工业,2005(3):11-12.
[7] Henry Goldstein,Patrick L T,Etzer Chicove,et al.Light Stable Hop Extracts and Method of Preparation[P].US,4767640.1988.
[8] Patrick L T,Michael A V,Jay R R,et al.Preparation of Tetrahydroiso-α-acids by the Hydrogenation of the Metal Salts of Iso-α-acids[P].US,5767319.1998.
[9] 王少君,王岩,翟宾,等.四氢异 α-酸的合成[J].大连轻工业学院学报,1999,18(4):314 -316.
[10] 罗介仁,陆豫,吴芬.酒花中α-酸的氢化方法的初步研究[J].食品科学,1997,18(11):25 -26.
[11] 王梅.分光光度计法检测异 α-酸[J].啤酒科技,2005,(1):72-74.
[12] John P M,Susan M,Jianping Xu,et al.Spectrophotometric Analysis of Isomerized alpha-acids[J].Am Soc Brew Chew,2002,60(3):98 -100.
Technology Optimization on Hydrogenation of Isomerized α-Acids in Isomerized Hops Extracts
Yun Jian-min1,Dong Yan-hu1,Pu Lu-mei2,Xue Hua-li2,Lian Wen-qi1
1(College of Food Science and Engineering,Gansu Agricultural University,Lanzhou 730070,China)
2(College of Science ,Gansu Agricultural University,Lanzhou 730070,China)
The factors influencing the hydrogenation of isomerized α-acid were inspected by using the single factor screening experiment,including hydrogenation temperature,pH,hydrogen pressure,hydrogenation time,the catalyst amount and the concentration of isomerized a-acid in hops extracts.Plackett-Burman design was employed to evaluate the effects of the 5 factors mentioned above on hydrogenation of iso-α-acid.It showed that concentration of isomerized a-acid,hydrogen pressure and pH were the three most important factors.On the basis of that,the technological parameter of hydrogenation of isomerized α-acids was optimized by adopting the orthogonal design L9(34).The results showed that the order of affecting hydrogenation of iso-α-acid was the concentration of iso-α-acid > hydrogen pressure>pH,and the optimum technological parameter of hydrogenation was respectively the concentration of iso-αacid 55mg/mL,hydrogen pressure 0.2MPa,pH10,the amount of catalyst 3%.The content of tetrahydro iso-α-acid in hydrogenation extracts was up to 58.89%,and the hydrogenation percent conversion of iso-α-acid was 89.73%.
Hydrogenation technology;Tetrahydro iso-α-acids;Isomerized hops extracts
博士,教授。
*“十一五"国家科技支撑计划项目(2007BAD52B07)
2011-02-17,改回日期:2011-04-02
