抗变色仿金稀土铜合金的耐蚀行为
2011-11-23罗利阳朱安印陈景林张晓男
罗利阳, 朱安印, 陈景林, 李 周, 梁 军, 张晓男
(1. 中南大学 材料科学与工程学院,长沙 410083;2. 中国印钞造币总公司 沈阳造币技术研究所,沈阳 110042)
抗变色仿金稀土铜合金的耐蚀行为
罗利阳1, 朱安印1, 陈景林1, 李 周1, 梁 军2, 张晓男2
(1. 中南大学 材料科学与工程学院,长沙 410083;2. 中国印钞造币总公司 沈阳造币技术研究所,沈阳 110042)
设计并制备一种新型的抗变色仿金稀土铜合金。采用金相组织分析、中性盐雾试验、质量损失法、电化学阻抗谱和扫描电镜等手段对比研究所设计合金与现有造币用H72-1-1合金的组织结构、抗变色性能和耐蚀性能。结果表明:所设计合金退火组织细小、均匀,在3.5%NaCl溶液中保持不变色的时间较H72-1-1合金的延长了25%。在3.5%NaCl溶液中浸泡腐蚀过程中,所设计合金形成了一层均匀致密、完整的腐蚀产物膜,减缓了腐蚀的进程,其耐腐蚀性能优于H72-1-1合金的,腐蚀速率为10.3 μm/a;所设计合金电荷转移电阻Rct、Warburg扩散阻抗ZW与H72-1-1合金的相比都有大幅度的提高,腐蚀过程阻力增加。
仿金合金;铜合金;抗变色性能;耐蚀性能
铜及铜合金以其亮丽的光泽、优良的导电性、导热性、耐蚀性和易加工性而被广泛应用于仪器仪表、建筑装饰、造币、艺术品、能源及电子等领域[1−3]。然而,铜合金在生产、储运与使用过程中容易形成较薄的腐蚀膜而变色,这不仅影响其美观,而且影响其导电性和可焊性[1,4−5]。铜合金因其色泽美观,世界多国均采用其作为造币材料,铜合金硬币坯饼的变色问题在世界造币行业普遍存在,例如,我国流通币、特种纪念币所采用的黄色铜合金 H72-1-1[6]就存在储运和使用过程中的变色问题,因此,铜及其合金的变色问题亟待解决。为此,国内外学者研究了多种抑制铜合金表面变色的方法,如无机钝化法[1]、BTA法[7−8]和涂层法[9]等,但是,这些防变色、防锈处理技术还远远不能满足生产厂家的要求,主要表现在防变色时间不长、耐侯性不好等方面[10]。
为了解决目前造币用铜合金材料(H72-1-1合金)在生产和使用过程中的变色问题,本文作者与中国印钞造币总公司沈阳造币技术研究所合作,通过优化合金成分,设计制备了一种新型的仿金铜合金,采用金相组织分析、中性盐雾试验、质量损失法、电化学阻抗谱和扫描电镜等手段考察了两种铜合金的组织结构、抗变色性能和耐腐蚀性能。
1 实验
优化并制备了一种成分为CuZnAlNi-Re-Me的新型仿金铜合金(以下简称合金 1),其化学成分如表 1所列。

表1 所设计合金的化学成分Table 1 Chemical composition of designed alloy (mass fraction, %)
分别采用电解铜、纯锌、纯铝、纯镍、Cu-Me及Cu-Re中间合金为原料,利用中频感应炉在石墨坩埚中熔炼上述铜合金。铣去合金铸锭表面缺陷后,直接冷轧变形50%,经690 ℃、30 min中间退火后,进行第2次冷轧,变形量为50%。按上述退火制度退火后进行第3次冷轧,变形量为50%,最终在690 ℃、1 h退火得到所需样品。
中性盐雾实验:将经过第3次冷轧的样品冲压成d 30 mm 坯饼,将坯饼在 690 ℃退火 1 h,然后用Spaleck Z11型光饰机进行光饰,在重庆汉巴实验设备有限公司生产的SFT025F型综合腐蚀实验箱内进行抗变色性能测试。实验箱温度为(35±1) ℃,湿度为80%,饱和蒸气温度为(35±1) ℃,实验溶液为3.5%NaCl溶液,实验时间为2~256 h。
静态腐蚀实验:腐蚀实验样品尺寸大小为 50 mm×25 mm×2 mm,将样品全浸入腐蚀液并静置腐蚀28 d,每隔7 d更换一次溶液,腐蚀溶液用蒸馏水配制,试剂为分析纯,腐蚀液为 3.5%NaCl溶液。腐蚀试样取出后,用1:1 HCl溶液除去表面腐蚀产物,并根据质量损失法计算平均腐蚀速率。在清洗腐蚀产物的同时,也将同种材料未经腐蚀的空白试样浸入盐酸中轻轻振荡,而后测量计算单个样品表面的质量损失,以对样品在盐酸清洗过程中的腐蚀质量损失进行校正。腐蚀速率的计算公式如下:

式中:R为腐蚀速率,μm/a;m为实验前试样质量,g;mt为实验后试样质量,g;mk为空白试样的质量损失,g;S为试样的总表面积,cm2;t为实验时间,h;ρ为材料密度,kg/m3。
交流阻抗谱(EIS)测试:采用Princeton公司生产的PARSTAT2273电化学系统测量 EIS。采用三电极体系,辅助电极为铂电极,参比电极为饱和甘汞电极(SCE),工作电极为铜合金,工作面积为1 cm2。实验前,将工作电极浸泡在 3.5%NaCl溶液中,待其腐蚀电位稳定后进行测试。EIS测量施加的正弦电位幅值为10 mV,扫描频率范围为0.01~100 kHz。对数扫描,测试60个频率,使用Zview软件解析阻抗数据。
扫描电镜观察与能谱分析:采用Sirion200场发射扫描电镜对在腐蚀介质中浸泡腐蚀30 d后样品的表面及断面进行形貌观察和能谱分析。
2 结果与分析
2.1 合金的金相显微组织
图1所示为H72-1-1合金和所设计合金经690 ℃退火1 h后的金相组织。可以看出,两种合金的退火组织均为再结晶组织,所设计合金的再结晶组织较H72-1-1合金更加细小、均匀,可见,稀土元素的加入具有明显细化晶粒的作用。
2.2 中性盐雾实验
图2所示为两种合金在中性盐雾实验过程中不同时间下表面的变色情况。通过肉眼观察可以看出,经光饰处理的合金1硬币坯饼与H72-1-1合金比较,合金1坯饼在盐雾环境下2.5 h开始局部变色,H72-1-1合金坯饼在 2 h后开始局部变色。在相同时间下,H72-1-1合金较合金1变色程度高,当实验时间达到256 h时,H72-1-1合金表面光泽消失,明显变色且轻微发花,颜色为暗褐色,所设计的合金1表面仍有少量残留光泽。可见,所设计合金 1的抗变色性能较H72-1-1合金的明显提高。

图1 两种合金经690 ℃保温1 h后的金相组织Fig.1 Metallographs of two alloys after annealed at 690 ℃ for 1 h: (a) Alloy H72-1-1; (b) Alloy 1

图2 两种合金在3.5%NaCl溶液中抗变色实验照片Fig.2 Photos of resistance glossy fading experiment of two alloys in 3.5% NaCl solution: (a) Alloy H72-1-1; (b) Alloy 1

表2 两种合金在3.5%NaCl溶液中抗变色实验结果Table 2 Resistance glossy fading experiment results of two alloys in 3.5% NaCl solution
表2所示为两种合金在3.5%NaCl溶液中抗变色实验结果。从表2两种合金在中性盐雾实验过程中保持不变色的时间可以看出,所设计的合金1保持不变色时间较H72-1-1合金延长了25%,说明其抗变色性能优于H72-1-1合金的。
2.3 静态腐蚀实验
两种合金在 3.5%NaCl腐蚀介质中的平均腐蚀速率如表3所列。从表3可以看出,在3.5%NaCl腐蚀液中,所设计合金1的平均腐蚀速率为10.3 μm/a,与H72-1-1合金相比,表现出更好的耐腐蚀性能。

表3 两种合金在3.5%NaCl溶液中的平均腐蚀速率Table 3 Average corrosion rate of two alloys in 3.5% NaCl solution
2.4 EIS测试结果
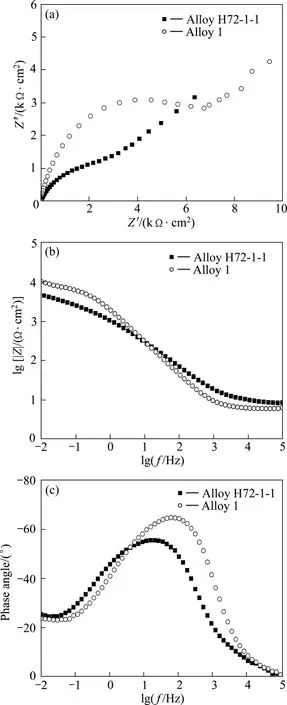
图3 两种合金的交流阻抗谱Fig.3 EIS spectra of two alloys: (a) Nyquist plot; (b), (c)Bode plot
图3 所示为两种合金的交流阻抗谱。从图3(a)可以看出,两种合金 Nyquist谱的变化规律基本一致,阻抗谱的高频部分从接近x轴坐标原点开始,高频端近似为一个半圆弧;当频率低至0.01 Hz时,阻抗虚部仍没有到达x轴,低频端近似为一条直线,呈明显的扩散阻抗特征。但是,在高频部分,H72-1-1合金的半圆弧直径较小,合金 1的半圆弧直径较大,与H72-1-1合金相比产生了较大的阻抗。从Bode图也可看出,在高频部分(lg f =3~ 5),阻抗模值lg|Z|模值较小,且基本上保持不变,这是典型的溶液电阻Rs所表现出的阻抗特征;在中频区域(lg f = −0.5~3), lg|Z|—lgf曲线是斜率约为−1的直线,两种合金的最大相位角分别约为−55°(H72-1-1 合金)、−65°(合金 1),这是由溶液与电极(lg f =−2~−0.5)双电层(EDL)引起的;在更低的频率区间,lg|Z|并没有趋于一个固定值,仍在增长,但是增长速度趋缓,这是由于在更低的频率区间,电容性元件的作用越来越小,此时扩散过程起主要作用[11]。此外,在低频部分,合金1的阻抗模值lg|Z|较 H72-1-1合金的大幅度提高。总之,Nyquist图和Bode图均表明合金 1在腐蚀过程中的腐蚀阻力较H72-1-1合金的增加了许多,耐蚀性能得到大幅度提高。
根据阻抗谱图特征,建立了相应的物理模型及等效电路,如图4所示。其中,Rs为溶液电阻,Rct为电荷传递电阻,O为Warburg扩散阻抗元件或者有限层扩散阻抗元件,并由它产生 Warburg阻抗 ZW,CPE(Constant phase element)为常相位角元件,通常用来表示电极与溶液之间界面的双电层电容。在图4所示的等效电路中,CCPE表示溶液与金属界面的双电层(EDL)电容。在通过电化学阻抗谱来建立等效电路时,常相位角元件CPE是一个很有用的模型元件,它的阻抗Z可由式(2)计算得到[11]:

式中:Q0为当角频率ω=1 rad/s时的导纳(1/|Z|);j为虚数单位(j2=−1);ω 为角频率(ω=2πf);n 为 CPE 指数。通常,参数n的取值范围为0.5<n<1[12]。当n=1时,CPE等效于一个理想电容元件。一般情况下,CPE比理想电容能够更好地满足电化学体系,特别是当电极表面比较粗糙或者是氧化物膜层随着距离膜层远近发生扩散传递时[13]。
在Zview拟合软件中,Warburg扩散阻抗由参数ZW,R和ZW,T来表示。当扩散过程为有限层扩散时,由扩散过程引起的阻抗可由式(3)计算得到:

表4 所建等效电路的各元件参数Table 4 Elements parameters of equivalent circuit
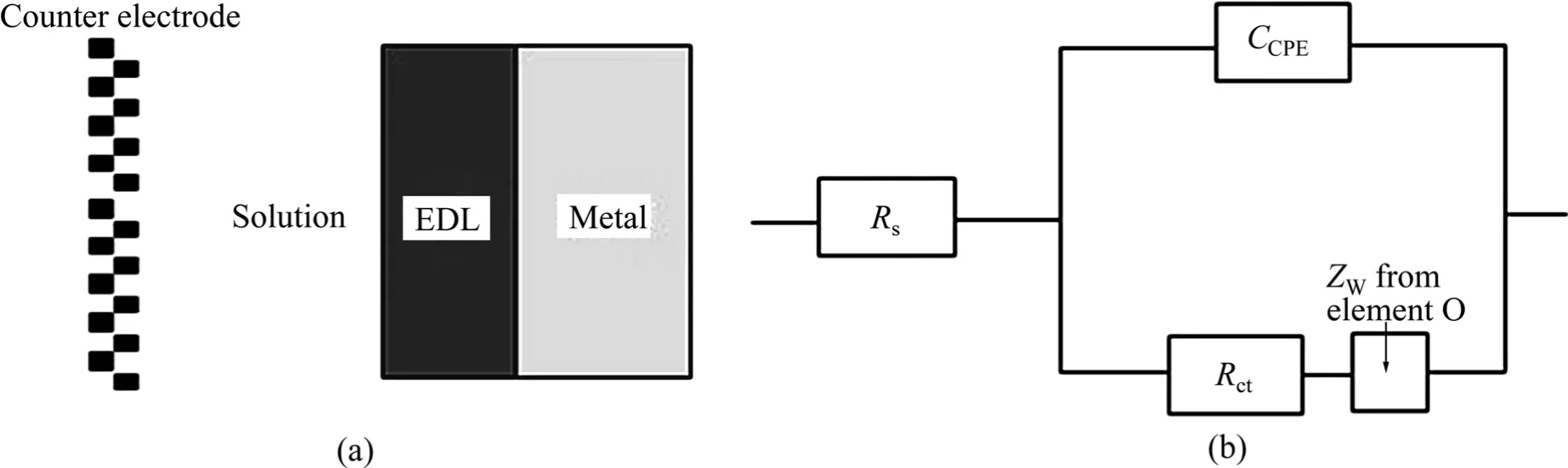
图4 EIS数据对应的物理模型及相应的等效电路Fig.4 Physical model (a) and its equivalent circuit (b) for fitting EIS data
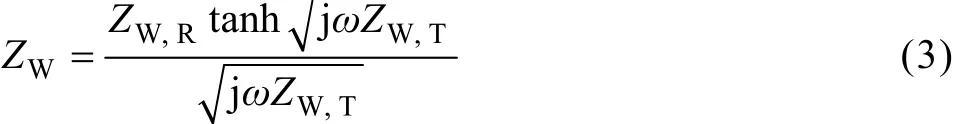
式中: ZW,T= L2/ D,L为有效扩散层厚度,D为粒子的有效扩散系数。
表4所列为依据所建等效电路拟合得到的各元件参数。可以看出,合金1的电荷传递电阻Rct、Warburg扩散阻抗ZW,R均比H72-1-1合金的有较大的提高,从而增加了腐蚀过程的阻力,在一定程度上减缓了腐蚀的进程,这与抗变色实验及静置腐蚀实验结果一致。
交流阻抗谱曲线吻合度系数χ2可通过Zview软件拟合软件、依据式(4)计算得到[14]:

式中:N为阻抗谱实际测得的点数;σ为Warburg系数;Zi′和 Zi″分别为实测阻抗的实部和虚部;Z′(ωi)和Z″(ωi)分别为通过等效电路模型拟合所得阻抗的实部和虚部。一系列对比等效电路列于表5(以H72-1-1合金为例),从表 5可以看出,对于本电化学体系,图4(b)所示的等效电路的 χ2值最小,约为 10−3,其吻合效果最好。
2.5 扫描电镜观察与能谱分析
图5所示为两种合金在3.5%NaCl溶液中浸泡腐蚀28 d后表面腐蚀形貌的二次电子像。图5(a)所示为合金1腐蚀后的表面形貌;图5(b)所示为H72-1-1合金腐蚀后的表面形貌。
由图5(a)可以看出,经过28 d浸泡腐蚀后,合金1表面的腐蚀产物呈细小的颗粒状,与基体结合紧密,有些颗粒团聚在一起,腐蚀产物膜完整而致密,未出现开裂或剥离现象;H72-1-1合金表面的腐蚀产物也呈细小的颗粒状,但是其腐蚀产物膜存在裂纹且局部区域已经脱落(如图5(b)中箭头A所示),从而重新暴露出合金基体,致使其保护效果变差,加速了合金的腐蚀。完整而致密的腐蚀产物膜层在腐蚀过程中对合金基体起保护作用,因此,图5从微观上印证了质量损失法和EIS测试的结果。
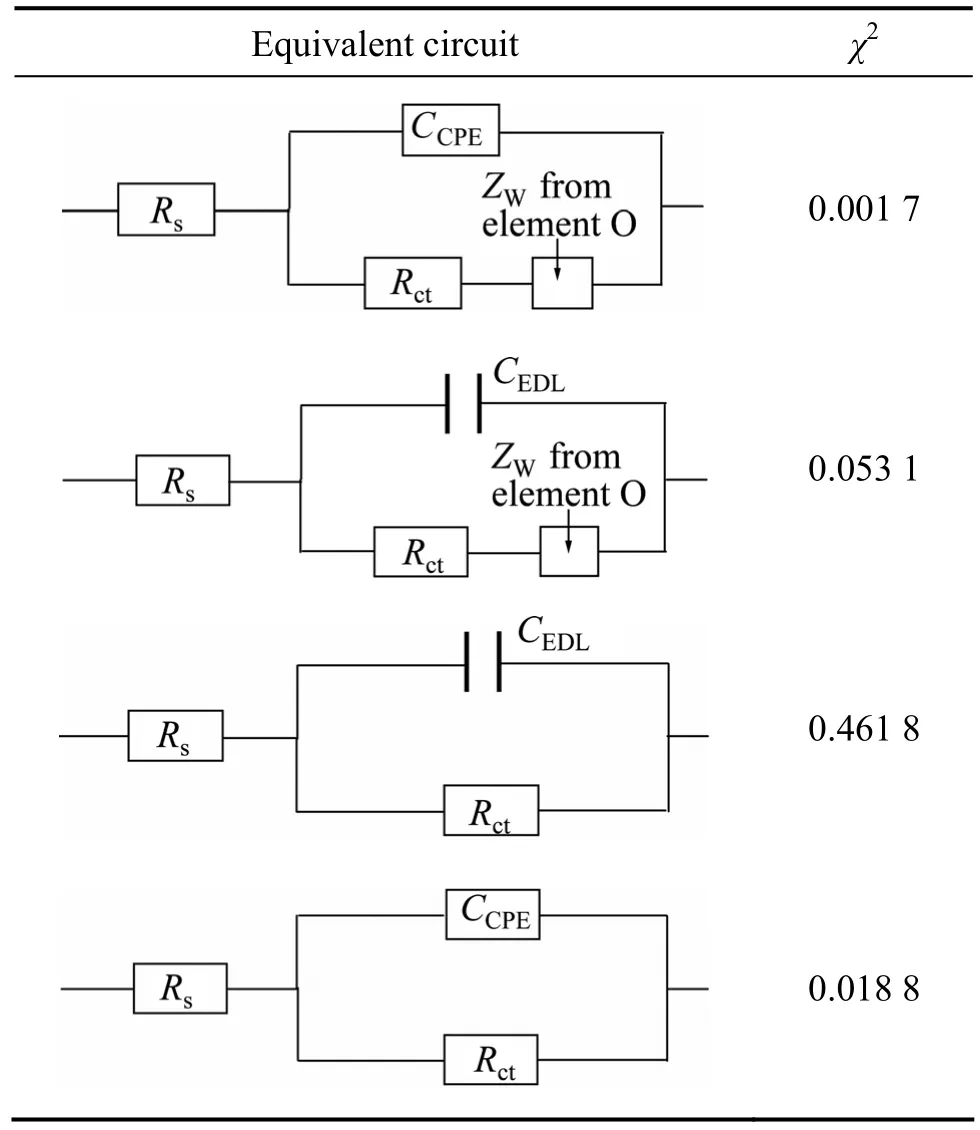
表5 用于模拟实验数据不同等效电路的吻合度系数χ2Table 5 Chi-squares χ2 of different equivalent circuits used in fitting experimental data
图6所示为两种合金在3.5%NaCl溶液中浸泡腐蚀28 d后的断面形貌。可以看出,合金1的腐蚀产物膜覆盖完整而均匀,其厚度约为7μm;而H72-1-1合金的腐蚀产物膜很薄(不足1 μm),而且覆盖不完整,局部膜层已经脱落(如图6(b)中箭头A所示),致使合金基体重新暴露出来,因而再次被腐蚀。

图5 两种合金在3.5%NaCl溶液中腐蚀28 d后的表面形貌Fig.5 Surface morhologies of two alloys after corroded in 3.5% NaCl solution for 28 d: (a) Alloy 1; (b) Alloy H72-1-1

图6 两种合金在3.5%NaCl溶液中腐蚀28 d后的断面形貌Fig.6 Morphologies of cross-section of two alloys after corroded in 3.5% NaCl solution for 28 d: (a) Alloy 1; (b) Alloy H72-1-1
通过对两种合金在3.5% NaCl溶液中浸泡腐蚀28 d后表面颗粒状腐蚀产物能谱分析可知,两种合金表面腐蚀产物中除了Cu元素外,还有O和Cl,而且这两种元素的质量分数较高(分别为17.96%和17.17%,以H72-1-1合金为例),说明O和Cl两种元素参与了腐蚀过程,由此推断腐蚀产物的主要成分是 Cu的氧化物、氯化物以及复杂的碱式氯化物等。
3 讨论
两种合金在 3.5%NaCl溶液中浸泡腐蚀的早期,可以观察到有一层气泡吸附在合金表面,在这一阶段,阳极过程主要是标准电极电位较负的 Zn优先溶解,而阴极过程则主要是H+还原成H2的过程,从而产生气泡吸附在合金表面。其反应式如下。

随着腐蚀过程的进行,合金表面部分区域发黄、发黑,这是因为在这个阶段,阳极过程以 Cu的氧化为主,Cu首先氧化成 Cu2O,然后再进一步氧化成CuO,而阴极过程则是O2的还原,其反应式如下[15]:

随后, C uCl−2在OH−的作用下,通过以下反应生成比较稳定的Cu2O[16]:

在溶解氧的作用下,Cu2O又通过以下两步反应生成CuO[17]:

在浸泡腐蚀后期,合金表面形成一层绿色薄膜,KATO等[18]和DRUSKA等[19]认为,经过长时间浸泡腐蚀后,腐蚀产物主要为Cu2Cl(OH)3、CuO及Cu2O,Cu2Cl(OH)3可通过以下反应生成[18]:

对于稀土元素的作用,毛向阳等[20]认为,稀土添加到铜及铜合金中后,具有净化组织、细化组织、改变夹杂物分布的作用,从而改善其加工性能、耐蚀和耐磨性能,机械性能及导电性能等。唐宁等[21]和张娟等[22]认为,由于稀土的电极电位较负,化学性质比较活泼,所以,稀土的加入使铝黄铜的自腐蚀电位降低;而稀土被氧化后,其氧化物与其他腐蚀产物一起在合金表面聚集成膜。这层膜致密、完整,且与基体结合紧密,它一方面能有效地将合金基体与腐蚀介质隔离,从而大幅度提高极化电阻,减小腐蚀电流,减缓腐蚀的进行;另一方面能较好地阻止锌从基体表面通过腐蚀产物向介质中扩散,在一定程度上抑制脱锌的发生。由本实验可以看出,稀土元素添加到铜合金中后,晶粒得到明显细化,合金具有良好的抗变色性能及耐腐蚀性能。
4 结论
1) 所设计合金显微组织与H72-1-1合金的相比更加细小、均匀。在中性盐雾实验中,所设计合金保持不变色的时间为2.5 h,较H72-1-1合金的延长了25%;在同一时间下,所设计合金的变色程度较H72-1-1合金的低,其抗变色性能明显优于H72-1-1合金的。
2) 所设计合金在3.5%NaCl溶液中浸泡腐蚀28 d后,合金表面形成一层均匀、致密、完整且与基体结合紧密的腐蚀产物膜,此膜能有效地将合金基体与腐蚀介质隔离,减缓了腐蚀的进程。
3) 建立了一个适合所设计合金体系的物理模型及等效电路,认为腐蚀过程中存在扩散过程,并由此产生了扩散阻抗;所设计合金的电荷转移电阻Rct和扩散阻抗ZW,R较H72-1-1合金的均有大幅度提高,由此增加了腐蚀过程的阻力,并在一定程度上减缓了腐蚀进程。
REFERENCES
[1] 王 鹏, 梁成浩, 张 婕. 铜及其合金防变色工艺研究现状[J].材料保护, 2007, 40(3): 52−55.WANG Peng, LIANG Cheng-hao, ZHANG Jie. Current state of research on anti-tarnishing technology for copper and its alloys[J]. Materials Protection, 2007, 40(3): 52−55.
[2] ALFANTAZI A M, AHMED T M, TROMANS D. Corrosion behavior of copper alloys in chloride media[J]. Materials and Design, 2009, 30(7): 2425−2430.
[3] CHEN J L, LI Z, ZHAO Y Y. Corrosion characteristic of Ce-Al brass in comparison with As-Al brass[J]. Materials and Design,2009, 30(5): 1743−1747.
[4] 吕雪飞, 李淑英. 环保型铜及其合金化学抛光与钝化新工艺[J]. 材料保护, 2006, 39(9): 25−27.LÜ Xue-fei, LI Shu-ying. Environmentally-friendly chemical polishing and passivation process for copper and its alloys[J].Materials Protection, 2006, 39(9): 25−27.
[5] 方景礼, 方 欣. 金属表面配合物保护膜述评(Ⅱ)—铜及铜合金的防变色配合物膜[J]. 材料保护, 2007, 40(11): 76−80.FANG Jing-li, FANG Xin. A review on the protective films composed of surface metallic complexes (Ⅱ)—Surface metallic complex film for anti-color-fading of copper and copper alloys[J]. Materials Protection, 2007, 40(11): 76−80.
[6] 王 鹏. 铜质币腐蚀变色机理及抗变色工艺研究[D]. 大连: 大连理工大学, 2009: 29−30.WANG Peng. Tarnishing mechanism and anti-tamishing techniques of copper and brass coins[D]. Dalian: Dalian University of Technology, 2009: 29−30.
[7] SHERIF E M. Effects of 2-amino-5-(ethylthio)-1, 3, 4-thiadiazole on copper corrosion as a corrosion inhibitor in 3%NaCl solutions[J]. Applied Surface Science, 2006, 252(24):8615−8623.
[8] SHERIF E M, PARK S M. 2-Amino-5-ethyl-1, 3, 4-thiadiazole as a corrosion inhibitor for copper in 3.0% NaCl solutions[J].Corrosion Science, 2006, 48(12): 4065−4079.
[9] 吕雪飞, 李淑英. 铜合金稀土钝化新工艺的研究[J]. 吉林化工学院学报, 2006, 23(2): 17−18.LÜ Xue-fei, LI Shu-ying. Study of a new passivation process with rare earth for copper alloys[J]. Journal of Jilin Institute of Chemical Technology, 2006, 23(2): 17−18.
[10] 李 锋, 刘 俊, 陈 颢. 铜及其合金表面钝化新工艺的研究[J].电镀与涂饰, 2005, 24(2): 15−17.LI Feng, LIU Jun, CHEN Hao. Study of a new passivation process for copper and its alloys[J]. Electroplating and Finishing,2005, 24(2): 15−17.
[11] ZHANG X H, PEHKONEN S O, KOCHERGINSKY N, ELLIS G A. Copper corrosion in mildly alkaline water with the disinfectant monochloramine[J]. Corrosion Science, 2002,44(11): 2507−2528.
[12] RAMMELT U, REINHARD G. On the applicability of a constant phase element (CPE) to the estimation of roughness of solid metal electrodes[J]. Electrochimica Acta, 1990, 35(6):1045−1049.
[13] BOUKAMP B A. A package for impedance/admittance data analysis[J]. Solid State Ionics, 1986, 18/19: 136−140.
[14] BOUKAMP B A. A nonlinear least squares fit procedure for analysis of immittance data of electrochemical systems[J]. Solid State Ionics, 1986, 20(1): 31−44.
[15] KEAR G, BARKER B D, WALSH F C. Electrochemical corrosion of unalloyed copper in chloride media—A critical review[J]. Corrosion Science, 2004, 46(1): 109−135.
[16] YUAN S J, PEHKONEN S O. Surface characterization and corrosion behavior of 70/30 Cu-Ni alloy in pristine and sulfide-containing simulated seawater[J]. Corrosion Science,2007, 49(3): 1276−1304.
[17] SANCHEZ S R, BERLOUIS L E A, SCHIFFRIN D J.Difference reflectance spectroscopy of anodic films on copper and copper base alloys [J]. Electroanal Chem, 1991, 307(1/2):73−86.
[18] KATO C, ATEYA B G, CASTLE J E, PICKERING H W. On the mechanism of corrosion of Cu-9.4 Ni-1.7 Fe alloy in air saturated aqueous NaCl solution[J]. Electrochem Soc, 1980, 127(9): 1897−1903.
[19] DRUSKA P, STREHBLOW H H, GOLLEDGE S. A surface analytical examination of passive layers on Cu/Ni alloys(Part Ⅰ)—Alkaline solution[J]. Corrosion Science, 1996, 38(6):835−851.
[20] 毛向阳, 方 峰, 谈荣生, 蒋建清. 稀土对铜及铜合金组织和性能影响的研究进展[J]. 稀土, 2008, 29(3): 75−80.MAO Xiang-yang, FANG Feng, TAN Rong-sheng, JIANG Jian-qing. Review on effects of rare earth on microstructure and properties of copper and copper alloy[J]. Chinese Rare Earths,2008, 29(3): 75−80.
[21] 唐 宁, 李 周, 程建奕, 肖 柱, 龚 深, 张德智. 稀土铝黄铜在 NaCl溶液中腐蚀行为的研究[J]. 材料热处理学报, 2007,28(6): 104−108.TANG Ning, LI Zhou, CHENG Jian-yi, XIAO Zhu, GONG Shen, ZHANG De-zhi. Study of corrosion behavior of aluminum brass with rare-earth in NaCl solution[J]. Transactions of Materials and Heat Treatment, 2007, 28(6): 104−108.
[22] 张 娟, 李 周, 陈 畅, 唐 宁, 张德智. 含铈铝黄铜的显微组织与性能[J]. 中国有色金属学报, 2008, 18(11): 1989−1994.ZHANG Juan, LI Zhou, CHEN Chang, TANG Ning, ZHANG De-zhi. Microstructure and properties of aluminum brass with Ce[J]. The Chinese Journal of Nonferrous Metals, 2008, 18(11):1989−1994.
Corrosion behavior of novel colour-stable imitation gold copper alloy with rare earth
LUO Li-yang1, ZHU An-yin1, CHEN Jing-lin1, LI Zhou1, LIANG Jun2, ZHANG Xiao-nan2
(1. School of Materials Science and Engineering, Central South University, Changsha 410083, China;2. Research Institute of Shenyang Mint, China Banknote Printing and Minting Corporation, Shenyang 110042, China)
A novel colour-stable imitation gold copper alloy with rare earth was designed and prepared. The microstructures, anti-tarnishing and corrosion resistance properties of the designed alloy and the existing mint metal of H72-1-1 were compared by means of metallographic analysis, neutral salt spray test, mass loss measurement,electrochemical impedance spectroscopy and scanning electron microscopy. The results show that the annealed microstructure of the designed alloy is fine and homogeneous, and discoloring time of the alloy in 3.5% NaCl solution is 25% longer than that of H72-1-1 alloy. The mass loss rate of the designed alloy is slightly lower than that of the H72-1-1 alloy in 3.5% NaCl solution, which can be attributed to the uniform and compact corrosion film which retards the corrosion process, and the corrosion rate is 10.3 μm/a. The charge transfer resistance Rctand the diffusion impedance ZWof the designed alloy increase much more greatly than those of the H72-1-1 alloy, which increases the corrosion process resistance.
imitation gold alloy; copper alloy; anti-tarnishing performance;corrosion resistance performance
TG 178
A
1004-0609(2011)07-1639-08
国际铜业协会“耐蚀铜合金”资助项目(MBP3553)
2010-06-23;
2010-08-25
李 周,教授,博士;电话:0731-88830264;E-mail:lizhou6931@163.com
(编辑 陈卫萍)
