甲磺酸帕珠沙星缓释微球的制备工艺研究
2011-11-11余楚钦许文杰
申 楼,余楚钦,许文杰
(1.广东药学院药物研究所,广东广州 510006;2.广州中山医医药有限公司,广东广州 510600)
甲磺酸帕珠沙星缓释微球的制备工艺研究
申 楼1,余楚钦1,许文杰2
(1.广东药学院药物研究所,广东广州 510006;2.广州中山医医药有限公司,广东广州 510600)
目的:制备甲磺酸帕珠沙星缓释微球,探索制备工艺对微球性能的影响。方法:以壳聚糖、明胶为缓释载体材料,采用正交设计,以药物与辅料比、水油相比、交联剂用量及搅拌速率为考察因素,以载药量、包封率、外表形态及平均粒径为指标,筛选最佳工艺条件。结果:优选工艺为A2B3C3D2,即药物与辅料比为25%、水油相比为10%、交联剂用量为15%、搅拌速率为800 r/min。结论:所得微球外表形态良好,包封率高,工艺稳定。
甲磺酸帕珠沙星缓释微球;海水浸泡伤;制备工艺;正交设计
甲磺酸帕珠沙星(Pazufloxacin Medilate,PZFX)属于第四代喹诺酮类抗菌药,对革兰阳性菌及革兰阴性菌具有强大的抗菌活性[1]。临床用于治疗尿路感染、呼吸道感染、外科感染等[2]。
在各种海上工作、活动中,海水浸泡伤发生率很高,此类损伤具有致病菌多、高渗透压、感染严重等特点,其治疗措施之一是早期使用抗生素[3-4],但至今尚无一种可推广应用的抗生素类敷料。将PZFX制成缓释微球用于该病早期治疗,可减少用药次数、稳定药物浓度、提高患者顺应性,可能会有很好的发展前景。
1 仪器与试药
1.1 仪器
HS7加热电磁搅拌仪 (德国IKA公司);SUB14三孔水浴锅(英国Grant公司);DLSB-510低温冷却循环泵(巩义裕华仪器有限公司);UV-1601紫外分光光度仪 (日本岛津公司);B203TR生物显微镜(重庆奥特光学仪器有限公司);十万分之一天平(德国Sartorius公司)。
1.2 试药
甲磺酸帕珠沙星原料(湖南华纳大药厂,批号:090904);壳聚糖(天津光复精细化工研究所);明胶(天津科密欧化学试剂有限公司);司盘-80(span-80,美国国际特品公司);液体石腊(深圳耀华化学试剂厂);戊二醛(广州化学试剂厂);其他试剂均为分析纯。
2 方法与结果
2.1 PZFX缓释微球制备
2.1.1 4%壳聚糖溶液的配制 将3 ml冰醋酸加入100 ml蒸馏水中,搅拌均匀,在搅拌下加入4 g壳聚糖,70℃水浴下保持搅拌30 min,使充分溶解,得4%壳聚糖溶液,备用。
2.1.2 10%明胶溶液的配制 将10 g明胶加入100 ml蒸馏水中,70℃水浴下保持搅拌15 min,使溶解完全,即得10%明胶溶液,备用。
2.1.3 制备方法 称取药物3.5 g,溶于适量蒸馏水中,加至盛有4%壳聚糖溶液、10%明胶溶液的2 L烧杯中,于50℃水浴、800 r/min搅拌下分别加入270 ml液状石蜡和6 g司盘-80,乳化分散20 min,迅速移至低温冷却循环泵中,3~6℃冰浴下缓慢加入2 ml戊二醛,搅拌20 min,再缓慢加入剩下的戊二醛,继续搅拌固化2 h,搅拌下加入400 ml丙酮,脱水20 min,取出,弃去上清液,于转速6 000 r/min离心20 min,弃去上清液,所得沉淀以适量乙醚洗涤,抽滤,弃去滤液,滤渣于35℃干燥,即得流动性较好的粉末状微球。
2.2检测波长选择
取PZFX适量,用0.1 mol/L的HCl溶液溶解并稀释制成8 μg/ml的溶液,照紫外分光光度法在200~400 nm波长范围内扫描,结果在247、332 nm波长处有最大吸收。另将各辅料按处方混合均匀,同法操作,结果在该波长处几乎无吸收。因为247 nm处吸收相对较大,故选择247 nm作为检测波长。见图1。

图1 PZFX在0.1 mol/L HCl溶液的UV吸收图谱
2.3 标准曲线制备
精密称取干燥至恒重的PZFX约20 mg,置50 ml量瓶中,加0.1 mol/L HCl溶液溶解并稀释至刻度,过滤,精密量取续溶液,分别加 0.1 mol/L HCl溶液制成 4、5、6、7、8、9 μg/ml的溶液,以0.1 mol/L HCl溶液为空白,在247 nm处测定吸光度,以浓度C为横坐标,以吸光度A为纵坐标进行线性回归,得回归方程:A=0.248 1C+0.036 37(r=0.999 4),该药在 4~9 μg/ml浓度范围内线性关系良好。
2.4 回收率试验[5]
精密称取PZFX适量,分别按处方量的80%、100%、120%投料于250 ml量瓶中,加入相应处方量的空白辅料,加入0.1 mol/L HCl溶液200 ml使溶解,加0.1 mol/L HCl溶液至刻度,摇匀,精密量取5 ml于100 ml量瓶中,加0.1 mol/L HCl溶液至刻度,摇匀,以0.1 mol/L HCl溶液为空白,在247 nm处测定吸光度,计算回收率,结果平均回收率为99.87%(n=9)。
2.5 载药量及包封率测定
精密称取微球样品20 mg,置50 ml量瓶中,加0.1 mol/L HCl溶液40 ml,摇匀,70℃水浴使完全溶解,加0.1 mol/L HCl溶液稀释至刻度,摇匀。再精密量取1.0 ml此液置25 ml量瓶中,加0.1 mol/L HCl溶液至刻度,摇匀,以0.1 mol/L HCl溶液为空白,在247 nm处测定吸光度,由标准曲线方程计算微球中药物含量,从而计算其载药量及包封率。结果:载药量为19.2%、包封率77.9%。计算公式:载药量=(微球中药物含量/微球总重量)×100%;包封率=(微球中药物含量/投药量)×100%。
2.6 微球的形态及粒径考察[6]
采用显微镜计数法、考察微球外表形态、粒径范围及平均粒径,每批不少于500粒,方法:取少量微球,用适量石蜡油稀释,搅拌均匀,于光学显微镜进行观察和拍照。结果:所得微球较圆整,分散性好,粒径在14~39 μm范围内者占90%以上,平均粒径为26 μm。见图2。
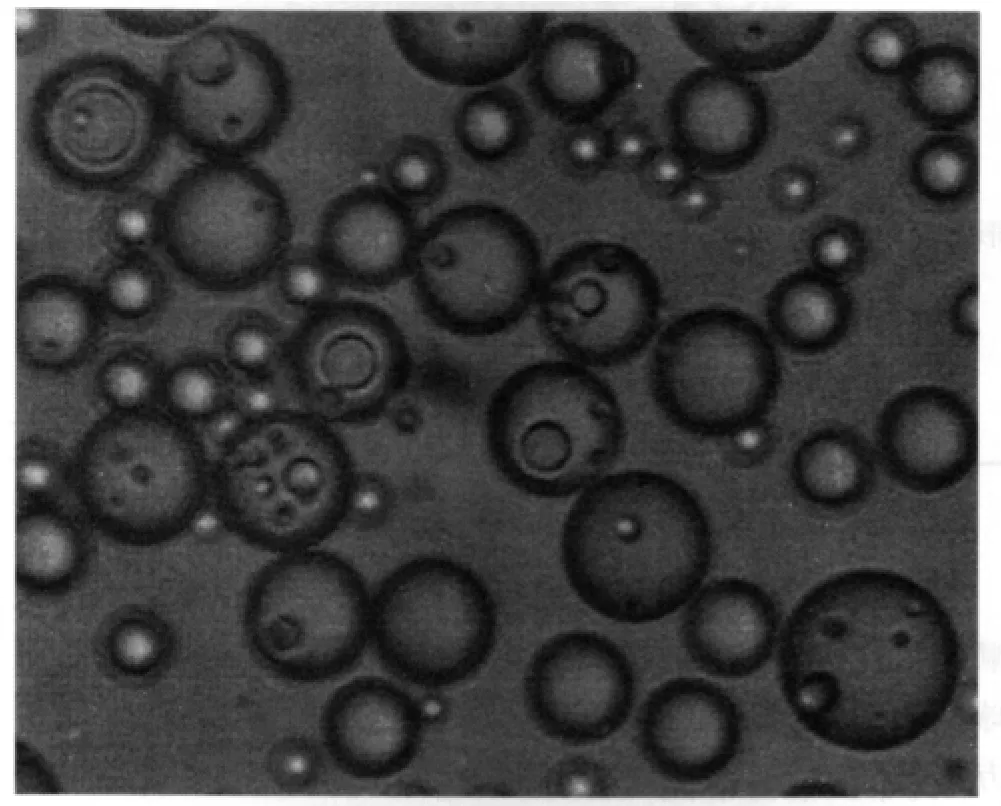
图 2 光学显微镜下PZFX微球(×100)
2.7 单因素考察
采用亲水性的吐温-80为乳化剂时,乳液易分层、不稳定,改用亲油性的司盘-80能很快形成稳定的乳液,故本实验选用司盘-80为乳化剂;实验中若反应时间过短,难以形成或形成的微球不圆整,经试验,固化时间约为2 h较理想;搅拌速度过低,微球之间易粘连且只有少数外表圆整,提高搅拌速度,则微球分散性好、圆整且粒径较小,因此初步选择700~900 r/min的转速。
2.8 正交试验设计
影响微球制备工艺的因素较多[7-8],在对乳化剂的种类及比例、反应时间及搅拌速度等单因素考察的基础上,选出影响工艺较显著的4个因素即药物与辅料比(A)、水油相比(B)、交联剂用量(C)、搅拌速率(D)为考察因素,以微球的载药量、包封率、形态、粒径为指标,采用 L9(34)正交表进行试验并综合评分来筛选最佳工艺。结果见表1、2。

表1 因素水平表

表2 正交试验设计表及结果
由表2可知,各因素对微球载药量及包封率影响的大小顺序依次为B>D>A>C,最佳处方工艺为A2B3C3D2;各因素对微球外表形态和粒径影响的大小顺序依次为B>D>A>C,最佳处方工艺为A2B3C3D1,主要影响因素为B和D,综合考虑最终确定处方工艺为A2B3C3D2,即药物与辅料比25%、水油相比10%、交联剂用量15%、搅拌速率800 r/min。
2.8 工艺验证试验
按上述优选的最优处方工艺,连续制备3批微球,分别考察其载药量、包封率、形态及粒径,结果3批微球的工艺重复性良好。见表3。

表3 PZFX微球的验证试验结果
3 讨论
本文采用单因素考察和正交试验,探索了药物与辅料比例、水油相比、乳化剂用量、交联剂用量、制备温度、搅拌速率对微球载药量、包封率、形态及粒径等的影响,从而筛选出最优工艺条件。由本实验可知,药物与辅料比、水油相比、乳化剂用量对粒径和外表形态影响相对较大,因此,本实验要制备粒径较小的微球,应采取下列方法:①减小水油相比;②增大乳化剂用量;③减小壳聚糖明胶溶液浓度,而交联剂用量、搅拌速率侧重于影响载药量和包封率,将交联剂的用量定为15%,因为通过预试验发现若用量过少或过多均会使载药量降低,原因可能是用量少,交联反应不完全所致;用量过多而载药量低,可能是速度较快而使固化时间缩短所致。搅拌速率定为700~900 r/min,因为实验中发现搅拌速率低于700 r/min时,微球粘连且包封率较低,搅拌速率高于900 r/min时,微球因受力不均而变形,亦影响形态和包封率。
[1]刘明亮,郭慧元.新喹诺酮类抗菌药甲磺酸帕珠沙星[J].中国新药杂志,2004,13(2):1164-1168.
[2]金阳,辛建保,杨晓,等.甲磺酸帕珠沙星治疗细菌性感染的多中心临床试验[J].中国医院药学杂志,2006,26(10):1225-1227.
[3]Chang WJ,Pien FD.Manine-acquired infections:hazards of the ocean ervironment[J].Postgrad Med,1986,80(4):30-32.
[4]沈宏亮,王强.海水浸泡创伤病理生理变化和救治措施的研究[J].第二军医大学学报,2003,24(12):1365-1367.
[5]王立敏,潘红芳,曲福军.HPLC法测定甲磺酸帕珠沙星原料及其制剂含量[J].中国药师,2005,8(12):999-1001.
[6]崔福德.药剂学[M].北京:人民卫生出版社,2008:411.
[7]常海涛.壳聚糖/聚乙烯醇复合药物缓释微球制备工艺的研究[J].应用科技,2008,16(14):21-23.
[8]孙瑞雪,史京京,郭燕川,等.明胶微球粒径控制的研究[J].高分子学报,2008,8(8):779-784.
Preparation research of Pazufloxacin Medilate sustained-release Microspheres
SHEN Lou1,YU Chuqin1,XU Wenjie2
(1.Institute of Drug Research,Guangdong College of Pharmacy,Guangzhou 510006,China;2.Guang Zhou Z.S.Y Pharmaceutical Co.Ltd.,Guangzhou 510600,China)
Objective:To prepare sustained-release Microspheres of Pazufloxacin Medilate and study preparations how to affect its quality.Methods:By orthogonal design method,the gelatin and chitosan were used as sustained-release material,the proportion of medicine and excipients,the proportion of water and oil,the amount of glutaraldehyde and the stirring rate were used as factors.The drug loading,encapsulation rate and average particle size were used as index to find the best condition.Results:The optimum condition was A2B3C3D2.The proportion of gelatin and chitosan was 25%,the proportion of water and oil was 10%,the amount of glutaraldehyde was 15%and the stirring rate was 800 r/min.Conclusion:The Microspheres were made good shape and large encapsulation rate,its preparation was stable.
Pazufloxacin Medilate sustained-release Microspheres;Seawater soaked wounds;Preparation;Orthogonal design
R943
A
1673-7210(2011)01(b)-060-03
申楼(1973-),男,工程师,从事制剂与药物新剂型研究。
2010-07-01)
