TiO2-CoFe2O4磁性复合材料制备及太阳光催化性能
2011-11-09张秀玲孙东峰韩一丹
张秀玲 孙东峰 韩一丹 王 静
(大连大学物理科学与技术学院,大连 116622)
TiO2-CoFe2O4磁性复合材料制备及太阳光催化性能
张秀玲*孙东峰 韩一丹 王 静
(大连大学物理科学与技术学院,大连 116622)
以四氯化钛、三价铁盐和二价钴盐为前驱体,采用超声波技术一步合成了TiO2-CoFe2O4新型复合光催化剂,运用VSM、XRD、TEM和UV-Vis技术进行了表征,以甲基橙为模拟污染物在太阳光照射下研究其光催化活性。结果表明:所制得的样品具有良好的顺磁性,其饱和磁化强度为212 Gs;样品中TiO2和CoFe2O4分别以锐钛矿相和尖晶石结构存在,粒径尺寸在40~50 nm之间;样品在紫外-可见区有很强的吸收。光催化结果表明复合催化剂具有较高的太阳光催化活性,循环使用3次,仍能保持良好的催化活性。
磁性;二氧化钛;复合材料;太阳光光催化剂
0 引 言
半导体光催化氧化降解有机物已成为环境污染治理的研究热点[1-3],作为一种应用广泛的光催化剂,TiO2以其无毒、催化活性高、氧化能力强、稳定性好而最为常用。在污水处理领域[4],悬浆型光催化反应器因其高比表面积和良好的分散性而受到普遍的关注。然而,由于受到从水中回收纳米TiO2微粒的困扰,悬浆型光催化反应器仍然受到很大的限制。为了克服催化剂分离的困难,研究者将TiO2负载在玻璃珠[5]、玻璃纤维[6]、沸石[7]等载体上制备负载型光催化剂。由于这些光催化剂载体较小的比表面积,降低了TiO2的负载量和光催化活性。另一方面,由于TiO2的带隙较大(~3.2 eV),只有在紫外光激发下才能产生光催化活性,而紫外光只占太阳光的3%~5%,极大地限制了它的应用。
近年来,关于可磁分离的磁载型光催化剂的研究已成为国内外研究的焦点[8-12]。该类催化剂既具备悬浮相光催化剂的高效性,又可利用磁性回收,克服了悬浮状TiO2粉末回收困难的缺点,具有广泛的应用前景。目前制备磁载TiO2光催化剂主要是通过两步法[13-16],即首先制备出具有结构稳定、磁饱和强度高的磁性颗粒,然后将TiO2负载到磁性颗粒上制得磁载TiO2光催化剂,此种方法制备工艺较复杂、制备周期长,不利于大规模工业生产。因此,减少工艺流程,缩短制备时间对可磁分离TiO2光催化剂的实用化具有重要意义。
本工作以四氯化钛、三价铁盐、二价钴盐为前驱体,采用超声波技术一步合成了TiO2-CoFe2O4新型复合光催化剂,该方法具有原料易得成本低廉,制备工艺简单,制备周期短等优点。所制得的TiO2-CoFe2O4复合光催化剂显示了良好的顺磁性,可通过外磁场进行有效的分离,便于回收和再利用;同时在制备过程中少量Fe3+和Co2+对TiO2进行了掺杂,拓展了复合催化剂的光响应范围,因而复合催化剂具有较高太阳光催化活性,为可磁分离TiO2太阳光催化剂的研究提供实验依据。
1 实验部分
1.1 TiO2-CoFe2O4复合光催化剂的制备
在冰水浴机械搅拌条件下,取6 mL TiCl4(分析纯,天津市光复精细化工研究所)加入溶有2 mL HCl的100 mL去离子水中,搅拌5 min得到TiCl4水溶液,以nTi∶nFe∶nCo=3∶2∶1,加入10.34 g Fe2(SO4)3· 9H2O(分析纯,北京化工厂)和3.50 g Co(NO3)2·6H2O (分析纯,上海化学试剂一厂),继续搅拌使反应体系混合均匀,启动加热装置;在体系温度至72℃时,启动超声波进行超声分散,用NH3·H2O调节体系pH值在8~10范围内,机械搅拌和超声分散作用下反应1 h得到固体样品;冷却后将上述固体样品经水洗、无水乙醇洗各3次,在100℃下烘干,500℃焙烧2 h,即得TiO2-CoFe2O4复合太阳光催化剂。
相同实验条件下,通过改变Fe2(SO4)3·9H2O和Co(NO3)2·6H2O(nFe∶nCo=2∶1)加入量,制备 TiO2与CoFe2O4物质的量的比值分别为1∶1,2∶1,4∶1,5∶1,6∶1的TiO2-CoFe2O4复合太阳光催化剂。为方便表述,我们将 TiO2-CoFe2O4复合太阳光催化剂中 TiO2与 CoFe2O4物质的量的比标记为:nT∶nCF,其中T表示TiO2,CF表示CoFe2O4。
1.2 样品表征
采用美国Lake Shore 7410型振动样品磁强计(VSM)对样品的磁性能进行测定(工作条件为室温)。采用日本岛津XRD-6000型X射线衍射仪(XRD)对样品相结构和相组成进行表征(Cu靶Kα辐射,λ= 0.154 18 nm,加速电压为40 kV,电流为30 mA,扫描范围为10°~80°,扫描速率为4°·min-1,步宽为0.04°)。利用H-600A型透射电子显微镜(TEM)研究样品的形貌和分散性(工作电压为75 kV)。采用美国瓦里安中国有限公司Cary100型紫外/可见分光光度计(UV-Vis)表征样品紫外-可见光吸收性能(对比基准物为BaSO4,扫描范围为200~800 nm)。
1.3 光催化活性评价
光催化活性评价是通过研究降解甲基橙实现的。在培养皿中放入50 mL浓度约为20 mg·L-1的甲基橙(分析纯,天津市天新精细化工开发中心)水溶液,对应加入1.0 g催化剂,搅拌均匀,放入暗箱中10 min使催化剂达到吸附平衡,然后放在太阳光下照射,每隔固定时间取样,离心,取上清液,采用721分光光度计 (上海菁华科教仪器有限公司)在468 nm处测定甲基橙的吸光度。在低浓度范围内甲基橙的吸光度和浓度之间有很好的线性关系,且遵守朗伯-比耳定律,以脱色率来衡量降解程度,试样的脱色率η以下式计算:

式中C0:甲基橙溶液的初始浓度(mg·L-1);C:不同光照时间甲基橙溶液的浓度(mg·L-1)。
2 结果与讨论
2.1 TiO2-CoFe2O4复合催化剂的表征
2.1.1 磁性能分析
图1为所制备的TiO2-CoFe2O4复合光催化剂的磁性能曲线。从图1中可以看出,在最大磁化场强下,TiO2-CoFe2O4复合光催化剂的饱和磁化强度为212 Gs。磁化过程中TiO2-CoFe2O4复合光催化剂基本没有磁滞现象,矫顽力和剩磁几乎可以忽略,这说明制备的光催化剂具有超顺磁性,即当外加磁场强度降到零时,所制备粒子的剩磁也几乎降到零。因此,在无外加磁场作用下,催化剂能够很容易地分散在反应体系中,当赋予悬浆反应体系外加磁场时,能够方便地回收催化剂。

2.1.2 XRD,TEM分析
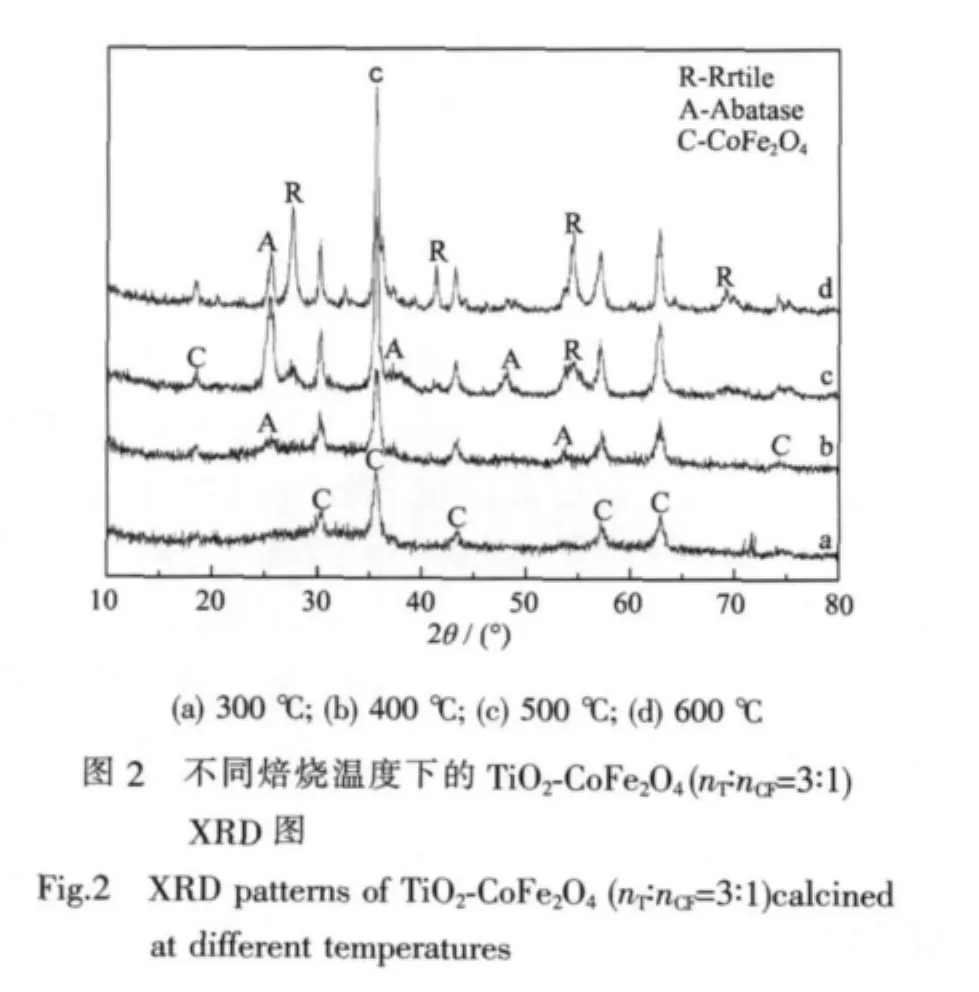
图2为TiO2-CoFe2O4(nT∶nCF=3:1)复合光催化剂在不同焙烧温度下XRD表征结果。从图2可以看出在温度低于300℃时,只存在明显的CoFe2O4的衍射峰,与PDF标准卡片相吻合,其中CoFe2O4以尖晶石结构存在。在焙烧温度为400℃时,样品的XRD图中出现了明显的TiO2锐钛矿(101)特征衍射峰(2θ= 25.4°)。在焙烧温度达到500℃时,在2θ为25.41°、38.72°、48.07°、53.93°和54.3°处出现的衍射峰分别对应锐钛矿TiO2的(101)、(004)、(200)、(105)和(211)特征峰,说明在此焙烧温度下TiO2主要以锐钛矿相存在。当焙烧温度升至600℃时,在2θ为27.3°出现了明显的金红石相的TiO2衍射峰,说明锐钛矿相的TiO2随着焙烧温度增加逐渐转化为金红石相。在复合体整个结晶过程中,始终没有其它中间相如CoTiO3或Fe2(TiO3)3的衍射峰出现,可能是由于中间相生成量较小,XRD测试检测不出。可以认为复合体中TiO2和CoFe2O4基本为各自生长,没有发生反应生成新的物相。
图3为TiO2-CoFe2O4(nT∶nCF=3∶1)复合光催化剂的TEM照片。从图3中可以看出TiO2-CoFe2O4复合材料为无规则形状的纳米颗粒,尺寸较小,颗粒的平均尺寸在40~50 nm之间。

2.1.3 UV-Vis分析
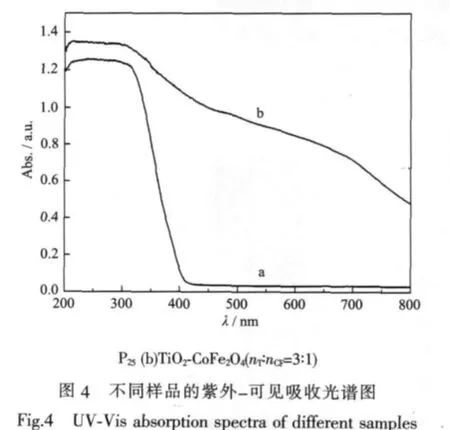
图4显示了P25和TiO2-CoFe2O4(nT∶nCF=3:1)复合光催化剂的紫外-可见吸收光谱。从图4 P25的吸收曲线可以看出锐钛矿型TiO2对光的吸收范围在200~400 nm,主要集中在紫外区域,对超过400 nm的太阳光几乎没有吸收。由图4 TiO2-CoFe2O4的吸收曲线可以看出,所制备的复合光催化剂在整个紫外-可见区域都有很强的吸收,在紫外光区域的吸收强度得到提高,并且吸收带边发生了明显的红移,在470~480 nm间。这可能是由于Fe3+掺杂使TiO2的价带位置向上移动,导带位置不变,从而使TiO2禁带宽度变窄;另一方面,刘秀华等[17]认为,由于Co2+和Ti4+的6配位离子半径比较接近,容易取代晶格位置上的Ti4+而形成CoTiO3或者进入晶格间隙,从而在晶格中产生了晶体缺陷,由于杂质能级或缺陷能级的出现,降低了带隙能,增强了对光的吸收。此外,TiO2-CoFe2O4复合光催化剂强的可见光吸收性能是由于磁性部分CoFe2O4在可见光区表现出的吸收所致。复合掺杂不但可以提高TiO2对紫外光的吸光度,而且可以使TiO2吸收光谱发生“红移”,提高了对太阳频谱的利用率,这对于开发日光型光催化剂十分有利。
2.2 TiO2-CoFe2O4复合光催化剂的光催化性能
不同TiO2和CoFe2O4物质的量的比的复合光催化剂的催化性能如图5所示。由图5可知,随着物质的量的比值的增加,TiO2-CoFe2O4复合光催化剂活性逐渐升高,在nT∶nCF=3∶1时,催化剂活性达到最大,TiO2含量进一步增大,催化剂活性略有下降。由于采用一步合成法,在复合催化剂的制备过程中部分Fe3+和Co2+对TiO2进行掺杂,其中少量Fe3+极易取代晶格位置上的Ti4+,发生缺陷生成反应[18],同时Co2+掺杂锐钛矿TiO2晶体后,使TiO2的Fermi能级降低,从而使电子-空穴在表面的复合几率降低,增强了光催剂的活性。当TiO2和CoFe2O4物质的量的比值小于3时,复合催化剂中TiO2的相对含量较小导致催化剂活性较低;随着物质的量的比值的增加,复合催化剂的活性逐渐升高,当nT:nCF=3:1时,在本实验条件下Fe3+和Co2+的掺杂量适中,从而复合催化剂具有较高的太阳光催化活性;TiO2含量进一步增大,离子掺杂相对量变小,TiO2表面引起的缺陷位置偏少,导致催化剂活性略有下降。综合考虑复合光催化剂的光催化活性和磁性能,我们选择nT∶nCF=3∶1为最佳实验配比。
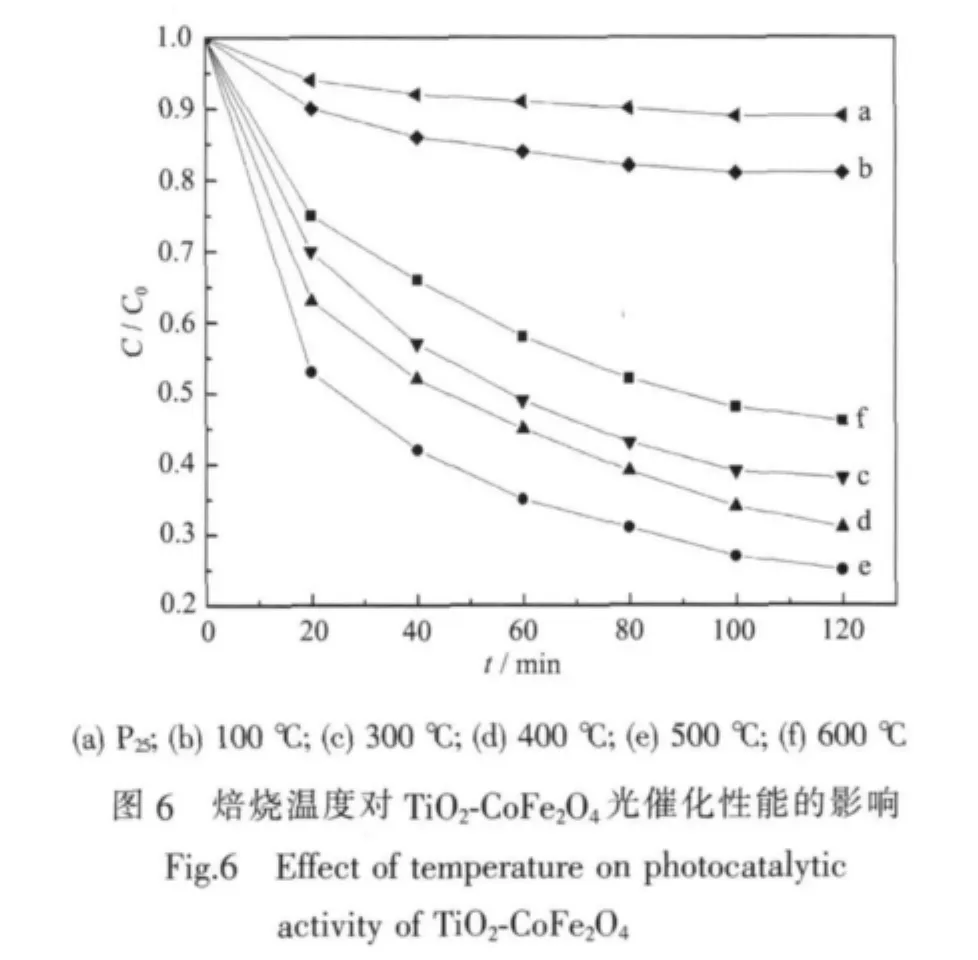
图6为nTiO2∶nCoFe2O4=3∶1的TiO2-CoFe2O4在不同焙烧温度的样品光催化降解甲基橙的实验结果。当焙烧温度由100℃升至500℃时,随着焙烧温度的升高,TiO2-CoFe2O4复合光催化剂的活性逐渐增大,在焙烧温度为500℃时催化剂活性达到最大;当焙烧温度进一步增加,光催化剂的活性下降,这一结果与XRD分析一致,证明锐钛矿相是催化活性相。在相同光照条件下,P25催化降解甲基橙的降解率仅为12%,这说明制备的TiO2-CoFe2O4复合光催化剂中TiO2的晶体结构不同于P25。Fe3+和Co2+掺杂TiO2锐钛矿相作为活性相,致使TiO2-CoFe2O4复合光催化剂具有较高的太阳光催化活性。

将TiO2-CoFe2O4复合光催化剂光催化降解甲基橙2 h,然后通过磁分离回收、烘干,循环使用3次测定其降解率分别为78.5%、77.3%和75.6%。这说明,随着重复使用次数的增加,TiO2-CoFe2O4复合光催化剂的光催化活性只是略微的下降,说明该催化剂具有良好的重复使用性能。
3 结 论
以四氯化钛、三价铁盐、二价钴盐为前驱体,采用超声波技术一步合成了TiO2-CoFe2O4复合光催化剂,并对其物理化学性能和太阳光催化性能进行了研究。主要结论如下:
(1)TiO2-CoFe2O4复合光催化剂的饱和磁化强度为212 Gs,具有超顺磁性;样品中的TiO2和CoFe2O4分别以锐钛矿相和尖晶石结构存在,TiO2和CoFe2O4基本为各自生长;TiO2-CoFe2O4复合光催化剂为无规则形状的纳米颗粒,颗粒的平均尺寸在40~50 nm之间;样品在整个紫外-可见区域有很强的吸收,并且吸收带边发生了明显的红移。
(2)TiO2-CoFe2O4复合光催化剂具有较高的太阳光催化活性,其中TiO2和CoFe2O4物质的量的比值和焙烧温度对其太阳光催化活性有着重要影响,光催化实验结果表明:在nT∶nCF=3∶1和焙烧温度为500℃条件下所制得的样品太阳光催化活性最好。
[1]Paramasivam I,Macak J M,Schmuki P.Electrochem. Commun.,2008,1(10):71-75
[2]Fu W Y,Yang H B,Li M H,et al.Mater.Lett.,2005,59: 3530-3534
[3]Li G Q,Liu C Y,Liu Y.Appl.Surf.Sci.,2006,253(5):2481-2486
[4]Woo L S,Drwieg J,Mazyck D,et al.Mater.Chem.Phys., 2006,96:483-487
[5]Eby G N,Lloyd F E,Woolley A R.Lithos.,2009,113:785-800
[6]Kuo C N,Chen H F,Lin J N,et al.Catal.Today,2007,122 (3/4):270-276
[7]Ko S,Pekarovic J,Fleming P D,et al.Mater.Sci.Eng.B, 2010,166(2):127-131
[8]ZUO Xian-Wei(左显维),FEI-Peng(费鹏),HU Chang-Lin (胡常林),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2009,25(7):1233-1237
[9]Uhm Y R,Woo S H,Kim W W,et al.J.Magn.Magn.Mater., 2006,304(2):781-783
[10]He Q H,Zhang Z X,Xiong J W,et al.Optical Mater.,2008, 31(2):380-384
[11]BAO Shu-Juan(包淑娟),ZHANG Xiao-Gang(张校刚),LIU Xian-Ming(刘献明).Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2003,19(9):925-928
[12]XU Shi-Hong(许士洪),FENG Dao-Lun(冯道伦),LI Deng-Xin(李登新),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2008,24(5):785-790
[13]Mourão H A J L,Malagutti A R,Ribeiro C.Appl.Catal.A:General,2010,382(2):284-292
[14]Rana S,Rawat J,Misra R D K.Acta Biomaterialia,2005,1: 691-703
[15]FuWY,Yang HB,LiMH.Mater.Lett.,2006,60:2723-2727
[16]ZHANG Xiu-Ling(张秀玲),GAO Shuai(高帅),YUAN Xue-De(袁学德),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2009,25(11):1912-1916
[17]LIU Xiu-Hua(刘秀华),HE Xiao-Bo(何小波),FU Yi-Bei (傅依备).Acta Chimica Sinica(Huaxue Xuebao),2008,66 (14):1725-1730
[18]Zhang Y,Shen Y,Gu F,et al.Appl.Surf.Sci.,2009,256(1): 85-89
Preparation and Sunlight Photocatalytic Properties of TiO2-CoFe2O4Magnetic Composite Materials
ZHANG Xiu-Ling*SUN Dong-Feng HAN Yi-Dan WANG Jing
(College of Physical Science and Technology,Dalian University,Dalian,Liaoning 116622,China)
A TiO2-CoFe2O4composite photocatalyst was prepared by one-step method with ultrasound technique using TiCl4、trivalent iron salt and divalent cobalt salts as precursors.The properties of the sample were characterized by VSM、XRD、TEM and UV-Vis techniques.The photocatalyst activity was evaluated by using methyl orange aqueous solution as the model contaminant in the sunlight.The results indicated that the TiO2-CoFe2O4composite photocatalyst showed good magnetic properties and the saturation magnetization was 212 Gs.The TiO2and CoFe2O4of the samples existed asanatase phase and spinel structure,respectively.The diameter of the TiO2-CoFe2O4particles was in the range of 40~50 nm.The spectrum response was from UV to visible region and the absorbance intensity remarkably increased.The photocatalyst showed highly photocatalytic activity in the sunlight and the activity was still good enough after 3 cycles.
magnetic;TiO2;composite material;sunlight photocatalyst
O614.41+1;O646.8;O614.81+1;O614.81+2
A
1001-4861(2011)07-1373-05
2011-01-05。收修改稿日期:2011-03-15。
辽宁省教育厅科技计划项目(No.L2010014)资助。
*通讯联系人。E-mail:xiulz@sina.com
