褐藻胶植物肠溶硬胶囊的制备技术
2011-11-06许加超刘天中张朝晖
张 东,高 昕,许加超,刘天中,张朝晖
(中国海洋大学,食品科学与工程学院,山东青岛266003)
褐藻胶植物肠溶硬胶囊的制备技术
张 东,高 昕*,许加超,刘天中,张朝晖
(中国海洋大学,食品科学与工程学院,山东青岛266003)
对褐藻胶植物肠溶硬胶囊的制备工艺进行了研究,并对最佳工艺条件下制备得到的胶囊进行成囊性、脆碎性、崩解时限、灼烧残渣等理化指标的测定。根据传统明胶硬胶囊的制备工艺及褐藻胶凝胶特性,实验确定褐藻胶肠溶硬胶囊工艺流程为溶胶、制胚、钙化、干燥、拔壳等,其中钙化过程中使用CaCl2溶液对褐藻胶胶囊毛胚进行直接钙化,使其形成酸不溶性凝胶,从而使褐藻胶胶囊具备肠溶性。通过单因素实验和正交实验确定最佳制备工艺为:以8cP褐藻胶为原料,胶液浓度12%,甘油添加量3%,2%CaCl2溶液钙化15s,胶囊含水量为15%。制备出胶囊的成囊性、脆碎性均符合药典对硬胶囊的要求,且在人工胃液中2h不溶,肠液中崩解时限为43±1min,完全符合药典对肠溶胶囊的要求。
硬胶囊,褐藻胶,正交实验,肠溶
1 材料与方法
1.1 实验材料
超低粘度褐藻胶(8cP,药品级) 购于青岛晶研化工有限公司。
1.2 实验方法
1.2.1 褐藻酸肠溶缓释硬胶囊制备的工艺流程 根据传统硬胶囊制备工艺及褐藻胶特性[8],确定褐藻胶肠溶缓释硬胶囊制备工艺为:溶胶→蘸胶制胚→钙化→干燥→拔壳→样品
1.2.2 操作要点
1.2.2.1 溶胶 称取褐藻胶加入蒸馏水(去离子),加入甘油,不断搅拌使之充分吸水膨胀溶解,室温下静置过夜除去泡沫,使胶液澄清备用。
1.2.2.2 蘸胶制胚 用胶囊模具,将模杆浸入胶液中沾制胶囊毛胚。先选好适宜规格的模杆固定于模板上,用适量润滑剂润滑。将模杆平稳握住,将上端向下浸入胶液中,待胶液全部浸没模杆约6~8s,即慢慢将模杆提起,离开胶液面,再将模杆翻起,翻转数次。
1.2.2.3 钙化 根据褐藻胶凝胶特性,选用适当钙制剂将胶囊毛胚钙化,形成酸不溶性褐藻胶凝胶,使胶囊具有肠溶性。
1.2.2.4 干燥 工业上使用流动的热空气,由于实验条件所限,本实验采取恒温恒湿箱进行干燥。与热空气相比,恒温恒湿箱可直接控制胶囊最终含水量,具有方便快捷准确的优点。
1.2.2.5 拔壳 用特制的胶囊钳将囊胚拔下。
1.2.3 影响成囊性效果的因素研究
1.2.3.1 成囊性 由于目前褐藻胶胶囊没有统一标准,按照中华人民共和国药典[9]和国标[10]中对明胶胶囊的要求,确定六项鉴定指标分别为壁厚、拔壳难易程度、色泽、插劈、气泡、瘪头薄头综合为成囊性,进行评定,分数为1~12,分数越高,成囊性越好。
1.2.3.2 胶液浓度对成囊性的影响 分别配制1%、3%、6%、9%、12%和15%的褐藻胶液,加入3%甘油,采用2%CaCl2溶液钙化15s,控制胶囊含水量为15%的条件下,以研究胶液浓度对成囊性的影响。
1.2.3.3 甘油含量对成囊性的影响 配制12%的褐藻胶胶液,分别加入1%、2%、3%、4%、5%的甘油,采用2%CaCl2溶液钙化15s,控制胶囊含水量为15%的条件下,以研究甘油含量对成囊性的影响。
1.2.3.4 钙化液浓度对成囊性的影响 配制12%褐藻胶胶液,加入3%甘油,分别采用1%、2%、3%、4%、5%CaCl2溶液钙化15s,控制胶囊含水量为15%的条件下,以研究钙化液浓度对成囊性的影响。
1.2.3.5 胶囊含水量对成囊性的影响 配制12%褐藻胶胶液,加入3%甘油,采用2%CaCl2溶液钙化15s,分别控制胶囊含水量为10%、15%、20%、25%、30%的条件下,以研究胶囊含水量对成囊性的影响。
1.2.4 正交实验设计 由上述单因素实验结果,固定胶囊含水量15%,以胶液浓度、甘油含量和CaCl2浓度为因素,以成膜性作为指标,设计L9(33)正交实验,因素水平如表1所示,对制得的样品进行成囊性测定。
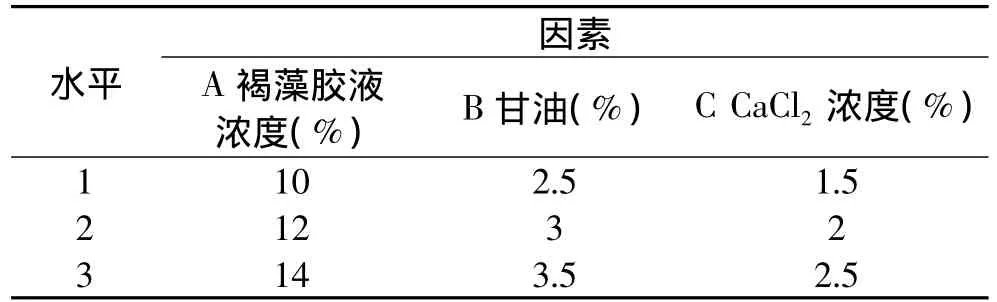
表1 L9(33)正交实验因素水平表
1.2.5 最优条件褐藻胶肠溶胶囊的制备及检测 通过之前的单因素实验和正交实验确定最优条件,对最优条件下制备出的胶囊进行成囊性、脆碎性、崩解时限、灼烧残渣等指标的测定。
2 结果与讨论
2.1 单因素实验结果
2.1.1 胶液浓度对成囊性的影响 胶液浓度对成囊性的影响如图1所示,可以看出,随着胶液浓度的增加成囊性逐渐增强,但在胶液浓度到达12%左右时成囊性开始下降。这是因为当胶液浓度低时,蘸胶制胚后,模具上的胶液过少,干燥后胶囊基本无法成型,出现破裂、囊壁过薄[11]现象;而当胶液浓度过高时,残留在模具上的胶液过多,使得囊壁过厚,不均匀且影响干燥时间。因此最适胶液浓度为12%左右。
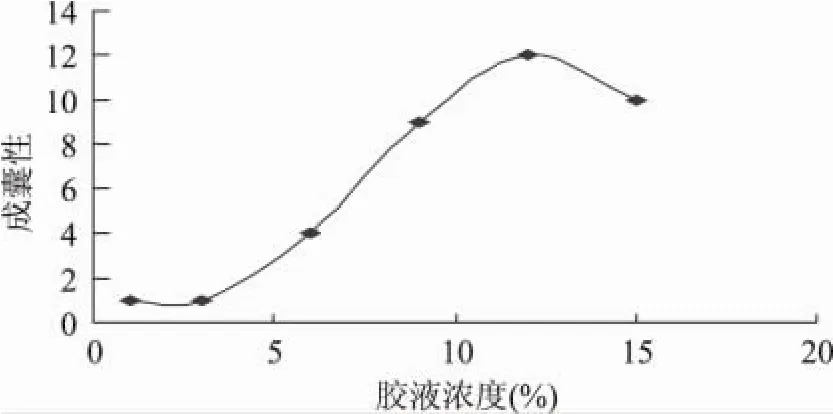
图1 胶液浓度对成囊性的影响
2.1.2 甘油含量对成囊性的影响 图2给出了甘油含量对成囊性的影响,可见甘油含量在2%~4%之间成囊性较好。甘油在药剂中常用作保湿剂和增塑剂,主要是由于甘油分子可以和水分子有较好的结合,调节水分含量,从而影响囊壳性质[12]。甘油含量的高低直接影响囊壳的拔壳难易程度和囊壳的成型。当甘油含量为3%左右时能满足囊壳对水分的要求,且相对恒定的水分含量可以减少囊壳受水分的影响。
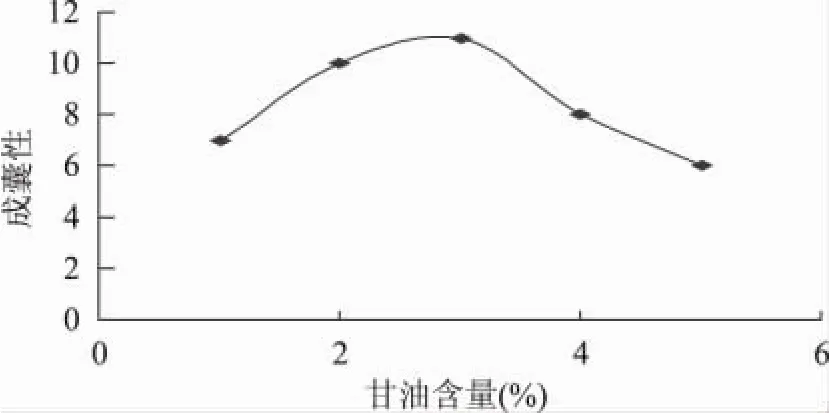
图2 甘油含量对成囊性的影响
2.1.3 钙化液浓度对成囊性的影响 钙化液有络合物型钙离子和直接钙化型Ca2+。由于络合物型钙离子钙化时间较长,工业生产中会增加成本,所以本实验采用CaCl2溶液进行钙化。结果如图3所示,可以看出,CaCl2溶液浓度在2%左右时胶囊成囊性最好,这是因为1%CaCl2溶液钙化15s时,钙化不完全,烘干时囊壳破损;4%CaCl2溶液以及5%CaCl2溶液浓度过大,钙化速度过快,使与CaCl2溶液接触的胶囊毛胚表面过于迅速的钙化,而靠近模具的毛胚胶液未能充分钙化,干燥后囊壳有褶皱且囊壳厚度不均一。
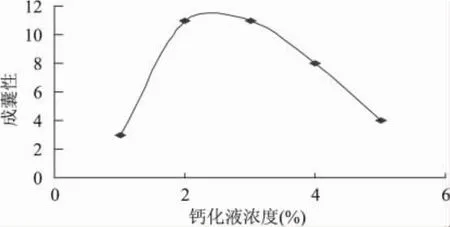
图3 钙化液浓度对成囊性的影响
2.1.4 胶囊含水量对成囊性的影响 图4为不同含水量胶囊的成囊性。可以看出,含水量在15%时成囊性最好,这是因为,当囊壳含水量为10%时,囊壳过于干燥,影响拔壳,且囊壳易碎;而当含水量超过20%时,囊壳又过于潮湿,胶囊成型不好,影响囊壳厚度。
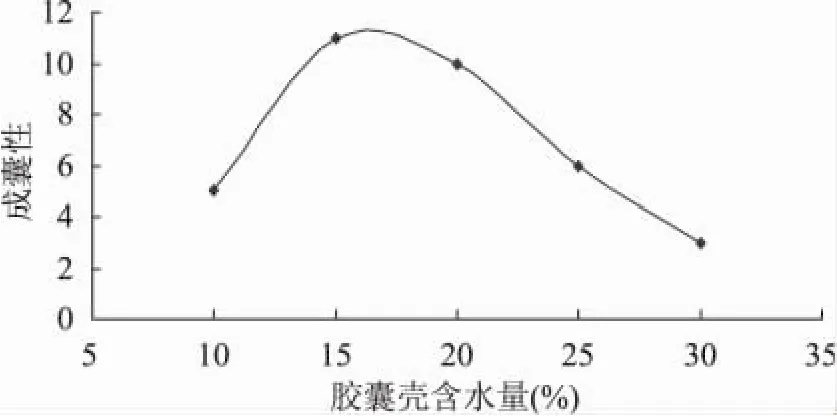
图4 胶囊含水量对成囊性的影响
2.2 正交实验结果
由表2可以看出,极差RA>RB>RC,可知影响成囊性的主要因素是胶液浓度,其次是甘油含量,最后是CaCl2浓度。最优的工艺条件是A2B2C2,即胶液浓度12%,甘油含量3%,CaCl2浓度2%。
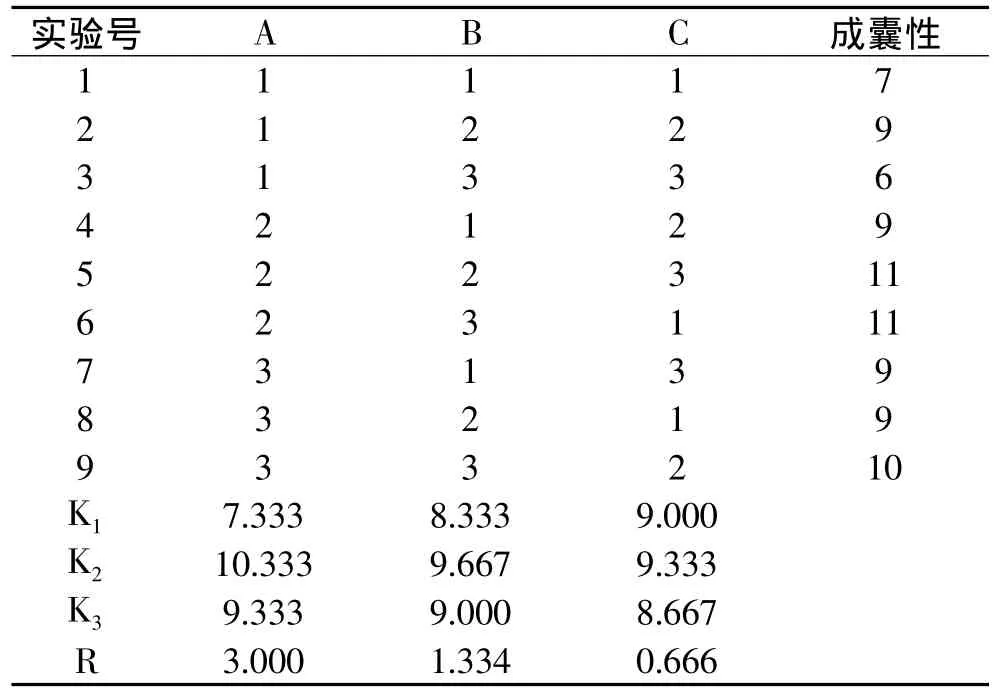
表2 正交实验方案及实验结果
2.3 最优条件制备出胶囊的理化指标
按上述实验得到的最优条件,即胶液浓度12%,甘油含量3%,CaCl2浓度2%,胶囊含水量15%制备出褐藻胶肠溶胶囊,进行成囊性、脆碎性、崩解时限、灼烧残渣等指标的测定。制备出的胶囊色泽均匀,有光泽,无明显色差,无沙眼,无黑点,2枚有变形,4枚有0.1mm的气泡,无皱纹,2枚有薄头,5枚破碎。囊壳壁厚为0.12±0.02mm。崩解时限按照药典中对肠溶胶囊的检测方法进行检测,在人工胃液中浸泡2h均无裂缝或崩解现象,在人工肠液中崩解时限为43±1min,完全符合药典对肠溶胶囊的要求。此外由于褐藻胶自身特性,含有大量金属离子,所以灼烧残渣含量较高,为26.4%±0.99%。总体上符合药典对硬质胶囊要求。
3 结论
本文对褐藻胶肠溶硬胶囊的制备工艺进行了研究,确定生产工艺为溶胶、制胚、钙化、干燥、拔壳等。选用8cP褐藻胶作为原料胶,运用单因素实验及正交实验确定最佳制作工艺为胶液浓度12%,甘油含量3%,CaCl2浓度2%,胶囊含水量为15%。并对生产出的胶囊进行理化指标的测定,崩解时限及成囊性都符合药典对硬胶囊的要求。
[1]郭燕峰.空心硬胶囊的发展状况[J].明胶科学与技术,2007,27(3):123-125.
[2]Digenis GA,Shah B.Cross-linking of gelatin capsules and its relevance to their in vitro-in vivo performance[J].Pharm Sci,1994,83:915-921.
[3]Berntsson O,Zackrisson G.Determination of moisture in hard gelatin capsules using near-infrared spectroscopy:applications to at-line process control of pharmaceutics[J].Pgarmceutical and Biomedical Analysis,1997,15:895-900.
[4]周涛.非明胶空心胶囊[J].明胶科学与技术,2005,25 (3):45.
[5]顾学裘.药剂专利手册[M].天津:天津科学技术出版社,1987.
[6]张小菊,姜小堂.羧甲基魔芋葡甘聚糖的制备及应用于空心胶囊的研究[J].食品科学,2004,25(10):200-203.
[7]庄绍冰,黄启权.白及空心胶囊及其质量标准[J].中国药学杂志1995,30(3):173.
[8]奚念朱,顾学裘.药剂学[M].第2版.北京:人民卫生出版社出版,1987∶98,275.
[9]中国药典[S].2000年版.北京:化学工业出版社,2005.
[10]马瑛,何秀芳,谢玉成.GB 13731-92药用明胶硬胶囊[S].北京:国家技术监督局,1992.
[11]黄超民.影响胶囊壁厚的因素[J].明胶科学与技术. 2004,24(2):72-73.
[12]骆涛.聚丙烯酸树脂制备肠溶胶囊壳的研究[D].浙江大学药学院,2006.
Preparation of algin enteric-coated capsules
ZHANG Dong,GAO Xin*,XU Jia-chao,LIU Tian-zhong,ZHANG Zhao-hui
(Food Science and Engineering College,Ocean University of China,Qingdao 266003,China)
The preparation of algin enteric-coated capsules was studied.Factors affecting preparation yields,such as concentration of alginate sol,calcification,drying,were studied by single and orthogonal experiments.The technological process of algin enteric-coated capsules was sol solution,balnk-making,calcification,drying,shelldrawing,and the optimal process conditions were as follows:the concentration of algin and glycerol was 12%and 3%respectively,and 2%CaCl2was used for calcification for 15s,and the water content of algin enteric-coated capsules was 15%after drying.The disintegration time and combustion remains was(43±1)min and 26.4% ± 0.99%,while the appearance quality met the requirement of Chinese pharmacopoeia too.
capsules;algin;orthogonal experiments;enteric-coated
TS201.1
B
1002-0306(2011)03-0321-03
空心胶囊是最常用的药品装填材料之一,具有亮丽的外观,可掩蔽药物的异味,易于吞服,使消费者易于接受,功能因子的生物利用度高,辅料用量少,在胃肠道中崩解快,一般服后3~10min即可崩解释放功能物质[1]。现有空心硬胶囊多以动物明胶为壁材制备。但由于明胶属于蛋白类物质,吸湿性强,并能把吸收的水分转移给内容药物,使药品吸潮变质,导致质量不合格和有效期短[2]。且蛋白质类物质遇醛类物质易发生交联固化反应。这些都限制了动物明胶硬质胶囊的使用范围,如不宜充填易吸湿、易风化和与囊材发生反应的填充物(如含醛基的物质)[3];此外明胶胶囊在体内的崩解性能容易波动,往往会使药物的有效成分难以准确释放。明胶溶液的粘度受温度影响很大,在生产过程中很容易因温度变化导致的粘度变化而使胶囊制备工艺控制发生困难。近来,采用非动物性原料制备硬质胶囊受到了重视[4]。日本公布了一种由聚乙二醇或其衍生物进行聚合生产硬质空性胶囊的技术。瑞士胶囊公司开发了一种以淀粉为原料,通过添加适量增塑剂制备的空心缓释硬胶囊VEGA GELS[5]。张小菊[6]等人将魔芋精粉主要成分葡甘聚糖经羧甲基化改性后,用作空心胶囊的囊材。庄绍冰等人用中药白的干燥块茎获得的多糖来制备空心胶囊[7]。植物性的褐藻多糖胶不仅具有安全的优点,而且其与金属阳离子的交联特性使其具有不用的强度和崩解特性。本文研究了褐藻胶肠溶硬胶囊的制备技术,为空心胶囊的生产提供理论依据,具有重要意义。
2009-12-16 *通讯联系人
张东(1985-),男,硕士生,研究方向:水产高值化利用。
新世纪人才计划(NCET-07-0779);国家自然科学基金(30771674);山东省科技攻关计划项目(2008GG1005008)。
