鱿鱼丝氧化三甲胺热分解模拟体系的研究
2011-11-06周德庆
靳 肖,周德庆,孙 永
(1.中国海洋大学食品科学与工程学院,山东青岛266003; 2.中国水产科学研究院黄海水产研究所,山东青岛266071)
鱿鱼丝氧化三甲胺热分解模拟体系的研究
靳 肖1,2,周德庆2,*,孙 永2
(1.中国海洋大学食品科学与工程学院,山东青岛266003; 2.中国水产科学研究院黄海水产研究所,山东青岛266071)
以氧化三甲胺为底物,添加铁(Ⅱ),建立了鱿鱼丝氧化三甲胺体外模拟体系,研究了加热温度、加热时间和pH对氧化三甲胺(TMAO)热分解作用的影响,同时与鱿鱼丝水提液中氧化三甲胺热分解规律进行对比。结果表明,随着温度升高,氧化三甲胺热分解反应越剧烈;在加热30min后,甲醛(FA)和二甲胺(DMA)的生成量基本稳定;当pH为5.0时,铁(Ⅱ)对氧化三甲胺热分解的促进作用最明显,为今后研究控制非酶途径产生甲醛提供理论参考和技术支持。
氧化三甲胺,铁,热分解,模拟体系,甲醛
1 材料与方法
1.1 材料与仪器
供试鱿鱼丝样品 青岛某公司产品,于2009年3月29日生产,以及市面上购买的5种不同厂家的鱿鱼丝,用粉磨机打碎备用;氧化三甲胺 Fluka公司; Trisbase Biosharp公司;甲醛标准液(10.8mg/kg) 中国计量科学研究院;其余试剂 均为分析纯。
BP221S电子分析天平 西法赛多利斯公司;粉磨机 佛山市顺德区方胜电器实业有限公司; DELTA 320 pH计 梅特勒;T-18 basic匀浆机IKA;SZ-1型快速混匀器 江苏金坛市金城国胜实验仪器厂;HH-2数显恒温水浴锅 国华电器有限公司;723A可见光分光光度计 上海精密科学仪器有限公司。
1.2 实验方法
1.2.1 鱿鱼丝水提液的制备 称取秘鲁鱿鱼丝粉末10g,加入100g蒸馏水,浸泡2h,过滤,滤液备用。
1.2.2 TMAO-Fe(Ⅱ)模拟体系的制备 配制2mmol/L FeCl2、20mmol/L TMAO、20mmol/L Trisbase -醋酸pH7.0缓冲液,备用。
1.2.3 不同加热温度对TMAO-Fe(Ⅱ)模拟体系的影响 将模拟体系溶液分装于具塞试管中,再置于水浴锅中,分别于不同温度(20~100℃)下反应20min,测定FA和DMA含量,每个反应温度做3个平行。
1.2.4 不同加热时间对TMAO-Fe(Ⅱ)模拟体系的影响 将模拟体系溶液分装于具塞试管中,再置于100℃水浴中反应不同时间(0~60min),测定FA和DMA含量,每组做3个平行。
1.2.5 不同初始pH对TMAO-Fe(Ⅱ)模拟体系的影响 对模拟体系溶液的pH进行调节(pH3~10),然后将不同pH模拟体系溶液分装于具塞试管中,100℃加热30min,测定FA和DMA含量,每组做3个平行。
1.2.6 鱿鱼丝pH的测定 称取鱿鱼丝样品10g,加入100mL蒸馏水,用均质机均质2min后,用pH计测定。
1.2.7 甲醛和二甲胺含量的测定 甲醛含量采用乙酰丙酮显色法测定[12],5mL反应液以蒸馏水补齐至10mL,加入 1mL乙酰丙酮显色,沸水浴中加热10min,流水冷却后在413nm波长下测定甲醛含量。
二甲胺含量按Dyer[13]等人建立的方法测定,略有改动,吸取反应液5mL于25mL具塞试管中,加入1mL铜氨试剂和10mL 5%二硫化碳-甲苯溶液,40~50℃水浴5min,快速混匀器混合5min,加入1mL 30%醋酸溶液,涡旋振荡至甲苯层澄清,吸取上层甲苯层于另一试管中,加入0.4g无水硫酸钠脱水,在440nm波长下比色测定。
2 结果与讨论
2.1 不同加热温度下TMAO-Fe(Ⅱ)模拟体系中FA与DMA的含量变化
外界的反应温度会影响TMAO热分解反应的进程,图1a反映了TMAO-Fe(Ⅱ)模拟体系中FA与DMA随着反应温度变化的趋势。总体来看,随着反应温度的增加,模拟体系中FA和DMA含量相应增加,而且温度越高,最终生成的FA和DMA含量越多。
同时对照图1b,随着温度的上升,FA、DMA含量均呈上升趋势,其中当温度高于50℃时,上升趋势明显(p<0.05),特别是90~100℃生成量极显著(p<0.01)。Xue[14]等人研究显示,秘鲁鱿鱼肌肉中的TMAOase的耐热温度为50℃,而鱿鱼丝水提液中的FA和DMA的含量在100℃加热20min仍有上升,即鱿鱼丝体内存在FA生成的非酶分解途径。结果表明,TMAO-Fe(Ⅱ)体系随着温度的变化规律与鱿鱼丝中TMAO热分解规律一致,且随着温度的升高,FA和DMA含量均呈上升趋势。
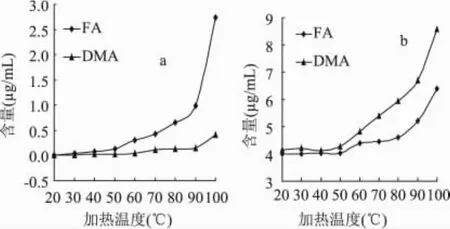
图1 不同温度下不同体系产生的FA和DMA含量变化注:a:TMAO-Fe(Ⅱ)模拟体系;b:鱿鱼丝水提液产生的,反应条件:pH=7时,加热20min。
2.2 不同加热时间下TMAO-Fe(Ⅱ)模拟体系中FA与DMA的含量变化
在pH7.0,100℃对TMAO-Fe(Ⅱ)模拟体系加热0~60min,研究了不同加热时间对于TMAO热分解的影响。由图2a所示,在100℃条件下进行加热反应,FA和DMA的生成量呈随反应时间的增加而增加的趋势。反应初始阶段,FA和DMA的生成量为0,随着加热时间的延长,FA和DMA生成量增加;在加热时间为30min时FA和DMA的生成量分别达到1.99μg/mL和1.16μg/mL;在加热时间为30~60min之间时,FA和DMA的生成量基本上不再随着加热时间的增加而增加。推测可能是TMAO反应达到完全,或是Fe2+在TMAO加热过程中被氧化成Fe3+,而Fe3+对TMAO失去作用所致。
同时对照图2b,在30min内TMAO热分解生成的FA和DMA含量迅速升高,FA和DMA含量在加热30min后分别增加了 1.3倍和2.5倍;随后在30~60min之间,FA和DMA的含量缓慢增加。结果表明,在100℃加热60min过程中TMAO仍在热分解,可以推测鱿鱼丝中的TMAO发生化学分解生成了FA和DMA。
两者对比可知,TMAO-Fe(Ⅱ)模拟体系随着加热时间的变化规律与鱿鱼丝中TMAO热分解规律一致,且随着加热时间的延长,FA和DMA含量均呈上升趋势,当加热到30min时,FA和DMA含量基本保持稳定。
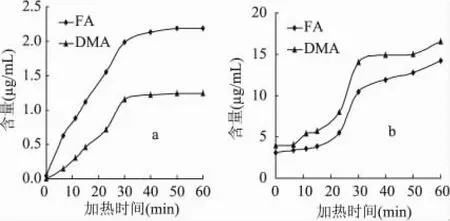
图2 不同加热时间下不同体系产生的FA和DMA含量变化注:a:TMAO-Fe(Ⅱ)模拟体系;b:鱿鱼丝水提液产生的,反应条件:pH=7时,加热温度100℃。
2.3 不同初始pH下TMAO-Fe(Ⅱ)模拟体系中FA与DMA的含量变化
TMAO-Fe(Ⅱ)体系经过100℃加热30min后,研究了不同初始pH对TMAO热分解反应的影响。如图3所示,在pH为3.0~5.0的酸性条件下,随着pH的增加,FA和DMA的生成量急剧升高,当pH为5.0时,FA和DMA的生成量都达到最大值,分别为8.22μg/mL和2.80μg/mL;pH为6.0~10.0时,FA和DMA生成量呈降低趋势。综上所述,当pH为5.0时,TMAO-Fe(Ⅱ)热分解过程中FA和DMA的生成量最高。不同pH对FA和DMA的生成量可能与Fe的存在形式有关。

图3 不同pH下TMAO-Fe(Ⅱ)模拟体系中产生的FA和DMA含量变化注:反应条件为100℃,加热30min。
选择六种鱿鱼丝进行pH的测定,结果如图4所示。共有三种鱿鱼丝的pH在6.0以上,分别为1号、2号和5号,最高的为5号样品,达6.32;最低的为6号,仅为5.29,比最高的5号样品低16.3%。据报道[15],pH可能会影响到食品的风味,而且不同种类的鱿鱼因原料本身性质的不同,加工工艺也存在差异。

图4 不同鱿鱼丝的pH
3 结论
3.1 建立了鱿鱼丝TMAO热分解反应的体外模拟体系,该体系可以使TMAO分解生成FA和DMA。
3.2 加热温度、加热时间和pH对TMAO-Fe(Ⅱ)体系中FA和DMA产生有影响,随着温度升高,TMAO -Fe(Ⅱ)的热分解反应越剧烈;在加热时间为30min时,FA和DMA的生成量基本稳定;在pH为5.0时,TMAO-Fe(Ⅱ)热分解生成的FA和DMA达到最大值。结果与鱿鱼丝水提液中FA和DMA产生具有相似规律性,推测鱿鱼丝甲醛的产生可以来源于体内TMAO化学分解途径。
[1]周德庆,马敬军,曾名勇.乙酰丙酮法测定水产品中甲醛含量结果不确定度研究[J].海洋水产研究,2003,24(3): 234-237.
[2]吴富忠,黄丽君.鱿鱼及制品中甲醛来源与产生规律探索[J].中国公共卫生管理,2006,22(3):256-268.
[3]韩宏伟.水产品中甲醛本底含量及生成机制研究进展[J].外国医学卫生学分册,2008,35(4):254-256.
[4]励建荣,朱军莉.秘鲁鱿鱼丝加工过程甲醛产生控制的研究[J].中国食品学报,2006,6(1):200-203.
[5]Fu X Y,Xue C H,Miao B C,et al.Effect of processing steps on the physico-chemical properties of dried-seasoned squid[J]. Food Chemistry,2007,103:287-294.
[6]Castell C H,Neal W E,Smith B.Formation of dimethylamine in stored frozen sea fish[J].J Fish Res Board Can,1970,27:1685 -1690.
[7]Kimura M,Seki N,Kimura I.Enzymic and nonenzymatic cleavage of trimethylamine-N-oxide in vitro subzero temperatures[J].Nippon Suisan Gakkaishi,2002,68:85-91.
[8]Spinelli J,Koury J B.Some new observations on the pathways of formation of dimethylamine in fish muscle and liver[J].J Agric Food Chem,1981,29:327-331.
[9]Yancey P H,Clark M E,Hand S C,et al.Living with water stress:Evolution of osmolyte systems[J].Science,1982,217:1214 -1222.
[10]俞其林,励建荣.食品中甲醛的来源与控制[J].现代食品科技,2007,23(10):76-78.
[11]Ferris J P,Gerwe R D,Gapsi G R.Detoxication mechanisms.Ⅱ.The iron-catalyzed dealkylation of trimethylamine oxide[J]. Journal of the American Chemical Society,1967,89(20):5270 -5275.
[12]SC/T 3025-2006.水产品中甲醛的测定[S].
[13]DyerW J,MounseyY A.Aminesin fishmuscle. II.Development of trimethylamine and other amines[J].J Fish Res Board Can,1945,6:359-367.
[14]Fu X Y,Xue C H,Miao B C,et al.Purification and Characterization ofTrimethylamine-N-oxide Demethylase (TMAOase)from Jumbo Squid(Dosidicus gigas)[J].J Agric Food Chem,2006,54:968-972.
[15]Morita k,Kubota K,Aishima T.Investigation influence of pH and parts on sensory characteristics and volatile components in boiled squid using experimental designs[J].Food Sci,2002,67: 848-854.
Study on thermal decomposition of trimethylamine-N-oxide model systems of shredded squid
JIN Xiao1,2,ZHOU De-qing2,*,SUN Yong2
(1.College of Food Science and Engineering,Ocean University of China,Qingdao 266003,China; 2.Yellow Sea Fisheries Research Institute,Chinese Academy of Fishery Sciences,Qingdao 266071,China)
With trimethylamine-N-oxide(TMAO)as substrates with iron(Ⅱ),the trimethylamine-N-oxide model system of shredded squid was established.Effects of heating temperature,heating time and pH on thermal decomposition of the model system and water extraction of TMAO from shredded squid were studied and compared.The results showed that with the temperature increased,the reaction of thermal decomposition of trimethylamine-N-oxide was severe.After heating for 30min,the content of formaldehyde(FA)and dimethylamine (DMA)remained stable.When pH value was 5.0,Fe2+could promote the thermal decomposition of trimethylamine -N-oxide most obviously.It was expected to provide theory reference and technical support for controlling the formaldehyde in non-enzymatic pathway.
trimethylamine-N-oxide;iron;thermal decomposition;model system;formaldehyde
TS254.1
A
1002-0306(2011)03-0106-03
甲醛(formaldehyde,FA)是一种原生质毒,具有强烈刺激性气味,对人的神经系统、肺、肝脏均可产生损害[1],被我国食品卫生标准规定不能作为食品添加剂应用于食品。然而近年来,对鱿鱼及其制品的监督检查中经常检出甲醛[2],也因此引起人们的广泛关注。目前认为水产品中内源性甲醛主要通过两种途径产生:一为生物途径,主要是酶及微生物参与;另一条为非酶途径,主要是高温过程的热分解[3]。励建荣[4]、Fu[5]等调查了秘鲁鱿鱼丝整个加工工艺中甲醛的变化趋势,发现其中蒸煮和焙烤两道工序甲醛生成最快,而这两个环节都是高温过程,酶催化生成甲醛的作用贡献不大,而甲醛生成却仍很明显,说明鱿鱼丝在高温处理过程中有化学分解等途径参与甲醛的生成。海产品中的氧化三甲胺(trimethylamine-N-oxide,TMAO)可以通过酶途径或非酶途径降解为FA和二甲胺(dimethylamine,DMA)[6-8]。TMAO存在于大多数海洋动物中,主要起到调节渗透压的作用[9],也是鱼类鲜美味道的主要来源[10]。但是,TMAO本身化学性质稳定,在高温下不会分解,推测鱿鱼体内存在一些物质可能导致 TMAO分解。Spinelli[8]等人研究发现Fe(Ⅱ)、抗坏血酸等可以促进鱼体内TMAO非酶途径分解。Ferris[11]等人证实了TMAO在Fe(Ⅱ)催化下能够生成FA和DMA。本文以TMAO和Fe(Ⅱ)为反应物,与鱿鱼丝的水提液做对比,确立了最简单的TMAO非酶作用反应模型体系,并且研究了加热温度、加热时间和 pH对TMAO非酶途径热分解的影响,确定了不同条件下产生甲醛、二甲胺的情况,为今后研究控制非酶途径产生甲醛提供理论参考和技术支持。
2010-03-09 *通讯联系人
靳肖(1984-),女,硕士研究生,研究方向:水产品质量安全。
国家自然科学基金资助项目(30871949)。
