SRB对AZ91镁合金在两种培养基中腐蚀行为的影响
2011-10-30方世杰刘耀辉
方世杰,刘耀辉,乔 健,张 伟
(1洛阳理工学院 机电工程系,河南 洛阳471023;2吉林大学 材料科学与工程学院 汽车材料教育部重点实验室,长春130022;3中国科学院 长春光学精密机械与物理研究所,长春130033)
SRB对AZ91镁合金在两种培养基中腐蚀行为的影响
方世杰1,2,刘耀辉2,乔 健3,张 伟1
(1洛阳理工学院 机电工程系,河南 洛阳471023;2吉林大学 材料科学与工程学院 汽车材料教育部重点实验室,长春130022;3中国科学院 长春光学精密机械与物理研究所,长春130033)
AZ91镁合金是目前工业中应用最为广泛的镁合金材料,占镁合金件总用量的90%左右[1]。与其他金属材料相比,AZ91的耐腐蚀性能较差,需要经过表面耐腐蚀处理后才能够正常使用。即使这样,零件表面的保护层也往往容易受到磕、碰、划等机械损伤,使基体直接曝露于腐蚀环境中;同时在镁合金件的实际使用过程中也发现,腐蚀主要发生在基体上,因此对于AZ91镁合金基体的腐蚀研究具有重要意义。长期以来,金属的微生物腐蚀主要集中于核能、发电、石油及海洋工业等领域,微生物腐蚀研究也仅限于碳钢、不锈钢、铜、镍等金属或合金上[2-4]。但随着镁合金在航空航天、汽车工业中的大量应用,微生物对镁合金的腐蚀影响已经开始引起人们的关注[5]。在诸多微生物当中,硫酸盐还原菌(Sulfate-Reducing Bacteria,SRB)是目前被公认的对金属腐蚀危害最大,也是研究最为广泛的微生物物种之一[6]。已有文献研究表明,硫酸盐还原菌能够引起ZM-5铸造镁合金的腐蚀[5]。
本实验以AZ91镁合金为研究材料,以SRB单一菌种为实验微生物,在两种培养基溶液中,使用挂片浸泡法,并通过扫描电镜、能谱分析及腐蚀失重等综合手段研究了SRB对AZ91腐蚀行为的影响,并对其腐蚀机理进行了探讨。
1 实验
1.1 菌种来源
实验菌种为SRB,取自中科院金属研究所。菌种经多次分离、纯化,并选择生物活性较高的SRB纯培养作为实验菌种。
1.2 实验材料
实验材料为AZ91镁合金。挂片尺寸20mm×15mm×2mm,使用200,400,600,800#SiC水砂纸逐级打磨到800#,实验前将挂片放入洁净工作台中用紫外线灭菌20min。
1.3 培养基准备、培养条件和实验方法
实验采用两种成分的培养基溶液,溶液I:API培养基+0.3g/L硫酸亚铁铵+0.1g/L维生素 C;溶液II:API培养基。API培养基为美国石油协会(A-merican Petroleum Institute,API)推荐的标准培养基[7],具 体 成 分 如 下:0.5g/L Na2SO4,1.0g/L NH4C1,0.1g/L CaCl2,0.5g/L K2HPO4·3H2O,2.0g/L MgSO4·7H2O,3.5g/L C3H5NaO3,1.0g/L酵母浸粉。溶液pH值均调节为7.20,(121±1)℃下蒸汽灭菌20min。含菌溶液的初始菌量浓度为6.50×103个/mL,将试样放入溶液中,在(30±1)℃下连续浸泡14d。对比实验使用无菌溶液,放入试样,密封后与含菌溶液一起培养。为了表述方便,在溶液号后加“-0”表示无菌溶液,加“-1”表示含菌溶液,具体的溶液编号及成分如表1所示,表中的“+”表示含有,“—”表示不含有。

表1 实验溶液的成分Table 1 Composition of experimental solution
1.4 菌量和腐蚀速率测量
溶液菌量计数使用XB-K-25型血球计数板测量。腐蚀挂片总数为12片,分为4组,每组3片,腐蚀速率取3个挂片的平均值。腐蚀失重使用0.0001g电子天平,在1%AgNO3+15%CrO3溶液中沸煮15min以去除腐蚀产物,清洗、干燥后,用失重法计算平均腐蚀速率,计算公式如下:

式中:v表示试样平均腐蚀速率,mm/a;w为试样起始质量,g;w0为去除腐蚀产物后试样质量,g;t为实验时间,h;A为试样面积,m2;ρ为金属密度,g/cm3。
2 结果与讨论
溶液I中的硫酸亚铁铵和维生素C是API培养基中普遍采用的添加成分。前者提供的Fe2+能与SRB的代谢物S2-反应生成黑色的FeS,作为判断细菌活性和 H2S生成的重要依据[8]。同时Fe2+也是SRB细胞中多种酶的活性基成分,与维生素C一样,均能够刺激SRB的生长和繁殖。
2.1 平均腐蚀速率
AZ91在4种溶液中连续浸泡14d的平均腐蚀速率见表2。AZ91在溶液I中的腐蚀速率均高于溶液II,前者的腐蚀速率是后者的15~18倍;在含菌溶液中的腐蚀速率均低于相应的无菌溶液;将腐蚀速率按从大到小排列:vI-0>vI-1>vII-0>vII-1。这表明,AZ91在含菌溶液中的腐蚀敏感性均低于相应的无菌溶液。由于维生素C促进细菌生长,但不会直接腐蚀金属;而硫酸亚铁铵中少量的SO42-和NH4+能为细菌生长提供少量营养,但不具有大幅提高合金腐蚀速率的作用,因此硫酸亚铁铵中的Fe2+是造成AZ91腐蚀速率大幅提高的原因。

表2 AZ91分别在4种溶液中连续浸泡14d后的平均腐蚀速率Table 2 Average corrosion rates of AZ91immersed in the four solutions for 14d,respectively
2.2 腐蚀形貌特征
浸泡14d后,4种挂片去除腐蚀产物后的表面形貌见图1。试样I-0表面形成大面积、网络状连续分布的溃疡状腐蚀;试样I-1表面也形成较大面积的溃疡状腐蚀,但腐蚀区分布不连续;试样II-0和II-1表面仅在局部区域出现点蚀坑,点蚀坑数量较少。

图1 浸泡14d后,试样I-0(a),I-1(b),II-0(c)和II-1(d)去除腐蚀产物后的表面形貌Fig.1 Surface morphologies of sample I-0(a),I-1(b),II-0(c)and II-1(d)viaremoval of corrosion products after 14dimmersion
2.3 腐蚀形貌特征
浸泡14d后,试样I-1表面及溶液中均覆盖黑色沉淀物;试样II-1表面及溶液中只形成乳黄色沉积物,两种含菌溶液均有刺鼻的H2S产生。无菌试样I-0和II-0表面无黑色沉淀,溶液也无H2S气体产生。

图2 浸泡14d后,试样I-0(a),I-1(b),II-0(c)和II-1(d)的表面腐蚀产物形貌Fig.2 Surface morphologies of corrosion products of sample I-0(a),I-1(b),II-0(c)and II-1(d)after 14dimmersion
图2和图3分别给出了4种试样表面的腐蚀产物形貌及XRD分析。由XRD分析可知,无菌试样I-0和II-0表面的腐蚀产物成分相同,由NH4MgPO4·6H2O,Al2O3,Al(OH)3,Al4Ca和 AlPO4构成。从衍射峰强度判断,NH4MgPO4·6H2O为主要腐蚀产物。其他腐蚀产物皆为含Al化合物,Al来自于金属阳极的溶解,由于AZ91中的Al含量较低,且Al相对于Mg较耐腐蚀,因此所形成的含Al化合物的含量较低。挂片I-1和II-1只能检测到微弱的NH4MgPO4·6H2O峰,表明腐蚀产物含量较少,其他腐蚀产物从XRD图谱已不能识别,需要结合EDS进行进一步分析。4种试样表面均形成NH4MgPO4·6H2O腐蚀产物膜,但是腐蚀产物的形态和分布具有明显差异。试样I-0表面腐蚀产物为粗大的竹叶状晶体,长度约为2~3mm,膜结构疏松;试样I-1的腐蚀产物为细小的针状晶,长度约为0.5~1mm,数量较少;试样II-0的腐蚀产物为短粗的柱状晶,长度约为1mm,膜结构疏松;试样II-1表面腐蚀产物为细密的短针状晶体,长度约为0.5mm,膜结构致密。

图3 浸泡14d后,试样I-0(a),I-1(b),II-0(c)和II-1(d)的表面腐蚀产物XRD分析Fig.3 XRD analyses of corrosion products on sample I-0(a),I-1(b),II-0(c)and II-1(d)surface after 14dimmersion
2.4 腐蚀表面SEM形貌及EDS能谱分析
图4和图5分别给出了腐蚀14d后,4种试样表面的微观形貌和能谱分析。挂片I-0表面含有元素C,O,Mg,Al,P,Ca,Fe和Zn,与 XRD分析结果对比,EDS进一步检测到了Fe和Zn。试样I-1表面除了检测到上述元素外,还检测到S。试样II-0表面含有元素C,O,Mg,Al,P,Ca,Cl和 K;试样II-1表面没有检测到Cl,其他成分与试样II-0相同。
Iverson[9]认为,EDS同时检测到Fe和S时,应有FeS生成。目前关于SRB影响下的低碳钢腐蚀理论之一,就是FeS作为大阴极与钢构成电偶腐蚀,促进碳钢的溶解[8]。从合金在海水中的电偶序可知,镁合金的非平衡电位约为-1.20V,碳钢约为-0.40V,前者远远小于后者,表明镁合金的电偶腐蚀倾向大于碳钢。因此挂片I-1上的FeS沉积物会与镁合金构成电偶腐蚀,FeS作为阴极促进了阳极的溶解。
挂片I-0表面检测到Fe和Zn,但是目前Fe和Zn在无菌溶液中以何种形式存在,如何对基体腐蚀产生作用尚不清楚,还有待于进一步的研究。

图4 浸泡14d后,试样I-0(a),I-1(b),II-0(c)和II-1(d)表面的SEM 形貌Fig.4 SEM micrographs of sample I-0(a),I-1(b),II-0(c)and II-1(d)after 14dimmersion
试样II-0表面检测到Cl,表明有Cl-的吸附和聚集。Cl-半径极小,有强穿透性和高的活性,是强侵蚀性离子。Cl-对镁合金的腐蚀作用有两个方面:一是Cl-在保护膜的缺陷中聚集,使膜溶解从而引起基体的点蚀;另一方面Cl-可以直接参与阳极的溶解过程,它在参与阳极溶解的过程中有如下规律[10]:

图5 浸泡14d后,试样I-0(a),I-1(b),II-0(c)和II-1(d)表面的 EDS能谱分析Fig.5 EDS analyses of sample I-0(a),I-1(b),II-0(c)and II-1(d)after 14dimmersion
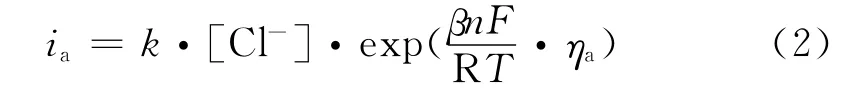
式中:ia为阳极电流密度;k为波尔兹曼常数;[Cl-]为氯离子浓度;β为阳极反应的传递系数;n为反应电子数;F为法拉第常数;R为摩尔气体常数;T为绝对温度;ηa为阳极的超电势。Cl-对阳极溶解具有活化作用,随Cl-浓度增加,阳极溶解电流密度增加。但是Mitrovic-Scepanovic[11]的研究表明,当 Cl-浓度达到0.002~0.02mol/L时才能使镁合金活化,引发点蚀。本实验的Cl-离子的浓度约为0.0121mol/L,在此临界浓度范围中,因此Cl-能够诱发挂片II-0的点蚀。
试样II-1表面没有检测到Cl-,由于SRB会吸收部分Cl-来调节细胞中水的渗透压,以维持细菌正常的代谢,因此降低了Cl-的浓度,影响了Cl-向金属表面的富集。但是溶液中含有H2S,Garner等人[12]认为SRB产生的H2S是点蚀活化剂,促进金属点蚀。密闭容器中,SRB产生的 H2S有1/3以氢硫酸,2/3以HS-形式存在,溶液中的H2S在空气/水界面处保持动态平衡[13]。Salvareza等人[14]的研究表明硫化物加入到含Cl-溶液中,碳钢的耐蚀性下降,硫化物对金属的活化由HS-引起。从耐腐蚀性上讲,AZ91远低于碳钢,因此试样II-1的点蚀是由HS-的活化作用或由HS-与Cl-的共同作用引起的。
由SEM形貌可知,试样I-1和II-1表面出现典型的杆状SRB细胞,表明SRB可以在AZ91表面附着并形成生物膜,生物膜由SRB细胞、胞外高聚物和腐蚀产物组成。试样I-1生物膜中的细菌数量较多,分布较密;试样II-1膜中细菌数量明显较少,分布稀疏。这种差异来自于溶液成分的不同,由于溶液I-1中含有硫酸亚铁铵和维生素C,两者刺激了SRB的生长和繁殖。而溶液II-1中由于缺少这两种成分,细菌生长、代谢相对迟缓,因此生物膜中细菌数量较少。结合腐蚀速率测量可知,生物膜的存在延缓了金属的腐蚀。这是因为生物膜具有吸收或阻挡溶液中侵蚀性离子(Fe2+和Cl-)向合金表面的扩散和吸附,因此延缓了基体的腐蚀。
2.5 菌量和溶液pH
表3给出了浸泡14d后,生物膜和溶液菌量、腐蚀前后溶液的pH值。试样II-1生物膜及溶液菌量均大于试样I-1的相应菌量,然而SEM观察却显示试样II-1生物膜中的SRB细胞数量明显高于试样I-1。这是因为溶液I-1中含有的硫酸亚铁铵和维生素C促进了细菌的生长和繁殖,SRB在对数生长期大量繁殖,菌量的剧增大量消耗了溶液中的营养物质,同时产生大量细菌代谢产物H2S;进入生长衰退期后,有毒物质H2S的不断积累抑制了细菌的生长,同时由于营养匮乏使得生物膜中活菌数量大幅减少。而在溶液II-1中不含硫酸亚铁铵和维生素C,细菌生长相对迟缓,处于生长对数期时细菌增长量也相对较小,所以营养消耗和H2S产量也较少,从而使得生物膜中活菌数量反而较多。由于SRB的大量繁殖加剧了溶液I-1中的N和P消耗,从而显著抑制NH4MgPO4·6H2O的生成;而在溶液II-1中,由于N和P的供应充足,同时生物膜中的细菌不断消耗金属表面的营养,使得NH4MgPO4·6H2O晶粒不容易长大,形成较为细小致密的腐蚀产物。
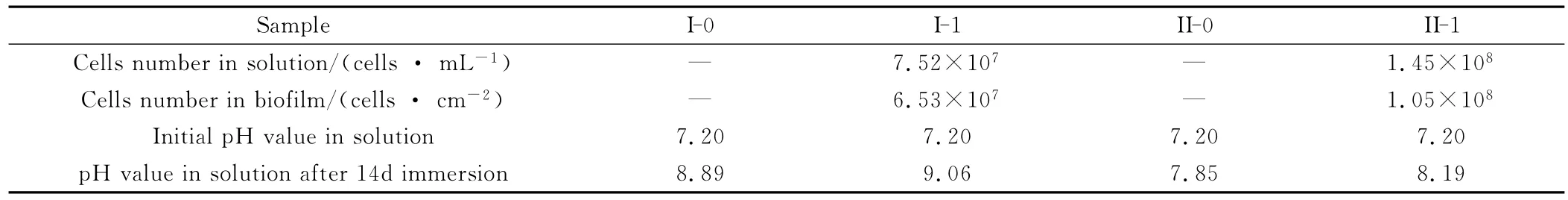
表3 浸泡14d后试样表面生物膜和溶液中的菌量以及溶液的pH值Table 3 SRB cells number in biofilm and SRB medium,and pH values of solutions after 14dimmersion
pH值测量显示,浸泡14d后4种溶液的pH值差别不大,在7.85~9.06之间,呈弱碱性。这表明金属腐蚀程度的差异并不是由于溶液pH值的变化引起的。但不同介质pH值改变的机理却不同。无菌溶液pH值的升高来自于阴极区的析氢反应,析氢反应要消耗溶液中的H+,从而使pH值增加。同为无菌溶液,溶液I-0的pH值要高于溶液II-0,尽管目前尚不知道无菌溶液中加入Fe2+是如何加剧试样I-0腐蚀的,但是这种阳极溶解速率的增加,会导致阴极析氢反应速率增加,阴极反应消耗的H+更多,所以溶液的pH更大。含菌溶液的情况相对复杂,由于细菌的存在会产生复杂的化学反应,这些化学反应都有可能影响溶液的pH值。根据实验现象和实验结果可以推测含菌介质pH升高的原因可能分为以下两个过程:(1)在浸泡初期,细菌数量较少,金属表面的阴极反应仍以析氢反应为主。(2)随着SRB数量和活性的增加,细菌将SO42-还原成S2-,随后S2-同溶液中的H+结合生成H2S气体释放。H2S气体的释放使得溶液的pH值进一步升高。将含菌溶液的pH值与相应的无菌溶液相比较可知,前者的pH值均大于相应的后者的pH值,原因很可能是H2S的释放引起pH值的进一步增大。溶液I-1的pH值大于溶液II-1,这是由于金属表面产生了FeS沉淀,成为电偶腐蚀的阴极,促进了镁阳极的溶解并且加剧阴极的析氢反应,使得溶液的pH值增大;同时Fe2+能够提高SRB细胞活性,使得细胞代谢物H2S产量增加,溶液中的H+浓度进一步下降,最终导致溶液I-1的pH值大于溶液II-1。
综上所述,培养基中的Fe2+,Cl-和 HS-等侵蚀性离子,是引起镁合金腐蚀敏感性增加的主要原因。生物膜的形成会对基体产生双重作用:一方面是SRB产生的HS-对基体的腐蚀作用;另一方面是生物膜对侵蚀性离子的吸收和阻挡作用,即对基体的保护作用。由于溶液的腐蚀性大于生物膜的腐蚀性,使得生物膜对基体的腐蚀作用被掩盖,而对基体的保护作用显现出来。在这些侵蚀性离子中,Fe2+的侵蚀作用最强,SRB的存在对溶液中的Fe2+产生如下影响:(1)部分Fe2+作为营养源被SRB细胞吸收利用;(2)Fe2+与H2S反应生成FeS沉淀沉积到瓶底;(3)生物膜胞外聚合物(Extracellular Polymeric Substance,EPS)中的阴极官能团能和Fe2+结合生成络合物,阻挡了Fe2+向金属表面的吸附,因此SRB的存在抑制了AZ91的腐蚀。
3 结论
(1)SRB可以在AZ91表面附着、生长并形成生物膜,生物膜的存在抑制了AZ91的腐蚀。
(2)AZ91在含硫酸亚铁铵和抗坏血酸的API培养基中所形成的生物膜,SRB数量较多,分布均匀,腐蚀产物较少,膜结构疏松,对基体的保护作用较弱;在API培养基中形成的生物膜,其SRB数量较少,细胞分布不均匀,但腐蚀产物较多且膜结构致密,对基体具有较好的保护作用。
(3)溶液中硫酸亚铁铵中的Fe2+明显促进了SRB的新陈代谢,但是会在镁合金表面形成FeS沉淀,显著促进AZ91的腐蚀。
[1]SONG G,ATRENS A,WU X,et al.Corrosion behaviour of AZ21,AZ501and AZ91in sodium chloride[J].Corrosion Science,1998,40(10):1769-1791.
[2]CHONGDAR S,GUNASEKARAN G,KUMAR P.Corrosion inhibition of mild steel by aerobic biofilm[J].Electrochimica Acta,2005,50(24):4655-4665.
[3]RAO T S,KNAIR K V.Microbiologically influenced stress corrosion cracking failure of admiralty brass condenser tube in a nuclear power plant cooled by freshwater[J].Corrosion Science,1998,40(11):1821-1836.
[4]WAGNER P,LITTLE B.Impact of alloying on microbiologically influenced corrosion-a review[J].Materials Performance,1993,32(9):65-68.
[5]朱绒霞,李亚会.航空发动机滑油系统镁合金微生物腐蚀与防护[J].轻金属,2004,(12):35-36.
[6]MIRANDA E,BETHENCOURT M,BOTANA F J,et al.Biocorrosion of carbon steel alloys by an hydrogenotrophic sulfate-reducing bacterium Desulfovibrio capillatus isolated from a Mexican oil field separator[J].Corrosion Science,2005,48(9):2417-2431.
[7]BOOTH G H,EFORD L,WAKERLY D S.Microbiological battery induced by sulfate-reducing bateria[J].British Corrosion Journal,1988,23(3):242-245.
[8]ANGELL P,URBANIC K.Sulphate-reducing bacterial activity as a parameter to predict localized corrosion of stainless alloys[J].Corrosion Science,2000,42(5):897-912.
[9]IVERSON W P.Research on the mechanisms of anaerobic corrosion[J].International Biodeterioration & Biodegradation,2001,47(2):63-70.
[10]查全性.电极过程动力学导论[M].北京:科学出版社,1978.
[11]MITROVIC-SCEPANOVIC V,BRIGHAM R J.Localized corrosion initiation on magnesium alloy[J].Corrosion,1992,48(9):780-784.
[12]GARNER A,NEWMAN R C.Thiosulfate pitting of stainless steels[A].Corrosion 91[R].Houston,TX:NACE International,1991.186.
[13]GIBSON G R.Physiology and ecology of the sulphate-reducing bacteria[J].Journal of Applied Bacteriology,1990,69(6):769-797.
[14]SALVAREZZA R C,VIDELLA H A.Passivity breakdown of mild steel in sea water in the presence of sulfate reducing bacteria[J].Corrosion,1980,36(10):550-554.
Influence of SRB on Corrosion Behaviour of AZ91Magnesium Alloy in Two Kinds of Culture Media
FANG Shi-jie1,2,LIU Yao-hui2,QIAO Jian3,ZHANG Wei1
(1Department of Mechanical and Electrical Engineering,Luoyang Institute of Science and Technology,Luoyang 471023,Henan,China;2Key Laboratory of Automobile Materials of Ministry of Education,College of Materials Science and Engineering,Jilin University,Changchun 130022,China;3Changchun Institute of Optics,Fine Mechanics and Physics,Chinese Academy of Sciences,Changchun 130033,China)
采用浸泡法、扫描电镜(SEM)和X射线能谱仪(EDS)研究了硫酸盐还原菌(SRB)在两种培养基中,对AZ91镁合金腐蚀行为的影响及其腐蚀机理。结果表明:在培养温度为(30±1)℃的条件下,SRB可以在AZ91表面附着、生长并形成生物膜,生物膜的存在抑制了AZ91的腐蚀。AZ91在含硫酸亚铁铵和维生素C的培养基中所形成的生物膜,其结构疏松,对基体的保护作用较弱。同时硫酸亚铁铵中的Fe2+明显促进了SRB的新陈代谢,但是会在镁合金表面形成FeS沉淀,显著加速AZ91的腐蚀。
AZ91镁合金;硫酸盐还原菌;生物膜;腐蚀;培养基
Soaking method,SEM and EDS analyses were applied to evaluate the influence and mechanism of sulfate-reducing bacteria(SRB)for the corrosion of AZ91magnesium alloy in two kinds of culture media.The results show that,SRB can adhere and grow on the surface of AZ91,and then form a biofilm.The biofilm inhibits the corrosion of AZ91at(30±1)℃.The biofilm formed in the culture medium with(NH4)2Fe(SO4)·6H2O and C6H8O6is loose,and plays a weak protective role for the matrix.Furthermore,Fe2+ions in(NH4)2Fe(SO4)·6H2O improve the metabolism of SRB significantly,however,they can form the deposition of FeS,which accelerates the corrosion of AZ91.
AZ91magnesium alloy;SRB;biofilm;corrosion;culture medium
TB172.5
A
1001-4381(2011)09-0056-06
吉林省科技发展重点项目(20040315);河南省教育厅自然科学研究计划项目(2010B430019)
2010-01-20;
2011-07-08
方世杰(1973-),男,工学博士,副教授,主要从事金属的腐蚀与防护研究,联系地址:河南省洛阳市洛阳理工学院王城校区机电工程系(471023),E-mail:fangshijie8827@163.com
