盐酸克林霉素注射液处方及生产工艺的初步研究
2011-10-25张连忠
张连忠
(唐山师范学院 生命科学系,河北 唐山 063000)
盐酸克林霉素化学名 6-(1-甲基-反-4-丙基-L-2-吡咯烷甲酰氨基)-1-硫代-7(S)-氯-6,7,8-三脱氧-L-苏式-a-D-半乳辛吡喃糖苷盐酸盐,属林可霉素类抗生素,为林可霉素的衍生物,抗菌谱与林可霉素相同,抗菌活性较林可霉素强4~8倍。它对革兰氏阳性需氧菌、链球菌、葡萄球菌具有抗菌活性,对多种厌氧菌、衣原体、支原体和钩形虫也具有抗菌活性[1,2]。它的作用机制是与细菌核糖体的50s亚基结合,通过抑制肽链的延长而抑制细菌蛋白质的合成,通过去除细菌表面 A蛋白质和绒毛状外衣,使其易被吞噬和杀灭[3];同时它对机体免疫系统有增强免疫调节作用,能够增强多型核白细胞的吞噬和杀菌功能,还可以改变细菌表面活性并能够抑制细菌毒素的产生。克林霉素在多形核白细胞和巨噬细胞内积聚,使浓度超过细胞外40倍,这也许是克林霉素具有较强杀灭细胞内细菌能力的原因。克林霉素也可有效的减少或防止多糖—蛋白复合物的形成,使细菌不易粘附到骨组织,从而易被巨噬细胞和抗生素所杀灭[4]。本研究仅从抗氧剂、pH值范围、活性炭脱色条件、活性炭用量以及灭菌条件五个方面对盐酸克林霉素注射液进行研究,以期获得该注射液的最佳处方及比较优化的相关生产工艺指标。
1 材料和方法
1.1 仪器药品
CLASS-VP型高效液相色谱仪(日本岛津公司);pH-3C数字酸度计(杭州东星仪器设备厂);VC(天津天泰精细化学品有限公司);活性炭(北京大力精细化工厂)。
1.2 盐酸克林霉素注射液(0.75g/10mL)制法
在配制容器中加入配制用量50%的注射用水,称取处方量盐酸克林霉素加入到容器中溶解,另取处方量的氯化钠、枸橼酸钠,加入至药液中,搅拌至溶解,再加入2%的枸橼酸溶液调节pH值,然后加入一定量的活性炭,搅拌15min,粗滤脱碳,最后加入注射用水至规定量,滤液经0.22µm的过滤器过滤,灌装机灌装到安瓿瓶中并熔封,灭菌。
1.3 抗氧剂的选择
为了提高注射液的稳定性,采用了注射剂中常用的抗氧剂如VC、L-半胱氨酸、EDTA-2Na、Na2S2O5、Na2S2O3等,进行筛选试验比较。取表1中处方量的原辅料加50mL水溶解,用2%的枸橼酸溶液调节pH值为4.5时,加入100mL水定容,抽滤,分装于安瓿瓶中并熔封,115℃流通蒸汽30min灭菌。采用加速试验方法(按市售包装温度40℃±2℃、相对湿度75%±5%的条件放置)考察样品的稳定性,在60℃条件下分别放置 5d、10d,采用高效液相色谱法[5]测定含量的变化(含量测定的方法如下),同时观察澄明度的变化。
1.3.1 色谱条件与系统适用性试验
用十八烷基硅烷键合硅胶为填充剂;以磷酸二氢铵溶液(取磷酸二氢铵2.88 g,加水溶解成1 000mL,用80%磷酸溶液调节pH=3.0)-甲醇(210: 300)为流动相;检测波长为214nm。理论塔板数按克林霉素峰计算,应不低于1 300。
1.3.2 测定法
精密量取本品2mL,置100mL量瓶中,用流动相稀释至刻度,摇匀,取10µL注入液相色谱仪,记录色谱图,另取克林霉素对照品适量,同法测定。按外标法以峰面积计算供试品中C18H33ClN2O5S的含量。
1.4 pH值范围的筛选
按盐酸克林霉素注射液质量标准要求 pH值应在 3.5~5.5,加入适量弱酸调节不同pH值。在加热前检测克林霉素的百分含量(方法见 1.3),并观察注射液的外观。100℃加热2h后同样记录这两项指标的结果,与加热前进行对比,考察注射液的稳定性。
1.5 活性炭脱色条件的选择
为了减少杂质对注射剂的影响,在工艺研究中选择活性碳处理药液。试验在不同pH值条件下,加入0.3%活性碳,分别置水浴 80℃加热 10min,照含量测定方法测定相对含量,并观察盐酸克林霉素注射液的外观颜色,以探索活性炭脱色的最佳条件。
1.6 活性炭用量的选择
调节pH至4.0时,分别加入0.1%、0.2%、0.3%的活性炭,分别置沸水浴加热10min,照含量测定方法测定相对含量,并观察注射液的外观,以期找到活性炭的最佳用量。
1.7 灭菌条件的选择
采用流通蒸气115℃ 30min、流通蒸气115℃ 45min、热压121.5℃ 20min和热压115℃ 30min四种不同的灭菌方式。考察不同灭菌条件下,对盐酸克林霉素注射液的颜色、含量、pH值、有关物质的影响(有关物质采用高效液相色谱法[5]测定。具体测定方法如下)。分别取同一批号样品4份,在不同灭菌条件下进行试验,选择最佳灭菌条件。
1.7.1 色谱条件与系统适用性试验
用十八烷基硅烷键合硅胶为填充剂;以磷酸二氢钾溶液(取磷酸二氢钾6.8g,加水溶解成1000mL,用氢氧化钠溶液调节 pH=7.5)-乙腈(65: 35)为流动相;检测波长为214nm。理论塔板数按克林霉素峰计算,应不低于2 000。
1.7.2 测定方法
取本品,用流动相制成每1 mL中含10.0mg的溶液,作为供试品溶液;精密量取适量,用流动相稀释制成每 1mL中含0.4mg的溶液,作为对照品溶液。取对照溶液10µL注入液相色谱仪,调节检测灵敏度。使主成分峰的峰高约为记录仪满量程的10%;再精密量取供试品溶液10µL,注入液相色谱仪,记录色谱图至主峰保留时间的2倍。供试品溶液色谱图中,以克林霉素主峰相对保留时间为1计,林可霉素相对保留时间为0.17,克林霉素B相对保留时间为0.53;差向克林霉素的相对保留时间为0.72。林可霉素峰面积占总峰(除溶剂及辅料峰外)面积的百分含量不得过 5.0%;克林霉素B不得过2.0%,差向克林霉素不得过1.0%,各杂质峰面积的和不得大于对照溶液主峰面积的2.5倍(10.0%)。
2 结果和分析
2.1 抗氧剂的选择结果

表1 处方中不同抗氧剂及用量的筛选
试验结果表明,选择0.02g EDTA-2Na作为抗氧剂,克林霉素相对含量下降最小,并且盐酸克林霉素注射液的外观澄清无色,符合规定,因此制备工艺中可选用 EDTA-2Na作为抗氧剂,用量0.02g。
2.2 pH值范围的筛选结果
由表2可见,pH>5.0时样品含量下降较大,溶液出现沉淀,pH值低时样品较稳定,但 pH值过低时对肌体的刺激性较大,因此工艺中选择pH值在4.0~4.5范围内。

表2 不同pH条件下样品的热稳定性考察
2.3 活性炭脱色条件的选择结果
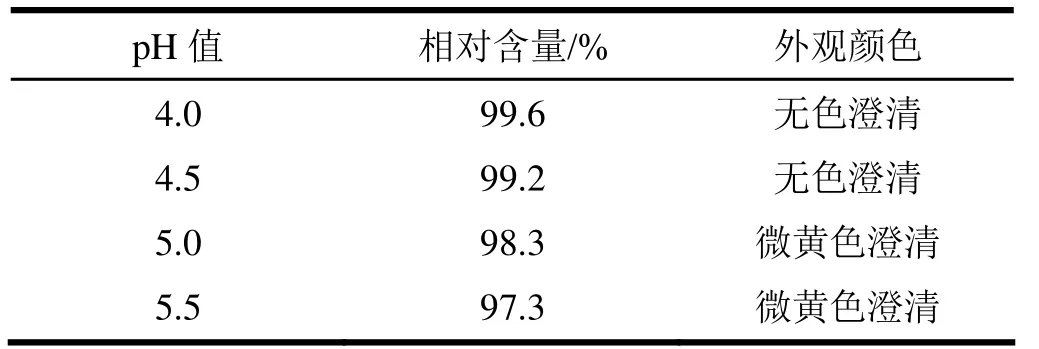
表3 活性碳在不同pH值的注射液中对含量的影响
由表3可见,不同pH值对溶液颜色略有影响,pH为4.0时,含量下降最小,外观符合规定,因此制备工艺中可选用pH值4.0时,加入活性碳脱色。
2.4 活性炭用量的选择结果

表4 活性炭用量的筛选
由表4可见,活性炭用量为0.2%时,脱色后外观无色澄清,含量下降不明显,因此工艺中选择活性炭用量为0.2%。
2.5 灭菌条件的选择结果
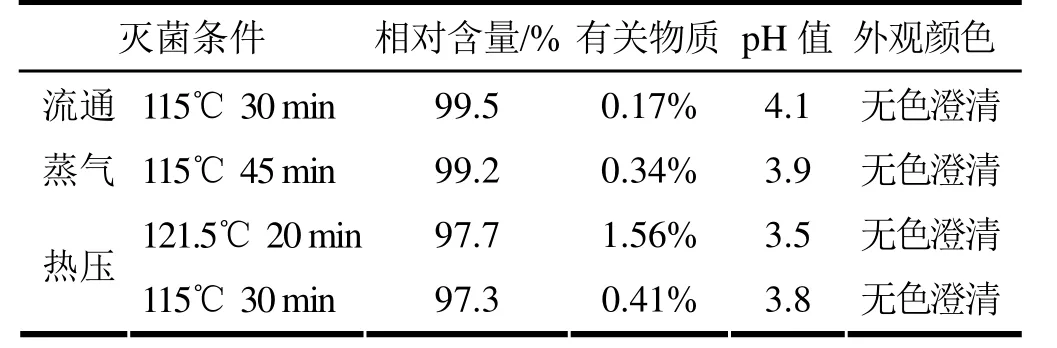
表5 注射液灭菌条件的选择
由表5可见,灭菌条件不同对样品的含量和外观影响很大,综合比较四种不同的灭菌方式,流通蒸气灭菌 115℃30min克林霉素相对含量及pH值下降最小,有关物质量增加最少,因此选择灭菌条件为流通蒸气115℃ 30min。
3 讨论
盐酸克林霉素是一种半合成抗生素,其盐酸盐易溶于水,微溶于乙醇,不溶于乙醚,化学性质较稳定。但其水溶液的稳定性略差,结构中的硫苷键在酸性或金属作用下极易发生水解,从而影响药液的稳定性。因此注射剂中应加入适量抗氧剂,以提高注射剂的稳定性;加入氯化钠调节药液等渗,减少注射液对血管的刺激性;加入柠檬酸调节注射液的pH值,保证其长期放置的稳定性。
在国家食品药品监督管理局制定的国家药品标准当中,盐酸克林霉素注射液的性状应为无色或几乎无色的澄清液体。另外,在对该药品进行各项研究时,都应该保证使药品当中的克林霉素的相对含量不会下降太多。综合以上两点,在进行抗氧剂筛选及相关指标优化时,主要从克林霉素相对含量下降情况和注射液外观是否澄清无色两个方面来考虑。在所进行的五项试验当中,最终选择的结果都能保证注射液的澄清无色,克林霉素的相对含量下降最少。
4 结论
EDTA-2Na作为盐酸克林霉素注射液的抗氧剂较好。pH4.0时加入0.2%活性炭进行脱色;选择流通蒸气115℃进行灭菌30min是比较优化的生产工艺指标。
