燃煤烟气中汞去除的研究进展
2011-10-22马丽萍邓春玲许文娟
崔 夏,马丽萍,邓春玲,许文娟,毛 宇
(昆明理工大学环境科学与工程学院,云南 昆明 650093)
进展与述评
燃煤烟气中汞去除的研究进展
崔 夏,马丽萍,邓春玲,许文娟,毛 宇
(昆明理工大学环境科学与工程学院,云南 昆明 650093)
燃煤电厂是最主要的汞排放源,本文介绍了电厂燃煤过程中汞的存在形态及影响汞去除率的主要因素;通过介绍燃煤电厂的基本烟气净化流程,指出利用现有烟气净化设备协同除汞的可行性;并较为详细地论述了各种汞排放控制技术的研究进展,同时对烟气脱汞技术的研究趋势进行了展望。
汞;燃煤烟气;脱汞技术;吸附
燃煤汞污染是近年来世界公认的继燃煤硫污染之后的又一大污染问题,其中燃煤电厂是最主要的汞排放污染源,因此控制电厂汞污染的排放已经成为环境保护的重要议题。我国能源结构中煤的比例高达 75.9%[1],而煤炭的平均汞含量为 0.22 mg/kg[2],由于我国燃煤技术普遍落后,导致汞污染尤为严重。美国预计到 2018年国内汞排放将减少69%,其能源部(DOE)为此选择了8项新的实验项目用于燃煤电厂的排汞控制。美国根据燃煤种类对燃煤电站的最低汞排放量作了要求,烟煤、亚烟煤、褐煤的排放标准分别为0.96 μg/MJ、2.8 μg/MJ和4.4 μg/MJ[3]。目前,我国对燃煤电厂烟气中汞的控制尚处于起步阶段,并无具体的汞排放限制,仅在《新污染源大气污染物排放限值》中规定汞及其化合物的最高允许排放浓度为0.012 mg/m3。
1 燃煤烟气中汞的存在形式及其影响因素
1.1 燃煤烟气中汞的存在形式
燃煤烟气中汞的存在形式有单质汞(Hg0)、二价汞(Hg2+)和颗粒态汞(HgP)3种。由于燃烧炉内的高温,绝大多数的汞都被分解成单质汞并以气态形式存在于烟气中。气态二价汞易溶于水,易被湿法洗涤系统所捕获而脱除;颗粒态汞易被电除尘器等去除;而单质汞挥发性高且难溶于水[4-5],是相对比较稳定的形态,因此烟气气态单质汞的去除始终是烟气中汞污染控制的难点。
1.2 影响汞形态的主要因素
1.2.1 气体组分
燃煤烟气成分复杂,一般认为烟气中汞的氧化主要是含氯物质(如C12、HCl等)与汞作用的结果,即烟气中汞的氧化态物质主要是氯化汞[6]。其次,烟气中的汞可能与O2、SOx、NOx等物质发生化学反应生成HgO、HgSO4等氧化态物质。再者,飞灰由于比表面积、孔径、孔比表面积、孔容积和孔分布的不同,主要影响颗粒态汞的含量。因此,烟气组成对烟气中汞形态的影响不可忽视。
Laudal等[7]在实验室不同气体组分及含量(SO2、Cl2、HCl和 NO/NO2的含量分别为 1500 mg/kg、10 mg/kg、50 mg/kg和600/300 mg/kg)条件下,采用Ontario-Hydro方法对汞的氧化进行了初步研究 ,给出了不同气体组分及含量存在时氧化态汞与元素汞的大致比例,可以在某种程度上说明气体组分不同对汞形态分布的影响,进而影响后续烟气处理设施对汞的去除。如表1所示。
1.2.2 燃煤种类
不同种类的煤中各元素含量不相同,因此产生的烟气和飞灰成分也不相同。煤种是影响煤燃烧过程中汞释放的重要因素。如表2所示,国家能源技术实验室(NETL)报道指出了一定条件下燃烧不同煤种时烟气中不同形态汞的大致含量[8]。不同煤种中氯含量的差别对烟气中汞形态有较大影响。它可直接将单质汞氧化为二价汞,并且反应速度快,较易发生。除氯以外的其它成分对烟气中汞的形态也有影响[9]:燃烧高硫煤则烟气中Hg2+含量较低;煤中铁因能催化氧化汞而增加汞进一步被颗粒物质捕获的概率;在燃烧过程中钙因与氯反应而减小了氯对汞的氧化能力。因此,燃烧高钙低氯含量的亚烟煤和褐煤的烟气中Hg0的含量较高;而燃烧烟煤的烟气中Hg2+的含量较高。

表1 不同气体组分存在条件下汞的形态分布[7]
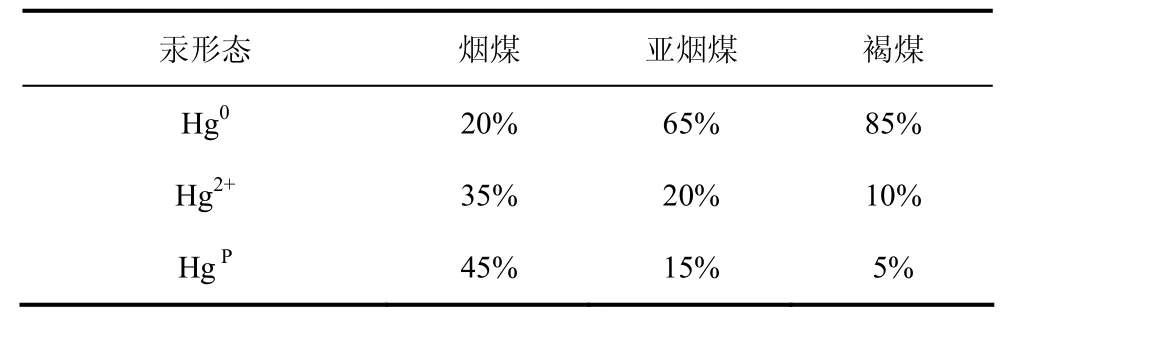
表2 不同煤种燃烧各形态汞的大致含量[8]
1.2.3 燃煤温度
随着煤燃烧时间的增加,汞总释放率呈现递增趋势,但热解时间对汞的形态分布影响却很小。汞总释放率随着温度的升高几乎呈线性关系增长,而且随着燃煤温度的升高,元素汞占总汞的比例呈现出先增大后减小的趋势。单质汞在燃烧过程中始终是气态汞的主要形态,而且随着热解温度的升高,单质汞占总汞的比例变大,当温度达到 500℃左右时该比例达到93.5%左右[10]。
2 利用现有气体净化设备(APCDs)脱汞
对现有 APCDs进行改造,使其在脱氮、脱硫的同时能去除烟气中的汞,即利用协同控制的思想,同时脱氮、脱硫除汞。如图1所示,国外使用的最普遍的气体净化流程为:烟气从燃烧器(Boiler)出来,首先通过用于脱硝SCR装置,接着通过用于去除颗粒态污染物的布袋除尘器(FF)或者静电除尘器(ESP),最后通过主要是用于去除SOx的湿式脱硫装置(WFGD),随后直接通过烟囱(Stack)外排[11]。

图1 最普遍的气体净化流程(APCDs)[11]
总体来说,燃煤烟气中颗粒态汞(HgP)含量较少,结合各种吸附剂喷入法(SDA),FF/ESP可以有效地去除这部分颗粒态汞,与 ESP相比,CS-ESP和 HS-ESP的去除率稍低,分别为27%和4%。由于 Hg2+的水溶性,烟气通过湿式脱硫装置(WFGD)后,Hg2+的脱除率可以达到90%,但Hg0的去除率几乎为 0,为此可以通过各种氧化法(例如SCR、化学氧化法等)先将Hg0氧化,再与WFGD结合,可以达到高的汞去除率。
由于煤的类型、飞灰特性和具体 APCDs的不同,总的汞去除率从0~98%不等。表3列举了不同煤种在各种APCDs协同的作用下汞的去除效率。可以看出:在同等 APCDs条件下,与亚烟煤和褐煤相比,烟煤表现出高的汞的去除率;燃烧相同煤种后的烟气经含有WFGD、FF的APCDs后汞的去除率较高。
3 脱汞吸收剂注入技术
3.1 活性炭/改性活性炭
活性炭对汞的吸附机理比较复杂,相应吸附机理的研究也比较多[13-14]。如果对活性炭进行改性、活化处理,那么活性炭的吸附能力将大大增强。常用于活性炭改性的元素有硫、碘、溴、氯等[15-16]。

表3 不同煤种在现有烟气控制设备下对汞的去除率[12]
近年来,对于活性炭改性的研究也更多更深入。杨宏旻等[17]的研究结果表明:在实验室条件下,利用 HCl、Cu(NO3)2·3H2O、Cu(NO3)2·3H2O混合NH4Cl溶液分别改性后的活性炭对单质汞的吸附能力均高于未改性活性炭,且所获得的汞吸附能力顺序为为AC-CuO<AC-HCl<AC-CuO(Cl)。Chi等[18]将10 mg/m3的活性炭和0.3 mg/kg的碘同时注入实验室模拟的含飞灰的废气中,汞的去除率高达90%。Hu等[16]为研究不同表面的活性炭对汞吸附的影响,在实验室条件下通过蒸气活化和采用ZnCl2化学改性制备了不同的活性炭。他们发现通过蒸气活化制备的活性炭不具备吸附汞的能力,而在相同的实验条件下经ZnCl2改性的活性炭则显示出很强的汞的吸附能力。因此,他们认为活性炭对汞的吸附是一个化学吸附的过程。赵鹏飞等[19]建立了表征活性炭表面的饱和簇模型,采用量子化学的密度泛函理论,对单质汞在活性炭以及氯改性活性炭表面的吸附进行了研究。他们发现单质汞吸附在未改性活性炭表面主要依靠较弱的物理吸附;而单质汞吸附在含氯活性炭表面时,活性炭表面会自发生成HgCl;同时电荷密度和键布局的结果表明HgCl可以稳定地存在,并增加了活性炭对单质汞的吸附能力。
3.2 活性碳纤维
活性碳纤维(ACF)具有发达的孔结构和大比表面积(是活性炭的2倍以上),而且微孔多(1.42 nm),微孔内有较大的吸附势,同时微孔直接开口在固体表面,气态汞可直接扩散进入微孔,所以活性碳纤维吸附速度快,吸附容量大,而且再生时水合硫酸也容易在孔中扩散,便于洗脱[20]。
任建莉等[21]的实验结果表明,经浓硝酸湿氧化处理、部分脱附处理和经空气氧化处理的活性碳纤维的吸附性能均得到不同程度提升,并且他们认为脱汞性能的提高是由于改性后ACF表面C=O和COOH含量增加。Fan等[22]将CeO2/ACF用于对单质汞的去除实验中,发现负载 CeO2能明显的加强活性碳纤维对单质汞的去除率。当负载量为6%时,在不同煅烧温度条件下催化剂对汞表现出相似的吸附效果;CeO2/ACF对汞的去除效果随着温度的增加而增加,当温度超过150 ℃后,其吸附效果逐渐下降;此外,实验气中的NO、SO2气体对汞也有很好的氧化作用。
3.3 飞灰
飞灰对烟气中的各种污染物均有一定的吸附活性[14],除飞灰中未燃碳对汞有较强的吸附作用外[15],飞灰炭表面的氧化官能团和卤素的存在均可以提高对汞的吸收[25]。因此作为活性炭廉价的替代品,飞灰未燃碳表现出了极大的应用潜力。
孟素丽等[26]研究了烟气成分对燃煤飞灰中汞的吸附影响。他们发现在CO2-O2-N2的体系中,单独加入SO2,飞灰的汞吸附能力与SO2的浓度有密切的关系;单独加入HCl,在HCl浓度较低时,飞灰的汞吸附能力随着HCl浓度的增加而逐渐增加,在体积分数 50×10-6左右达到最佳吸附效果,而后飞灰的汞吸附能力有所降低;单独加入 NO,大大促进了飞灰对汞的吸附。同时加入HCl和SO2时,飞灰对汞的吸附效果要好于单独加入SO2,但比单独加入HCl时要差一些;再加入NO后飞灰对汞的吸附效率与吸附量都得到很大的提高。赵永椿等[27]经实验研究发现,煤级的不同是造成飞灰脱汞性能差异的主要原因;碳含量并不是决定飞灰对汞的吸附能力的关键因素,各向异性碳颗粒尤其是多孔网状结构碳含量是决定飞灰脱汞能力的重要因素。
3.4 钙基类物质
目前脱除燃煤烟气中的汞所采用的钙基类物质主要有 CaO、Ca(OH)2、CaCO3、CaSO4·2H2O。钙基类物质的脱除效率与燃煤烟气中汞的化学形态有很大关系。钙基类物质[28]如Ca(OH)2、CaO对Hg2+的脱除率最高可达到85%,但对于单质汞的吸附效率却很低。因此,一些学者进行了改性钙基类对汞吸附的研究。赵毅等[29]利用汞渗透管产生的气态单质汞和其它烟气主要气体成分模拟烟气条件,在固定床实验台上进行了改性钙基吸附剂吸附单质汞的实验研究。他们发现:Ca(OH)2吸附Hg0效果较差,SO2的存在对Ca(OH)2吸附Hg0有促进作用;经改性的普通高活性钙基吸附剂对Hg0吸附效果比消石灰稍强,SO2的存在促进了普通高活性钙基吸附剂对Hg0的吸附;有添加剂的高活性钙基吸附剂对Hg0的吸附效率比普通高活性钙基吸附剂增加约30%,当有SO2存在时,有添加剂的高活性钙基吸附剂对Hg0的吸附效率略低,而穿透时间延长。
3.5 高分子壳聚糖
壳聚糖(chitoosan,CS)又称脱乙酰几丁质,是一种储量极为丰富的天然碱性高分子多糖,因壳聚糖分子中含有大量的—NH2和—OH基团,可以螯合重金属离子,形成网状稳定螯合物,被广泛应用于环保领域[30-31]。
高鹏等[32]首次利用自制的壳聚糖类吸附剂对实验模拟燃煤烟气中的汞进行吸附脱除,发现在80℃时对汞的吸附率达96.34%。壳聚糖吸附剂脱除汞的反应是化学反应占主导,理论上最佳吸附反应温度为80~120 ℃。并推测壳聚糖吸附剂脱除汞的反应活性基是—NH2,而不是—OH;其吸附机理为4个游离—NH2、或者2个游离—NH2与2个—OH和一个汞离子或汞原子螯合成环。随后高鹏等[33]又采用在线检测法检测了纯氮气气氛下及模拟烟气气氛下高分子化合物壳聚糖吸附剂对单质汞的吸附特性,通过红外光谱分析验证了所推测的汞的吸附机理的正确性。Zhang等[34]用KBr、KI和H2SO4对壳聚糖进行改性,发现碘、硫酸和壳聚糖中的—NH2发生了化学反应。适量硫酸的加入可以极大地提高壳聚糖类吸附剂的脱汞效率;与溴改性吸附剂相比,碘改性吸附剂更能够大大提高吸附剂的脱汞效率;并且用KI和H2SO4一同改性吸附剂,在3 h后几乎可以达到100%的去除率;由于存在活性位(例如 SO42-和—NH2),湿度可以增加对汞的吸附能力,因此适当提高吸附温度可以提高其脱汞效率。
3.6 矿物类吸附剂
虽然矿物类吸附剂的脱汞效率并不占优势,但由于其具有储量丰富、价格低廉、对环境无毒无害等优点而广受关注,实际操作中需对矿物类吸附剂进行改性以提高其吸附能力。
丁峰等[35]在固定床反应器上研究了硅酸盐矿物吸附剂对模拟烟气中单质汞的脱除能力。研究发现热活化不能提高凹凸棒石、丝光沸石等矿物吸附剂对单质汞的脱除能力,而提高吸附温度有利于对单质汞的脱除;在30 min内膨润土的吸附率为1029 ng/g,是凹凸棒石的近2倍;在120 ℃时丝光沸石表现出对单质汞的氧化能力,但其本身吸附效果不明显。Lee等[36]用各种胺、酰胺、硫醇、尿素等官能团和硫、硫化钠、多硫化钠等活性添加剂改性硅胶、氧化铝、分子筛、沸石和蒙脱石用于汞的吸附实验,虽然一些含硅官能团的物质能有效去除液态水中的重金属离子,但却没有很好地去除烟气中的汞,从而说明不同相的汞的去除机理是不同的;在众多的硫、硫化钠、多硫化钠浸渍非碳基样品中,多硫化钠浸渍的蒙脱石在 70 ℃表现出稳定的汞吸附能力。Li等[37]进行了关于天然沸石、膨润土和蛭石及其化学改性剂作为吸附剂脱除气态汞的实验研究。他们发现,用MnO2、FeC13金属氧化物对矿石样品进行化学改性后,吸附时间大为延长。其原因在于在吸附剂表面发生了化学反应,化学吸附过程有效增加了吸附能力。因此,可进一步通过改变化学浸渍试剂,继续提高改性吸附剂的吸附能力。
3.7 新型吸收剂
Abu-Daabes和 Pinto[38]研究了一种可从烟气中直接去除气态HgCI2的新型螯合吸收剂。该吸收剂主要由附着在多孔硅胶培养基上的活性超细表层结构组成,通过鳌合团表面的熔融盐产生螯合作用。经元素分析发现,它对汞的理论吸收能力高达 33 mg/g。该吸收剂适用于烟气处理最后阶段的低温区域,最高的操作温度是135 ℃。对HgC12的动力吸附能力评估显示,该吸收剂是非常有效的,最低的吸收能力是12 mg/g,由检测产物可知螯合物的形成是由巯基丙氨酸配体和捕集的 HgCl2共同完成的。
4 非吸收剂注入技术
4.1 SCR处理实施中的脱汞
在研发各类高效SCR催化剂时,一些学者本着协同控制的思想对 SCR同时除汞作用进行了相关的研究。
Yang等[39]根据两组对比实验指出,在整个空气污染控制装置(APCD)中添加SCR处理过程后,汞的去除效率从48%提高到88%。周劲松等[40]做了SCR反应中单质汞在钒基上的氧化实验,结果表明钒基对Hg0和HCl均具有吸附作用,且钒基对HCl的吸附作用强于对 Hg0。Hg0的氧化是通过对钒基上与Hg0邻近的HCl的氧化作用实现的。Presto和Granite[41]用贵金属作催化剂来氧化汞,指出金和钯也可用于 SCR反应中作为催化剂来达到除汞的目的。Straube等[42]对 SCR-NH3系统中催化剂V2O5/TiO2的吸附脱汞性能作了测试,因汞在V2O5/ TiO2表面以化学吸附形式(Hg-O)被吸附,所以V2O5/TiO2表现出对汞的良好吸附效果。其研究还指出低浓度HCl能促进汞的脱除,但高浓度HCl气体则不利于汞的吸附脱除,SO2和 NH3对汞的吸附效率的影响甚微。同时Fan等[22]指出脱硝的低温SCR催化剂CeO2/ACF因其对汞的高去除率和稳定性在汞脱除实验中表现出汞吸附方面很大的潜力。Lei等[43]发现低温 SCR-NH3系统的MnOx/TiO2催化剂也具有良好的脱汞效果,而且该催化剂是以化学吸附形式(Hg-O)对汞进行吸附脱除。
以上研究表明,用SCR系统进行同时脱硝脱汞是现实可行的,这对改造现行的脱硝设备进行脱汞具有重要的指导意义。虽然单独用SCR的各种催化剂对汞表现出良好的去除效果,但SCR系统的反应机理和动力学十分复杂,汞的加入对催化剂的脱硝效果造成的影响尚不清楚,因此相关的研究工作还需进一步深入。
4.2 Mercu-RE法
Mercu-RE法[44]是一种利用可再生吸附剂去除烟气中汞的方法,且吸附剂可以循环利用。此方法基于贵金属可以重复性的吸附汞并且在高于燃煤烟气温度几百摄氏度的条件下又可以脱附汞的特性。Mercu-RE法有以下几大优势:①无论汞以何种形态存在,去除率都可超过95%;②与其它很多方法相比,可以大大减少汞的控制费用;③减少固体、液体废物中汞的污染;④潜在地减少了生态系统中的汞。
Mercu-RE法去除汞包括以下几个步骤:在烟气温度为 300~400 ℉、流量为 105CFM(1 CFM=0.4719 L/s)的实际烟气条件下,每立方米单元模块捕获10 μgHg;用未捕获汞的单元模块替换已捕获汞的单元模块;通过净化气体对捕获汞的单元模块在600~700℉条件下加热8 h,从而形成一个更高浓度的汞气流;捕获收集净化气体中的高浓度汞;使脱附的捕获汞的模块用于再次更替使用;随后将要再生或废弃的汞集中转运。
5 结语及展望
活性炭对燃煤烟气中汞的脱除效率最高可达90%以上,经改性后能进一步提高其利用率,但运行成本过高;向燃煤烟气中直接注入硫、氯等可以很大程度提高飞灰对汞的吸附率,飞灰作为一种去除汞的廉价吸附剂受到越来越多的关注;钙基吸附剂主要吸附Hg2+,对于单质汞的吸附效率却很低,因此单独使用此方法对火电厂烟气除汞意义不大,但可以结合氧化法同时进行协同脱除;矿物类吸附剂经济性高,去除率低,应结合本身的特性来选择活性剂改性;具有较大吸附能力和再生能力的新型吸附剂,因其对汞的控制费用较高,应将注意力放到其再生能力的研究上。
从烟气净化装置控制汞的方面来看,应努力提高现有设备的利用率。可先利用各种氧化剂将 Hg0氧化为Hg2+,然后用WFGD脱除;或利用对汞具有较高催化活性的 SCR催化剂,使得 SCR、FF/ ESP、WFGD 三者联合脱汞,尽而实现汞、二氧化硫、氮氧化物的联合控制。
虽然目前关于吸附剂与烟气各组分之间的反应已经有了较多的研究,但若想将其应用到实际的工业实践当中,仅依靠目前的实验室研究是远远不够的,对汞吸附及其反应机理研究仍需进一步深入。应考虑到烟气化学组成、质量传递、物理吸附、化学吸附和现有烟气控制设备各方面因素,建立起综合的数学模型,从而将具体的吸附剂应用于特定燃煤电厂进行模拟预测。另外,加强燃煤过程中汞的析出规律以及汞污染控制的基础理论研究,对在实际中吸附剂的选择和效率具有十分深远的意义。
[1]张绍强,张运章.我国煤炭资源、生产与环境概况[J].环境保护,2006(13):53-57.
[2]郭欣,郑楚光,贾小红,等. 300MW煤粉锅炉烟气中汞形态分析的实验研究[J].中国电机工程学报,2004,24( 6 ):185-188.
[3]Apogee Scientific Inc. Assessment of low cost novel sorbens for coal-fired power plant mercury control[OL]. http://www.osti.gov/ bridge/servlets/purl/835235-AL9b5h/native/835235.pdf.
[4]赵毅,刘松涛,马宵颖,等.改性粉煤灰吸收剂对单质汞的脱除研究[J].中国电机工程学报,2008,28(20):55-60.
[5]黄治军,段钰锋,王运军,等.改性氢氧化钙吸附脱除模拟烟气中汞的试验研究[J].中国电机工程学报,2009,29(17):56-62.
[6]高洪亮,周劲松,骆仲泱,等.燃煤烟气中汞氧化的动力学机理[J].动力工程,2007,27(6):975-979.
[7]Laudal D L,Brown T D,Nott B R.Effects of flue gas constituents on mercury speciation[J].Fuel Processing Technology,2000,65-66:157-165.
[8]Pavlish J H,Holmes M J,Benson S A.Application of sorbents for mercury control for utilities burning lignite coal[J].Fuel Processing Technology,2004,85(4):563-576.
[9]Galbreath K C,Zygarlicke C J.Mercury transformations in coal combustion fue gas[J].Fuel Processing Technology,2000,65(3):289-310.
[10]王卉,刘玲,杨宏旻,等.热解温度和时间对煤热解过程中汞析出的影响[J].洁净煤燃烧与发电技术,2009,5(8):20-23.
[11]Pudasainee D,Lee S J,Lee S H,et al. Effect of selective catalytic reactor on oxidation and enhanced removal of mercury in coal-fired power plants[J].Fuel,2010,89(4):804-809.
[12]Feeley T J,Brickett L A,Palko A O. Field testing of mercury control technologies for coal-fired power plants[OL]. DOE/NETL Mercury R&D Program Review,U.S.DOE,May 2005. http://www.netl. doe.gov/technologies/coalpower/ewr/pubs/mercuryR&D-v4-0505. pdf.
[13]Hu C X,Zhou J S,Luo Z Y,et al. Effect of oxidation treatment on the adsorption and the stability of mercury on activated carbon[J].Environmental Science,2006,21(6):1161-1166.
[14]Luo Z Y,Hu C X,Zhou J S,et al. Stability of mercury on three activated carbon sorbents[J].Fuel Processing Technology,2006,87:679-685.
[15]邓先伦,蒋剑春.除汞载硫活性炭研发[J].林产化工通讯,2004,38(3):13-16.
[16]Hu C,Zhou J S,He S,et al. Effect of chemical activation of an activated carbon using zinc chloride on elemental mercury adsorption[J].Fuel Processing Technology,2009,90(6):812-817.
[17]杨宏旻,张斌.侯文慧,等.负载CuO/Cl活性炭的气态汞脱除特性[J].南京航空航天大学学报,2009,6(24):814-818.
[18]Chi Y,Yan N,Qu Z,et al.The performance of iodine on the removal of elemental mercury from the simulated coal fired flue gas[J].Journal of Hazardous Materials,2009,166(2-3):776-781.
[19]赵鹏飞,郭欣,郑楚光.活性炭及氯改性活性炭吸附单质汞的机制研究[J].中国电机工程学报,2010,30(23):40-45.
[20]李开复,吕春祥,凌立成. 活性炭纤维的脱硫性能[J].燃烧化学学报,2002,30(1):89-95.
[21]任建莉,陈俊杰,罗誉娅,等.活性炭纤维脱除烟气中气态汞的试验研究[J].中国电机工程学报,2010,5(7):28-34.
[22]Fan X P,Li C,Zeng G,et al.Removal of gas-phase element mercury by activated carbon fiber impregnated with CeO2[J].Energy Fuels,2010,24(8):4250-4254.
[23]赵毅,孙小军,许佩瑶,等.烟气同时脱硫脱氮的高活性吸收剂的表征及脱除机理研究[J].中国科学:技术科学,2006,6(3):326-340.
[24]Lopez-Anton M A,Diaz-Somoano M,Martinez-Tarazona M R. Retention of elemental mercury in fly ashes in different atmospheres[J].Energy Fuels,2007,21(1):99-103.
[25]López-Antón M A,Abad-Valle P,Diaz-Somoano M,et al. The influence of carbon particle type in fly ashes on mercury adsorption [J].Fuel,2009,88(7):1194-1200.
[26]孟素丽,段钰锋,黄治军,等.烟气成分对燃煤飞灰汞吸附的影响[J]. 中国电机工程学报,2009,20(12):66-73.
[27]赵永椿,张军营,刘晶,等.燃煤飞灰吸附脱汞能力的实验研究[J].中国科学:技术科学,2010,4(6):385-391.
[28]刘妮,程乐鸣,骆仲泱,等.钙基吸收剂微观结构特性及其反应性能[J].化工学报,2004,55(4):635-639.
[29]赵毅,刘松涛,马宵颖,等.改性钙基吸附剂的汞吸附特性实验研究[J].中国电机工程学报,2009,29(8):50-55.
[30]苏海佳,贺小进,谭天伟.球形壳聚糖树脂对含重金属离子废水的吸附性能研究[J].北京化工大学学报,2003,30(2):19-22.
[31]郭敏杰,刘振,李梅.壳聚糖吸附重金属离子的进展[J].化工环保,2004,24(4):262-265.
[32]高鹏,向军,毛金波,等.高分子化合物壳聚糖脱除燃煤烟气中汞的实验研究[J].中国电机工程学报,2006,24(26):24-26.
[33]高鹏,向军,张安超.壳聚糖吸附剂脱除燃煤模拟烟气中汞的试验研究[J].中国环境科学,2010,6(6):733-737.
[34]Zhang A Y,Xiang J S,Lu S,et al. Preparation,characterization,and application of modified chitosan sorbents for elemental mercury removal[J].Industrial & Engineering Chemistry Research,2009,48(10):4980-4989.
[35]丁峰,张军营,赵永椿,等.天然矿物材料吸附剂脱除烟气中单质汞的实验研究[J].中国电机工程学报,2009,29(35):65-70.
[36]Lee J Y,Ju Y,Keener T C,et al. Development of cost-effective non carbon sorbents for Hg(0)removal from coal-fired power plants[J].Environmental Science & Technology,2006,40(8):2714-2720.
[37]Li R J,Zhou J S,Hu C X,et al. Application of novel sorbents for mercury vapor removal from simulated flue gases [J].Chinese Society of Electrical Engineering,2007,27(2):48-53.
[38]Abu-Daabesma M A,Pinto N G.Synthesis and characterization of a nano-structured sorbent for the direct removal of mercury vapor from flue gases by chelation[J].Chemical Engineering Science,2005,60(7):1901-1910.
[39]Yang H M,Pan W P.Transformation of mercury speciation through the SCR system in power plants [J].Journal of Environmental Sciences,2007,19(2):181-184.
[40]He S,Zhou J,Zhu Y,et al.Mercury oxidation over a vanadia-based selective catalytic reduction catalyst[J].Energy & Fuels,2009,23(1):253-259.
[41]Presto A A,Granite E J.Noble metal catalysts for mercury oxidation in utility flue gas[J].Platinum Metals Review,2008,52(3):144-154.
[42]Straube S,Hahn T,Koeser H,et al.Adsorption and oxidation of mercury in tail-end SCR-DeNOxplants:Bench scale investigation and speciation experiments[J].Applied Catalysis B:Environmental,2008,79(3):286-295.
[43]Lei J,Sreekanth P M,Smirniotis P G,et al. Manganese oxide/ titania materials for removal of NOxand elemental mercury from flue gas[J].Energy Fuels,2008,10(3):10-21.
[44]Turchi C S,Stewart R M,Broderick T E. Removal and recovery of vapor-phase mercury from fue gas using regenerable sorbents[OL]. http://www.netl.doe.gov/publications/proceedings/98/98ps/pspa-16. pdf,accessed October 2006.
Research progress of removing mercury from coal-fired flue gas
CUI Xia,MA Liping,DENG Chunling,XU Wenjuan,MAO Yu
(School of Environmental Science and Engineering,Kunming University of Science and Technology,Kunming 650093,Yunnan,China)
Mercury emissions from coal-fred power plants are believed to be the largest source of anthropogenic mercury emissions. This paper illustrates the form of mercury and the main factors which affect the elimination rate of mercury. Through the introduction of the air pollution control devices(APCDs),synergistic control is feasible by taking advantage of existing APCDs. The research progress of mercury emission control is summarized. The absorbents for mercury assorption,such as active carbon,activated carbon fiber,ash,polymeric chitosan,natural mineral sorbents,and new kinds of absorbents are summarized. Recent advances in non-injection mercury sorption technologies are reviewed. Future research directions are suggested.
mercury;flue gas;technology for mercury removal;adsorption
X 701
A
1000–6613(2011)07–1607–07
2010-11-22;修改稿日期:2010-12-28。
教育部留学回国人员启动基金项目。
崔夏(1986—),女,硕士研究生,研究方向为废物资源化利用。E-mail cuixia.summer@163.com。联系人:马丽萍,博士,教授,研究方向为固体废物资源化利用、大气污染控制。E-mail maliping22@sina.com。
