Sn-SO /ZrO 2固体超强酸催化合成乙酸丁酯
2011-10-13王芳
王芳
(扬州工业职业技术学院,江苏扬州225127)
王芳
(扬州工业职业技术学院,江苏扬州225127)
采用sol-gel法制备了固体超强酸以及催化剂,用Hammett指示剂法对催化剂酸强度进行表征,并考察了其对乙酸和正丁醇的酯化活性,实验结果表明,Sn(Ⅳ)SZ的活性优于和Sn(Ⅱ)SZ。实验优化条件为:醇酸物质的量比为1.4:1,Sn(Ⅳ)SZ催化剂用量为0.5 g(乙酸0.41mol),反应时间为3~4 h,乙酸转化率可达96%以上。
固体超强酸;催化;乙酸丁酯
本文通过锡离子掺杂改性制备的固体超强酸合成乙酸正丁酯,着重考察了反应的催化条件,在最适宜的反应条件下反应3~4 h,催化合成乙酸正丁酯的酯化率可达96%以上。
1 实验部分
1.1 试剂与仪器
ZrOCl2·8H2O试剂采用工业品。负载用的金属盐选用SnCl4、SnCl2,均为化学试剂。95%乙醇、苯、乙酸、正丁醇、氨水均为分析纯试剂。
气谱为日本岛津GC-17A气相色谱仪。催化剂的HO值采用指示剂法测定。
1.2 固体超强酸的制备
1.2.1称取一定量的ZrOCl2·8H2O
固体置入烧杯中,加入一定量的去离子水配成质量分数为8%的溶液,混合均匀后,在快速搅拌下向溶液中滴加25%~28%的氨水,调节pH≈9,室温陈化24 h后抽滤,反复洗涤至无Cl-(用0.1mol/L的AgNO3检验)。将沉淀在高压釜中383K乙醇醇化处理8h,然后研磨成100~120目的细粉,用0.5mol/L的H2SO4溶液(按15mL/g细粉)浸渍1h,过滤后再烘干,并置于马福炉中焙烧4h即得醇化催化剂。
1.2.2用金属离子对其改性
将金属盐SnCl4或SnCl2溶于0.5 mol/L的H2SO4得到0.2mol/L金属盐溶液,并用此溶液(按15mL/g细粉)浸渍Z(rOH)41 h,使金属离子和负载在Zr(OH)4上,过滤后在383 K烘干,然后置于马福炉中823 K焙烧4 h即得固体超强酸,简写为:Sn(Ⅳ)SZ和Sn(Ⅱ)SZ。
1.3 试验方法
在装有分水器、温度计和回流冷凝器的三颈烧瓶中,加入一定量的乙酸、正丁醇、苯和固体超强酸催化剂,摇匀后,取样测定其酸值,加热反应物至有回流时开始记录反应时间。反应物加热回流分水,每隔1 h取样测定其酸值,至几乎无水分出为止。
产物的分离纯化可先用适量的Na2CO3溶液洗去未反应的酸,再水洗,无水MgSO4干燥后,常压或减压蒸馏,截取沸点处的馏分,用气相色谱仪测定分离出的产品纯度为99.5%。
反应前后分别取反应液0.5mL,以酚酞作指示剂,用0.1mol/L的NaOH水溶液滴定,然后按下式计算反应酯化率C。
C=(V1-V2)/V1×100%
式中V1、V2分别为反应前后0.5mL反应液消耗NaOH水溶液的毫升数。
2 结果与讨论
2.1 固体超强酸催化剂的酯化催化活性
43 g正丁醇和25 g乙酸反应,20mL苯作为带水剂,催化剂的用量为0.5 g,考察不同催化剂对醇酸酯化反应的催化活性。由图1可以看出,ZrO2和Zr(OH)4对醇酸酯化反应转化率与不加催化剂时相当,没有催化活性。而(Ⅳ)SZ和Sn(Ⅱ)SZ三个固体超强酸催化剂在对醇酸酯化反应均具有很高的催化活性,反应3 h后酯化率均高达90%左右,其中Sn(Ⅳ)SZ对醇酸酯化反应的催化活性明显高于和Sn(Ⅱ)SZ的催化活性。
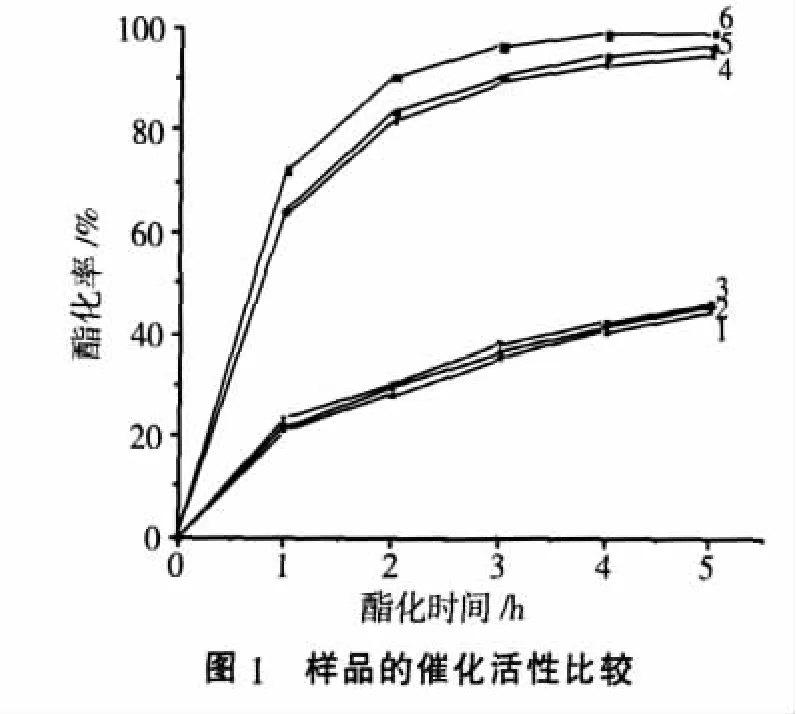
2.2 催化剂用量对酯化率的影响
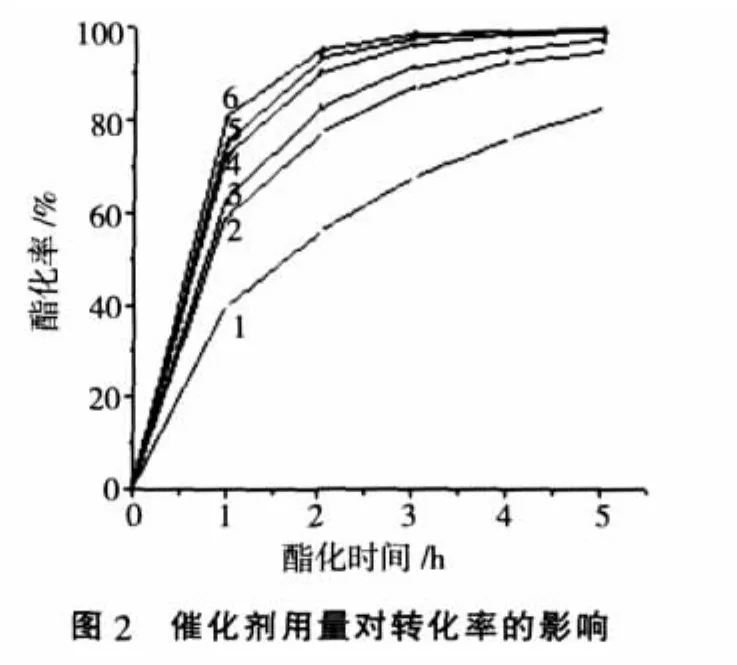
43 g正丁醇和25 g乙酸反应,20mL苯作为带水剂,考察Sn(Ⅳ)SZ用量对酯化反应催化活性的影响。
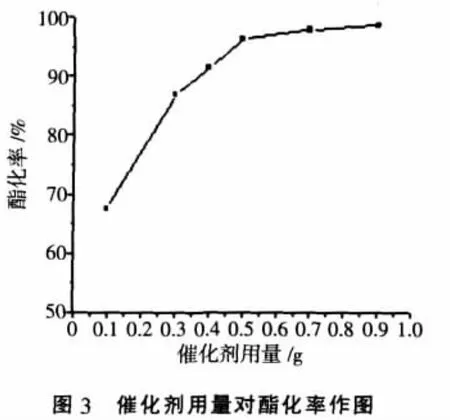
图2结果表明,加入0.1 g催化剂,反应2 h后酯化率只有55.7%,随着催化剂用量增加,乙酸转化率直线上升。但用量增大到一定程度后,酯化率增加的幅度已不明显。反应3h后(见图3)催化剂用量为0.5 g和0.9 g对醇酸酯化的酯化率接近,酯化基本完全,说明采用0.5 g的催化剂用量时,已显示了足够的催化活性,因此较理想的催化剂用量为乙酸重量的2%。
2.3 醇酸物质的量比对酯化率的影响
采用25 g乙酸,0.5 g Sn(Ⅳ)SZ催化剂,50mL苯作为带水剂,改变醇酸比进行实验,反应时间为4.0 h,结果见表1。由表可见,醇酸物质的量比为1.0∶1时,反应4 h后酯化率为84.0%,当醇酸物质的量比为1.4∶1时,反应4 h后酯化率明显提高,为92.9%,增加正丁醇的用量有利于酯化率提高,这是因为增大正丁醇的用量,有利于反应向生成酯的方向移动而提高酯化率。但提高到一定程度(醇酸物质的量比>1.4∶1)后,酯化率反而有所下降,这可能是由于醇的用量过多时,酸的浓度下降;同时也相对降低了催化剂的浓度。所以最适宜的醇酸物质的量比为1.4∶1。
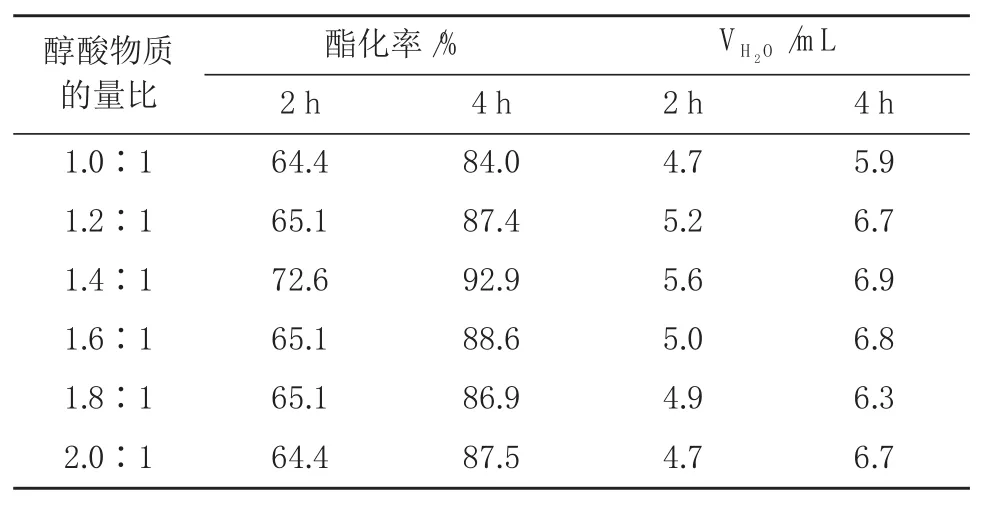
表1 正丁醇与乙酸物质的量比对转化率的影响
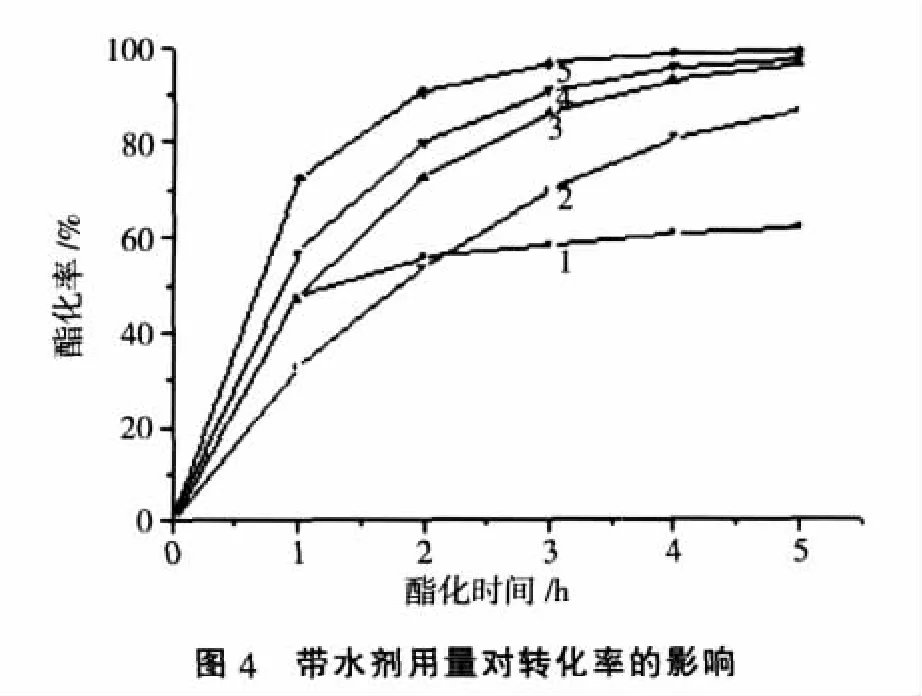
2.4 带水剂用量对酯化率的影响
酯化反应是一个可逆的失水反应,加入带水剂可缩短反应时间,提高酯化率,但其用量要适宜。43 g正丁醇和25 g乙酸反应,0.5 g Sn(Ⅳ)SZ催化剂,考察了苯的用量对酯化反应催化活性的影响。
苯的用量首先取20mL,其中15mL将油水分离器充满(反应体系中只有5mL),从图4可以看出,随着带水剂用量的增加,酯化反应速率逐渐降低,这是因为加入过多带水剂,不仅相对降低了醇和酸的浓度,还使反应回流温度降低。另外,如果苯的用量小于20mL,刚开始回流将起不到苯和水共沸脱水的作用,不利于水的分出。如果不加带水剂苯,反应2 h后酯化率是55.6%,随着反应的时间的延长,酯化率增加不明显,反应5h后酯化率也只有61.7%。所以在该反应条件下,带水剂苯的最佳用量为20mL。
2.5 催化剂的酸强度测定
固体超强酸的酸强度用Hammett函数Ho表示。指示剂为:对硝基甲苯,Ho=-11.35;间硝基氯苯,Ho=-13.16;2,4-二硝基甲苯,Ho=-13.76;2,4-二硝基氯苯,Ho=-14.52;结果见表2。从表2中的Ho值可以看出,经823 K焙烧的及Sn4+、Sn2+离子掺杂改性的均具有超强酸性,并且经过金属离子掺杂后的催化剂酸性有所增强。

表2 固体超强酸的酸强度
3 结论
3.1823K焙烧的SO2-4/ZrO2、Sn(Ⅳ)SZ和Sn(Ⅱ)SZ三个超细纳米固体超强酸催化剂在对醇酸酯化反应均具有很高的催化活性,特别是SnCl4的掺杂引入明显地改善了的酯化活性,两者的协同效应使Sn(Ⅳ)SZ样品催化活性优于(Ⅱ)SZ催化剂。
3.2从反应条件对酯化反应的催化活性影响可知:催化剂Sn(Ⅳ)SZ用量0.5 g(占乙酸重量的2%),醇酸物质的量比为1.4∶1,带水剂苯的用量为20mL,乙酸正丁酯的酯化率的最高,反应时间为2 h、3 h和4 h时酯化率分别为90.3%、96.3%和98.5%。
Study on the Catalytic Synthesis of n-Butyl Acetateby the Tin doped Solid Superacid
WANG Fang
(Yangzhou Polytechnology Institute,Yangzhou Jiangsu 225127,China)
SO2-4/ZrO2and Sn-SO2-4/ZrO2solid superacids have been prepared with sol-gelmethod.The acid strength of catalyst has been studied by Hammett indicator method,and their esterificattion activity for n-butanol with acetic acid has been examined.Activity of Sn(Ⅳ)SZ catalysts in esterificattion was better than activity of SO2-4/ZrO2and Sn(Ⅱ)SZ.The results showed that the optimum conditions were as follows:the molar ratio of n-butanol to acetic acid was 1.4∶l,the weight of the catalyst was 0.5 g(if the weight of acetic acid was 0.41 mol),the reaction time was 3~4 h,the yield of butyl acetate was about 96%.
solid superacid;catalysis;butyl acetate
10.3969/j.issn.1008-1267.2011.01.006
O643.3
A
1008-1267(2011)01-015-03
2010-10-12
王芳(1981-)女,江苏盐都县人,助教,硕士研究生。
