川西獐牙菜的化学成分研究(Ⅱ)
2011-09-29周永福黄飞燕文荣荣李干鹏
周永福,黄飞燕,文荣荣,李干鹏
(云南民族大学化学与生物技术学院民族药资源化学国家民委-教育部重点实验室,云南昆明 650500)
川西獐牙菜的化学成分研究(Ⅱ)
周永福,黄飞燕,文荣荣,李干鹏
(云南民族大学化学与生物技术学院民族药资源化学国家民委-教育部重点实验室,云南昆明 650500)
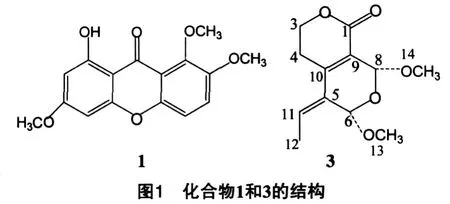
川西獐芽菜(Swertia mussotiiFranch)是藏族民间常用的单方草药,在对采自云南迪庆藏族自治州香格里拉县的川西獐牙菜的进一步研究中,采用现代分离分析技术又从该植物 70%乙醇提取物的乙酸乙酯部分分离鉴定了 8个化合物,它们是:1,2,6-三甲氧基 -8-羟基酮(1),1,3-二甲氧基 -8-羟基酮 (2),川西獐芽菜内酯 I(3)、獐芽菜苦苷 (4)、龙胆苦苷 (5)、獐芽菜苷 (6)、豆甾醇 (7)和β-谷甾醇 (8).其中,化合物 3是首次从该属植物中分到.对这些化合物进行了抗糖尿病的药理筛选,发现化合物 1对醛糖还原酶的抑制率为 18.3%(10-5mol/L).
川西獐牙菜;酮;醛糖还原酶抑制剂
川西獐芽菜 (Swertia m ussotiiFranch)俗名“藏茵陈”,为龙胆科獐牙菜属植物 (Swertia),是藏族民间常用的单方草药,具有清热解毒,利胆退黄之功能,可治疗肝炎、黄疸型肝炎、肝胆等疾病[1-2].由于云南有丰富的獐牙菜属植物资源,我们一直在开展獐牙菜属植物的化学成分研究[3].在前期的研究工作中,从采自云南迪庆藏族自治州香格里拉县的川西獐牙菜中分离鉴定了 11个单体化合物[4].在我们进一步的研究中,采用现代分离分析技术又从该植物 70%乙醇提取物的乙酸乙酯萃取部分分离鉴定了 8个化合物,它们是:1,2,6-三甲氧基 -8-羟基酮 (1),1,3-二甲氧基 -8-羟基酮 (2),川西獐芽菜内酯 I(3)、獐芽菜苦苷 (4)、龙胆苦苷 (5)、獐芽菜苷 (6)、豆甾醇 (7)和β-谷甾醇 (8).其中,化合物 3是首次从该属植物中分到.对这些化合物进行了抗糖尿病的药理筛选,发现化合物 1对醛糖还原酶的抑制率为18.3%(10-5mol/L).
1 实验部分
1.1 材料与仪器
NMR谱用 BrukerAV-400型超导核磁共振仪测定,以 CDCl3或 CD3OD作溶剂,T MS为内标;薄层色谱硅胶 GF254和柱色谱硅胶 (0.077~0.054 mm)均为青岛海洋化工厂产品;RP-18和葡聚糖凝胶 LH-20购自Merck公司.安捷伦 LC-1100液相色谱仪、二极管阵列检测器 (DAD)、制备柱 (7μm,21.2mm ×250mm)、安捷伦半制备反相柱 (5μm,9.4 mm×250 mm),所用溶剂为工业纯 (重蒸),其它试剂为化学纯或分析纯.
植物样品于 2006年 5月采自云南省香格里拉县海拔 3 500 m的山沟和山坡上,经云南省迪庆州藏医院扎西泽仁医师鉴定为川西獐牙菜(Swertia m ussotiiFranch).
1.2 提取和分离
风干的川西獐牙菜全草 9.5 kg粉碎后用 70%的乙醇浸提取,共 4次,每次 4 h,提取液滤过、合并、浓缩得棕色浸膏约 980 g,然后依次用石油醚、乙酸乙酯和正丁醇萃取 5次.乙酸乙酯萃取部分 168 g依次用 50∶1~1∶10的石油醚 -乙酸乙酯梯度洗脱,得到 4个流份 A1~A4.A2流份经硅胶柱层析和葡聚糖凝胶 LH-20柱色谱分离得到化合物 1、2、7和 8;A3流份经硅胶柱层析和高效液相色谱 RP-18柱制备得到化合物 3;A4流份经葡聚糖凝胶 LH-20柱层析和反复硅胶柱层析得到化合物 4、5和 6.
2 结果与讨论
2.1 结构鉴定
化合物 1淡黄色粉末,分子式为 C16H14O6,1HNMR(CDCl3,400MHz)δ:13.3(-OH),7.33(1H,d,J=9.2Hz,H-3),7.16(1H,d,J=9.2Hz,H-4),6.33(1H,d,J=2.0Hz,H-7),6.31(1H,d,J=2.0Hz,H-5),4.00(3H,s,1-OCH3),3.93(3H,s,2-OCH3),3.88(3H,s,6-OCH3);13C NMR(CDCl3,100MHz)δ:181.9(C=O),166.4(s,C-6),163.9(s,C-8),157.2(s,C-4b),151.0(s,C-4a),149.3(s,C-1),148.9(s,C-2),120.5(d,C-3),115.8(s,C-8b),112.8(d,C-4),104.1(s,C-8a),96.9(d,C-7),92.1(d,C-5),61.8(q,1-OCH3),57.2(q,2-OCH3),55.8(q,6-OCH3).以上数据与文献[5]对照基本一致,化合物1鉴定为 1,2,6-trimethoxy-8-hydroxyxanthone.
化合物 2淡黄色粉末,分子式为 C15H12O5,1H NMR(CDCl3,400MHz)δ:12.8(-OH),7.74(1H,dd,J=1.6,8.0Hz,H-7),7.24(1H,t,J=8.0Hz,H-6),7.17(1H,dd,J=1.6,8.0Hz,H-5),6.48(1H,d,J=2.0Hz,H-2),6.30(1H,d,J=2.0Hz,H-4),3.99(3H,s,1-OCH3),3.86(3H,s,3-OCH3);13C NMR(CDCl3,100MHz)δ:180.7(C=O),166.7(s,C-3),163.2(s,C-1),157.5(s,C-4a),148.2(s,C-8),146.2(s,C-4b),123.5(d,C-6),121.4(s,C-8a),116.6(d,C-7),115.5(d,C-5),103.8(s,C-8b),97.5(d,C-2),92.7(d,C-4),56.4(q,1-OCH3),55.8(q,3-OCH3).以上数据与文献[6]对照基本一致,化合物 2鉴定为 1,3-dimethoxy-8-hydroxyxanthone.
化合物 3无色油状物;分子式为 C12H16O5;1H NMR(400MHz,CD3Cl3)δ:1.90(3H,d,J=7.2Hz,H-12),2.56(1H,dt,J=17.2,4.0Hz,H-4a),2.65(1H,m,H-4b),3.59(3H,s,H-13),3.65(3H,s,H-14),4.38-4.46(2H,m,H=3),5.47(1H,d,J=1.6Hz,H-8),5.48(1H,d,J=0.8Hz,H-6),6.22(1H,dq,J=1.2,7.2Hz,H-11).13CNMR(100MHz,CD3Cl3)δ:163.2(s,C-1),65.0(t,C-3),22.8(t,C-4),130.7(s,C-5),95.0(d,C-6),94.1(d,C-8),119.9(s,C-9),143.8(s,C-10),133.7(d,C-11),14.3(q,C-12),55.6(q,C-13),57.3(q,C-14).以上数据与文献[7]对照一致鉴定为 (Z)-5-Ethylidene-3,4,5,6-tetrahydro-cis-6,8-dimethoxy-1H,8H-pyrano-[3,4-c]pyran-1-one.
化合物 4无色油状物,分子式为 C16H22O10;1H NMR(400MHz,CD3OD)δ:1.65(1H,d,J=14.0Hz,H-6a),1.82(1H,dt,J=4.8,14.0Hz,H-6b),2.83(1H,dd,J=1.2,8.8Hz,H-9),4.55(1H,d,J=8.0Hz,H-1′),5.62(1H,s,H-1),7.55(1H,s,H-3).13CNMR(100MHz,CD3OD)δ:99.2(d,C-1),154.9(d,C-3),108.9(s,C-4),64.4(s,C-5),33.8(t,C-6),66.0(t,C-7),133.9(d,C-8),51.9(d,C-9),121.3(t,C-10),168.1(s,C-11),100.3(d,C-1′),74.4(d,C-2′),77.8(d,C-3′),71.4(d,C-4′),78.5(d,C-5′),62.6(d,C-6′),以上数据与文献[8]对照基本一致,化合物 4鉴定为獐牙菜苦苷.
化合物 5无色油状物,分子式为 C16H20O9;1H NMR(400MHz,CD3OD)δ:18(1H,dd,J=9.2,8.0Hz,H-9),4.67(1H,d,J=8.0Hz,H-1′),5.01(1H,m,H-7a),5.10(1H,m,H-7b),5.21-5.28(2H,m,H-10),5.64(1H,m,H-6),5.68(1H,d,J=2.8Hz,H-1),5.74-5.82(1H,m,H-8),7.47(1H,d,J=1.6Hz,H-3).13CNMR(100MHz,CD3OD):δ98.6(d,C-1),150.7(d,C-3),105.0(s,C-4),127.0(s,C-5),117.2(d,C-6),70.9(t,C-7),135.0(d,C-8),46.6(d,C-9),118.6(t,C-10),166.3(s,C-11),100.2(d,C-1′),74.6(d,C-2′),78.0(d,C-3′),71.5(d,C-4′),78.5(d,C-5′),62.8(d,C-6′),以上数据与文献[8]对照基本一致,化合物 5鉴定为龙胆苦苷.
化合物 6分子式为 C16H22O9,无色油状物;1H NMR(400MHz,CD3OD)δ:1.68-1.80(2H,m,H-6),2.71(1H,dd,J=5.6,8.4Hz,H-9),4.38(1H,dd,J=1.6,11.2Hz,H-7a),4.46(1H,dd,J=2.4,11.2Hz,H-7b),4.68(1H,d,J=8.0Hz,H-1′),5.28(1H,d,J=10.4Hz,H-10a),5.33(1H,dd,J=0.8,10.4Hz,H-10b),5.53(1H,m,H-8),5.56(1H,d,J=1.2Hz,H-1),7.60(1H,d,J=1.6Hz,H-3).13CNMR(100MHz,CD3OD):δ98.0(d,C-1),154.0(d,C-3),106.1(s,C-4),28.5(d,C-5),25.9(t,C-6),69.8(t,C-7),133.4(d,C-8),43.8(d,C-9),120.9(t,C-10),168.6(s,C-11),99.7(d,C-1′),74.7(d,C-2′),77.9(d,C-3′),71.5(d,C-4′),78.4(d,C-5′),62.7(d,C-6′),以上数据与文献 [8]对照基本一致 ,化合物 4鉴定为獐牙菜苷.
化合物 7无色针状晶体,其薄层层析 Rf值及1H NMR、13C NMR数据与标准品一致,鉴定为 24R-Stigmast-5,22(E)-dien-3β -ol,即豆甾醇.
化合物 8无色针状晶体,其薄层层析 Rf值及1H NMR、13CNMR数据与标准品一致,鉴定为β-谷甾醇.
2.2 讨论
云南产獐牙菜属植物的研究工作还比较薄弱,迄今为止仅有 10余个品种见诸报道,相关的药理和化学成分研究工作都明显不足.因此,继续深入研究云南产獐牙菜属植物药、充分发掘和利用该属植物资源很有潜力.
我们对云南香格里拉县的川西獐芽菜的化学成分进行了继续研究,用乙酸乙酯萃取其乙醇提取物,通过植物化学方法分离鉴定了 8个化合物.其中化合物 3最早由国外学者从龙爪七叶科 (Potaliaceae)植物斐济金檀(Fagraea gracilipesA.Gray)中分离鉴定.我们首次从獐牙菜属植物中分离得到该化合物,国内还未见有该化合物的报道,所以将其命名为川西獐芽菜内酯 I.国内外的相关研究表明,酮具有很好的保肝、降血糖、抗氧化等作用,为了进一步阐明獐牙菜属植物的药效物质基础,对这些化合物进行了抗糖尿病的药理筛选,发现化合物 1对醛糖还原酶的抑制率为 18.3%(10-5mol/L).研究结果有助于川西獐芽菜的深入开发利用,通过比较不同獐芽菜品种之间的化学成分差异,对辨认药材品质和寻找习用药材的替代品,以及对于植物分类学研究均具有参考价值.
[1]贾敏如,李星炜.中国民族药志要[M].北京:中国医药科技出版社,2005:591-593.
[2]郭爱华.龙胆科獐牙菜属药用植物化学成分和药理作用的研究进展[J].山西中医学院学报,2005,1(6):57-59.
[3]张建胜,王雪梅,董秀华,等.川西獐牙菜化学成分研究[J].中药材,2009,32(4):511-514.
[4]文荣荣,董秀华,段沅杏,等.獐牙菜的化学成分研究[J].云南民族大学学报:自然科学版,2010,19(2):93-96.
[5]NAGEM T J,S ILVEIRA J C.Haploxanthone from haploclathra species[J].Phytochemistry,1989,28(8):2 211-2 212.
[6]YANG Xuedong,XU Lizhen,YANG Shilin.Xanthones from the stems of securidaca inappendiculata[J].Phytochemistry,2001,58(8):1 245-1 249.
[7]CAMB IE R C,LAL A R,R ICHARD C E F,et al.Chemistry of Fijian Plants.V.:Constituents of Fagraea gracilipes A.Gray[J].Chem Pharm,Bull,1990,38(7):1 857-1 861.
[8]王世盛,徐青,肖红斌,等.抱茎獐牙菜中的苷类成分 [J].中草药,2004,35(8):847-849.
(责任编辑王 琳)
Studies on Chemical Constituents in Swertia mussotii Franch
ZHOU Yong-fu,HUANG Fei-yan,WEN Rong-rong,LIGan-peng
(KeyLaboratory of EthnicMedicine Resources Chemistry,State Ethnic Affairs Commission&Ministry of Education,School of Chemistry and Biotechnology,Yunnan University ofNationalities,Kunming 650500,China)
As a continuation of our studies on chemical constituents ofSwertiaplant,from the over-ground parts ofSwertia m ussotiiFranch which is a traditional Tibetan medicine,eight compounds,1,2,6-Trimethoxy-8-hydroxyxanthone(1),1,3-Dimethoxy-8-hydroxyxanthone(2),(z)-5-Ethylidene-3,4,5,6-tetrahydrocis-6,8-dimethoxy-1H,8H-pyrano-[3,4-c]pyran-1-one(3),swertiamarin(4),gentiopicroside(5),Sweroside(6),Stigmasterol(7)andβ-sitosterol(8),were isolated.Their structures were deter mined by using conventional spectroscopic methods.Compound 3 was isolated from the genus for the first time.The effect of compound 1 on aldose reductase was 18.3%(10-5mol/L).
Swertia mussotii Franch;xanthone;aldose reductase in hibitors
R 284.1
A
1672-8513(2011)01-0014-03
10.3969/j.issn.1672-8513.2011.01.003
2010-10-15.
教育部科学技术研究重点项目(208132).
周永福 (1983-),男,硕士研究生.主要研究方向:天然药物化学.
李干鹏 (1972-),男,博士,教授.主要研究方向:天然药物化学.
