CdSe量子点的制备及其痕量汞离子的测定
2011-09-24李建华
李 英,张 勇,李建华,周 磊
(成都理工大学 材料与化学化工学院,四川 成都 610059)
(College of Materials and Chemistry& Chemical Engineering,Chengdu University of Technology,Chengdu 610059,China)
分析测试
CdSe量子点的制备及其痕量汞离子的测定
李 英,张 勇,李建华,周 磊
(成都理工大学 材料与化学化工学院,四川 成都 610059)
以巯基乙醇为稳定剂在水溶液中制备了CdSe量子点,分别考察了还原剂硼氢化钾、硒粉、氯化镉、巯基乙醇的用量和pH值等因素的影响,并以该量子点为探针,建立了荧光猝灭法测定痕量Hg2+的分析方法。结果表明,在最佳实验条件下,反应时间为25min、量子点浓度为5.0×10-5mol·L-1、pH值为7.0左右,Hg2+在1.0×10-6~8.0×10-8mol·L-1的浓度范围内对CdSe量子点有较强的猝灭作用,测定结果令人满意,且该方法具有较高的灵敏度和较宽的线性范围,体系的相对荧光强度与Hg2+浓度的线性方程:IF0/IF=1.135+0.00357ρ,线性回归系数r=0.9970。
CdSe;量子点;荧光猝灭;汞离子;痕量
(College of Materials and Chemistry& Chemical Engineering,Chengdu University of Technology,Chengdu 610059,China)
Abstract:The water-soluble CdSe quantum dots(QDs)modified with thioglycolic ethanolwe′re proposed for the determination of trace quantities ofmercury(Ⅱ)ion.Other factors affecting the usage of restore agent of boron hydrogenated potassium,selenium powder,cadmium chloride,thioglycolic ethanol,pH value and etc were determined.The determination method of fluorescence detection for trace Hg2+was established by using CdSeQDs as fluorescence probe.According to the best experiment conditions the results showed thatwhen the reaction time is 25 minutes,the CdSeQDs concentration is 5.0 ×10-5mol·L-1,the pH value is about 7.0,mercury(Ⅱ)ion concentration is 1.0×10-6~8.0×10-8mol·L-1,themethod having a strong role destruction to CdSeQDs.Themethod has high sensitivity and wide linearity range,and the determination results were satisfied.Tthe linear equation is IF0/IF=1.135+0.00357ρ,the linear regression coefficient r=0.9970.
Keywords:CdSe;quantum dots(QDs);fluorescence quenching;mercury ion;trace
量子点(Quantum Dots,QDs)是一种新型的荧光纳米粒子,是一种由II-VI族或III-V族元素组成的纳米颗粒,其直径小于其玻尔直径(一般小于10nm),以 CdS、CdSe、CdTe、ZnS 量子点的制备和应用最为典型。量子点具有发光稳定、激发光谱宽、发射光谱窄、荧光可调谐等优良的荧光特性[1],是一种很有发展潜力的荧光探针。由于半导体量子点的结构特点导致了其具有独特的量子尺寸效应和介电限域效应,并由此衍生出独特的发光特性,为半导体量子点的应用领域提供了良好的基础,更为在分析检测领域提供了广阔的应用前景[2-4]。汞在自然界中分布极广,环境中的汞主要来源于汞矿和其他金属的冶炼,氯碱工业和电器工业中的使用以及矿物燃料的燃烧。由于汞及其化合物属于剧毒物质,会导致人、畜中毒,因此,测定环境中的汞一直是人们关注和研究的热门课题。本文以巯基乙醇为修饰剂在水相中合成CdSe量子点,并以其为荧光探针,应用于痕量汞离子的分析,测定结果令人满意。
1 实验部分
1.1 仪器与试剂
98HW-1型恒温磁力搅拌器;F93型荧光分光光度计;pHS-25数显酸度计;AB104-N型电子分析天平;氮气装置;回流装置(自架)。
硼氢化钾、硒粉、巯基乙醇、CdCl2、NaOH 等,上述药品均为分析纯试剂,购于成都科龙试剂厂,二次蒸馏水。
Hg2+标准溶液,10-4mol·L-1储备液,临用前稀释。
1.2 实验方法
1.2.1 KHSe前躯体的制备 在三颈圆底烧瓶中加入60mL的二次蒸馏水,磁力搅拌下通N2除O230min,其间一直通N2除O2,然后加入0.0809g的KBH4、0.0395g的Se粉,反应由浑浊变澄清,制得澄清的KHSe前躯体溶液备用。
1.2.2 CdSe量子点的制备 在小烧杯中加入60mL的二次蒸馏水,通N2除O230min,加入CdCl20.3425g、巯基乙醇0.53mL,充分搅拌后用NaOH溶液调节溶液的pH值为9.5,制得CdCl2混合溶液并转入三颈圆底烧瓶中,然后再将上述制备的KHSe前躯体快速倒入三颈圆底烧瓶中,并快速通N2除O2,在100℃水浴中加热回流1h,制得CdSe澄清溶液(将溶液自然冷却至室温,然后关闭N2),待用。
2 结果与讨论
2.1 镉源与前躯体加入的先后顺序的影响
在制备CdSe量子点时,镉源与前躯体加入的先后顺序,对CdSe量子点的荧光强度有一定的影响,这是由于在量子点的形成过程中可分为两个阶段:瞬间分散成核(Temporally discretenucleation)和Ostwald成熟过程(Ostwald Ripening)。瞬间分散成核是通过快速注入反应物到反应容器中,使反应先驱物的浓度迅速达到成核阈值后快速、均匀成核来实现的,而后通过控制反应参数使反应溶液在现有核上慢慢生长。快速成核一定程度上降低了溶液的过饱和,使溶液浓度迅速降低到成核阈值以下,此后,反应中便不再有新核的产生。在Ostwald Ripening过程中,由于较小尺寸的颗粒具有高的表面能,会分解并重新沉积到较大的颗粒上,这时溶液中颗粒数量减少,而颗粒的平均粒径增加,Ostwald Ripening过程很好地锐化了纳米晶的尺寸分布。
简单地说,就是前躯体加入到镉源中时,HSe-与经修饰的Cd2+碰撞结合的效果优于镉源加入到前躯体中时两种离子的碰撞结合的效果,从而导致两者加入的先后顺序生成的CdSe量子点的荧光强度有所不同(如图1),因此,选择将前躯体加入到镉溶液中制备CdSe量子点溶液。
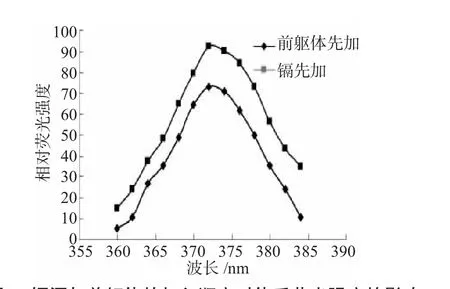
图1镉源与前躯体的加入顺序对体系荧光强度的影响Fig.1 Effectof reaction of Cadmium sourcewith the former body to order on the fluorescence of CdSe QDs
2.2 pH值的影响
由于巯基乙醇中含有巯基和羟基,其电离后将对量子点表面的缺陷部分进行修饰,改变了CdSe量子点表面上的非辐射复合中心,从而导致了量子点的荧光强度的变化。本实验分别考察了pH值为5.0、6.0、7.0、7.5、8.0、8.5、9.0、9.5、10.0、10.5、11.0、11.5、12.0 时,对制备的CdSe量子点的荧光强度的影响。实验表明,pH值在9.0~11.0范围内时,荧光强度较强且较稳定,pH值9.5时荧光强度达最大值。pH值小于9.0或者大于11.0时,体系的荧光强度有显著的下降。所以本实验选择pH值9.5时,制备CdSe量子点溶液。
2.3 还原剂用量的影响
还原剂KBH4与Se加入的多少,对制备CdSe量子点的荧光强度有一定的影响。CdCl2·2.5H2O是0.3425g、巯基乙醇为0.53mL、pH值为9.5的条件下,实验分别研究了 n(KBH4)∶n(Se)=1∶1、2∶1、3∶1、4∶1、5∶1、6∶1时,对制备的CdSe量子点的影响(见图 2a、b)。
由图2a、b上不难看出,适当过量的还原剂更有利于反应的进行,且产物的荧光强度也较大,但是过量太多的还原剂制备的CdSe量子点效果反而不好,可能是由于反应生成的K2B4O7以及过量的KBH4水解生成的KBO2阻碍了KHSe与镉离子的有效结合,从而影响了产物的荧光值。因此,在其他相同条件下本实验选择 n(KBH4)∶n(Se)等于 3∶1,即KBH4是0.0809g、Se粉是0.0395g制备CdSe量子点溶液。
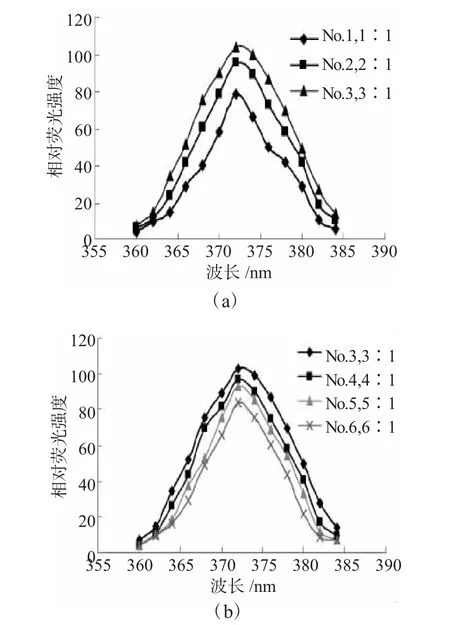
图2 还原剂的用量对CdSe量子点荧光强度的影响Fig.2 Effectof reaction of amount used of reducing agenton the fluorescence of CdSe QDs
2.4 CdCl2用量的影响
在实验中发现,Cd与Se粉的不同用量对实验结果也有显著的影响。本实验选择在KBH40.0809g、巯基乙醇为0.53mL、pH值9.5的条件下,分别考察了 n(Cd2+)∶n(Se)=2∶1、3∶1、4∶1、5∶1 时,对实验结果的影响,见图4。

图4 CdCl2用量对CdSe量子点荧光强度的影响Fig.4 Effectof reaction of amountused of Cadmium chloride on the fluorescence of CdSe QDs
由图4可见,随着镉源与硒粉的比的增加,制备的CdSe量子点的荧光强度有所增加,当n(Cd2+)∶n(Se)=3∶1时,荧光强度增加明显;随着镉硒物质的量的增加,荧光强度增加的并不显著,所以,在相同的条件下,实验选择了 n(Cd2+)∶n(Se)=3∶1,即 CdCl2·2.5H2O是0.3425g、硒粉是0.0395g时,制备所需要的CdSe量子点溶液。
2.5 巯基乙醇用量的影响
实验中发现,修饰剂巯基乙醇用量对制备CdSe有显著的影响,实验考察了巯基乙醇与Cd2+用量对生成 CdSe的影响,即 n(巯基乙醇)∶n(Cd2+)=3∶1、5∶1、7∶1、9∶1,其相对荧光强度见图5。

图5 巯基乙醇用量对CdSe量子点荧光强度的影响Fig.5 Effectof reaction of amountused of thioglycolic ethanol on the fluorescence of CdSe QDs
由图5可见,在镉溶液中加入巯基乙醇,当巯基乙醇与镉的用量比为3∶1时,虽然生成的CdSe量子点的荧光强度较好,但生成的是黄色浑浊溶液;继续增加巯基乙醇的用量,生成的CdSe量子点的荧光强度也较好,若继续增加巯基乙醇的用量,产物的荧光值明显下降,而且也浪费实验药品,所以,在其他相同的条件下本实验选择巯基乙醇与镉的用量比为5∶1,即巯基乙醇为0.53mL、CdCl2·2.5H2O是0.3425g合成所需要的CdSe。
2.6 Hg2+含量的测定
移取在最佳实验条件下制备的CdSe量子点溶液0.1mL,分别加入不同体积的Hg2+标准溶液,用二次蒸馏水稀释定容至25mL,调节pH值为7.0左右,室温下放置25min后进行荧光测定。按同样的方法作试剂空白(荧光强度记为F0),并计算出二者的相对荧光强度F0/F作图(如图6)。在线性范围内汞标液与荧光的相对强度有良好的线性关系/IF=1.135+0.00357ρ,线性回归系数 r=0.9970。
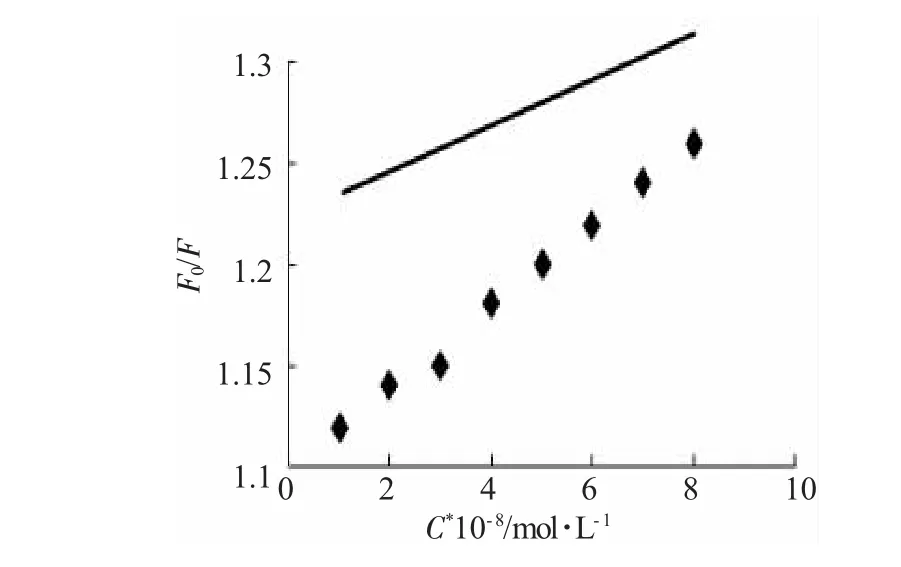
图6 标准曲线Fig.6 Standard curve
3 结论
本实验考察了在 n(KBH4)∶n(Se)∶n(CdCl2·2.5H2O)=3∶
1∶3、n(巯基乙醇)∶n(CdCl2·2.5H2O)=5∶1、pH 值 9.5 的条件下,用巯基乙醇修饰合成CdSeQDs溶液,并用此量子点作为荧光探针测定痕量的Hg2+,取得了令人满意的结果,为检测Hg2+提供了一种新方法。虽然Hg2+与巯基有较强的亲和力,但是由于巯基类化合物有毒,因此,今后应着力发展对环境温和、毒性小的修饰剂进行合成量子点,以期制备的量子点得到更广泛的应用。
[1]吴海霞,康敬万,李志锋,等.亚甲基蓝与DNA相互作用的电化学研究[J].分析测试学报,2006,25(4):1-5.
[2]张 毅.水溶性量子点碲化镉测定同型半胱氨酸的研究[J].分析测试学报,2008,27(8):844-847.
[3] Ma Ying,Yang Cheng,Li Nan,et al.A sensitive method for the detection of catecholamine based on fluorescence quenching of CdSenanocrystals[J].Talanta,2005,67(5):979-983.
[4]郑爱芳,方典军,陈金龙.功能化硒化镉量子点的制备以及作为汞离子荧光探针的研究[J].安庆师范学院学报(自然科学版),2008,14(2):39-44.
Preparation of CdSe quantum dots and determ ination of tracemercury(Ⅱ)ion
LIYing,ZHANG Yong,LIJian-hua,ZHOU Lei
O657.3
A
1002-1124(2011)03-0021-04
2010-12-06
李 英(1982-),女,汉族,安徽泗县人,硕士研究生,研究方向:环境分析化学。
张勇教授,硕士生导师。
