频发性室性期前收缩对扩张型心肌病患者炎症状态和心功能的影响
2011-09-11石少波梁锦军李鹏飞王欣欣
石少波 杨 波 梁锦军 李鹏飞 刘 凯 王欣欣
频发性室性期前收缩(frequent ventricular premature contractions,PVCs)是扩张型心肌病(dilated cardiomyopathy,DCM)主要伴发的室性心律失常之一,近年来研究发现 PVCs能引起扩张型心肌病样心力衰竭[1,2]。然而 PVCs是否加重原有的 DCM病情以及程度如何,临床资料还不多。本研究通过测定并比较两组患者的 hs-CRP水平、N端脑钠肽前体(NT-proBNP)水平、NYHA心功能分级、左心室舒张末内径和左心室射血分数,探讨 PVCs对 DCM的炎症水平和心功能影响,对 DCM伴 PVCs的诊断和治疗有一定的临床意义。
资料与方法
1.临床资料:入选病例为 2008年 11月 ~2010年 11月入住武汉大学人民医院心内科,符合中华医学会心血管病分会 2007年心肌病诊断与治疗建议诊断标准的DCM患者188例,其中合并 PVCs患者 128例(DCM+PVCs组),男性 98例,女性 30例;无 PVCs患者 60例(DCM组),男性 42例,女性 18例。所有患者按 1994年美国NYHA标准进行心功能分级。并排除高血压心脏病、冠心病、心脏瓣膜病、先天性心脏病、酒精性心肌病、心动过速性心肌病、心包疾病、系统性疾病、肺心病和神经肌肉性疾病,甲状腺疾病、使用激素或非甾体抗炎药物、糖尿病、60天内手术、癌症、慢性肾功能不全患者。
2.hs-CRP和 NT-proBNP水平测定:各组对象在入院次日清晨采血,采用日本 OLYMPUSAU 2700生化分析仪用透射免疫比浊法测定 hs-CRP浓度;使用美国罗氏公司 CobasE601免疫分析仪利用免疫电化学发光法测定 NT-proBNP浓度。
3.超声心动图检查:使用 GE公司 Vivid 7彩色多普勒超声显像仪,探头频率为 2.5MHz,测量左心室舒张末内径(left ventricular end-diastolic dimension,LVEDD)和左心室射血分数(left ventricular eject fraction,LVEF)。
4.统计学处理:采用 SPSS 17.0软件处理分析数据,计量资料用±+s差表示,两组间比较采用两独立样本t检验;计数资料用百分比表示,两组间比较采用卡方检验;等级资料也用均数 ±标准差表示,两组间用Wilcox on秩和检验;均以 P<0.05为差异有统计学意义。
结 果
1.一般资料比较:两组患者年龄、性别构成均无统计学差异(P>0.05)。DCM+PVCs组与 DCM组比较 NYHA分级 3.02±0.62级、2.68±0.66级,(P<0.05);≥Ⅲ级人数构成比分别为 104/128、34/60,差别有统计学意义(P<0.01)(表1)。
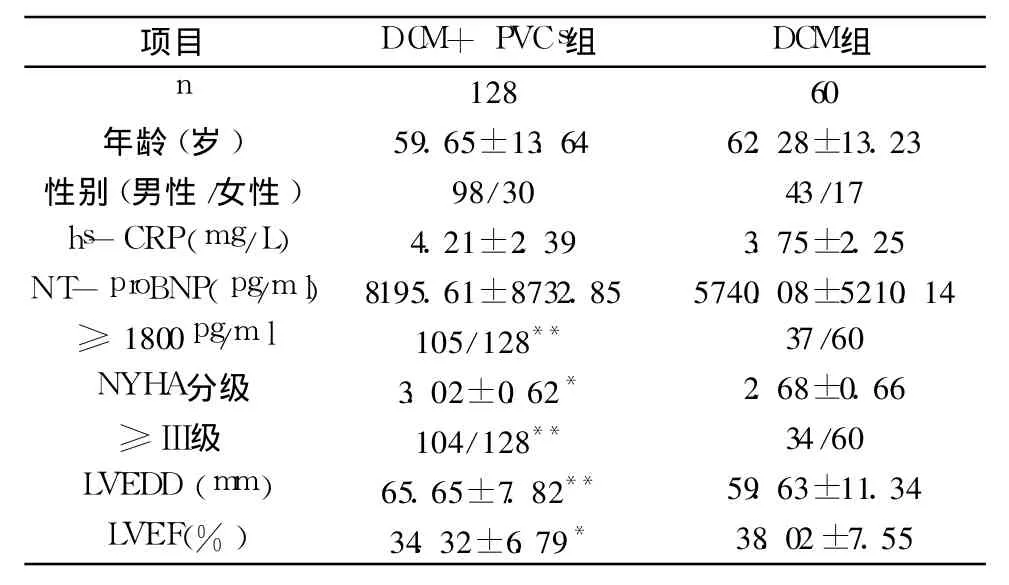
表1 两组资料的比较
2.hs-CRP和 NT-proBNP浓度的比较:hs-CRP浓度 DCM+PVCs组为 4.21±2.39mg/L,DCM组3.75±2.25mg/L,差别无统计学意义(P>0.05)。NT-proBNP浓度 DCM+PVCs组为 8195.61±8732.85pg/m l,DCM组为 5740.08±5210.14pg/ml,P>0.05;≥1800pg/m l人数构成比分别为 105/128、37/60,差异有统计学意义(P<0.01)。
3.超声心电图结果比较:DCM+PVCs组和 DCM组的 LVEDD分别为 65.65±7.82mm、59.63±11.34mm,差别有统计学意义(P<0.01);LVEF分别为 34.32%±6.79%、38.02%±7.55%,差异有统计学意义(P<0.05)。
讨 论
本研究结果显示,PVCs对 DCM患者的 hs-CRP水平无影响,但是 DCM+PVCs组患者的 NYHA分级更高,NT-proBNP≥1800pg/ml者更多,LVEDD更大,LVEF更低,表明患者的心力衰竭和左心室功能损害更严重。上述结果提示 PVCs加重 DCM患者的心功能损害,但对炎症状态无影响。
DCM主要特征是左心室或双心室心腔扩大和收缩功能障碍,伴或不伴心力衰竭,常伴有心律失常,患者常死于心力衰竭和心律失常导致的心脏性猝死,年病死率和猝死率分别是 25%~45%、30%[3]。DCM的发病机制还未完全阐明,大量研究表明 DCM与持续性病毒感染和自身免疫反应有关,研究证实炎症参与到了疾病进程中。hs-CRP是炎症状态中非常敏感的非特异指标,一些研究发现 DCM患者的 hs-CRP水平升高,认为炎症因子参与了心肌细胞肥大、纤维化、钙化,在 DCM发病和维持中起着重要作用[4]。许多研究发现炎症在许多心律失常发生、发展中也起了重要作用,例如心房颤动、室速等[5]。本研究中两组患者的 hs-CRP水平无差别,可能是参与这两种疾病的炎症都是非特异性炎症的原因。
PVCs是 DCM伴发的主要室性心律失常之一,DCM患者心脏扩大,纤维化等改变共同构成了 PVCs的电生理基础,PVCs常起源于右室流出道,也可起源于左心室流出道、心尖部、基底部、侧壁、Valsalva窦,DCM患者伴发 PVCs的临床表现多样,如心悸、气短、晕厥等,PVCs也是 DCM患者心脏性猝死的危险因子[6]。近年来多项临床研究发现 PVCs导致的扩心病样心力衰竭,主要表现在 LVEDD、LVEF等左心室功能损害上,然而经射频消融成功治疗 PVCs后心功能完全恢复正常[1,7,8],这种由 PVCs诱发的心肌病应为心动过速性心肌病(tachycardiomyopathy,TCM),已于 2009年 4月被欧洲和美国心律学会正式列为室性心动过速(ventricular tachycardia,VT)导管射频消融(RFCA)的适应证,逐渐引起了临床的关注。但是其确切机制还未阐明,可能与心肌能量储备耗竭,心内膜下至心外膜下血流比异常,冠状动脉血流减少致心肌缺血,心肌细胞钙电流异常,细胞外基质重构,自由基氧化应激损伤等,进而引起心功能不全。另外,Wijnmaalen等在非 DCM患者中研究得出了相似的结果:PVCs组患者心室张力和功能降低,射频消融成功治疗 PVCs后心室功能恢复正常[9]。这两方面的研究进展均证实 PVCs损伤患者心功能。通常人们认为 PVCs是温和、良性的,普遍认为 PVCs只是致命性室性心律失常的一个危险信号,即使是在器质性心脏病中也未受到足够的重视,然而越来越多的研究证实PVCs对心功能的损害是缓慢的、长期的,有时甚至是不可逆的[8]。在治疗方面,虽然 PVCs的药物治疗仍是主要方式,但是介入治疗如 RFCA、ICD等已经取得了长足的进展,使得药物治疗不佳的 PVCs有了新的选择与希望[10,11]。无论患者有无器质性心脏病,RFCA治疗 PVCs的成功率都可达 90%左右,治疗后均显示心功能得到进一步改善[9,12]。结合本研究,可以认为 DCM一出现 PVCs,PVCs就参与到疾病的进程当中,不仅仅只是引发室速、室颤等心律失常方面的后果,可能会更早更广泛地影响患者心功能;药物或介入治疗 DCM患者的 PVCs不仅仅能体现在预防心脏性猝死上,可能更早更有效地体现在改善患者的心功能,提高患者生活质量上。
有时 PVCs与 DCM的因果关系很难分清,虽然临床上一定的认识,例如通过患者的年龄、病史、家族史等进行辨别,但还需要进一步对临床资料进行总结和归纳。同时临床介入治疗 PVCs的样本都偏小,其治疗效果还需要更多的循证支持。
1 Blaauw Y.Reversal of ventricular premature beat induced cardiomyopathy by radiofrequency catheter ablation.Neth Heart J,2010,18(10):493-498
2 黄从新.室性早搏诱发的心动过速性心肌病.中国心脏起搏与心电生理杂志,2010,24(3):189-190
3 Zipes D P.ACC/AHA/ESC 2006 guidelines for management of patients with ventricular arrhythm iasand the prevention of sudden cardiac death--executive summary:A report of the American College of Cardiology/American Heart Association Task Force and the European Society of Cardiology Committee for Practice Guidelines(Writing Comm ittee to Develop Guidelines for Management of Patients with Ventricular Arrhythm ias and the Prevention ofSudden Cardiac Death)Developed in collaboration with the European Heart Rhythm Association and the Heart Rhythm Society.Eur Heart J,2006,27(17):2099-2140
4 Tatenkulova SN.Immunemechanisms of inflammation in dilated cardiomyopathy.Kardiologiia,2009.49(2):4-8
5 Aviles R J,Martin DO,Apperson-Hansen C,etal.Inflammation asa risk factor for atrial fibrillation[J].Circulation,2003,108(24):3006-3010
6 Adabag A S.Sudden cardiac death:epidemiology and risk factors.Nat Rev Cardiol,2010,7(4):216-225
7 Chugh SS.First evidence of premature ventricular complex-induced cardiomyopathy:a potentially reversible cause of heart failure.JCardiovasc Electrophysiol,2000,11(3):328-329
8 Baman T S.Relationship between burden of premature ventricular complexes and left ventricular function.Heart Rhythm,2010,7(7):865-869
9 Wijnmaalen A P.Beneficial effects of catheter ablation on left ventricular and right ventricular function in patients with frequent premature ventricular contractions and preserved ejection fraction.Heart,2010.96(16):1275-1280
10 Liang JJ.Sameablationmay be used for frequentprema tureventricular contractions and supraven tricular tachycardia.Medical Hypotheses,2009,73:818-820
11 梁锦军.射频消融治疗室性早搏触发特发性室性心动过速/心室颤动的病例分析.中华心律失常学杂志,2010,14(2):131-134
12 梁锦军.射频消融治疗高血压人群中室性早搏的中长期随访.武汉大学学报(医学版),2007,28(6):762-765
