含黄绿荧光蛋白基因的穿梭质粒表达载体的构建*
2011-09-03于德水沙长青张淑梅高继国
于德水, 高 娃**, 沙长青, 张淑梅, 高继国
(1.东北农业大学生命学院,黑龙江哈尔滨150030;2.黑龙江省科学院高技术研究院,黑龙江哈尔滨150090;3.黑龙江省科学院微生物研究所,黑龙江哈尔滨150010)
随着分子生物学技术的发展,分子标记技术日益成熟并用于根围生态学研究。现有的报告基因主要有:β- 半乳糖苷酶(Lacz)、β- 葡糖苷酸酶(GUS)、分泌型胎盘磷酸酯酶(SEAP)、萤火虫荧光素酶(LUC)等,但这些基因的检测都需要底物和辅助因子,因而在活体中的应用受到限制。绿色荧光蛋白(green fluorescent protein,GFP)是近年新兴的一种报告分子,该蛋白能够自身催化形成发色结构并在紫外线或蓝光激发下发出绿色荧光。作为报告基因,GFP是目前能在活细胞中表达的发光蛋白之一。作为荧光标记分子,GFP具有荧光强度高、不需要底物(或辅助因子)、无种属特异性、相对分子量小、易与其他蛋白融合、对细胞无伤害、易于检测、可在活细胞实时观察等特点,而优于传统的报告分子。GFP分子量相对较小,仅有27KD左右,它能与多种不同的蛋白质N端或C端融合而保持其天然蛋白的特性,是一种直观性很强的遗传标记物[1~3]。EYFP是GFP的突变体,是加强型GFP,具有检测方便、荧光稳定、易于构建载体且对活细胞无毒害,对目的基因的功能也没有影响,转化后细胞可以继续传代等特点。目前成为重要的报告因子在动物、植物和微生物学中广泛应用[4,5]。
本文采用基因重组技术将黄绿荧光蛋白基因重组到穿梭质粒表达载体上,构建了含黄绿荧光蛋白基因的大肠杆菌-枯草芽孢杆菌穿梭质粒表达载体,为生防枯草芽孢杆菌基因标记以及菌株定殖的研究提供必备的实验材料。
1 材料与方法
1.1 材料
1.1.1 菌株与质粒
本研究所用菌株与质粒见表1。

表1 菌株与质粒Table1 Strains and plasmid
1.1.2 培养基与培养条件
大肠杆菌用LB培养基(蛋白胨10g,氯化钠10g,酵母抽提物 5g,水 1000mL,pH7.0,121℃灭菌20min。),37℃培养震荡培养18h。
1.1.3 试剂
限制性内切酶,T4DNA连接酶,DNA回收试剂盒,化学试剂:自大连宝生物工程公司。
1.1.4 抗生素与溶液
氨苄青霉素(Amp),工作浓度 50μg/mL;氯霉素(Cm),工作浓度 10μg/mL。
溶液Ⅰ:50mmol/L葡萄糖,25mmol/LTris.HCl(pH8.0),10mmol/LEDTA(pH8.0);
溶液Ⅱ:0.2mmol/LNaOH,1%SDS;
溶液Ⅲ:5mmol/L乙酸钾60mL,冰乙酸11.5mL,双蒸水28.5mL;
TE:10mmol/L Tris.HCl (pH8.0),1mmol/L EDTA(pH8.0);
RNase溶液:10mg RNase溶于1mL 10mmol/LTris.HCl(pH7.5),15mmol/L NaCl中,于100℃加热15min,冷却后保存于-20℃。
1.1.5 仪器
台式高速离心机LG15-W,北京医用离心机厂;电热恒温水浴锅HWS24,上海一恒科技有限公司;电热恒温培养箱WMK-02,南京电器厂;紫外分光光度计LINDA,日本岛津公司;电子分析天平AEL-160,日本岛津公司;凝胶成像系统UVP,英国Cambridge紫外仪器有限公司。
1.2 方法
1.2.1 质粒提取
采用碱裂解法[6]从大肠杆菌中提取pEYFP和pHPS9质粒DNA。
活化含pEYFP和pHPS9质粒DNA的大肠杆菌,用-70℃保存的菌液划线接种于LB加相应抗生素固体平板上,37℃过夜培养;取单菌落转接于5mL LB+Cm(pHPS9)和 5mL LB+Amp(pEYFP)液体培养基中,37℃过夜培养;按1%接种量再分别转接于50mL LB加相应抗生素的液体培养基中,37℃过夜培养。次日取50mL菌液,在4℃,4000r/min转数下,离心10min,弃去上清液,用2mL含10mg Lysozyme的溶液Ⅰ溶解菌体,室温放置5min,加入4mL溶液Ⅱ,温和倒置数次使其混合均匀,置于冰上10min,再加入3mL溶液Ⅲ,快速倒置数次于冰上10min,以13000r/min转数离心30min,向上清液中加入0.6倍体积异丙醇,室温放置15min,在12000r/min转速数下离心30min,加入0.5mLTE溶解沉淀,再加入RNA酶10μL,放入37℃水浴中反应1h,加入等体积酚、酚-氯仿、氯仿抽提,用100%乙醇沉淀质粒DNA,用70%冰冷的乙醇洗1次,沉淀干燥后,溶于50μL TE中,置于-20℃冰柜中备用。
1.2.2 双酶切反应[7]
先用BamHI酶切 pEYFP和pHPS9质粒DNA,10μL反应体积中含1~2μg pEYFP或pHPS9质粒DNA,1μL 10×Bbuffer,1~2UBamHI,加入 ddH2O 补足体积。将反应管放于30℃水浴中2h后,置于70℃水浴10min,终止酶反应。再用EcoRI酶切,在上述反应液中加入 1~2U EcoRI,1μL 10×H buffer,加入ddH2O补足体积至20μL,将反应管放于37℃水浴中2h后,置于70℃水浴10min,终止酶反应。用酚-氯仿抽提酶切后的pHPS9质粒DNA,乙醇沉淀,用ddH2O溶解沉淀。酶切后的pEYFP进行1%琼脂糖电泳,回收约714bp的EYFPDNA片段。DNA片段回收采用试剂盒。
1.2.3 连接反应
10 μL反应体积中含有1μL 10倍连接缓冲液,2UT4DNA连接酶,适当浓度比的EYFPDNA片段与pHPS9质粒DNA,置于22℃水浴中连接4~6h,终止连接反应。
1.2.4 感受态细胞制作与转化
从平板上挑取E.coli.DH5α单菌落接种于5mLLB培养液中,37℃过夜培养,次日按1%接种量转接于50mLLB培养液中,在37℃水浴摇床中快速震荡培养至OD550=0.5。将培养液置于冰浴中10min之后,在4℃,5000r/min转速下离心5min,收集菌体,将菌体重新悬浮于25mL冰冷的50mmol/L CaCl2,10mmol/L Tris.HCl溶液中,冰浴中至少放置20min,在4℃,5000r/min转速下离心5min,将菌体再悬浮于2mL冰冷的50mmol/LCaCl2,10%甘油中,分成100μL体积一份,于4℃放置过夜后,立即放入-70℃冰箱中保存备用。
取100μL冷冻的感受态细胞放入冰浴中融化,加入 20μL 50mmol/LCaCl2,10mmol/L Tris.HCl溶液,再加入40~50ngDNA,混匀后,于冰浴中放置30min,立即放入42℃水浴中热刺激2min,取出后加入100 μLLB培养液于37℃水浴中放置1h。取100μL培养液涂布于加有IPTG和X-Gal的LB平板上,然后将LB平板放置于37℃温箱中过夜培养。
1.2.5 阳性重组子筛选与鉴定
随机挑选单菌落,用煮沸法快提质粒DNA,先用1%琼脂糖凝胶电泳初筛DNA分子量大于质粒载体(pHPS9)的重组子DNA,再用EcoRⅠ/BamHⅠ双酶切方法进一步验证重组子。
2 结果与讨论
2.1 质粒DNA浓度与纯度
用LB培养液过夜培养,取50mL菌液离心收集菌体,按方法所述提取质粒DNA,用紫外吸收法测定DNA纯度,琼脂糖电泳法测定DNA分子量大小。50mL菌液可以获得30μg pEYFPDNA和26μg pHPS9 DNA,经测定,其 OD260∶OD280=1.76,琼脂糖凝胶电泳表明DNA分子量与理论值相符。结果见图2。
2.2 表达载体的构建
按照图1构建表达载体。将EYFP基因连接到穿梭质粒表达载体pHPS9多克隆位点区。
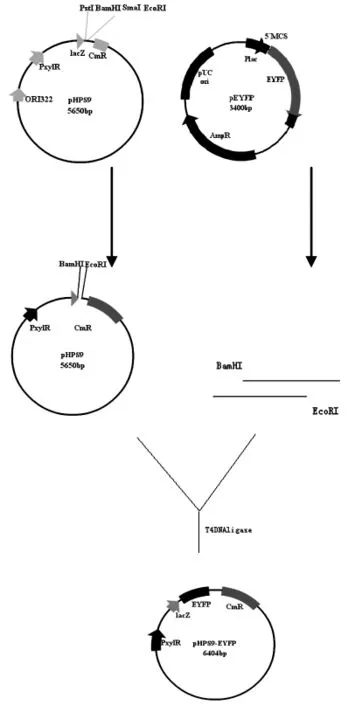
图1 表达载体的构建图Fig.1 Construction figure of expressing carrier
2.3 阳性重组子筛选与鉴定
10 μL连接液转化100μL感受态细胞,涂2个LB+Cm平板,37℃培养18h。每个平板上均有200多个转化子,随机挑取10个转化子,提取质粒DNA,并用EcoRⅠ/BamHⅠ双酶切下与EYFP基因大小一致的DNA片段,证明该转化子为阳性重组子。结果见图2、3、4。
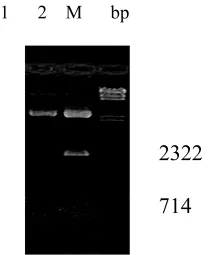
图2 质粒pEYFP DNA电泳图Fig.2 Electrophoresis map of plasmid pEYFPDNA EcoRⅠ/BamHⅠ双酶切电泳图

图3 质粒pHPS9-EYFP DNA电泳图Fig.3 Electrophoresis map of plasmid pHPS9-EYFPDNA

图4 阳性重组子双酶切结果Fig.4 Result of dual enzyme cut of positive recombinator M:λDNA/HindⅢMarker
3 结 论
利用DNA重组技术,成功地将黄绿荧光蛋白基因(EYFP)重组到大肠杆菌-枯草芽孢杆菌穿梭质粒表达载体pHPS9上,获得了含EYFP基因的大肠杆菌-枯草芽孢杆菌穿梭质粒表达载体pHPS9-EYFP,从而为生防菌株的基因标记提供了必要的材料。
[1]姚震声,陈中义,陈志谊.绿色荧光蛋白基因标记野生型生防枯草芽孢杆菌的研究[J].生物工程学报,2003,19(5):551~555.
[2]殷幼平,袁训娥,李强.生防菌枯草芽孢杆菌CQBS03的绿色荧光蛋白基因标记及其在柑橘叶片上的定殖[J].中国农业科学,2010,43(17):3555~3563.
[3]车建美,刘波,张彦.青枯病生防菌蜡状芽孢杆菌(ANTI-8098A)的绿色荧光蛋白基因(gfp)转导及其生物学特性的变化[J].农业生物技术学报,2010,18(2):337~345.
[4]王金林,闵军,周晓东.加强型黄绿色荧光蛋白和VEGF双基因载体在肝细胞共转染表达[J].中山医科大学学报,2002,23(4):254~256.
[5]张淑梅,王玉霞,李晶.基因标记枯草芽孢杆菌BS-68A在黄瓜上定殖[J].生物技术,2006,16(4):73~74.
[6]都艳霞,沙伟,张梅娟.碱裂解法提取重组质粒DNA及PCR验证[J].生物技术,2009,19(2)35~37.
[7]柴燕文,马晖玲,谢小冬.pBI121-Lyz-GFP表达载体的构建及其在和田苜蓿愈伤组织中的转化[J].农业生物技术学报,2008,16(5):842~846.
