185nm紫外光/氧化协同降解水体中微量苯的研究
2011-09-03朱承驻
陆 军, 朱承驻
(1.合肥工业大学 分析测试中心,安徽 合肥 230009;2合肥工业大学 资源与环境工程学院,安徽 合肥 230009)
0 引 言
随着现代工农业的迅猛发展,大量有机化学品的生产和使用与日剧增,从而引起大量有害、有毒物质进入水体,致使饮用水水源受到严重的污染和破坏。据报道,在我国近50%的重点城镇水源水质不符合饮用水水源的水质标准,在这些水体中均被检测出多种有机污染物,其中有些污染物具有“三致”危害的物质[1],因而严重地威胁着人类的生存和发展。
对于水源水质的变化,常规饮用水处理工艺已显得力不从心。近年来的研究发现,生物法处理存在降解极限,不可能处理到Ames致突变试验呈阴性的浓度以下(COD<7.5 mg/L),因而水处理新技术尤其是水体深度净化技术的开发研究已经成为环境科学研究领域的一个热点。光化学方法由于其在处理水污染方面的独特优势而成为处理水污染的重要方法之一[2]。
本文以环境中的常见污染物苯[3-4]为研究对象,系统地研究了通过185 nm紫外光与氧化剂联用技术协同降解水体中微量苯的最佳工艺条件和降解机理,以期寻求一种高效、可行、价廉的微污染水体的处理方法。
1 试验部分
1.1 试剂
苯(上海菲达工贸有限公司和桥分公司,分析纯),使用前按文献[5]步骤进行纯化处理后保存待用;K2S2O8(中国医药集团上海化学试剂公司,分析纯);30%H2O2(上海桃浦化工厂,分析纯);H2SO4、NaOH(分析纯)。
1.2 方法与装置
所用的紫外灯管外径为16 mm,功率为5 W,其发出的紫外光中185 nm占10%以上、254 nm占90%左右;聚四氟乙烯套管内外径分别为20 mm和25 mm;PHS-3C型酸度计(上海雷磁仪器厂);Finnigan MAT ITD800GC/MS/DS色质联用仪(美国Finnigan MAT ITD公司)。
实验采用纳秒级瞬态吸收光谱装置[6-7],采用266 nm激光,其能量为每脉冲7~10 mJ,动力学的模拟和分析采用英国Applied Photophysics公司的Pro-Kinetics软件。
1.3 实验方法
将一定量苯的水溶液从高位槽经进水口放入反应器中密封,光照一定时间后,测定溶液的CODCr。
CODCr的去除率为:

其中 ,ρ0和 ρt分别为光解前、后苯的 CODCr值。
废水中CODCr采用重铬酸钾光度法测定,产物采用GC/MS/DS色质联用仪进行分析。
2 结果与讨论
2.1 苯的紫外吸收光谱
3.3 ×10-3mol/L苯水溶液的紫外吸收光谱如图1所示。
由图 1可以看出,苯在 220 nm和 250~270 nm附近有2个吸收带,根据光化学反应定律,只有被分子吸收的光才能有效地引起分子的化学变化,若要使苯解离可用240~270 nm或短于215 nm的紫外光光解。
事实上,几乎所有的有机分子都能吸收小于210 nm的紫外光,这种光子的能量大于6.2 eV。而一般有机化合物的C—C键的能量为5.5 eV,C—H键的能量为4.4 eV,因此,几乎所有的有机分子吸收小于210 nm的紫外光子后均可以被分解(除C—F键外)。
但目前在实际工业中运用的小于210 nm的光源只有185 nm的紫外灯,它是由低压汞灯产生的185 nm和253.7 nm的混合光。国产低压汞灯含185 nm的紫外光占253.7 nm的4%~7%,而本实验所用的低压汞灯发射的紫外光185 nm可占253.7 nm的10%~14%。

图1 苯的紫外吸收光谱
从图1可看出,苯的另一个吸收峰在250 nm左右,253.7 nm光子的能量大约为 5.0 eV,按Proper定律,只有当激发态分子的能量足够使分子内最弱的化学键断裂时才能引起化学反应。从理论上250 nm的光子足以使有机分子中C—H(4.4 eV)断裂。因此,本文采用266 nm激光对苯溶液进行闪光光解,如图2所示。
从图2可见,苯在270~300 nm附近存在荧光而未见其他的瞬态物种。由此可见,尽管理论上苯吸收266 nm光子后已使苯解离,但由于苯环上C=C键能为8.4 eV,苯的振动核很多且参与共振结构的稳定性接近,共振能较大(150.5 kJ/mol),能量很快被分散开,因此只吸收光而不发生分解。

图2 氮气脱氧条件下苯水溶液的瞬态吸收谱
2.2 苯光解处理工艺条件的研究
2.2.1 苯的质量浓度对其光解效果的影响
在光照时间一定(1 min)、pH值为6的条件下,苯水溶液CODCr去除率均随着质量浓度的增加而成指数下降,如图3所示。这表明在光子能量一定的条件下,苯被降解的量也一定,由此可见,处理高质量浓度且难降解的有机废水(如用光量子技术)需要消耗大量的电能。
由于185 nm光子的能量为6.7 eV,水的HO—H键能为5.17 eV,因此,H2O吸收185 nm光子后会产生◦H和HO◦自由基[8]。因为单位体积水溶液中H2O分子数远大于有机分子数,因此185 nm光照有机废水其本质上是◦H和HO◦自由基与有机污染物分子的作用。只有极少数污染物分子吸收185 nm光子后分解。

图3 苯的 CODCr去除率与其质量浓度的关系
因为苯环上的碳碳键的键能为8.4 eV,碳氢键的键能为4.4 eV,因此在185 nm紫外光(6.70 eV)照射下,可以从苯环夺走 ◦H 自由基[9-10],化学方程式为:

2.2.2 苯溶液初始pH值对其光解效果的影响
改变水样的初始pH值,5 mg/L的苯溶液光解1 min后,结果如图4所示,从图 4可看出,CODCr去除率随pH值的增高而下降,这是由于在碱性条件下OH-是◦OH的淬灭剂[11-12],故苯的CODCr去除率较差,这也表明在此种光子条件下,光子照射水产生的◦OH和◦H是苯降解的主要途径。

图4 苯的CODCr去除率与初始pH值的关系
2.2.3 处理时间对苯溶液光解效果的影响
在近中性的条件下,5 mg/L的苯水溶液的光解情况与时间的关系如图5所示。从图5可以看出,CODCr去除率与时间呈指数上升的关系;光解5 min后,CODCr去除率可达90%左右。

图5 苯的CODCr去除率与处理时间关系
2.3 氧化剂对苯光解效果的影响
2.3.1 氧化剂加入量对苯光解效果的影响
研究结果表明,采用单纯的光解手段,降解效果主要由 H2O吸收185 nm光子后会产生◦H和HO◦自由基引起的,但约占90%的254 nm的紫外光未充分利用,因此,实验中尝试在被处理的苯水溶液中加入少量的Na2S2O8和H2O22种常用的化学氧化剂,利用它们在光解作用下产生的强氧化性粒子氧化降解水体中的有机污染物,以实现在较温和的条件下能达到较好的降解效果。在光照1 min、pH值约为6的条件下,加入氧化剂的量与含5 mg/L的苯水溶液的CODCr去除率的关系如图6所示。
由图6可知,苯的CODCr去除率与加入氧化剂的量成指数递增,但加入K2S2O8时的效果要明显高于加H2O2和单纯的光降解效果,这是由于S2O2-8在254 nm光照下分解成[13]SO4-◦,H2O2在光照下分解成◦OH自由基[14-15],◦OH自由基和 C6H6作用生成 C6H6—OH,然后C6H6—OH加合物解离成苯酚或在有氧条件下被氧化为C6H6—OHO2后再进一步分解[16-17],而SO4-◦则可与C6H6直接作用使其开环[18]。由于加入Na2S2O8的降解效果要比加入H2O2的效果好,所以,本文将对加入Na2S2O8的情况做进一步的研究。

图6 苯的CODCr去除率与氧化剂质量浓度关系
2.3.2 pH值对K2S2O8光解苯效果的影响
在光照1 min的条件下,改变加入5 mg/L K2S2O8的含5 mg/L的苯水溶液初始pH值,得到CODCr去除率与K2S2O8的pH值的关系如图7所示。
由图7可以看出,加入K2S2O8后在近中性条件下,苯的CODCr去除率高于酸、碱性条件,这是由于在酸性条件下,S2O82-可发生如下化学反应[19]:
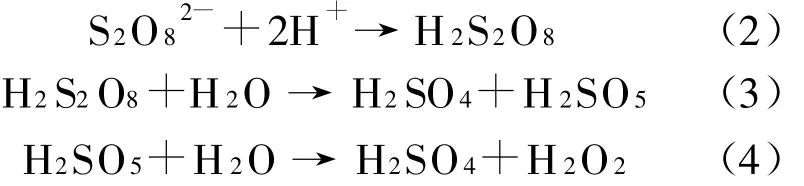

图7 苯的CODCr去除率与氧化剂的pH值关系
加入H2O2时的降解效果比加入K2S2O8的降解效果差,故加入K2S2O8后在中、碱性条件下,苯的 CODCr去除率高于酸性条件。又因为SO4-◦+OH-=OH◦+SO42-[20],而OH-是◦OH的强猝灭剂,所以在强碱性条件下的降解效果也不如近中性条件。
2.3.3 处理时间对K2S2O8光解苯效果的影响
加入5 mg/L K2S2O8的5 mg/L的苯水溶液,其CODCr去除率与处理时间的关系如图8所示,从图8可以看出,CODCr去除率与时间呈表观一级反应,当处理3 min时,苯的CODCr去除率可达到95%以上。

图8 苯的CODCr去除率与氧化剂处理时间关系
2.4 光解产物的定性分析
将5 mg/L的苯水溶液和含5 mg/L K2S2O8的5 mg/L的苯水溶液分别光解2 min,用二氯乙烷萃取后进行GC/MS分析,其苯水溶液的光解产物为苯酚、3-己烯醇、2-羟基2-甲基丙酸乙酯,而加入K2S2O8后的光解产物为苯酚、3-己烯醇、2-羟基2-甲基丙酸乙酯和2-己醇。
从产物分析结果可知,光解2 min后苯被降解成苯酚或被开环而生成醇等物质,这说明此种光解技术能有效降解水体中微量的苯。
3 结 论
本文通过实验研究了特种光量子技术处理水体中微量苯的可行性,确定了适宜的光解时间、溶液pH值以及加入氧化剂的影响等工艺条件,并对光解产物进行了定性分析。
(1)特种光量子技术能有效降解水体中微量苯,CODCr去除率在酸性条件时优于碱性条件,CODCr去除率与时间呈指数上升关系;光解5 min后,CODCr去除率可达90%左右。
(2)氧化剂的加入对水体中微量苯的作用明显,苯的CODCr去除率与加入氧化剂的量成指数递增,但加入K2S2O8时的降解效果明显高于加H2O2时的效果。处理3 min时加入K2S2O8的苯溶液的CODCr的去除率可达到95%以上。
[1]李圭白.高锰酸钾复合药剂强化过滤微污染水质的效能研究[J].环境科学学报,2002,22(5):664-670.
[2]朱承驻,张仁熙,舒小红,等.特种光量子技术降解水体中微量 4-氯酚[J].合肥工业大学学报:自然科学版,2007,30(1):73-76.
[3]寿卫国,滕小敏,薛振宇.苯的职业接触评估[J].职业卫生与应急救援,2006,24(2):80-82.
[4]唐森本,王欢畅,葛碧洲,等.环境有机污染化学[M].北京:冶金工业出版社,1996:12-20.
[5]谷珉珉,贾韵仪,姚子鹏.有机化学实验[M].上海:复旦大学出版社,1991:382.
[6]Zhu C Z,Ouyang B,Wang J Q,et al.Photochemistry in the mix ed aqueous solution of nitrobenzene and nitrous acid as initiated by the 355 nm UV light[J].Chemosphere,2007,67(5):855-861.
[7]董文博,朱承驻,房豪杰,等.乙腈溶液中 NO3自由基与联苯的反应机理[J].化学学报,2005,63(23):2147-2152.
[8]Ashton L,Buxtion G V,Stuart C R.T emperature dependence of the rate of reaction of OH with some aromatic compounds in aqueous solution[J].J Chem Soc Faraday T rans,1995,91(11):1631-1633.
[9]Kochany J,Bolton J R.Mechanism of photodegradation of aqueous organic pollutants,2:measurement of the primary rate constants for reaction of hydroxy l radicals with benzene and some halobenzenes using an EPR spin-trapping method following the photolysis of hydrogen peroxide[J].Environ Sci Technol,1992,26(2):262-265.
[10]Go rdon S,Schmidt K H,Hart E J.A pulse radioly sis study of aqueous benzene solutions[J].J Phys Chem,1977,81(2):104-109.
[11]朱世盛.仪器分析 [M].上海:复旦大学出版社,1983:61-169.
[12]Christensen H,Sehested K,Corfitzen H.Reactions of hydroxyl radicals with hydrogen peroxide at ambient and elevated temperatures[J].J Phys Chem,1982,86(9):1588-1590.
[13]M celroy W J,Waygood S J.Kinetics of the reactions of the SO4-radical with SO4-,S2O82-,H2O and Fe2+[J].J Chem Soc Faraday T rans,1990,86(14):2557-2564.
[14]Yu X Y,Barker J R.Hydrogen peroxide photolysis in acidic aqueous solutions containing chloride Ions,Ⅱ :quantum yield of◦HO(Aq)radicals[J].J Phy s Chem A,2003,107(9):1325-1332.
[15]朱承驻,张仁熙,郑光明,等.瞬态吸收光谱研究 H2O2与C6H6水溶液的反应机理[J].物理化学学报,2004,20(9):1112-1117.
[16]朱承驻,欧阳彬,房豪杰,等.利用瞬态吸收光谱技术研究水体中苯与亚硝酸的交叉反应机理[J].化学学报,2004,62(12):1115-1122.
[17]Jacob N,Balakrishnan I,Reddy M P.Characterization of the hydroxyl radical in some photochemical reactions[J].J Phys Chem,1977,81(1):17-22.
[18]M erga G,Rao B S M,M ohan H,et al.Reactions of OH and SO4-with some halobenzenes and halotoluenes:a radiation chemical study[J].J Phys Chem,1994,98(37):9158-9164.
[19]孟庆珍,胡鼎文,程泉寿,等.无机化学:下册[M].北京:北京师范大学出版社,1986:889-891.
[20]Furman O S,Teel A L,Watts R J.Mechanism of base activation of persulfate[J].Environ Sci Technol,2010,44(16):6423-6428.
