辣根过氧化物酶催化合成水溶性导电聚苯胺的研究
2011-07-25白利杰陈建波
白利杰,陈建波
(上海师范大学生命与环境科学学院,上海 200234)
自1977年首次发现掺杂碘的聚乙炔具有金属特性以来,导电聚合物受到了广泛关注。其中聚苯胺(PANI)由于结构多样、掺杂机制独特、稳定性高、应用前景广阔更是备受瞩目[1]。传统的聚苯胺合成方法有化学合成法和电化学合成法,但均存在因过氧化导致副产物较多的缺点。此外,聚苯胺在普通的有机溶剂和溶液中的溶解性很低,也限制了它在工业中的应用,因此人们致力于寻求更好的催化方式[1,2]。酶因为具有较高的催化效率及对底物高度的专一性,且其催化的聚合过程温和、环保,产物容易分离,副产物很少,因而酶催化在高聚物合成领域越来越受到人们的关注。目前已经应用于导电聚苯胺合成研究的生物酶包括辣根过氧化物酶(HRP)、漆酶、棕榈树过氧化物酶等[3~5]。
辣根过氧化物酶(HRP)是一种以铁卟啉为辅基的血红素蛋白,在H2O2存在时能催化苯酚、苯胺及其取代物聚合,由于稳定性较好、价廉,已被广泛应用于聚合物的合成。但是在一般条件下HRP酶催化苯胺聚合过程中会得到低分子量的寡聚体,这些由于快速聚合形成的非导电性的寡聚体因不溶于水而很快沉淀出来。这一问题可以通过引入聚阴离子模板来解决。聚阴离子模板能够促进苯胺单体的头尾连接,从而使高分子量的苯胺聚合物能够在水溶液中存在。文献报道可作为酶催化苯胺聚合模板的有聚苯乙烯磺酸钠(SPS)、聚乙烯磷酸盐(PVP)、磺化木质素(LGS)及 DNA(RNA)等[3,6~8]。
在酶催化制备导电聚苯胺过程中,酶不可避免地会受到体系中各种条件的影响,酶催化活性的变化最终影响导电聚苯胺的合成。目前,文献报道多侧重导电聚苯胺的合成,而对生物酶的变化研究较少,因此,对生物酶在催化导电聚苯胺合成过程中性质的变化并不十分清楚。为拓展酶催化导电聚苯胺的研究,作者以十二烷基硫酸钠(SDS)为模板,研究了在SDS胶束溶液中HRP催化聚合导电聚苯胺的影响因素,并对合成过程中HRP性质的变化进行了探索。
1 实验
1.1 试剂
辣根过氧化物酶,上海Kayon生物试剂公司;苯胺,分析纯,上海凌峰化学试剂有限公司;十二烷基硫酸钠,纯度≥99%,Sigma;其余试剂均为国产分析纯。
1.2 聚合反应
用pH值为1.0~4.0的缓冲溶液配制一定浓度的SDS溶液,加入10 mmol·L-1的苯胺单体和0.1 mL 10 mg·mL-1HRP溶液,将稀释的H2O2溶液逐滴加入(控制滴加时间为1 h)到反应体系中。滴加完毕,再继续反应16 h。用50%的丙酮-水溶液破乳,沉淀滤除后再用水洗,放入真空干燥箱,50℃干燥48 h得聚苯胺粉末。
1.3 HRP活性测定
反应在含有(或不含)10 mmol·L-1SDS的不同pH值的0.2 mmol·L-1Na2HPO4-柠檬酸缓冲溶液中进行,以10 mmol·L-1邻甲氧基苯酚为底物、HRP为催化剂,用H2O2引发反应后立即放置分光光度计监测470 nm处吸光度的变化。
以每分钟OD470变化0.01为1个酶活力单位(U)。
1.4 产物表征
用UV-双光束紫外可见分光光度计 (北京普析通用仪器有限责任公司)测聚合物的紫外可见光谱;用Nicolet 170SX型FTIR光谱仪(美国Nicolet)测聚合物的红外光谱,KBr压片法制样;用HMS-775型电导率仪(Lakeshore公司)测聚合物的电导率;用DTG-60H型热解重量分析仪(日本岛津公司)测聚合物的热稳定性。
2 结果与讨论
2.1 pH值对聚合反应的影响
pH值是合成导电聚苯胺过程中最重要的影响因素之一,苯胺只有在pH值低于4.6的条件下才能形成导电聚合物(苯胺的pKa为4.6)[9]。但酶活性在较低的pH值条件下会受到较大影响。研究了pH值在1.0~4.0范围内HRP催化苯胺聚合的反应,结果见图1。

注:[HRP]=0.1 mg·mL-1;[Aniline]=10 mmol·L-1;[SDS]=10 mmmol·L-1;[H2O2]=20 mmmol·L-1
实验中发现,将H2O2滴加到反应体系中后,pH值为1.0~3.0的反应体系均为翠绿色透明溶液,而pH值为4.0的反应体系则立即出现黑色沉淀。由图1可知,pH值为4.0的反应体系在700~900 nm范围内无吸收峰出现,而其在570 nm出现的吸收峰说明有非导电性的支链聚合物产生;当pH值降至3.0时,在700~900 nm范围内基本无吸收峰出现;当pH值为2.0时,在750 nm有很强的吸收峰,说明产生了导电聚苯胺;当pH值进一步降至1.0时,吸收峰减小且吸收峰的位置红移至715 nm左右[9,10]。
对聚合产物干燥处理后所得粉末进行电导率检测,结果表明pH值为1.0~2.0的反应体系得到了具有较高导电性的聚苯胺(表1),且pH值为2.0的体系得到的聚合物电导率最高。表明HRP催化导电聚合物的最适pH值为2.0,因此后续反应中选择体系的pH值为2.0。

表1 不同pH值条件下得到的PANI的电导率
2.2 HRP催化苯胺聚合作用的探讨
据文献报道,HRP在pH值低于4.3时会很快失去活力[11],而SDS是一种阴离子表面活性剂,常作为蛋白变性剂应用于SDS-聚丙烯酰胺凝胶电泳,因此SDS的存在将降低酶的活性。测定含有SDS或不含SDS的体系中HRP的活力,结果见图2。
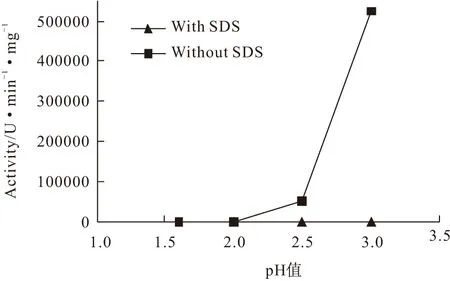
注:[HRP]=2.75×10-3 mmol·L-1;[Guaiacol]=10 mmol·L-1;[SDS]=10 mmol·L-1;[H2O2]=100 mmol·L-1
由图2可知,含有SDS的体系在pH值1.6~3.0范围内几乎不表现HRP活力;在不含SDS的体系中,pH值低于2.0时也几乎没有HRP活力;而pH值大于2.0时,HRP的活力随着pH值的增大显著增强。这说明低pH值和SDS的存在都是造成HRP失活的原因。
为进一步探讨HRP在导电聚苯胺聚合反应(以苯胺聚合体系在750 nm的吸光度表示,下同)中的作用,将HRP预先在沸水中处理15~30 min,使HRP在加入到聚合反应体系之前就已经失活,然后与未失活的HRP用于苯胺聚合反应进行比较,结果见图3。
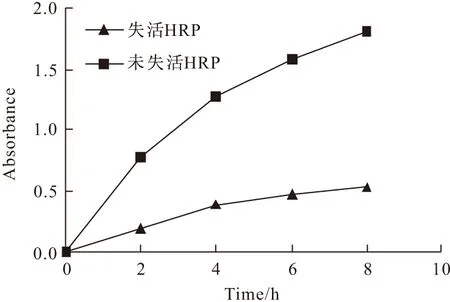
注:[HRP]=0.1 mg·mL-1;[Aniline]=10 mmol·L-1;[SDS]=10 mmol·L-1;[H2O2]=20 mmol·L-1
由图3可知,至少在8 h内,不论是否经过失活处理,HRP均能催化导电聚苯胺的合成。Nabid等曾运用铁卟啉和水溶性四磺酸化酞菁金属为催化剂催化苯胺聚合,得到了导电聚苯胺[12,13]。因此,推测虽然HRP分子中的蛋白部分因严苛的反应条件(低pH值和变性剂SDS的存在)而变性失活,但其活性中心的铁卟啉仍然能够不受环境条件的影响而发挥其催化苯胺聚合的作用。
2.3 H2O2浓度对聚合反应的影响
选择pH值为2.0的条件下考察H2O2浓度对苯胺聚合反应的影响,结果见图4。
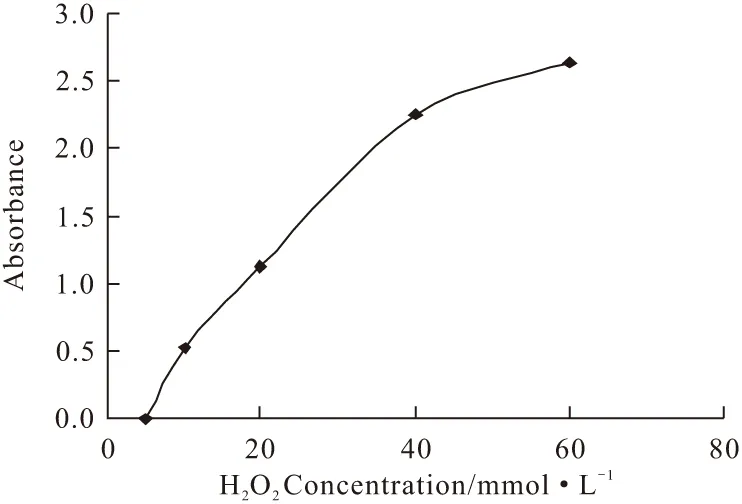
注:[HRP]=0.1 mg·mL-1;[Aniline]=10 mmol·L-1;[SDS]=10 mmol·L-1
由图4可知,随着H2O2浓度的增大,导电聚苯胺的吸收峰值也逐渐增强;当H2O2浓度达到60 mmol·L-1时,产物的吸收峰趋于平稳。但实验中观察到,H2O2浓度过高时(>20 mmol·L-1)会导致反应副产物的产生,同时考虑到较高浓度的H2O2会抑制HRP的活性,因此,选择H2O2浓度保持在20 mmol·L-1左右为宜。
2.4 SDS浓度对聚合反应的影响(图5)

注:[HRP]=0.1 mg·mL-1;[Aniline]=10 mmol·L-1;[H2O2]=20 mmol·L-1
由图5可知,SDS浓度为20 mmol·L-1时产物吸收峰很强,SDS浓度为40 mmol·L-1或小于10 mmol·L-1都会影响导电聚苯胺的生成。这是因为,SDS在水中可以形成胶束,这种胶束能够为苯胺单体的聚合提供适合的环境,在pH值为2.0的条件下,SDS带负电荷、苯胺单体带正电荷,因而SDS自组装形成的胶束将吸引苯胺单体在其周围聚集,进而促进水溶性导电聚合物的产生。SDS的浓度过低(<8.6 mmol·L-1)时在水溶液中就无法形成胶束,从而失去模板导向作用,使得聚合反应变慢,相同反应时间内导电聚合物的生成量较少。而SDS浓度太高又会显著降低HRP的活性,也不利于导电聚合物的生成。因此,选择SDS浓度在20 mmol·L-1为宜。
2.5 聚苯胺复合物的表征
2.5.1 FTIR(图6)
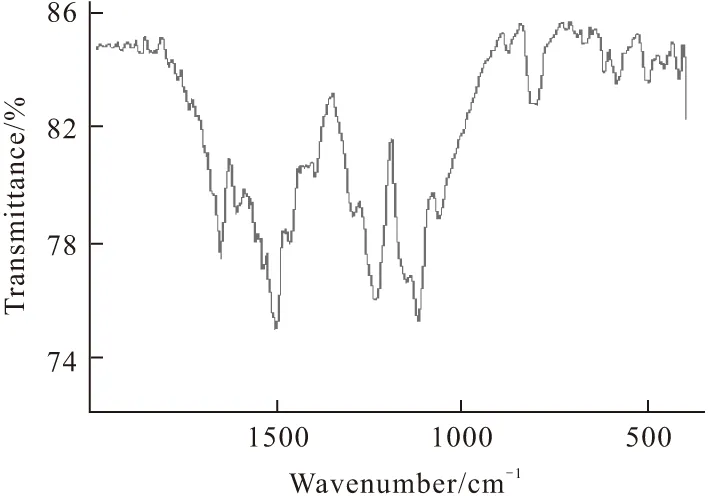
注:[HRP]=0.1 mg·mL-1;[Aniline]=10 mmol·L-1;[SDS]=10 mmol·L-1;[H2O2]=20 mmol·L-1
2.5.2 TGA(图7)

注:[HRP]=0.1 mg·mL-1;[Aniline]=10 mmol·L-1;[SDS]=10 mmol·L-1;[H2O2]=20 mmol·L-1
由图7可知,3种不同pH值下得到的PANI/SDS复合物在150℃以下都出现失重,在此温度范围内失重的应是水分。主要的失重出现在300℃以上,当温度升高到600℃时,3种PANI/SDS复合物保留率约30%,表明复合物具有较好的热稳定性。当温度升高到800℃时,pH值为3.0的条件下得到的PANI/SDS复合物保留率较其余两种稍高,因此其热稳定性相对较好。
3 结论
以HRP为催化剂,在SDS胶束水溶液中进行了水溶性导电聚苯胺的合成,对HRP在pH值1.0~4.0反应体系中催化导电聚苯胺合成的反应进行了研究。紫外可见扫描光谱分析和电导率测定的结果表明,在以SDS为模板的条件下,HRP催化水溶性导电聚苯胺合成的最适pH值为2.0、最适的SDS和H2O2浓度都在20 mmol·L-1左右。进一步测定HRP的活性发现,HRP pH值低于2.0时蛋白部分变性失活,但仍可催化导电聚苯胺的合成,推测HRP在催化导电聚苯胺的合成过程中主要依靠其活性中心的铁卟啉发挥其催化作用。运用FTIR和TGA等方法对合成的PANI/SDS复合物进行了表征,该复合物具有典型的导电聚苯胺复合物特征以及较好的热稳定性。
[1] Bhadra S,Khastgira D,Singha N K.Progress in preparation,processing and applications of polyaniline[J].Progress in Polymer Science,2009,34(8):783-810.
[2] Liu W,Kumar J,Tripat hy S,et al.Enzymatically synthesized conducting polyaniline[J].J Am Chem Soc,1999,121(1):71-78.
[3] Samuelson L A,Anagnostopoulos A,Shridahra Alva,et al.Biologically derived conducting and water soluble polyaniline[J].Macromolecules,1998,31(13):4376-4378.
[4] Karamyshev A V,Shleev S V,Koroleva O V,et al.Laccase-catalyzed synthesis of conducting polyaniline[J].Enzyme and Microbial Technology,2003,33(5):556-564.
[5] Sakharov I Y,Vorobiev A C,Castillo J J.Synthesis of polyelectrolyte complexes of polyaniline and sulfonated polystyrene by palm tree peroxidase[J].Enzyme and Microbial Technology,2003,33(1):661-667.
[6] Sangrama K S,Ramaswamy N,Sucharita R,et al.An enzymatically synthesized polyaniline:A solid state NMR study[J].Macromolecules,2004,37(11):4130-4138.
[7] Nagarajan R,Trypathy S K,Kumar J,et al.An enzymatically synthesized conducting molecular complex of polyaniline and poly(vinylphosphonic acid)[J].Macromolecules,2000,33(26):9542-9547.
[8] Nagarajan R,Liu W,Kumar J,et al.Manipulating DNA conformation using intertwined conducting polymer chains[J].Macromolecules,2001,34(1):3921-3927.
[9] Hu X,Zhang Y Y,Tang K,et al.Hemoglobin-biocatalysts synthesis of a conducting molecular complex of polyaniline and sulfonated polystyrene[J].Synthetic Metals,2005,150(1):1-7.
[10] Rodolfo C S,Jorge R G,Jose L A,et al.Template-free enzymatic synthesis of electrically conducting polyaniline using soybean peroxidase[J].European Polymer Journal,2005,41(5):1129-1135.
[11] Chattopadhyay K,Mazumdar S.Structural and conformational stability of horseradish peroxidase:Effect of temperature and pH[J].Biochemstry,2000,39(11):263-270.
[12] Nabid M R,Sedghi R,Jammat P R,et al.Synthesis of conducting water-soluble polyaniline with iron (Ⅲ) porphyrin[J].Applied Polymer Science,2006,102(3):2929-2934.
[13] Nabid M R,Sedghi R,Jammat P R,et al.Catalytic oxidative polymerization of aniline by using transition-metal tetrasulfonated phthalocyanine[J].Applied Catalysis A:Genaral,2007,328(1):52-57.
[14] Gu Y S,Chen C C,Ruan Z W.Enzymatic synthesis of conductive polyaniline using linear BSA as the template in the presence of sodium dodecyl sulfate[J].Synthetic Metals,2009,159(19-20):2091-2096.
